文摘
慢性阻塞性肺疾病(COPD)的特点是中性呼吸道的炎症反应,这些中性粒细胞炎症介质的产生。抑制炎性介质的产生可能是一个重要的策略治疗慢性阻塞性肺病和糖皮质激素是已知的通过抑制核factor-κB。然而,这个途径是重要的支持和抗炎基因的控制。
我们研究了地塞米松对生产的影响和炎性分泌白介素(IL) 1β和抗炎分泌IL - 1受体拮抗剂(sIL-1Ra)由人类中性粒细胞激活与肿瘤坏死因子(TNF) -α。
在体外,TNF-α-stimulated中性粒细胞产生大量IL-1βsIL-1Ra;这部作品被地塞米松抑制。然而,合成和分泌sIL-1Ra抑制在低浓度地塞米松IL-1β相比,显著改变了IL-1β:sIL-1Ra比率。这比改变导致更多的促炎症状态,视觉效果的增加细胞间粘附molecule-1表达人类内皮细胞。在活的有机体内,严重慢性阻塞性肺病患者使用吸入糖皮质激素减少血浆sIL-Ra水平与轻度到中度患者相比不是糖皮质激素治疗。
总之,地塞米松诱导的炎性改变IL-1β:sIL-1Ra细胞因子平衡中性粒细胞在体外,这可能导致缺乏内源性抗炎信号抑制炎症在活的有机体内。
慢性阻塞性肺疾病(COPD)的发病率正在增加,预计将成为第三个2020年世界上最常见的死因1。肺部慢性阻塞性肺病是一种炎症性疾病和治疗稳定的慢性阻塞性肺病患者常规抗炎治疗,如吸入糖皮质激素(gc)是无效的2。肺部的慢性炎症反应发现特征主要由中性粒细胞的积累,但巨噬细胞,b细胞和CD8 + t细胞也参与其中3。此外,增加中性粒细胞数量在支气管肺泡灌洗(BAL)流体诱导痰4和支气管活检标本5。这些中性粒细胞合成细胞因子,趋化因子和其他炎症介质导致肺部炎症和其他器官6- - - - - -8。有限的数据的影响吸入GCS在这些肺外的影响慢性阻塞性肺病9,10。
糖皮质激素引起其功能通过绑定到糖皮质激素受体(GR)。两个主要变体的GR GRαGRβ,表达各种炎性细胞和组织,包括中性粒细胞11。GRαligand-dependent转录因子,结合糖皮质激素(GRE)的DNA和响应元素,随后,调节GR目标基因12。GRα也被证明与其他转录因子相互作用,如激活蛋白(美联社)113和核因子(NF) -κB14,15,从而调节基因的转录。相比之下,GRβ不激活GR-responsive基因16,但已被证明在剂量依赖性抑制GRα的压制能力通过机制,迄今为止,不清楚。它可能涉及对格蕾丝的竞争或代数余子式,或形成GRα/ GRβ转录活性形成17。
抑制转录因子AP-1和NF-κB GCS已被确认是一个主要的机制来抑制免疫细胞的促炎细胞因子的生产18。然而,尽管gc的强大能力,抑制炎症反应,抑制neutrophil-driven炎症似乎不那么有效19。其他研究已经表明,方面引出对粒细胞促炎的影响,如增加白介素(IL) 1受体(IL-1R)类型我表达在人类中性粒细胞20.生存,长期嗜中性粒细胞在体外21,22,白细胞增多在活的有机体内23p38激活中性粒细胞和嗜酸性粒细胞24,25嗜酸性粒细胞,增加免疫球蛋白绑定25中性粒细胞,溶酶体酶的分泌增加26。因为不仅促炎症,而且抗炎,介质由转录因子控制NF-κB,方面会影响抗炎反应的表达式,这不是经常评估。
在本文中,我们报告一个免疫调节作用的GCS地塞米松IL-1β分泌,分泌IL-1R拮抗剂(sIL-1Ra)中性粒细胞。活化的中性粒细胞TNF-α诱导显著IL-1βsIL-1Ra蛋白质合成和分泌中性粒细胞在体外。正如所料,地塞米松抑制生产和分泌的促炎IL-1β中性粒细胞;然而,分泌sIL-1Ra比IL-1β更有效地抑制。这种差异导致了减少IL-1β:sIL-1Ra比率,可以增加细胞间粘附分子1 (ICAM)表达对人类脐静脉内皮细胞(HUVECs)在体外。有趣的是,最严重的慢性阻塞性肺病患者,接受吸入GCS显示降低等离子体IL-1Ra浓度与未经治疗的慢性阻塞性肺病患者和健康对照组相比,这可能表明,疾病严重程度,GCS吸入或两个表达下调抗炎细胞因子的生产在活的有机体内。
方法
患者和健康对照组
我们包括32诊断为慢性阻塞性肺病患者根据全球倡议对慢性阻塞性肺疾病(黄金)标准27。人口和吸入gc使用所示表1和2,分别。所有患者稳定的慢性阻塞性肺病没有恶化前4周的研究。其他炎症性疾病,心脏衰竭患者或口服GCS治疗被排除在外。健康,年龄的主题和无症状吸烟者没有被包括在研究慢性阻塞性肺病症状。乌得勒支大学医学中心的医学伦理委员会(荷兰乌得勒支)批准了这项研究,和所有的病人提供书面知情同意。
试剂
Ficoll-Paque是来自通用电气医疗集团(乌普萨拉,瑞典)。人血清白蛋白(HSA)是从Sanquin(阿姆斯特丹,荷兰)。地塞米松和RU38486(米非司酮)获得Sigma-Aldrich(圣路易斯,密苏里州,美国),在乙醇稀释。重组体人(rh) TNF-α从罗氏公司购买(美国印第安纳波利斯,)。rhIL-1β、rhsIL-1Ra anti-IL-1β和anti-IL-1Ra都从研发系统(英国阿宾顿)。Anti-actin (I-19)从圣克鲁斯生物技术(圣克鲁斯、钙、美国)。辣根过氧化物酶(合)耦合的二次抗体来自Dako(斯特鲁普、丹麦)。藻红蛋白(PE)共轭anti-ICAM-1(克隆mem - 111)是从Caltag(伯林盖姆、钙、美国)。Hydroxyethylpiperazine乙烷磺酸(玫瑰)缓冲RPMI 1640年从英杰公司购买(美国加利福尼亚州卡尔斯巴德)。其他材料都是试剂级。
粒细胞隔离
粒细胞从健康的捐赠者与全血100毫升实际上与柠檬酸三钠的(0.4% w / v, pH值7.4)。血液稀释和PBS含有柠檬酸三钠的2.5:1 (0.4% w / v, pH值7.4)和人类巴氏杀菌血浆蛋白的解决方案(4 g·L−1)。使用Ficoll-Paque粒细胞被离心分离。红细胞在等张细胞溶解,冰冷的氯化铵溶液(8.3 g·L−1NH4CL, 1 g·L−1KHCO3和37毫克·L−1EDTA),其次是离心在4°C。隔离后,粒细胞在PBS含有柠檬酸三钠的清洗和人类巴氏消毒血浆蛋白的解决方案,和resuspended HEPES-buffered RPMI 1640和0.5% (w / v) HSA补充。中性粒细胞的纯度> 95%,嗜酸性粒细胞作为主要污染物,但单核细胞< 1%。
免疫印迹分析
中性粒细胞(5×106细胞/样本)HEPES-buffered RPMI 1640 0.5% (w / v)补充保险公司被允许恢复为30分钟37°C。随后,细胞被刺激TNF-α(100 U mL−1)、地塞米松(10−6,10−8,10−10和10−12M)或组合3 h在37°C,在4°C与PBS洗一次,细胞溶解的样品缓冲(60毫米三-(羟甲基)甲胺盐酸盐(Tris-HCL) (pH值6.8),2%钠dodecylsulphate (SDS)、10%甘油、2%β-mercaptoethanol)和煮5分钟。蛋白质样本12% SDS-polyacrylamide凝胶分离和转移到Immobilon-P(微孔,阿姆斯特丹,荷兰)。杂交缓冲的膜被封锁(10毫米Tris-HCl (pH值8.0),150毫米氯化钠,0.1%渐变20)含有5% (w / v)奶粉(麋鹿,Campina、荷兰)1 h,其次是孵化主要抗体杂交缓冲0.5% (w / v)奶粉在一夜之间在4°C。膜清洗3×5分钟在杂交缓冲培养与二次抗体2 h,紧随其后的是3×5分钟洗在PBS杂交缓冲和最后一个洗。检测合活动所有西方的屁股都使用ECL +(通用电气医疗集团)和检测使用台风9410成像仪(通用电气医疗集团)。点密度分析使用Imagequant TL(通用电气医疗集团)。
sIL-1Ra和IL-1βelisa
血浆样本,sIL-1Ra(美国GA RayBio, Norcross)和一个高灵敏度IL-1βELISA试剂盒使用根据制造商的协议(研发系统)。对介质样品,sIL-1Ra (RayBio)和IL-1β(研发系统)ELISA试剂盒使用根据制造商的协议。
HUVEC文化和刺激
HUVECs隔绝人类脐带静脉如前所述29日。细胞培养的内皮细胞生长medium-2 (Lonza Walkersville,医学博士,美国)。单层细胞生长融合在5 - 7天。第二或第三段HUVECs被激活与IL-1β结合IL-1Ra 3 h,沾PE-conjugated anti-ICAM 30分钟,洗两次,分析在FACSCalibur流式细胞分析仪(正、布雷达,荷兰)。
统计分析
数据意味着±扫描电镜。正常的数据没有显著异构使用单向方差分析差异进行分析,其次是图基测试的方法事后分析、t检验,使用SPSS 15.0(美国SPSS Inc .,芝加哥,IL)或Graphpad棱镜4(美国Graphpad软件,拉霍亚,CA)。的假定值< 0.05被认为是具有统计学意义。
结果
TNF-α诱发合成pro-IL-1β和中性粒细胞sIL-1Ra剂量和时间的方式
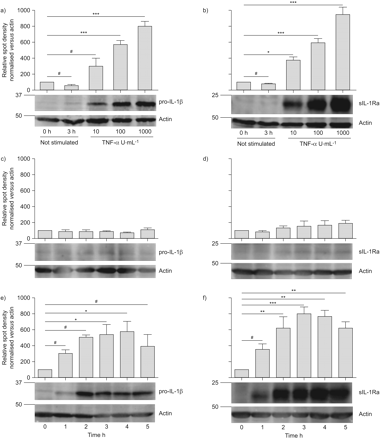
各种促炎介质与慢性阻塞性肺病的严重程度有关,但对在这一过程中抗炎细胞因子。职业之间的比例和抗炎介质将最终确定炎症反应的影响。因为中性粒细胞COPD的发病机制中发挥重要作用,我们调查是否中性粒细胞合成IL-1βIL-1Ra新创在与促炎中介TNF-α刺激。首先,我们研究了剂量和时间依赖性的TNF-α-induced pro-IL-1β人类中性粒细胞和sIL-1Ra蛋白质合成。TNF-α诱导细胞内pro-IL-1β(31 kDa)和sIL-1Ra (23 kDa)剂量依赖性的方式(图1一个和b,分别)。没有细胞内或细胞相关裂解IL-1β(kDa 17日)后被西方墨点法刺激中性粒细胞(数据没有显示)。TNF-α-stimulated中性粒细胞合成后pro-IL-1β和sIL-1Ra 1 h,它增加到最大值3 - 4 h和拒绝在5 h后刺激。中性粒细胞处理车辆控制没有合成pro-IL-1β或sIL-1Ra (图1氟)。基于这些结果,100 U·毫升−1TNF-α3 h用于进一步的实验。
肿瘤坏死因子(TNF) -α诱发pro-interleukin 1β和分泌IL - 1受体拮抗剂(IL) (sIL-1Ra)蛋白质合成在一个时间和剂量依赖性的方式。中性粒细胞(5×106细胞·毫升−1)刺激a - b)表示的浓度为3 h TNF-α37°C或氟)表示时间e、f)或C, d)没有100 U·毫升−1TNF-α在37°C。中性粒细胞在样品缓冲和细胞溶解蛋白质样本通过免疫印迹分析,c, e) anti-IL-1β或b, d, f) anti-sIL-1Ra, anti-actin加载控制。分子质量标记显示左边的每一个污点。数据意味着±扫描电镜(n = 6)。单向方差分析,其次是图基测试的方法事后分析,是用于执行统计分析。#:不显著;*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
地塞米松抑制TNF-α-induced IL-1βIL-1Ra蛋白质生产的中性粒细胞
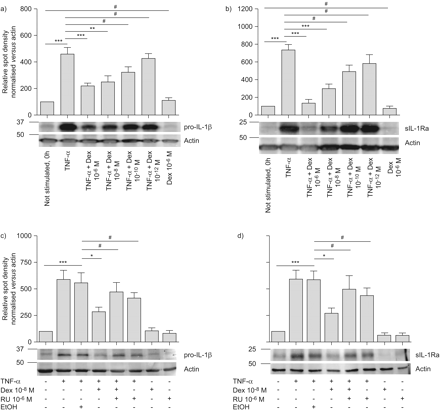
抗炎治疗基于GCS旨在减少炎症细胞的促炎介质的合成。为了评估的影响GCS地塞米松IL-1β和sIL-1Ra TNF-α-induced合成,我们与TNF-α刺激中性粒细胞(100 U·毫升−1)单独或TNF-α结合不同浓度地塞米松(10−6,10−8,10−10和10−12米)。中性粒细胞刺激TNF-α-induced pro-IL-1β的合成和sIL-1Ra蛋白质水平(图2一个和b)。地塞米松抑制了TNF-α-induced pro-IL-1β以及sIL-1Ra蛋白质合成方式存在剂量依赖的相关性,而单独使用地塞米松pro-IL-1β或sIL-1Ra(上显示无显著抑制作用图2一个和b)。值得注意的是,地塞米松(10−6米)减少TNF-α-induced sIL-1Ra生产82%;然而,它降低了TNF-α-induced IL-1β产量只有52%。地塞米松抑制TNF-α-induced pro-IL-1β和sIL-1Ra合成是通过GR介导,因为添加一个RU38486过剩,竞争GR拮抗剂30.得罪地塞米松的抑制作用显著,而没有影响TNF-α-induced pro-IL-1β和sIL-1Ra合成在缺乏地塞米松(图2 c分别和d)。因此,dexamethasone-induced GR信号有更强的抑制作用TNF-α-induced sIL-1Ra比IL-1β生产,这意味着在这些条件下促炎的平衡。
地塞米松(Dex)抑制肿瘤坏死因子(TNF) -α-induced白介素(IL) 1β和分泌IL - 1受体拮抗剂在中性粒细胞(sIL-1Ra)蛋白质合成。中性粒细胞(5×106细胞·毫升−1)pre-incubated表示数量的敏捷和RU38486(俄文)15分钟和刺激汽车控制或TNF-α(100 U·毫升−1)3 h 37°C。中性粒细胞在样品缓冲和细胞溶解蛋白质样本通过免疫印迹分析,c) anti-IL-1β或b, d) anti-IL-1Ra, anti-actin加载控制。实验表明代表至少三个实验。数据意味着±扫描电镜(n = 6)。单向方差分析,其次是图基测试的方法事后分析,是用于执行统计分析。EtOH:乙醇。#:不显著;*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
地塞米松抑制TNF-α-induced sIL-1Ra和IL-1β中性粒细胞的分泌
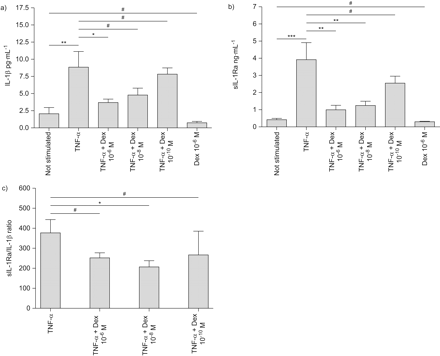
sIL-1Ra和IL-1β都活跃在细胞外环境中,细胞内生产并不一定反映细胞因子的分泌中性粒细胞。因此,我们调查sIL-1Ra和IL-1β中性粒细胞分泌到培养基TNF-α刺激后地塞米松的存在与否。为了量化分泌sIL-1Ra IL-1β,我们进行elisa。刺激中性粒细胞与TNF-α(100 U·毫升−13 h)导致的生产和分泌9 pg·毫升−1IL-1β和4 ng·毫升−1sIL-1Ra (图3和b,分别)。预处理与地塞米松抑制中性粒细胞sIL-1Ra和IL-1βTNF-α-induced分泌。然而,分泌sIL-1Ra从中性粒细胞刺激TNF-α地塞米松抑制在低浓度(10−8米)。当摩尔浓度的分泌IL-1β和sIL-1Ra计算,TNF-α-stimulated中性粒细胞比IL-1β合成sIL-1Ra 377倍,表明强烈的抗炎反应启动炎性刺激。有趣的是,TNF-α和地塞米松减少IL-1β:sIL-1Ra 1:238比率,1:206 1:267 10−10,10−8和10−6分别为M地塞米松(图3 c)。这表明IL-1Ra强烈的抑制能力方面存在时减少。
地塞米松(Dex)抑制肿瘤坏死因子(TNF) -α-induced IL-1βsIL-1Ra蛋白质分泌中性粒细胞。中性粒细胞(5×106细胞·毫升−1)pre-incubated表示数量的敏捷15分钟和刺激与车辆控制或TNF-α(100 U·毫升−1)3 h 37°C。)白介素(IL) 1β和b)分泌IL - 1受体拮抗剂(sIL-1Ra)由ELISA测定,遵循制造商的协议。数据意味着±扫描电镜(n = 6)。c)比值分泌IL-1βsIL-1Ra计算。单向方差分析,其次是图基测试的方法事后分析,是用于执行统计分析。#:不显著;*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
不同比率的重组人类sIL-1Ra IL-1β调节TNF-α-induced ICAM-1表达内皮细胞
的影响来说明不同IL-1β:sIL-1Ra比率炎性微环境,我们使用ICAM-1表情HUVECs作为生物读出IL-1β活动。HUVECs激活rhIL-1βICAM-1表达增加剂量依赖性的方式(图4)。rhsIL-1Ra (100 pg·毫升−1)剂量依赖性得罪IL-1β-induced ICAM-1表情HUVECs抑制浓度中位数(IC50)1.47 ng·毫升−1(图4 b)。需要100倍超额rhsIL-1Ra抑制IL-1β-induced ICAM-1表达了80%。评估的变化IL-1β:sIL-1Ra摩尔比,我们用10倍刺激HUVECs ELISA-measured IL-1β和sIL-1Ra (图3和b),因为这种诱导ICAM-1 HUVECs表达式(图4)。对应于TNF-α-stimulated中性粒细胞,88.5 pg·毫升−1rhIL-1β和39.1 ng·毫升−1rhIL-1Ra未能诱导显著ICAM-1 HUVECs表达式(图4摄氏度)。然而,类似于中性粒细胞刺激与TNF-α结合10−847.9 M地塞米松,pg·毫升−1rhIL-1β和12.4 ng·毫升−1rhIL-1Ra诱导显著ICAM-1表达式。这些结果表明,甚至IL-1β浓度较低(47.9与88.5 pg·毫升−1),减少的比率IL-1β:sIL-1Ra增加ICAM-1 HUVECs表达式。这些结果清楚地表明,严密的赞成和抗炎介质之间的平衡决定炎性反应。
改变白介素(IL) 1β:分泌IL - 1受体拮抗剂(sIL-1Ra)比率增加细胞间粘附分子1 (ICAM)表达对人类脐静脉内皮细胞(HUVECs)。与表示的浓度)HUVECs刺激重组人类(rh) IL-1β3 h和ICAM-1表达式通过流式细胞仪测定(n = 3)。数据描绘成中间通道荧光(MCF)和在任意单元(AU)。b) HUVECs刺激100 pg·毫升−1rhIL-1β结合表示浓度rhsIL-1Ra 3 h和ICAM-1表达式被流式细胞仪测量。相对抑制rhIL-1β诱导ICAM-1表达式通过rhsIL-1Ra HUVECs显示(n = 3)。y= -12.83 ln (x)+ 54.978,r2= 0.9868。c) HUVECs刺激了rhIL-1β结合rhsIL-1Ra对应数量以3 h和ICAM-1表达式的ELISA是衡量流式细胞术(n = 5)。单向方差分析,其次是图基测试的方法事后分析用于执行统计分析。#:不显著;*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
降低COPD患者的血浆sIL-1Ra吸入方面
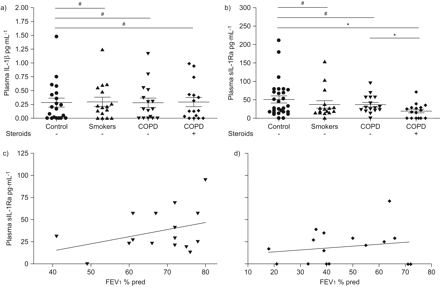
评估吸烟和gc使用的影响,我们测量IL-1βsIL-1Ra健康控制的等离子体,无症状吸烟者和慢性阻塞性肺病患者和没有每日吸入gc使用。所示使用的大量吸入类固醇表2。所有的研究对象是年龄和没有区别在1 s (FEV用力呼气量1健康控制和无症状吸烟者(之间)表1)。慢性阻塞性肺病患者没有GCS治疗范围之间的黄金阶段,我和三世,而慢性阻塞性肺病患者GCS范围从黄金第四阶段II,导致FEV的显著差异1在两组之间。表达IL-1β很低,测量组之间没有明显不同(图5和表1)。sIL-1Ra,然而,显示趋势是低没有GCS治疗无症状吸烟者和慢性阻塞性肺病患者与健康对照组相比,而在COPD患者显著降低日常GCS吸入的方案(图5 b)。sIL-1Ra COPD患者的表达,没有与FEV gc使用不相关1(图5 c - d)。
白介素(IL) 1β和分泌IL - 1受体拮抗剂(sIL-1Ra) ELISA健康对照组血浆样品,无症状吸烟者和慢性阻塞性肺疾病(COPD)患者。血浆样本收集,IL-1β和b) sIL-1Ra ELISA测定。-:的意思。胡须代表扫描电镜。使用一个未配对t检验进行统计分析。#:不显著,*:p < 0.05。相关的慢性阻塞性肺病患者的血浆sIL-1Ra c)没有(r2= 0.1280,p = 0.1737)和(r d)2= 0.344,p = 0.4913)吸入类固醇治疗在1 s (FEV用力呼气量1)。% pred: %预测。
讨论
与GCS治疗炎性疾病通常旨在减少炎症细胞的促炎细胞因子的生产,尽管其功效在抑制中性粒细胞炎症很差2。最近的研究表明,gc能够诱导这些细胞的促炎反应20.- - - - - -26。我们测试的假设GCS影响TNF-α-induced pro和抗炎细胞因子的合成和分泌中性粒细胞。因此,我们监控生产促炎IL-1β和抗炎sIL-1Ra TNF-α-induced中性粒细胞缺乏,存在不同数量的地塞米松。一些介质,如血清淀粉样蛋白A,集落刺激因子(gm - csf),脂多糖(LPS)和TNF-α,可以通过中性粒细胞诱导pro -抗炎介质31日- - - - - -38。我们选择TNF-α因为这种细胞因子升高血清和平衡稳定的慢性阻塞性肺病患者39- - - - - -41和它的行动NF-κB是有据可查的42,43。
我们的研究支持了数据表明sIL-1Ra32- - - - - -35和IL-1β36,37在中性粒细胞TNF-α刺激后合成增加,而争议存在的实际分泌IL-1β中性粒细胞。IL-1β中性粒细胞在分泌物刺激与已经观察到的有限合伙人35,而其他研究报告没有有限合伙人——酵母聚糖-或gm - csf -诱导IL-1β分泌33,35。造成这种差距的原因可能是由于不同的解释发现的浓度的相关性。在施罗德的研究et al。33,很难知道IL-1β水平低是观察,而Altstaedtet al。44确实发现较低,但可检测,增加IL-1β酵母聚糖刺激。实际上,我们还发现低但可检测水平(9 pg·毫升−1)的IL-1βTNF-α刺激,Marucha观察到类似的范围et al。37。这些浓度的检测范围内我们的ELISA (1 - 250 pg·毫升−1),但远低于那些由单核细胞在体外33。中性粒细胞产生的低水平可能仍然在炎症条件下生理有关在活的有机体内,因为嗜中性粒细胞数量出现在网站的炎症,如落下帷幕的COPD患者和类风湿性关节炎患者滑液45,46的单核细胞,往往几次。因此,我们建议,中性粒细胞炎性IL-1β和抗炎sIL-1Ra的重要来源。
中性粒细胞能够合成sIL-1Ra IL-1β新创,这被认为是通过激活NF-κB介导的47- - - - - -49。方面已被证明抑制转录因子的活动14,15,这促使我们探讨地塞米松对IL-1β和sIL-1Ra蛋白质合成的影响。有趣的是,我们发现,地塞米松治疗减少合成和分泌比IL-1βsIL-1Ra更有效率,从而影响这些分泌il - 1的支持和抗炎平衡家庭成员。地塞米松显示差影响的机制(pro) IL-1βsIL-1Ra蛋白质合成和分泌尚不清楚,但可能躺在转录后机制,如mRNA的稳定性50、蛋白质翻译51和/或蛋白质的稳定性22。促炎IL-1β之间转移平衡,抗炎sIL-1Ra被发现在活的有机体内在一些慢性炎症性疾病,如风湿性关节炎,溃疡性结肠炎、克罗恩病和慢性阻塞性肺病52- - - - - -55。最近,Reddyet al。56和Aksentijevichet al。57特征sIL-1Ra基因的突变,导致IL-1β高反应性。
同意Sapeyet al。54,我们观察到一个降低COPD患者每天使用吸入sIL-1Ra GCS与健康对照组相比,无症状吸烟者和慢性阻塞性肺病患者没有GCS治疗。这可能表明,在活的有机体内吸入GCS下调抗炎细胞因子的生产。然而,吸入或口服GCS已被证明影响IL-1βsIL-1Ra水平血清,而其他细胞因子,如interferon-γ-induced protein-10,单核细胞趋化蛋白1和可溶性肿瘤坏死因子受体2,受到影响9。或者,低水平的sIL-1Ra可能是由于疾病严重程度,由于慢性阻塞性肺病患者GCS吸入疗法FEV最低1。然而,观察,FEV之间不存在相关性1和等离子sIL-1Ra水平在慢性阻塞性肺病组不支持这个假说(图5 c - d)。因此,我们的数据无法区分sIL-1Ra水平低的假设中发现慢性阻塞性肺病患者的血清可能通过使用吸入类固醇或疾病严重程度。此外,这些低sIL-1Ra中性粒细胞的贡献水平在活的有机体内还有待建立。这还需要进一步的研究,以解决这些假设。
的促炎的能力IL-1β:sIL-1Ra比率被HUVECs使用ICAM-1表达式显示为一个生物宣读。我们研究的一个限制是,净IL-1β炎症效应:sIL-1Ra比上层清液的中性粒细胞无法确定,因为1)许多其他公认的炎症因素存在于上层的可能影响ICAM-1表情HUVEC细胞和2)上层清液包含TNF-α和地塞米松对HUVEC细胞影响ICAM-1表达式。因此,我们测试了不同比率的IL-1β:sIL-1Ra用重组蛋白。rhIL-1β能够诱导ICAM-1表情HUVECs剂量依赖性的方式(图5)。rhIL-1β-induced (100 pg·毫升−1与rhIL-1Ra) ICAM-1表达被抑制,IC501.47 ng·毫升−1(1:15比例),这是按照先前公布的数据58,59。作为100 pg·毫升HUVECs强烈回应−1rhIL-1β,我们乘IL-1βsIL-1Ra浓度测量ELISA 10倍。> 100 pg·毫升的浓度−1IL-1β存在的关节炎患者滑液60和慢性阻塞性肺病患者落下帷幕41根据中性粒细胞的数量,现在网站的炎症,这些浓度可能达成。88.5 pg·mL的结合−1rhIL-1β和39.1 ng·毫升−1rhsIL-1Ra,对应的浓度以ELISA TNF-α-stimulated中性粒细胞,并没有引起重大HUVECs ICAM-1表情。然而,47.9 pg·毫升−1rhIL-1β结合12.4 ng·毫升−1rhsIL-1Ra,对应TNF-α10−8M地塞米松诱导ICAM-1 HUVECs显著的表达(图4摄氏度)。这些结果表明,即使减少rhIL-1β,比rhsIL-1Ra决定了生物效应。sIL-1Ra的重要性是由天然sIL-1Ra-deficient演示的人患有严重的自身免疫性疾病56,57。rhsIL-1Ra (Anakinra)是非常有效的治疗这些疾病,也用于治疗慢性炎症性疾病61年,如类风湿性关节炎等62年和青少年特发性关节炎63年。天然受体拮抗剂是有效的促炎信号的抑制炎症介质。这表明,这种不平衡的IL-1βsIL-1Ra导致炎症的恶化。此外,由人类巨噬细胞激活IL-1β分泌增加三倍由于inflammasome蛋白的突变NALP3导致严重autoinflammatory障碍,强调严格IL-1β和sIL-1Ra之间的平衡的重要性64年,65年。
总而言之,我们想强调,重要的是要评估新药的抑制作用在生产支持和抗炎介质。抑制NF-κB是最重要的一个目标创新抗炎治疗66年尽管抗炎介质,如sIL-1Ra,也被这种方法。认真解决GCS生产抗炎细胞因子的影响在活的有机体内将是重要的,因为低宿主内源性抗炎反应可能加重炎性疾病。
确认
我们要感谢l . Cron(荷兰内梅亨大学医学中心,奈梅亨,)她的批判阅读手稿。
脚注
支持声明
这项研究受到了研究荷兰的哮喘基金会的资助项目3.2.03.63数量。
感兴趣的语句
一份声明中对l . Koenderman可以发现www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2009年的10月28日。
- 接受2010年6月24日。
- ©2011人队