摘要
令人信服的证据表明,微血管密度(MVD)是早期非小细胞肺癌(NSCLC)的预后标志。然而,它在接受多种治疗的III期非小细胞肺癌淋巴结转移中的作用尚不清楚。
142例III期NSCLC患者的淋巴结,在德国肺癌合作组的一项试验中接受治疗,评估了MVD。中位随访时间为7.39年。MVD与人口统计学和肿瘤相关变量及生存率相关。
MVD(中位数33.9)与生存没有相关。然而,在接受肿瘤切除患有负边缘(R0)的多模式处理的第IIIA患者中,具有高MVD的患者显着延长了4.96年的中位数,与1.99 YRS为1.99 YRS,用于低MVD(P = 0.041)。COX回归分析显示,MVD是R0-切除阶段IIIa(危害比0.417)的预后因子。Furthermore, a significant correlation of MVD to stage was observed, with significantly lower MVD in stage IIIA than IIIB (p = 0.0062), and a significant correlation of MVD to histological subtype was observed, with adenocarcinoma revealing the highest scores (p = 0.0001).
淋巴结转移内血管新生的增加是NSCLC患者更好生存的预后指标。因此,MVD的测量可能有助于选择未来新辅助治疗的患者。
血管生成是一个复杂的、多步骤的过程,从已有的血管系统中形成新的微血管,参与大多数实体肿瘤的生长、维持和转移1.几份报告已经证明,通过肠道微血管密度(MVD)评估的新血管体系与各种肿瘤的临床病理因子和患者结果进行了显着的相关性2.
关于肿瘤内MVD表达的非小细胞肺癌(NSCLC)中血管生成活性的预后相关性,高MVD已被确定为预测转移和生存差的预后因素3..此外,原发性肿瘤内的血管内皮生长因子和其他血管生成生长因子的高表达被认为是NSCLC患者结果减少的独立指标4.然而,大多数研究都是针对早期肺癌进行的,对于NSCLC患者转移特别是淋巴结转移中血管生成对预后的影响知之甚少。
在局部晚期IIIA和IIIB期伴有纵隔淋巴结转移的NSCLC中,单纯局部区域治疗(手术或放疗)的远期疗效令人失望。术前化疗(放疗)后进行手术的多种治疗方法可以改善预后并使手术成为可能,即使在IIIB期疾病中也是如此5,6.然而,这些治疗方案仍在开发中7.抗体治疗和酪氨酸激酶抑制剂的增加提高了鉴定患者亚组的兴趣,即使在多层态方法中,也能受益于额外的全身治疗。抑制肿瘤血管生成已经被评估为治疗策略,并对新的肺癌疗法的发展具有极大的承诺。目前正在调查各种不同的抗血管生成药物,或已被许可用于治疗肺癌4.
在本研究中,德国肺癌合作组织(GLCCG)的一项试验中,在开始多模式治疗策略之前,局部晚期NSCLC患者的淋巴结转移中新生血管的临床意义8通过将MVD与存活率相关,对治疗的反应以及进一步的预后因素进行检查。
材料和方法
病人和治疗
我们研究了142例局部晚期、未治疗的III期NSCLC患者的纵隔淋巴结活检石蜡包埋标本。在GLCCG的一项随机III期试验中,纳入患者的标准是充分具有代表性的治疗前活检材料,用于MVD分析和治疗,该试验经机构审查委员会批准,并在www.clinicaltrials.gov(nct00176137.)8.简单地说,在目前的方案中,III期NSCLC患者(必须有侵袭性纵隔分期)根据中心和分期(IIIA或IIIB)进行分层,然后随机进行治疗。治疗包括三个周期的顺铂55 mg·m−2(第1天和第4天)/ etoposide 100 mg·m−2(第1-4天)(PE),其次是高度放射疗法(HFRT)(45灰色; 2×1.5灰色·日−1),同时加卡铂100 mg·m−2/长春定3mg(第1、8、15天),然后手术。对于不能手术或(R1/2)切除阳性的患者,附加hfRT (24 Gray;2×1.5灰色·天−1)提供。对照组患者计划接受3个周期的PE治疗,随后进行手术和常规分割放疗(1.8 Gray·day)−1)为54 Gray,如果患者不能手术或接受R1/2切除,为68.4 Gray。如果患者对该方案没有书面同意或没有足够的组织学标本,则被排除在外。
评估了以下变量在患者队列中的分布情况以及它们与预后的可能相关性:患者年龄、性别、组织学亚型、治疗组的随机分组、分期、诊断时的淋巴结状态、原发肿瘤切除边缘(阴性(R0))与阳性(R1, R2)),完全或不完全切除。完全切除定义为R0切除,切除最上部纵隔淋巴结不转移。
MVD的免疫系统研究与评价
加工石蜡包埋的活检标本的连续切片,用于用抗CD31抗体(克隆JC / 70A,工作稀释1:100; Dako,Hamburg,Germany)进行免疫组织化学识别微血管内皮细胞的免疫组化鉴定。通过碱性磷酸酶/抗碱性磷酸酶双桥技术(Dako-Apaap套件; Dako)进行免疫组化定位。在染色之前,将组织切片在二甲苯中脱糖,以梯级乙醇系列再水化,并用蛋白酶K处理,用于抗原检索。将初生抗体在4℃下施加过夜。根据制造商的说明进行后续步骤。使用快速的红色衬底(DAKO)用于对磷酸酶活性(室温10分钟10分钟)启动。切片用0.1%(w / v)血红素染色。
如前所述,血管生成的程度是通过每个切片和两个切片中三个独立热点内的微血管计数来确定的9,10.MVD定义为每0.26 mm微血管的平均计数2场区域(即。×400字段)。观察者间和交叉变异的中位数较低(分别为2%和4%)。根据国际共识报告,确定全组MVD中位数,将患者分为高(>中位数)和低(≤中位数)两组10.
统计分析
(分类)MVD和明确的预后因素的关联(即。使用Fisher的确切测试检查了性爱,组织学亚型,治疗臂,阶段,淋巴结状态,切除术和切除状态的随机化。为了检查(分类)MVD和患者年龄的关联,应用U-Test。
时间 - 事件变量的分布采用Kaplan-Meier法估算,并且比较是基于对数秩检验。中位随访由逆Kaplan-Meier方法来估计。所有潜在的预后因素评估和MVD使用Cox比例风险模型进行测试。
所有报告的p值均为双侧,显著性水平为0.05。统计分析是探索性的而不是确证性的。没有对多次试验进行调整。所有计算均使用SAS软件包(SAS Institute Inc., Cary, NC, USA)进行。
结果
病人的特点
本研究的受试者是142例在GLCCG III期试验中接受治疗的NSCLC患者8.有114名男性和28名女性,中位数(范围)为59岁(33-69)YRS。患者特性如表1所示⇓.鳞状细胞癌65例,腺癌62例,大细胞癌15例。77名患者被随机分配到实验组,65名患者被随机分配到对照组。诊断为IIIA期59例,IIIB期83例。88例患者接受手术,其中73例接受R0切除,51例完全切除。R0切除患者中38例为IIIA期,35例为IIIB期。
MVD在非小细胞肺癌
所有患者的中位微血管计数为33.9(每个×400, 0.26 mm2场)的9.25-69.5一个四分位数间距。患者被分成两组以高(> 33.9)和低(≤33.9)MVD,基于整个组的中值MVD。Representative lymph node biopsy tissue specimens from lung cancer patients are shown in figure 1⇓对于低浓度肿瘤(图1a⇓)和肿瘤高(图1b⇓)MVD。
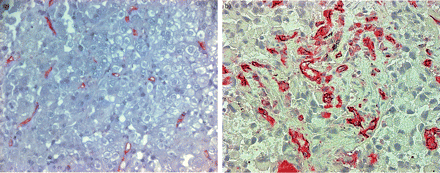
用抗cd31抗体对非小细胞肺癌淋巴结转移组织片进行免疫组化染色,定量微血管密度(MVD)。a)低MVD和b)高MVD标本的切片。原来放大×200。
A significant correlation of MVD with stage was noticed (p = 0.0062). In stage IIIA, the median MVD was 22.4, while in stage IIIB the median MVD was 40.6. Concerning the nodal status, a high MVD correlated significantly with an advanced lymph node status (N3; p = 0.019). Furthermore, a statistically significant association could be detected between MVD and the histological subtype (p = 0.0001). While 69.4% of patients with adenocarcinoma had a high MVD, this was only 33.2% in squamous cell carcinoma. Moreover, a statistically significant association between MVD and sex could be detected (p = 0.019). There was no statistically significant correlation between MVD and patient age, resection margins, resection status or treatment arm (data not shown).
MVD与总生存率和无复发生存率的相关性
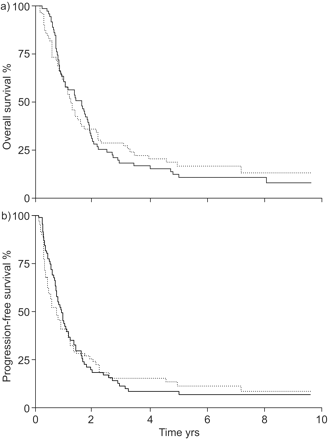
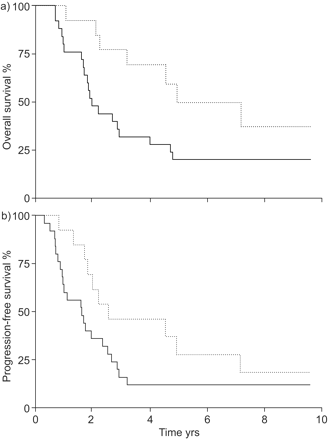
中位(范围)随访时间为7.39(0.14 ~ 9.63)年。在分析的所有142例患者中,总生存期(OS)和无进展生存期(PFS)在高水平患者之间没有差异与低MVD(P = 0.80和P = 0.87分别;图2A⇓b)然而,在接受肿瘤R0切除术的IIIA期患者中,高MVD患者的OS显著延长,中位MVD为4.96年,而低MVD患者的中位生存期为1.99年(p = 0.041)。PFS也延长(2.57与1.62年),但未达到统计学意义(p = 0.089;图3⇓b).为了排除并发疾病可能干扰OS分析的可能性,进行了死亡率分析,该分析显示大多数死亡与肿瘤相关,并没有改变该分析的结果(数据未显示)。
Kaplan-Meier估计了所有分析患者(n = 142)的总体生存率和b)无进展生存率。····微血管密度(MVD) >33.9;——:MVD≤33.9。Log rank a) p = 0.80, b) p = 0.87。
a)总体和b)阶段的无进展存活的kaplan-meier估计,阶段非血管细胞肺癌患者患有阴性外科切除率的患者,根据中学微血管密度(mvd)为33.9(n = 38)。a)与低MVD( - - MVD≤33.9; P = 0.041)的患者相比,在高MVD(···MVD> 33.9)的患者中,整体存活率显着延长。b)无进展的存活也延长但未达到统计学意义(P = 0.089)。
整组患者根据淋巴结状态,治疗臂,切除余量和切除状态进行了进一步的亚组分析。这些因素被选中,因为它们可能会影响结果并干扰MVD的预测影响6,8.亚组分析对整个患者人群的中位MVD(33.9)和各自亚组的中位MVD进行分析。
在IIIA期分析中,亚组MVD中位数为22.4。在这里,中位随访时间为9.31年,MVD高(中位PFS 1.84年)患者的PFS明显延长,而MVD低(中位PFS 0.89年;p = 0.05)和R0切除的IIIA患者(p = 0.03)。OS在IIIA期亚组中显示出类似的相关性(2.26与1.62年);但无统计学意义(p = 0.15)。
对于IIIB期、N2或N3淋巴结状态的患者,实验组或对照组治疗,R0切除或完全切除,OS和PFS均无明显差异与低MVD(数据未示出)。
单因素Cox回归分析确定,IIIA期和R0期切除患者的MVD是独立的预后生存因素(风险比0.417,p = 0.04), IIIA期亚组分析(截断值22.4)是PFS的预后参数(风险比0.580,p = 0.05)。此外,多因素Cox回归分析显示切除状态(完全与不完全)是整个患者群体中生存的独立预后因素(p = 0.009)。
讨论
本研究的目的是在多层疗法的情况下,研究III型NSCLC阶段III NSCLC患者淋巴结转移患者淋巴结转移的临床意义。尽管在理解NSCLC的分子生物学方面取得了进展,但其治疗仍然挑战。到目前为止,在局部高级NSCLC中发起化疗之前,缺乏临床分层类别,这将允许预测对治疗的反应。最近的研究表明,血管生成在NSCLC的发病机制和疾病进展的机制中起着重要作用4.
本研究首次在一大批患者中证明,接受包括肿瘤R0切除在内的多种治疗的IIIA期NSCLC患者的纵膈淋巴结转移与MVD显著相关。与低MVD患者相比,转移灶内MVD程度高的患者生存率显著提高。
其他几个人已经报道了NSCLC中的MVD和预后的关联。目前的数据符合Chandrachud的报告et al。11研究显示,血管密度较高的非小细胞肺癌患者的生存时间一般较长。然而,与目前的结果和钱德拉楚德的结果相反et al。11,大多数其他作者所述描述了高MVD是NSCLC中存活的差的预后因素。
有几个因素必须考虑。首先,大多数的这些报告原发性肿瘤内微血管密度调查目的的同时,本研究淋巴结转移中确定MVD。研究由Angelettiet al。12对可比人群的调查产生了与目前研究相反的结果,表明原发肿瘤内的高MVD是一个负面的预后因素。这可能是因为比较原发性肿瘤和淋巴结转移的MVD是不可靠的。Edel的一项研究支持了这一假设et al。13他的研究仅证明了单个乳腺癌肿瘤中血管生成水平与转移淋巴结之间的不同联系。此外,Guidiet al。14显示只有淋巴结转移的MVD与生存相关,而原发性乳腺癌的MVD与生存无关。
其次,大多数关于MVD在NSCLC中的作用的报道确定了早期肺癌的血管生成,而本研究探索的是局部晚期NSCLC患者。由于不同阶段的NSCLC预后差异显著,因此需要谨慎进行比较。
然而,最重要的区别可能是其他作者仅研究手术治疗的患者,而本研究中患者一个多学科综合治疗的理念内处理。强化综合化疗集成到一个综合治疗策略导致不同的预后改善Ⅲ期非小细胞肺癌5,这可能是本报告中MVD程度高的患者生存率更高的一个解释。肿瘤微循环是药物向肿瘤细胞输送的重要因素15,更高密度的血管可以假设化学疗法的可达性,以增殖肺癌细胞,即。药物递送的功效可能是肿瘤中的高得多具有高度MVD的比在具有低MVD的肿瘤。这一假设的支持来自通过VOLM研究et al。16据相比,据显示,与化疗敏感的肿瘤相比,均显示MVD在化疗抗性NSCLC肿瘤中显着降低。
另外,通过诱导内皮细胞凋亡的细胞毒性化学疗法的直接抗血管生成机制可能有助于消除肿瘤细胞。实际上,已经描述了对内皮细胞以及真实抗血管生成效应的直接毒性作用在体外和在体内不同细胞抑制药物模型(例如蒽环类、长春花生物碱和紫杉醇)17- - - - - -20..这一假设也可以解释安杰莱蒂实验结果的不同et al。12以及目前的研究,这很可能与不同的治疗方式有关。在目前的研究中,所有患者都接受了强化化疗,而在Angeletti的报告中,只有大约三分之一的患者接受了强化化疗et al。12chemotherapeutically治疗。此外,必须考虑放疗或放化疗的影响,因为肿瘤内的缺氧会导致对放疗的耐药性。假设,在高血管化的肿瘤病变中,氧合可能得到改善,导致对治疗的反应增强,从而提高生存率。这一假设得到了一些报道的支持,这些报道已经表明,在接受放化疗的实体肿瘤中,更高的MVD与更好的反应和生存率显著相关15,21..
最后,我们观察到MVD与多模治疗期IIIa IIIA患者的更好存活率相关,但没有在完全切除的人中显着。完全切除的定义为R0切除,没有最高的去除纵隔淋巴结的转移累及,是III阶段NSCLC中增强存活的指标8.因此,我们的发现可能支持我们的假设,即血管化程度增加的淋巴结转移与低MVD的淋巴结转移相比,对化疗/放疗的反应更好。即使R0切除后最上纵隔淋巴结受累,MVD高的患者比淋巴结转移内MVD低的患者生存率更高,这可能与放化疗的作用有关。
与上述报告的一些差异也可能是由于评估MVD方法的细节会影响其作为预后指标的价值,例如抗体(CD31,CD34或von Willebrand因子)或MVD是否在肿瘤的周边或中心评估22..根据国际共识,CD31是拟议的intr内umvd量化标准10.然而,必须严格讨论的是,CD31估计淋巴结转移内的MVD可能导致假阳性结果23..尽管如此,我们在淋巴结内的MVD估计仅在替代原始淋巴结结构的大转移性病变中进行。
应当深入讨论了为什么MVD是IIIA期生存的唯一一个积极的预测。但是,人们必须考虑到III期非小细胞肺癌的患者异构收集和IIIB期非小细胞肺癌是生存显著减少与IIIA期相比。此外,R0切除只能在IIIB期患者比IIIA期的患者比例较低执行,这表明在IIIB期患者不宜切除状态的影响结果最。这一假说是由发现,切除状态是在分析整个患者群体生存的独立因素的支持。此外,生存局部晚期非小细胞肺癌依赖于其他方面,如合并症和其他分子和免疫因素。然而,我们不能排除我们的亚组分析导致I型错误的大量增加。然而,我们的分析是没有证据确证水平,并作为当前的分析是探索性的,我们没有评估预先指定的零假设。此外,在目前的分析中相当大的一部分,朝高的患者MVD更好的生存趋势发现,虽然没有达到统计学意义。
腺癌是最近报道的血液中最常见的肺癌类型,是女性中最常见的组织学类型和无论是性别的24..因此,我们观察到MVD与组织学亚型显著相关,并且腺癌更常出现高MVD,这是非常显著的。Yuan也得到了类似的结果et al。25.,对于腺癌患者的患者展示显着高于抗鳞状细胞癌的MVD。
目前研究的另一个值得注意的结果是MVD与分期和淋巴结状态的相关性。这些观察结果与其他的一致25.- - - - - -27.,强调了血管生成在非小细胞肺癌进展中的重要影响,并为我们研究结果的可靠性提供了支持。
总之,本研究为IIIA期NSCLC患者接受多模式R0切除术后淋巴结转移内MVD的预后意义提供了证据。MVD增加的患者生存率更高。因此,MVD可能是一种潜在的有用的预测标志物,在多模式治疗策略治疗的患者中,应该进一步探索作为治疗分层的潜在工具。
支持声明
目前治疗这些患者的临床试验由德国波恩癌症援助组织资助。它登记于www.clinicaltrials.gov与参考号码nct00176137..
感兴趣的语句
没有宣布。
致谢
我们感谢C. Sauerland(医学信息学和生物疗法,Münster大学,德国Münnster大学)为她的技术援助为M.恩格斯(医学,血液学/肿瘤大学)的优秀统计建议和N. Sellhast(德国Bochum大学,Bochum大学,德国病理学研究所)为她的支持。
脚注
通过回答有关本文的问题获得CME认证。你可以在本刊印刷版的背面或网上找到这些资料www.www.qdcxjkg.com/current.dtl
- 收到了2008年8月6日。
- 接受2009年1月20日。
- ©ERS期刊有限公司