抽象的
异源抗性结核分枝杆菌(MTB)被定义为同一患者的抗结核(TB)药物的敏感和抗性生物的共存。MTB的杂收被认为是初步抵抗的初步阶段。迄今为止,已证明了没有导致MTB杂项的机制。
来自乌兹别克斯坦塔什干的35名结核病患者的临床标本和培养物采用基因型MTBDR分析法(德国尼伦Hain Lifescience)进行分析,该方法旨在检测与利福平和异烟肼耐药性相关的基因突变。使用分枝杆菌散布重复单位可变数量串联重复分型、spoligotyping和IS对异质耐药病例进一步进行基因分型6110.指纹识别。
在7例(20%)中发现了对利福平和/或异烟肼的杂蛋白。在其中五分之一中,杂一是由两种不同的菌株引起的,并且通过单一的北京基因型菌株引起。后一种情况有他们的结核病的复发历史。
首次,已经使用逐步分子生物学方法证明了两种不同机制的结核病:1)具有两种不同菌株的超育,这对临床感染控制从业者感兴趣;2)将单一菌株分成易感和抗性生物体。后一种机制最有可能与治疗质量差有关,并可作为未来结核治疗方案的质量标志物。
多药耐药性(MDR)对世界结核病(TB)的增加健康问题缩影。根据全球抗结核耐药耐药监测的第四次报告1.,在乌兹别克斯坦塔什干观察到世界上最高的MDR-TB(60%)。
耐多药结核病的定义是结核分枝杆菌(MTB)至少以Isoniazid(INH)和利福平(RMP)复合物。大多数耐受INH的抗性是由密码子315(S315T)的突变引起的凯特基因2..超过95%的耐力抗性病例由81bp核心区域中的一个或多个突变确定rpoB基因2.,3..
一些结核病患者含有或不受阻力的MTB生物的混合群体,这是一种称为杂收的现象4..以前的研究表明,TB杂化率的相关性高度低估4..迄今为止,已经描述了缺点,RMP,乙胺醛和链霉素。使用几个亚文化的常规药物易感性测试(DST)检测到它5.,或通过使用基于PCR的技术同时检测野生型(WT)和突变序列,例如限制片段长度多态性6.,测序7.或“线探针测定”8..
MTB的杂收被认为是初步抵抗的初步阶段。到目前为止,解决结核病杂项的机制的研究缺乏。本研究的目的是系统地分析杂收对INH和RMP的原因。基因型MTBDR检测(Hain LifeScience,Nehren,Nehren)用于鉴定乌兹别克斯坦塔什干直接观察治疗战略(DOTS)中心的TB患者的这种病例。
材料和方法
临床标本
收集了35例肺结核患者的35例,用于参加塔什干中心中心的患者。这些被送到了德国的Gauting的Supronational参考实验室(SNRL),在该市的耐药调查框架中进行DST。斯普拉包括连续的样本,于2月10日加工(1169-1185案),2月22日(1565-1579例),2006年5月15日(4070-4072例)。调查员(H.Hoffmann)处理样品并不知道患者的临床历史。所有斯普拉都是现象。它们是自发生产并在观察中收集的。
患者的临床资料和治疗史如表1所示⇓.患者的数据保持匿名。该研究在卫生部,乌兹别克斯坦卫生部道德批准。
细菌分离株
经过几次修改,sputa按照国际结核病和肺病联合会的建议进行了处理9使用净化N- 乙酰 - 半胱氨酸 - NaOH方法。接种生长检测后,剩余的沉积物用于基因型MTBDR测试。当液体培养物转阳性时,分离株是亚培养的,并且在分枝杆菌生长指标管中进行含有INH和RMP的一线药物进行DST(MGITTM值;Becton-dickinson,海德堡,德国)在BactecTM值MGIT 960孵化器(Becton-Dickinson)在制造商的协议之后。
将净化的标本或培养的细菌在100℃下灭活20分钟,然后超声处理。离心悬浮液并用于PCR的上清液。扩增和测序凯特和rpoB使用标准协议使用具有引物RPOB-F(5'-GGG AGC GGA CCC A-3')的标准协议进行的基因座,RPOB-R(5'-GCG GTA CGG CGT TTC GAT GAA C-3'),KATG-F(5'-CGG CGC ATG GCC ATG AAC GAC GTC-3')和KATG-R(5'-CCG GCA CCG GCG CCG TCC TTG-3')。
基因型MTBDR测定
基因型MTBDR测定根据制造商的推荐使用5μlDNA提取物和Taq聚合酶(Invitrogen,Karlsruhe,Germany)进行。测试检测基因突变rpoB和凯特基因并基于多重PCR,然后逆转扩增子与各自的WT和突变探针杂交。使用从Sputa提取的DNA的PCR循环适用于爆炸的优化方法等等。10..
结果
表型和基因型DST
根据常规DST,35个分离物的13(37%)是MDR(INHR,rmp.R)有10例(28%)对异烟肼(INH)耐药R,rmp.S)和12(34%)易受INH和RMP的影响(INHS,rmp.S;表2.⇓)。只有对RMP的抵抗没有抵抗力(INHS,rmp.R)。
基因型MTBDR被直接施用至净化的烟库,后来涂覆细菌培养物。当施用于培养物时,用突变检测到19个分离物(54%)凯特和14(40%)突变rpoB基因(表2⇑)。Sputa的测试结果与来自除三种病例的培养物中的那些,随后将其鉴定为氟或RMP。在四个案例中,rpob-具体的杂交信号显着较弱,产生不确定的测试结果。
缺点和/或rmp
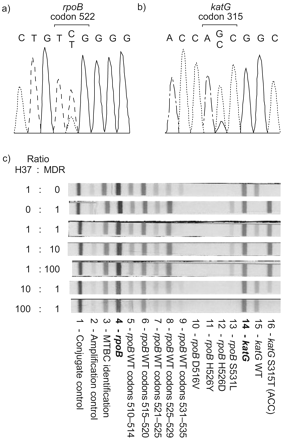
在7例(20%)中,有证据表明杂项或RMP(图1⇓)。在三种情况下抵抗INH(1171,1571和4071),凯特WT和S315T特异性杂交带同时可见。在其中两个(4071和1571)中,杂蛋白和培养物中可见,并且在一个(1171)中仅在培养后看到。
基因型MTBDR(Hain LifeScience,Nehren,German)检测到七种结核病患者的杂蛋白。基因型MTBDR直接施用于痰中,后来施用于培养物。同时检测野生型(WT)和特定突变频段凯特和/或rpoB在所有七个病例中都可见(圆圈)。如测序所示,病例1575中缺失的WT带对应于突变S522L。显示了常规药物敏感性试验(DST)的结果。RMP:利福平;异烟肼;S:易感;R:抗性;MTBC:结核分枝杆菌复杂的。
在五个案例中,rpoB杂交模式向RMP表示杂项(图1⇑); 其中一例(病例4071)同时表现出对异烟肼的异质耐药性。在1567例、4071例和4072例中,痰和培养物对RMP均表现出明显的异质耐药性。在病例1177中,痰中检测到WT带和两条突变带(S531L加H526Y),这与三种不同生物体共存的情况一致。培养后S531L特异性条带消失。在案件1575中,所有rpoB在痰中可以检测到WT信号,而在培养物中WT带3(密码子521-525)消失,表明WT被突变生物体过度生长。在所有7例对任何一种药物的异质耐药病例中,表型DST的结果与突变,即抗性,有机体。
异质电阻的验证
通过测序来确认WT和突变序列的共存rpoB和凯特PCR产物分别为所有7例(图2A⇓b)。为了检查杂交模式的再现性,重复基因型MTBDR测定并补充基因型MTBDRPLUS,并从杂管的情况下含有七种痰和培养物。结果与第一个(未显示的数据)表示一致。此外,使用基因型MTBDR对SNRL质量评估菌株的64 MTB培养物的分析未显示出杂管的病例(表3⇓). 因此,同时检测WT和突变带不太可能是由于非特异性杂交。
基因型MTBDR(Hain LifeScience,Nehren,German)的特异性试验。通过测序确认A和B)杂菌。示例测序结果显示A)野生型(WT)序列(TCG)和密码子522的突变(TTG)rpoB(案例1575)以及B)CoCon 315的WT(AGC)和突变(ACC)凯特(案件1571)。c)使用不同混合物使用不同的敏感参考菌株H37RV(对利福平(RMP)和异烟肼(INH))的不同混合物产生人造杂芳抗度,并且衍生自Suprantational参考实验室的多药(MDR)菌株(耐rmp和inh)质量评估应变收集。用基因型MTBDR测试混合物。MTBC:结核分枝杆菌复杂的。
为了评估允许同时可视化WT和突变信号所需的WT和突变生物的相对比例,使用不同的易感和抗菌细菌的不同混合物制备人造杂项,然后进行DNA提取和基因型MTBDR。WT和突变带在WT的比率为1:1,10:1和1:10的抗性菌株时同时可见(图2C⇑)。当比例为1:100或更低时,较低浓度应变的杂交信号消失。因此,基因型MTBDR似乎是检测MTB的杂机率的可靠和特异性方法,条件是生物体的相对比例≥10%。
杂硼酸盐MTB分离物的表征
区分杂项的缺点和/或RMP的发生源自不同MTB菌株的感染或用单个菌株分离成两种生物体的感染,将Miru-VNTR键入键入痰样品和培养物。在用两个菌株感染的情况下,应在痰和/或培养中检测两个不同的MTB基因型。在四种情况下(1171,1571,1575和4071),在两个或更多个位置同时检测到两个不同的等位基因(表4⇓)表明存在两种不同的基因型菌株。在1177,1567和4072的情况下,只看到单一基因型。
为了估计北京基因型的相关性杂蛋白患者,从培养物中进行了Spoligotyping。北京基因型菌株主要在亚洲和前苏联中发现15..1177,1567和4072的Spoligotyping含有对应于北京基因型的模式(图3A⇓). 病例1171、1571和4071的Spoligo模式不能归属于已知模式,但显示出强信号和弱信号的混合,与两种不同菌株的混合一致。
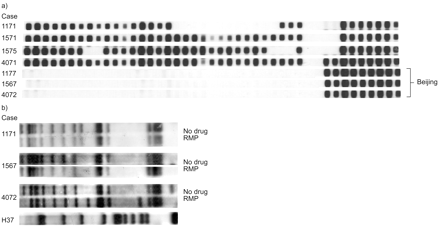
SpoliGotyping和指纹分析。a)来自杂氮患者的培养物的Spoligotyping鉴定了北京基因型的三个案例。壳体1575的Spoligo-模式对应于SpoliGotype H4。b)是6110.1177,1567和4072的指纹识别从在不存在或在利福平(RMP)存在下生长的培养物中。作为控制,是6110.显示来自菌株H37RV的指纹。
虽然Miru-VNTR键入在北京基因型的情况下表明单株菌株,但不能排除两种不同的北京基因型菌株的存在。因此,是6110.对不存在或存在RMP的培养物进行指纹图谱分析。如果感染两种北京菌株,则应从RMP上选择的耐药菌和在无药培养基中生长的混合菌中获得不同的模式。是6110.键入与菌株1177和1567的相同模式,但与菌株4072的细微差异(图3B⇑)在后面的情况下表明用两种不同的北京菌株感染。
对临床数据的评价显示,在三种情况下,TB已经新诊断,而4例患有治疗失败或复发历史(表5⇓)。生物学和临床资料的比较显示,所有“新案例”都感染了两种不同的菌株。两种单株菌株的病例是“复发”。值得注意的是,北京基因型的所有三种病例都表现出复发史,而在四个非北京案件中,三个是新的,一个经历过“治疗失败”(表5⇓)。因此,在北京基因型菌株的情况下复发或治疗失败的风险更高。
讨论
在本研究中,对来自塔什干的35名结核病患者进行了分子调查,确定了7例(20%)异质耐药病例。首次证明了两种异质抗性机制,即两种不同的结核分枝杆菌菌株共存,并将单个菌株分离为抗性和敏感性微生物。这些机制与新病例、治疗失败和复发的临床实体有关。目前的研究表明,在新病例中,两种不同菌株共存的情况普遍存在,而在治疗失败和复发时,单一菌株分离的情况普遍存在。
由具有两种不同菌株的感染引起的杂振异是通过已经感染的患者的Superfection用另一种MTB菌株的患者进行化学解释。对于三个新病例,潜在的TB感染的超级敏感似乎是最好的解释,尽管超级纤维可以触发预先存在的潜伏结核病的假设,但到目前为止从未被证明过16..相比之下,有活跃的TB患者的SuperInfection一再证明,特别是抗性北京基因型菌株17.,18.. 这一机制可以解释有复发或治疗失败史的患者因感染两种菌株而产生的异质耐药性。
高结核病发病率肯定会增加超育的风险。乌兹别克特TB医院可能是具有抗性菌株的超敏的风险部位。将在未来的研究中调查这一点,可能为感染控制从业者提供有价值的信息。
由于感染单一菌株而产生的异质耐药性很可能是由于在抗结核治疗不足的选择性压力下分离到易感和耐药的生物体。许多报告描述了由于治疗不当而导致的耐药性演变19..无效的治疗可能是由于患者的不合规,药物的药物质量差,或病原体的预先存在性。值得注意的是,由于单株菌株引起的杂动术患者都有复发历史。因此,疗法不足的阳性选择性压力可以扩增抗性生物以通过基因型MTBDR测定检测的比例。如果是这样,用单株菌株的杂项率可以作为抗结核病治疗计划质量的指标,这可能对公共卫生从业者提供帮助。
在目前的研究中,由单株菌株感染引起的杂振是仅由北京基因型菌株引起的。单一核苷酸多态性在不匹配修复基因中使北京基因型能够比其他基因型更容易获得抗性相关的突变20..这种观察和北京基因型在中亚国家的主要职位可能解释为什么在本患者组中只观察到北京基因型菌株。此外,由于北京菌株感染引起的杂项与复发史相有关。这符合先前的研究报告复发或治疗失败与越南北京基因型之间的关联21.和新加坡22..
Tb中20%的杂项的速率类似于用渣的发现等等。6.,谁报告了17%的率。其他研究报告率明显降低8.,23.,24..这种差异可能取决于几个因素。首先,TB患者组和研究现场影响杂收率。在目前的TB患者中,观察到高率的MDR-TB,40%以前的治疗失败或复发。同样,在垃圾场的研究中等等。6.,仅包括来自危险因素的患者如先前抗TB治疗的DNA样本。其次,将测定直接施用于临床标本,增强了检测杂收的可能性4.,24..第三,同时测试临床试样和细菌培养物进一步改善了杂收的检测。
总之,迄今为止,在结核病中,特别是在高度流行地区,异质耐药性是一种被低估的现象。在目前的研究中,异源耐药性主要是由不同基因的共同感染引起的结核分枝杆菌菌株,当然受到塔什干肺结核发病率的高发病率。需要进一步的患者进行更多的研究来估计流行病学和杂收的临床影响。
支持声明
在乌兹别克斯坦耐药调查框架中,通过KFW Bankengruppe(法兰克福)和全球基金对抗艾滋病,结核病和疟疾(日内瓦,瑞士)的全球基金进行药物敏感性测试。
利益陈述书
可以找到对这项研究的兴趣表www.www.qdcxjkg.com/misc/statements.shtml
致谢
目前的作者要感谢L. Slutzka(IML,Gauting,德国)和A.Van den Brandt(国家分枝杆菌参考实验室,Bilthoven,荷兰),以实现其优秀的技术援助。
- 已收到2008年6月13日。
- 认可的2008年9月23日。
- ©ers Journals Ltd