抽象
O的生物学2是极其复杂的,并违反了一个全面而简要的总结,展示了它的作用,整个动物和植物王国。在2006年意大利陶尔米纳肺科学会议(陶尔米纳)上,这篇必要的简短介绍将探讨O2只有在哺乳动物的细胞内,即使这是一项艰巨的任务。
系列“缺氧:ERS肺科学大会”
由N.韦斯曼主编
这是这个系列的第一个
传统上,生理学家考虑如何Ø2从环境到线粒体,即。运输过程和限制因素。代谢学家考虑O的作用2在能源发电通过氧化磷酸化,即。作为细胞过程的底物和调节器,包括其自身的使用。生物化学家认为,除其他外,O2作为反应性O的来源2自由基(ROS)和O两者如何2(或其缺乏)和ROS可能影响许多基因的转录。病理学家和临床医生考虑不足和过剩两个Ø影响2关于组织的结构和功能。氧气是在一个显着的,集成的系统,科学家们才刚刚开始拼凑的中心,本介绍该系列的目标是描述可能发生这种多方面的融合。
O2运输
肺
多年来,呼吸学者对氧的兴趣2主要集中在理解O2没有(或不)从空气到肺毛细血管的血液得到。Stimulated originally by wartime needs ∼60 yrs ago, several generations of researchers1- - - - - -6已经开发出了当前生理理解的O2随着新思想和新技术的出现,运输达到相当复杂的水平。目前,人们对通风、血液流动、两者的分布以及气体交换已经有了很多了解6,7。科学家已经能够确定时的气体交换的扩散限制在肺部出现,在健康和疾病8,9,并认识到肺气体交换影响组织内的气体交换反之亦然也就是说,这个系统明显地整合在整个身体里。
组织
与肺部的交换相比,很少有人注意到氧合反应是如何发生的2交付通过组织或器官的动脉血液供应不(不)到在该组织中线粒体。有趣的是,基本相同的生理屏障如在肺中潜在地阻碍ö2组织内转运:生理O的异质性2供应与办理O生化需求2;组织中的血管的红血细胞和线粒体之间扩散迁移限制;降低交付通过低血流量,血红蛋白或O-2饱和;和分流需要它周围血组织元素。这些都“内的道路”证明更难以捉摸的表征,从而了解比他们的同行肺,但慢慢地,被做成了这些过程也是如此。还有很长的路要走,特别是通过多器官衰竭标记严重疾病。已评估的一个系统是骨骼肌。这是展示集成一个有用的模式,围绕细胞氧张力牯(PO2)。
基于核磁共振光谱测量细胞质肌红蛋白饱和度10,肌红蛋白几乎完全处于静止饱和,这意味着胞质PO2必须与静脉血相当接近。然而,细胞内的PO2falls during exercise to remarkably low but stable levels of ∼0.4–0.5 kPa (3–4 mmHg), indicated by a myoglobin O2∼50%的饱和。这种低PO2,表示O之间的平衡2供应和O2需求,有许多卓越的影响和后果,并提出了如下几个问题。
1.人们应该关注这样的低点吗PO2因为缺氧(供应跟不上需求)或这是一个调节值(即。常氧),用作主要的生物的目的呢?记住线粒体能够在如此低的全速运行PO2水平11,很容易认为,一个PO20.4-0.5 kPa(3-4毫米汞柱)是运行系统所需的全部能量。事实上,更多的会造成浪费,可能会导致过量的ROS生成,因此,可能会导致细胞O2毒性。换句话说,这个系统可能被调节到一个细胞PO2of 0.4–0.5 kPa (3–4 mmHg), which is advantageous.
2.此外,这种低PO2意味着PO2从红细胞到线粒体的梯度最大,有利于O的扩散转运2, O的唯一路径2到达线粒体。然而,一个需要梯度最大化的系统表明O2从红细胞到线粒体的转运是扩散受限的,有很多证据支持最大摄氧量的概念12- - - - - -14。反过来,这意味着极大的O2利用是有限的本身的运输,而不是由能力的细胞使用O2这一点也有证据14- - - - - -16。
3.低PO2在局部血流调节中也很重要,因为局部缺氧会扩张局部组织微血管17- - - - - -19,导致流量的时间和地点的增强代谢率增大到帮助匹配ö2供应至O2所需要的。因此,很容易假设这个低PO2被调节到优化ö2交通工具。
4.下面将更详细地提到lowPO2价值观导致基因激活的系统,是上调的反应减少PO2在设计用于扩充○方式2可用性。这种情况通过缺氧诱导因子(HIF)系统20但也可能通过其他途径发生。例如,低PO2增强血管内皮生长因子(VEGF)的肌肉表达21,很可能发生(至少部分)通过HIF-1α22。随着时间的推移,这可能导致血管生成,这允许更大的血液流动,以支持更大的代谢率。我们很容易推测出肌肉,而不是低细胞内的PO2运动时,适应性基因表达(即。运动训练)可能不会发生。
总之,PO2在运动过程中,由于多种截然不同但又相互补充的原因,肌细胞的内部急剧下降2运输;2)以调节ROS产生;3)调节局部灌注,服务地方代谢需要;4)以调节至匹配ö代谢反应的速度2可用性;5)刺激适应性基因表达,增强未来锻炼。
O2纸巾:吃得太多或太少都不好
近年来,O-的研究2发生了一些戏剧性的新变化。而不是简单地担心如何2运输时,研究人员已经把注意力转向如何Ø2(特别是它的减少或过量来自改变的运输)可能会影响细胞、组织和器官的功能;O2远不止是能量产生的基底(图1⇓)。
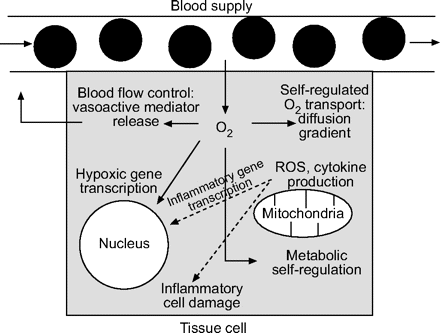
O的多重功能2在组织细胞内。虽然这个方案不太可能描述O2影响细胞结构和功能,说明了氧张力在细胞活动如运输、代谢、炎症和基因转录中的作用。ROS:活性氧。
研究人员已经知道了过量的O2引起肺Ø2毒性多年。从最初的生理描述清楚的是过量ö2导致高水平的活性氧、炎症和组织损伤。多年来人们也一直知道氧的减少2造成严重的干扰,如在心脏组织坏死,脑,四肢,内脏,等。缺氧性肺血管收缩影响肺循环,最终有助于潜在致命的疾病,如高海拔肺水肿23。研究人员已经认识到,外周组织的急性缺氧会引起血管舒张,从而代偿性地恢复O2运输和持续降低的O-2(例如在发育和出生后早期,生命会刺激一些特征性的变化,包括肺活量和血氧饱和度的增加2运输能力24- - - - - -26。此外,出生后O减少2能刺激典型的反应,其中最明显的是过度通气通过化学感受器刺激和红细胞增多通过促红细胞生成素和促红细胞生成素显然都有恢复O型血的作用2可用性。
尽管有这些恢复反应,高海拔的缺氧对身体产生了越来越极端和有害的影响。而有些人可以在没有呼吸辅助的情况下登上8848米高的珠穆朗玛峰227,尽管事实上,灵感PO2峰顶仅5.3-6.0 kPa (40-45 mmHg)28和动脉PO2is only 3.3–4.0 kPa (25–30 mm Hg)29,man cannot live and reproduce at altitudes ∼>5,000 m for more than short periods of time三十。基本上,每个器官都受到这种程度的缺氧的影响,瘦体重的减少,大脑、胃肠和生殖系统的紊乱发展到无法忍受那样的海拔高度。
即使在海平面和没有实质疾病本身,睡眠呼吸障碍产生导致被认为是不利的,对机体许多答复缺氧的水平。缺氧和复氧的周期报道引起全身炎症反应,可能通过ROS31,从而导致全身性高血压的自主神经系统的临床上重要的失调32,33而且,似乎易患代谢综合征34。
O2有关的病理生理学:机制
随着这些年来这些表型反应逐渐被分类,研究已经开始关注O2导致功能的变化,那就是机制。据了解,在许多组织中,将O高和低的水平2促进更多的ROS生成,这些ROS本身可能导致炎症、信号和基因激活。已知O的水平改变了2在许多组织中直接影响基因表达。HIF的在缺氧,恢复性反应有关的许多基因的调控的首要作用,已成为近年来的主要故事之一20。缺氧对HIF的稳定作用35它提供了足够的这种因子来引起一系列基因的转录激活,而这些基因的蛋白质起着平衡可用氧的减少的作用2,现在已经被很好地理解了。在hif调控基因中,最显著的是编码糖酵解途径酶、葡萄糖转运体、促红细胞生成素和VEGF的基因。毫无疑问,这些机制将被证明是复杂的,远比这个微不足道的描述复杂得多。
O2:它是如何被感知的
怎样的O水平2可以感测启动的诸多后果上述遗骸一个“热门话题”与各种传感器的证据4,36在线粒体水平,HIF系统内ROS可能还有其他的产生过程。有趣的是,许多Ø2-依赖的途径被更好地理解,似乎相关的反应不能单独用缺氧来完全解释。例如,它可能是那个O2-缺氧时肌肉中独立的信号通路可能参与VEGF的激活。
O2基因组:因果关系
了解这些多,变化和复杂的信号通路的细节仍然是一个重大的挑战。但是,这些都阐明,即使有将仍然存在,需要确定它们的重要性。一些已经确立无疑,但相应的基因操作战略将需要发展到肯定别人的重要性。作为一个例子,有可能讨论骨骼肌。它已经发现,VEGF确实是肌肉的主要血管生长因子。体内该基因在通过使用酶Cre-LoxP位技术条件性敲除成年小鼠的缺失表明,肌肉毛细血管的三分之二的区域消失,其中VEGF是基本上不存在37。≥8周后毛细血管未恢复,细胞凋亡明显。类似的结果也出现在终身全肌肉VEGF删除上,使用的是交叉繁殖策略,从胚胎阶段开始删除VEGF,但仅在肌肉中38。值得注意的是,这些发现表明,该基因和组织不存在足够的平行或代偿途径。用类似的方法删除肺中的VEGF也会产生重大影响39特别是细胞凋亡和类似肺气肿的表型,但这是否在人类临床肺气肿中起作用还有待确定。
总结
本迢迢介绍了2006年陶隆科学大会的目的是简要介绍一些在O3生物学研究的显着进展2在过去的世纪:从在其运输到它是如何充当信号传导分子生理利益;它是如何影响组织的结构和功能在高或低的浓度时;和可用性等的变化如何影响基因组的反应大概设计在这种情况下恢复功能。这些O的多面性2作为一个卓越的、综合的运输、利用、信号和发病机制的系统而存在。
本系列将继续讨论O的许多方面2并将引导参与者沿着新的道路在无休止的探索中了解其非常复杂的生物学。
感兴趣的语句
没有宣布。
- 收到了2007年11月19日。
- 接受2007年12月23日。
- ©ERS杂志有限公司












