抽象的
哮喘的特征在于,响应各种刺激的过度通气道,称为Airway HyperRespersive(AHR)。以前的小鼠菌株的比较表明,增加气道狭窄的速度与基线气道反应性相关。这些数据促使调查诱导AHR的模型,以查看气道缩小动力学是否相关体内响应能力。
在尝试再现哮喘的一些特征,敏化BALB / C小鼠并进行过敏原暴露的短暂或慢性期。短暂的曝光涉及与鼻内鸡蛋卵蛋白的两个挑战(OVA在).慢性暴露涉及6个为期2天的OVA期在挑战,每个挑战之间以12分隔 天。对照组小鼠接受鼻内盐水刺激。结果包括肺切片的视频显微测量(气道狭窄的大小和速度),体内呼吸生理测量和形态学分析的组织学染色。
与盐水对照相比,既不是短暂的也不是慢性过敏原暴露导致更大的气道狭窄和增加的速度。在长期攻击过敏原的小鼠中检测到呼吸道中的结构变化,例如脚酚细胞增生,龈上纤维化和增加的收缩组织。
总之,过敏原挑战后对甲素的反应性增加可能不是由于平滑肌的内在变化本身的,而是以在肺的其他变化,这最终表现为增大呼吸阻力。
哮喘是一种慢性炎症性肺病,其特征是可变气流阻塞、气道炎症和气道高反应性(AHR)。AHR是指与正常个体相比,暴露于支气管收缩激动剂(如乙酰胆碱和组胺)后气道变窄的能力增加1. 尽管正在进行的气道炎症和气道重塑被认为起主要作用,并且在过敏性哮喘的短暂动物模型中,白细胞介素(IL)-13水平的升高似乎对AHR是必要和足够的,但导致AHR的病理生理学机制仍不清楚2,3..有人提出,这些过敏介质可以直接在气道平滑肌(ASM)上行动,以增加收缩响应4.气道重塑描述了在哮喘学中观察到的气道墙的结构变化,包括ASM肥大和/或增生,气道纤维化和粘液生产增加。
ASM收缩体内既不是等距也不等渗而是auxotonic,其中ASM缩短抵抗由周围肺实质的附件施加一个增加的负载,平行的弹性元件(即。细胞外基质)和粘膜折叠。虽然我们知道等距力的测量不能完全再现体内在这种情况下,许多研究使用等长力的产生作为收缩功能的指标5- - - - - -9. 许多研究者使用等长力产生作为AHR的指标;然而,等轴测力测量目前被认为低估了气道反应性的差异。最近,气道收缩动力学,即最大狭窄和狭窄速度,被认为是AHR更相关的标志物,从而增加了气道功能障碍可能由平滑肌本身的异常引起的可能性。先前的研究已经检测了未过敏的未过敏犬的气道平滑肌动力学5,大鼠10.和老鼠6,7,11.但是,在本作者的知识,没有其他团体使用了过敏原诱发的AHR的小鼠模型来研究气道收缩力度。幼稚小鼠品系之间以前比较显示增加的气道变窄相关因素速度与气道反应性6.因此,本研究的目的是检查ASM介导的气道缩小动力学,并确定这是否可以考虑对甲素的反应性增加体内在过敏性哮喘的小鼠模型中。
材料和方法
动物
雌性BALB / C(野生型)小鼠购(哈兰斯普拉格Dawley公司,印第安纳波利斯,IN,USA)。Mice were aged 6–8 week (chronic protocol) or 10–12 week (brief protocol) and housed in environmentally controlled, specific pathogen-free conditions for 1 week prior to and for the duration of the experiments. All experimental procedures were approved by the Animal Research Ethics Board at McMaster University (Hamilton, ON, Canada), and conformed to the National Institute of Health guidelines for experimental use on animals.
敏感
如前所述,BALB/c小鼠致敏12..简单地说,小鼠在第1天和第11天接受了含硫酸铝钾的卵清蛋白(OVA)腹腔注射和鼻内OVA (OVA)在)在第11天。
曝光
对敏化的BALB / C小鼠进行短暂或慢性过敏原暴露方案。简短的协议涉及OVA的两个2天在(在25μL盐水中100μg)挑战。慢性议定书涉及六天的OVA在,每次分开12天(10周内总共12个曝光)。对照小鼠进行相同的敏化方案,但接受鼻内盐水曝光。在最终暴露于过敏原或盐水和慢性小鼠后4周进行了24小时,在最后暴露于过敏原或盐水后4周进行了24小时,对小鼠进行了24小时。在每个方案中研究了单独的小鼠(10种盐水控制,10个过敏原)(简要介绍与对照),并用薄肺切片技术进行分析。
解决方案
琼脂糖型 - VII溶液(4%(重量/体积); Sigma Chemical Corp.,St Louis,Mo,USA)在60℃下蒸馏水溶解在蒸馏水中,冷却至37℃并与2×浓度的Hanks的平衡混合盐溶液(HBSS)在37℃下给予2%琼脂糖-HBSS溶液。
肺片制备
肺切片如前所述在小鼠中制备13.稍加修改。简单地说,小鼠被CO安乐死2接着终端放血。气管露出,使用平端的19号针头,随后胸壁去除以暴露肺部插管。The lungs were inflated with ∼1.2 mL 2% agarose-HBSS solution at 37°C. To clear the airway lumen, 0.1–0.2 mL of air was injected to flush the agarose-HBSS solution out of the airways into the alveolar tissue. The lungs were rinsed with 1×concentration HBSS at 4°C and the whole mouse preparation was placed at 4°C for 15 min. The lungs were removed and placed in HBSS at 4°C for an additional 30 min to ensure the complete gelling of the agarose within the lungs. The lungs were separated into individual lobes and bathed in cold HBSS. Using a tissue slicer (model EMS-4000; Electron Microscope Sciences, Fort Washington, PA, USA), ∼120 μm thick slices from the right upper lobe were cut in HBBS at 4°C.
组织切片培养基
肺切片转移到Dulbecco's Modified Eagle's培养基(Invitrogen公司,Carlsbad, CA, USA),加入15mm 4-(2-羟乙基)-1-哌嗪乙烷磺酸缓冲液,l-谷氨酰胺和盐酸吡哆醇,补充青霉素链霉素、两性霉素B,l抗坏血酸,转铁蛋白,硒和胰岛素,然后在37℃下温育过夜。
图像采集
将肺切片置于两个玻璃盖卡瓦之间,并用一块尼龙网(CMN-300-B;小型零件,迈阿密湖,佛罗里达州,美国)放在显微镜(尼康TMD,尼康加拿大公司,米西索加,加拿大,佛罗里达州)的台上,并以100倍放大率观看。选择肺切片进行研究的前提是:1)感兴趣的气道没有琼脂糖;2) 观察纤毛搏动;3)气道上皮完整。用数字电荷耦合器件相机(CV-252;尼康),一个帧采集板和图像采集软件(视频Savant;IO工业,伦敦,安大略省,美国)。以延时方式捕获帧(用于测试帧速率影响的数据除外,该数据以1的速率执行) 每5帧 s) 对于过敏原实验方案,存储在数百帧的标记图像格式(.tif)堆栈中,并使用Scion图像分析软件(Scion Corporation,Frederick,MD,USA)进行分析。特别是,通过将大于给定亮度的所有像素定义为白色,将具有10位灰度分辨率的图像转换为二进制图像(例如透过内腔看到的背景),以及所有亮度较低的黑色(例如组织)。此外,所有连续的白色像素被确定为对象/粒子,不包括任何有界对象小于一个给定的大小(定义的用户比气道管腔面积小得多,但比任何过往的碎片),然后在任何对象(白色)像素的数量大于截止值计算。考虑到气道腔和视野内任何物体(实质/壁组织或碎片)之间的亮度差异,阈值水平的微小变化对所做的绝对测量几乎没有影响,也不会对本文所报告的相对变化产生任何影响(即。在给定记录中从开始完成的直径的变化)。
在体外气道狭窄测量
肺切片用1×concentration HBSS超压5min,以获得基线。在记录基线图像后,将1 μM乙酰胆碱连续注入肺切片制备液5分钟。伯格纳和桑德森13.已经证明这种浓度的乙酰胆碱能引起几乎最大的反应。使用Scion软件(Scion corporation),通过像素求和测量气道面积与时间的关系。截面积为17000 ~ 44000 μm2(对应于直径范围145–235 μm)。气道狭窄表示为与初始气道面积测量值相比气道面积减少的百分比。采用简单数学算法(SigmaPlot;Systat软件公司,美国加利福尼亚州里士满点),它以数字方式区分面积与时间的关系(计算内腔面积中每个点之间的斜率)与时间图)。
体内对甲胆碱反应性的测定
使用Flexivent™啮齿动物呼吸机系统(科学呼吸设备Inc.,Canada)获得呼吸生理学测量。基于总呼吸系统抵抗力的响应来测量对甲磺酰胺的反应(R.卢比)增加静脉内剂量的甲素(每组n = 10)。每只小鼠用Avertin麻醉(2,2,2-三溴乙醇;西格玛 - Aldrich Canada Ltd.,Oakville,加拿大)通过IP注射液240 mg·kg−1随后用钝的18·仪表针进行了气管造口,然后连接到Flexivent™计算机控制的小型动物呼吸机(科学呼吸设备Inc.)。动物是通风的准正弦,(150呼吸·min−1,10. mL·kg−1,在spiratory/expiratory time ratio of 66.7% and pressure limit of 30 cmH2O)。A script for the automated collection of data was then initiated, with the positive end-expiratory pressure (PEEP) level set at 2 cmH2O和小鼠默认通气。小鼠在呼吸机上稳定后,用25号针头插入颈内静脉。采用潘库溴铵(0.03 mg·kg)治疗瘫痪−1静脉注射)以防止测量过程中呼吸困难。为了提供恒定容积的病史,数据采集之前先进行6秒的总肺容量扰动(峰值振幅25 cmH2O)。在20秒后,静脉内注射盐水,然后注入10,33,100和330μg·kg−1乙酰甲胆碱(ACIC,布兰特福德,ON,加拿大)。For each dose, a maximum of 13 “QuickSnap-150” perturbations (single sinusoidal inspiration/expiration ratio of 0.4 s duration with a volume amplitude relative to weight of 10 mL·kg−1)进行〜45秒,然后通过6-S TLC后续10秒。在允许鼠标被动地过滤1 s后,每次呼吸抵抗2 cmh的正压2O.呼吸力学(R卢比和弹性电阻(E卢比))通过同时记录气道压力,使用多元线性回归来从同时记录气道压力,在肺中或流出的气流中,以将这些数据拟合到小鼠呼吸系统的以下线性单隔室模型:
P= (E卢比×V)+(R卢比×V”)+Po(1)
在哪里P是压力,Po呼气末压是否由呼气末正压(PEEP)确定,V为容积和V”流。最后一次注射完成后,将小鼠从呼吸机中取出进行进一步的组织收集。监测心频、血氧饱和度通过红外脉冲Oxymetry(Biox 3700; Ohmeda,Boulder,Co,USA)使用标准耳探针放置在鼠标后肢的近端部分上。
肺组织和形态
肺部的处理如前所述14..琼脂输注后,左叶固定在福尔马林中24小时,然后将左肺切成两半并嵌入石蜡中。用以下污渍切割和评估横截面(3μm厚):核酸Schiff,Picro-Sirius红色和α-平滑肌肌动蛋白(SMA)。
统计分析
所有数据都表示为平均值±扫描电镜n表示使用的动物数量。从每只动物的一个肺切片上只使用一个气道。组间比较采用未配对t检验,p值<0.05为显著性。
结果
短暂或慢性过敏原暴露增加BALB/c小鼠的乙酰甲胆碱反应性
为了证实过敏原暴露方案与小鼠胆碱能反应性增加有关,体内在BALB/c小鼠短暂或慢性过敏原暴露后测量呼吸功能(这些小鼠与用于肺切片实验的动物分离)。这些小鼠的最大R值显著增加卢比与相应的生理盐水对照组(n = 10;p < 0.05;图1⇓).同样的观察结果在同样处理过的小鼠中进行,使用流量阻断法测量了对乙酰胆碱的呼吸反应(数据未显示)。12..
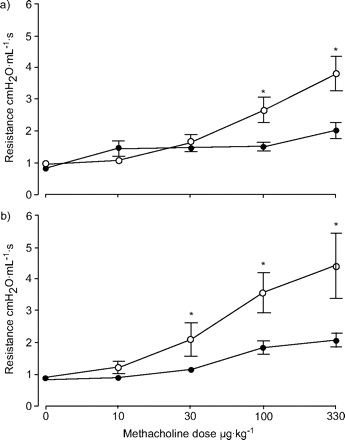
a)短暂暴露于生理盐水(•)或卵清蛋白(OVA;〇)或b)长期暴露于生理盐水(•)或OVA(〇)4周后。数据以平均值±表示扫描电镜。n =每组10个。*:与相应的对照动物相比,P <0.05。
实验技术验证
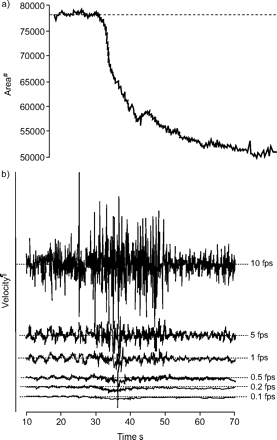
肺切片技术的几个技术方面已经得到验证:膨胀程度;琼脂糖的浓度;以及各种气道尺寸15..为了评估估计收缩速度的最佳数据采集速率,我们以每秒10帧(fps)的速度进行了一次记录,并通过选择合适的帧(例如每个第10帧获得有效的1 fps的有效视频速率)。然后分析后者以进行收缩的速度。
图形 2a⇓显示对乙酰胆碱的约束响应的10-FPS记录的一段,并且在图2B中的顶部跟踪中给出了由120-S部分的120-S部分(开始〜30s开始)的瞬时速度估计⇓.后者的噪声主要是由于肌肉抽搐引起的气道腔区从一帧到下一帧的微小变化而产生的,这是Bergner和Sanderson之前描述的一种现象13..其他可能的噪声源(<5%)可能与通过视场的碎片漂移和/或照明的细微变化有关。这种噪声可能会妨碍对气道闭合峰值速度的准确测定。
数据采集率(视频帧速率)对气道狭窄速度估计的影响。a)对乙酰胆碱的反应(10−5 M) was recorded at 10 frames perSE.电导率(fps)。b)提取一段120秒的记录片段,在胆碱能刺激开始前~ 30秒,并将其降低为不同的帧率,随后分析气道狭窄速度。#:以像素数测量;¶:1,000 pixels·s−1.
图形 2b⇑还显示了在有效视频速率为5帧/秒(仅包含其他帧)时获得的速度估计,以及更慢的有效视频速率降至0.1帧/秒(仅100帧/秒)。将视频速率降低到1或0.5 fps,大大降低了速度估计中的固有噪声,揭示了一个潜在的频率为~ 0.33 Hz的振荡,以及乙酰胆碱诱发收缩的峰值速度本身. 将有效视频速率进一步降低至0.1 fps消除了振荡,只留下收缩速度的逐时刻估计。基于此分析,0.2 选择fps作为最佳记录速率。
短暂或慢性过敏原暴露后气道狭窄动力学
为了探讨过敏原诱导的甲素反应性是否伴随着胆碱能引起的气道狭窄的更大速度和/或幅度,从BALB / C过敏原的动物和对照动物获得肺切片。在1μm使用乙酰胆碱以评估响应性,已显示该浓度基本上最大效果11.,15.,16.如图1所示⇑没有表明敏感性有变化,完全的浓度-反应关系是不必要的。
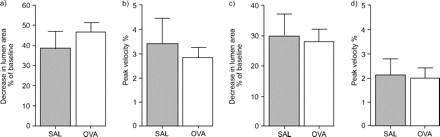
呼吸响应于1μm乙酰胆碱的气道最大缩小在暴露的小鼠和盐水对照小鼠之间没有显着差异(图3A⇓),也不是缩小差异的峰值速度(图3B⇓).同样,在慢性过敏原暴露后,既不是气道的最大缩小(图3C⇓),也没有缩小的速度(图3d⇓)对1 μM乙酰胆碱的反应差异有统计学意义(p < 0.05)。
呼吸道缩小动力学后,b)短暂过敏原暴露和c,d)慢性过敏原暴露。a,c)过敏原暴露后肺切片响应乙酰胆碱(1μm)的最大气道变窄。与盐水解小鼠相比,过敏原小鼠之间没有发现显着差异。B,D)气道响应乙酰胆碱(1μm)在过敏原暴露后鼠肺切片响应乙酰胆碱(1μm)的峰值速度。与盐水解小鼠相比,过敏原小鼠之间没有发现显着差异。数据以平均值±表示扫描电镜.SAL:生理盐水暴露小鼠;卵清蛋白暴露小鼠。
气道墙体结构的过敏原诱导变化
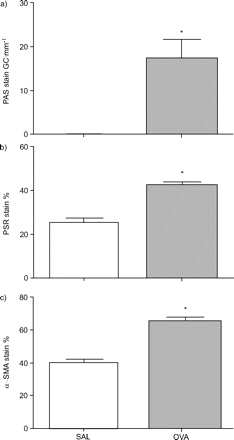
为了检查慢性过敏原暴露后Balb / C小鼠中的气道重塑索引,如前所述,通过形态学分析染色并评估石蜡包埋的切片13..含粘蛋白、周期性酸-希夫阳性杯状细胞数量显著增加(图4a)⇓),上皮下胶原沉积(图4b⇓)和α-SMA染色(图4c⇓)与慢性过敏原小鼠的气道,与盐水对照小鼠相比(P <0.05)。
小鼠慢性暴露于生理盐水(SAL)或卵清蛋白变应原(OVA)后气道形态的变化。采用形态测定法进行染色评估:a) PAS染色法测量上皮细胞中每毫米基底膜长度的含粘蛋白、周期性酸-席夫(PAS)阳性杯状细胞(GC);b)以Picrosirius red (PSR)染色百分比测定胶原蛋白;c)在上皮下20 μm区域以α-平滑肌肌动蛋白(SMA)染色百分比测量收缩成分。数据以平均值±表示扫描电镜。*:与相应的对照动物相比,P <0.05。
讨论
本作者使用两种既定的过敏原型AHR,提供了过敏原诱导的对甲素碱评估的反应性的证据体内与使用的肺组织中测量的狭窄速度或缩小的狭窄速度或大小无关体外肺片技术。
近年来,过敏原暴露的实验模型已用于哮喘的研究和与其相关的病理生理学变化。本作者的实验室表征了一系列短暂过敏原暴露的小鼠模型,导致瞬态AHR12..虽然该模型已被研究其气道反应性,气道炎症通过Bronchoalveolar灌洗(BAL)和组织切片,给作者知识,没有数据解决气道收缩动态是否在短暂过敏原暴露后改变了气道收缩动态。
目前的结果表明,在暴露于过敏原的小鼠和生理盐水对照组之间,最大变窄和峰值速度都没有差异。考虑到BAL -2型t辅助细胞因子IL-4、-5和-13的增加已经在本模型和其他过敏原暴露简短模型中报道过,两组之间没有发现差异是令人惊讶的12.,17.,18..这些发现导致了一种假设,即气道中存在的炎症介质可以影响气道收缩的动态特性,从而提供了一种可能的机制来解释体内在模型中观察到的AHR。实际上,众所周知在体外避险气道平滑肌至IL-13可以增加特异性(carbachol)和非特异性(KCl)收缩4.在本研究中,存在存在的任何炎症介质体内,容易在过夜温育期间,以及由表面灌流实验本身期间丢失。进一步的实验是必要的,以地址的细胞因子水平的改变是否与之前以下变应原激发存在于肺切片的组织。本研究的另一个限制是舒张反应并没有在这两组动物的比较。
除了描述的简短的过敏原暴露模型,主动致敏BALB/c小鼠的慢性过敏原暴露是另一个成熟的模型,包括与哮喘气道相关的几个病理特征。在目前的慢性过敏原暴露模型中,AHR在最终过敏原暴露后持续≥8周,远远超过急性炎症事件的解决14..气道的结构改变,通常称为气道重塑,可能是导致AHR持续的部分原因体内.目前的假设是这些变化也将在肺切片中的气道动态中表现出来在体外.在本研究中,在慢性过敏原暴露后4周观察到小鼠中的呼吸道重塑索引增加。具体地,在左叶中的第一代气道中观察到耻骨上胶原蛋白的沉积增加,增加的收缩组织和脚卵细胞元化。目前的研究结果与Ellis的先前研究一致et al。14.以及其他文献报道17.,19..有趣的是,在慢性过敏原暴露后,尽管BALB/c小鼠显示气道重塑指数增加,但未观察到最大变窄或峰值速度的显著增加。一种可能的解释是,鼻内过敏原输送系统可能不会将过敏原分配到小气道(直径为>200 μm)在体外学习。然而,本作者以前曾表明,结构变化存在于左叶的第一代气道,以及右叶的小气道,这表明这些变化在整个支气管树发现14..其他慢性过敏原型尚未确定下呼吸道的结构变化程度17..
对消极调查结果的替代解释体外评估气道功能可能是,小气道用来检查最大变应物引起的变窄和速度的变化,可能不会有助于评估气道功能障碍体内尽管反复接触过敏原后出现了结构变化。事实上,观察到过敏原诱导的AHR体内可能表明阻力的变化来自大气道相对于小气道。Sapienza之前就注意到了这一点et al。20.大鼠吸入乙酰胆碱后肺阻力的变化主要是由于大气道水平的变化,而不是小气道。因此,在本作者的实验室中,暴露于过敏原的小鼠的AHR报告可能也表明了大气道的阻力变化,尽管这一假设尚未得到验证。第三种可能是胶原蛋白沉积的增加可能是对过度气道狭窄的保护。这一理论得到了Palmans报告的观察结果的支持et al。21.在延长过敏原暴露的大鼠模型中。在该研究中,在连续过敏原暴露后4周后观察到伴随AHR减少的胶原沉积的增加,然后在12周暴露后进一步增加。Palmans.et al。21.理由是胶原蛋白的增加会使气道壁变硬,从而减少任何给定量的ASM缩短引起的气道狭窄。此外,平滑肌内和周围沉积的胶原增加也可能干扰平滑肌收缩,从而导致AHR降低22..
在本研究中,体内对methacholine反应性的测量是整个呼吸系统,这可能反映气道腔直径以外的腔室,包括肺实质。因此,应用于这些测量的气道反应性术语可能是不准确的,因为非气道事件可能扮演重要角色。因此,双方达成一致意见的原因之一可能是体内和体外过敏原暴露后的反应性变化是过敏原诱导的变化的重要组成部分体内通过在气道直径的真实变化之外介导的测量。这些可能包括肺实质抗性的变化23.或增加气道直径的异质性24.但在气道阻力的实际变化。虽然本作者并未在乙酰甲胆碱诱发的R进行的恰恰是增加的详细分析卢比发生在过敏原之后,在此提出的数据可能表明,增加对乙酰胆碱的反应可能不仅仅是由于气道变窄增加。
总之,一个体外应用肺切片技术评估过敏原暴露后胆碱能诱导的气道收缩动力学。虽然增加了对乙酰胆碱的反应体内,在BALB/c小鼠品系中,在短暂或慢性暴露于过敏原后,气道收缩动力学没有显示出差异。小鼠气道高反应性体内可能是在平滑肌动力学的内在变化之外的因素,并且反映了使用本发明薄肺切片技术观察到的呼吸道的变化。
支持声明
通过加拿大卫生研究院提供的研发计划赠款支持该研究
感兴趣的语句
有关这项研究的兴趣声明可在www.www.qdcxjkg.com/misc/statements.shtml
致谢
本提交人士您要感谢M. Sanderson和Y. Bai(Massachusetts Medical School大学,伍斯特,Ma,USA)的帮助,以帮助肺切片技术。
- 已收到2007年6月28日。
- 接受2007年11月6日。
- ©ers Journals Ltd