摘要
气道结构的改变,统称为气道重塑,在各种慢性肺病中导致气流阻塞。虽然组织学为气道壁重塑的结构提供了有价值的见解,但这项技术是有侵袭性的,不允许纵向分析气道壁的尺寸。计算机断层扫描技术的进步允许评估气道壁的尺寸,并非常适合于无创调查气道壁重塑的发病机制和评估新的治疗干预措施。本文的目的是回顾计算机断层扫描在调查气道的结构和功能在健康和疾病。
气道结构的改变,统称为气道重塑,导致各种肺部疾病中的气流阻塞,包括:哮喘、慢性阻塞性肺病(COPD)和囊性纤维化(CF)。气道重塑定义为气道壁的细胞和分子成分的组成、含量和组织的变化;这些变化可直接导致气道狭窄和/或夸大气道平滑肌收缩的效果。气道重塑的检测和定量一直建立在组织学检查的基础上。这些研究提供了关于气道重塑过程和后果的有价值的信息,但需要获得气道的外科或解剖样本,并且在设计上必须是横断面的。需要采用无创方法来进一步研究气道壁重塑的发病机制,评估随时间变化的变化,并评估旨在减弱或逆转这些结构变化的新的治疗干预措施。计算机断层扫描(CT)技术的进步使得评估气道壁厚度和横截面积成为可能在活的有机体内这与组织学检查相当(图。 1.⇓)。然而,可以从CT获得的信息基本上比组织学检查所获得的信息更薄。例如,CT不能区分气道壁的哪个部件增厚。尽管有这种限制,但衡量多个气道相对,不禁止和反复提供重大潜在优势的能力。目前物品的目的是审查CT在调查气道结构和健康和疾病中的功能。虽然综述了定性和定量研究,但由于其固有的优点,因此强调了定量研究,因为它们直接反映了该成像模型所基于的数字数据。
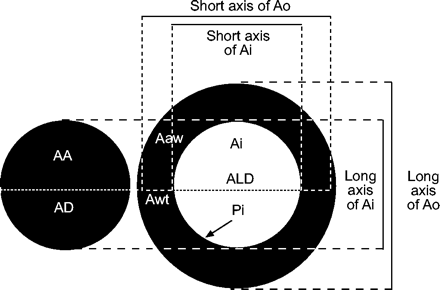
计算机断层扫描(CT)-估算气道管腔和管壁以及伴随肺动脉的尺寸。这个示意图显示了气道和血管的CT图像上的各种测量,这些图像经常伴随气道和血管。线性测量包括:气道周长(Pi);外气道区(Ao)和管腔区(Ai)的长轴和短轴;壁厚(Awt);气道管腔直径;气道外径(AoD = ALD+Awt);和动脉直径(AD)。各种线性尺寸的比值包括:ALD/AD;Awt /广告; Awt/ALD; as well as long to short axis ratios, which are a measure of the obliquity of the section. The area dimensions include: Ai; airway wall area (Aaw); outer airway area (Ao = Aaw+Ai); and arterial area (AA). Ratios of various areas include: Ai/AA; Aaw/AA; and percentage wall area (WA% = Aaw/Ao×100%). The square root of Aaw is often derived, since it is relatively linearly related to Pi. Finally, airway dimensions can be referenced to body surface area (例如Aaw / BSA和Awt / BSA)。
一般的方法
最初设计用于评估气道结构的CT扫描涉及薄层图像(通常为1-2) 使用“停止和拍摄”协议获取,并使用边缘增强算法(称为高分辨率CT(HRCT)协议)重建。通常,存在≥10 由于辐射问题和使用轴向技术获得真正连续图像的局限性,图像之间的距离为mm。大多数已发表的分析技术都是使用这些采集范式开发和验证的,除非屏气时间和辐射暴露不是一个问题,例如在对模型或模型的研究中动物。即使螺旋CT扫描仪的出现,也没有显著改变这种方法。螺旋CT扫描仪可以在手术台不断移动的同时获取图像。然而,多探测器行CT(MDCT)的引入和普及扫描仪已经完全改变了CT图像采集的方法。现在可以在单次屏气期间获取整个胸部的薄层图像,通常称为体积成像,0.5–1 mm厚的切片。此外,这些扫描仪产生真正的各向同性体素,允许图像重建,其中Z维度sion(切片厚度)与X和Y(平面内)的尺寸相同分辨率。各向同性体素使得在任何位置测量真实横截面上的气道成为可能,使用图像的回顾性重建来获得气道的横截面图像。已经开发了许多复杂的算法,允许这种角度校正和测量管壁和管腔1-4.. 因此,可以针对临床或研究问题进行研究,以最大限度地提高图像质量,同时最大限度地降低辐射剂量。容积CT还可以生成最大强度投影和最小强度投影(MIN-IPS)图像,MIN-IPS图像已被证明在检测细微肺气肿方面特别有用5..
通常在悬浮的灵感期间获得用于分析气道的图像。一些调查人员提出了使用肺活动量的门控,因为气道扩张肺部体积的增加;腔面积和壁面积与腔区域的比例随肺体积的函数而变化。此外,成像研究的目标通常是气道尺寸的比较(在个体之间或随时间的个体内的情况下),因此重要的是以相同或非常可比的肺部体积比较同一气道的图像。实验动物研究6.已经表明,气道在二螺母压力下完全扩张> 10 CMH2O、 并建议,如果做出合理的吸气努力,在不需要肺活量门控的情况下对气道进行长期比较可能是合理的。相反,病变气道的面积-压力曲线可能异常。如果这些气道的顺应性低于正常,则进行扫描时的肺容积和经肺压力可能对气道尺寸产生更重要的影响。
CT扫描的儿童和婴儿谁不能自愿屏住呼吸提出了一个重要的问题的气道分析。小于4岁的婴儿通常使用镇静剂,并在安静呼吸时进行扫描;结果图像有大量的运动伪影,一般不适合评估气道结构。为了解决这个问题,龙和同事们7.-9.开发并应用了一种称为“容积控制CT”的CT技术,在呼吸暂停期间以标准容积扫描镇静婴儿。婴儿呼吸过度,伴随胸壁扩张的低碳酸血症和海岭-布吕尔反射导致呼吸暂停,持续时间足以获取图像。
因为大多数航空公司之前进行了CT研究的多层螺旋CT扫描仪的引入,因为许多机构没有能力控制肺容积CT扫描期间,这些技术提供的更精确的理论优势尚未证明,需要进一步研究。研究人员不得不求助于其他方法来匹配气道,比如Niimi最近的一项研究等.10在一系列CT研究中,可以很容易地识别和测量大的中央气道,并在干预前后进行比较。
大型航空公司的定量评估
在使用CT测量气道尺寸的最初研究中,研究人员依靠手工追踪气道图像11-15.这些技术非常耗时,易于错误。因此,已经开发了计算机辅助和自动化技术以测量气道内腔和墙壁尺寸。第一种用于测量气道腔的这种方法使用Hounsfield单元(HU)阈值截止值。该技术涉及识别气道,并测量腔内的X射线衰减值。McNitt-gray.等.16报告称,通过包括-500 HU和King阈值以外的所有像素,可以准确测量气道腔区等.17报告阈值为−577 HU产生的误差最小。然而,最常用的测量气道管腔和管壁面积的方法依赖于“全宽半最大值”(或“半最大值”)技术。这种方法要求在管腔中放置一个种子点,并沿此点向气道壁各方向投射的射线测量x射线衰减值。当射线进入肺壁时,衰减会增加,然后随着它进入肺实质而减小。在腔面衰减到最大衰减的一半和实质面衰减到局部最小衰减的一半之间的距离被认为是壁厚(图2)⇓)18那19.虽然这种方法提供了一个标准化和无偏的测量,但它有局限性。当使用这种方法的CT扫描测量与幻影和解剖标本进行比较时19CT扫描总是高估气道壁面积而低估管腔面积。这些系统误差是由多种因素造成的,包括:CT扫描仪的空间分辨率有限;CT切片内气道的方向角;扫描仪检测边缘的能力(点扩展功能);使用的重建算法;使用的分析技术;无法观察上皮的折叠。中野等.19已经表明,半最大方法导致小支气管测量中的非常大的分数误差。出于这个原因,诸如最大似然方法之类的技术20.和得分引导侵蚀17已经开发了。
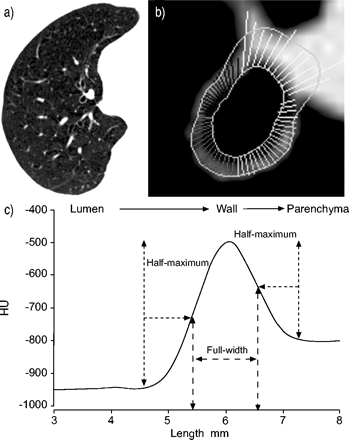
c)用半最大值全宽度算法测量气道壁。图中显示了从管腔穿过气道壁进入实质的射线的代表性x射线衰减曲线。壁的厚度是利用射线进入和离开壁时x射线衰减变化的半最大值点确定的。给出了典型的计算机断层扫描图像(A)和气道放大视图(b)。可以看到射线开始于腔壁的边界,并延伸到外缘。值得注意的是,一些射线延伸到肺动脉,因为动脉具有与气道壁相似的x射线衰减值。这些射线被手动删除,外部气道边界从剩余射线使用数学样条函数估计。胡:Hounsfield单位。
当气道被切向剖切时,由于容积平均而产生的误差尤其重要,大多数气道也是如此。国王等.17试图补偿剖面的倾斜度,方法是在测量剖面的每一侧的两个剖面上,利用同一气道的质心来定义每个气道与垂线的偏差角。萨巴等.21已开发出一种替代技术,用于测量未切割横截面的气道。这种方法需要在气道腔和壁上拟合一个椭圆,并且在校正斜切气道测量误差方面显示出巨大的潜力。这些技术声称比更常用的技术更精确,但尚未普遍应用,可能是因为所涉及的复杂算法的可用性有限。
小型航空公司的定量评估
在许多气道疾病中,气流阻塞的重要部位是小气道22-24.据报道,可以使用CT测量呼吸道流量小于0.5毫米直径的腔25.,但是,如前所述,当使用常规临床扫描参数获得数据时,气道测量有很大的误差19. 然而,中野等.26比较了不同程度气道阻塞吸烟者的CT扫描和组织学检查的气道测量。他们将组织学上测量的小气道(直径1.27 mm)的管壁面积与平均内径为3.2 mm的大气道的管壁面积百分比进行了比较,发现两者之间存在显著的相关性(R2= 0.57;P = 0.001)。这些数据表明,至少对于COPD来说,通过CT更准确地评估较大支气管的气道尺寸,可以提供小气道重塑的估计。引起小气道阻塞的病理生理过程很可能也发生在功能影响较小的大气道。
即使使用了自动气道检测,也只能在任何时间对任何个体进行有限数量的测量,因此,气道维度的异质性问题对于受试者之间和受试者内部的比较都很重要。王等.27.通过将扫描内的变化与扫描之间的变化进行比较,测量气道中的异质性。然而,本研究没有解决基线气道维度的异质性问题,这对于在临床研究中确定对气道维度的定量评估之前估计是重要的。松山等.28使用MDCT扫描仪在正常受试者身上获得的连续2mm切片,测量从中央到周围气道的气道壁尺寸。他们报告了单个扫描中气道管腔和壁尺寸的各种测量值的变化,以及从肺门到周围距离的函数。这些数据对于评估观察到的差异或变化是真实的还是仅仅在测量变化范围内是有价值的28.
另一种研究气道太小而不能用CT显示的方法是进行呼气扫描,并评估气体捕获的程度和程度(图3)⇓)。疾病中狭窄的气道异质性导致气道接近的区域肺部体积的变化,而这反过来又导致肺部密度的异质性在临时到期时扫描29-34.利用呼气的CT扫描的限制是低肺体积呼吸困难。呼气扫描的一致性可以通过肌肉门控助引,但需要进一步研究来证明这些技术在研究小型气道疾病方面的价值。
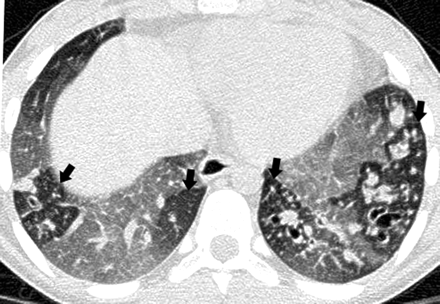
囊性纤维化患者肺基底呼气高分辨率计算机断层扫描显示双侧气陷区(箭头)。
肺衰减的异质性也存在于吸气的扫描,其中它归因于马赛克灌注。通过小气道阻塞对肺的区域的通风降低导致血管性降低和CT衰减。血流对正常肺部的再分配导致血管性和CT衰减增加。这种降低和衰减和灌注增加的这种组合称为马赛克灌注。肺灌注的区域变异可能是气道疾病的间接指标,因为气道狭窄的单位会收到较少的通风,因此将具有低区域肺泡氧气张力和缺氧血管收缩。
航空公司的定性评估
许多CT评分系统已经开发出来,可以评估气道异常的程度和分布。这些评分系统已经应用于多种疾病35-45..评分系统依赖于对气道疾病的直接和间接征象的主观检测和分级,如气道壁增厚、支气管扩张、马赛克灌注和/或气体诱骗46.-50..然而,定性研究对图像的显示设置(窗口宽度和水平)很敏感,容易出现阅读器内部和内部的变化,而且很耗时,因此也很昂贵。而对于支气管扩张和气体潴留的诊断,观察者之间有相当好的共识50.主观分析在评估气道壁增厚方面的价值非常有限。一项使用螺旋CT的研究表明,与传统HRCT相比,由于切片相邻,MDCT扫描可能改善观察者之间对支气管扩张的一致性51.,但不太可能改善气道壁厚度的主观分析。
哮喘气道成像
气道尺寸
哮喘的特征在于慢性气道炎症,气道重塑和壁厚,以及可逆的气流阻塞由于,部分,对气道平滑肌收缩61.那62..哮喘患者的CT扫描表明,支气管内腔区域的减少和增加率增加,响应各种刺激和气道壁增厚,除了马赛克灌注和喘气捕获63.-68..林奇等.65.发现77%的哮喘患者和153(36%)在哮喘患者中评估的429间支气管的患者具有内部支气管直径,肺动脉直径为1。备注,患者没有支气管直径比> 1.5。正如林奇所突出的那样等.65.,哮喘患者的支气管扩张可能部分反映了肺动脉内径的减少,由于血容量的变化或局部缺氧,或可能是生理上的;在这一患者群体中诊断轻度支气管扩张应谨慎。轻度支气管扩张的检测可能是个问题,特别是当动脉或气道腔发生变化有其他原因时,例如发生在高海拔地区(IE。缺氧血管收缩)69..
许多调查人员在正常和哮喘的受试者中比较了气道内腔区域。Beigelman-Aubry.等.70与对照前支气管扩张剂相比,在哮喘上展示了较低的基线气道内腔区域,但在沙丁胺醇后废除了差异。此外,据报道,哮喘患者在一秒钟内强迫呼气量(FEV1) < 60%(平均±sd与正常对照组(0.65±0.16)和FEV正常或轻微下降的哮喘患者(0.48±0.11)相比1值(分别为0.60±0.16和0.60±0.18)71.相反,奈米等.72与正常组相比,无论疾病严重程度如何,哮喘患者右尖上叶支气管管腔面积均未减少。
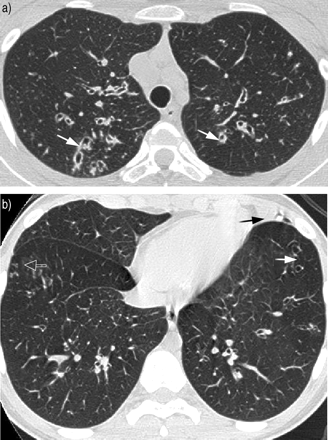
冈西加等.73使用CT扫描量化在正常和哮喘受试者中吸入甲素产生的气道狭窄程度。他们能够清楚地识别中等大小的气道的气道缩小(图4⇓)。气道缩小的模式没有区别(IE。大与与正常受试者相比,哮喘患者的气道狭窄程度相同,但正如预期的那样,哮喘患者使用的乙酰甲胆碱剂量要低得多73.哮喘患者气道腔区频率分布轻微向小气道腔方向偏移,气道壁明显增厚。
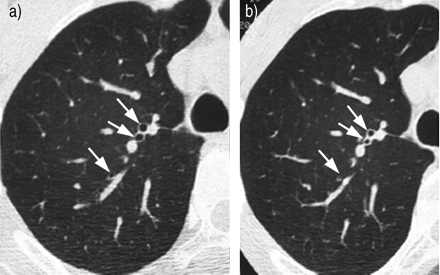
哮喘患者右上叶高分辨率ct扫描图,摄于(a)服用甲胆碱前后。吸入一剂甲胆碱后,一秒钟内强迫呼气量减少约20%的支气管直径(箭头)可以清楚地看到。
棕色的等.74在吸入乙酰甲胆碱后无法深吸气的正常受试者中,随着吸入乙酰甲胆碱浓度的增加,测量气道狭窄。他们证实了气道管腔狭窄,并且在任何可以评估的气道大小中都不倾向于更大的狭窄。戈尔丁等.75报告FEV下降更大1在哮喘内吸入甲素后的小气道的气道内腔,而不是正常的受试者。王等.27.最近的研究表明,在哮喘患者的大气道中,气道狭窄是不均匀的,而且这种不均匀性比对照受试者更大。
棕色的等.76在哮喘患者和正常人中测量的由深吸气引起的气道扩张。研究发现,深吸气在基线时将气道扩张到相当的程度,但在吸入甲胆碱后,深吸气在哮喘患者中导致支气管进一步狭窄,而在正常受试者中则导致支气管实质扩张。提示哮喘患者深吸气后支气管扩张不充分是由于哮喘受试者平滑肌对拉伸的反应异常。
所有关于成人和儿童相关研究14那34那66.那72那77-79表明哮喘患者的气道壁厚度增加,即使哮喘是轻微的。壁增厚程度与哮喘的持续时间和严重程度以及气道阻塞程度有关66.那72那77那79. 新美等.72作为疾病严重程度的函数(基线FEV,显示出哮喘的右顶线节段支气管壁的逐渐增厚1)但是,令人惊讶的是,与对照组或轻度哮喘患者相比,重度哮喘患者的气道管腔面积没有差异。有趣的是,对于一定程度的气流阻塞,与COPD患者相比,哮喘患者的右心尖支气管的气道壁要厚得多18那72.
气道壁厚度与气道反应性之间的关系是有趣的。由于气道高反应性被认为是哮喘严重程度的标志,因此可以预期,气道高反应性与气道壁厚呈正相关。计算模型研究表明,外膜、固有层和/或平滑肌层的增厚都可能导致对收缩激动剂的过度反应。事实上,Boulet等.80发现有更厚的气道的个人更响应。相比之下,很少等.66.并没有发现气道壁厚度与气道高反应性之间的关系,这在Niimi等.81谁发现,需要增加呼吸抗性所需的甲磺胺与哮喘中的气道壁厚无关。事实上,这些作者报道说,甲胆碱剂量 - 反应曲线的斜率与气道壁厚相反。这种发现可能的解释可能是,至少在一些受试者中,加强气道的过程使它们变得更加致密,因此,对诸如甲素等刺激的敏感性较小82.
奈伊等.10有报道称,右根尖段支气管的厚度,根据体表面积调整,随着哮喘确诊时间的延长而增加。他们还发现了800µg吸入倍氯米松Q.D.对于12周导致右顶末节间支气管的厚度显着降低,尽管降低没有将气道维持到年龄匹配的无症状对照组的尺寸10.
气体被困
可以在吸气扫描上看到肺衰减减少,但在呼气扫描上更加明显83.在哮喘学中,据报道,吸气CT上的低衰减区域(LAA)65.那84最可能是由细支气管梗阻引起的局部缺氧肺血管收缩继发的肺血流再分配的结果63.那85.
在呼气扫描中,气道关闭和/或排空率的区域差异可显著增强肺衰减的异质性。虽然这种“气体滞留”即使在肺功能正常的无症状个体中也很明显86在哮喘患者中明显增高,气困程度与肺功能异常有关33那34那48.那70那87.
mitsunobu.等.32表明在哮喘的恶化期间,吸气扫描上的平均肺密度降低。金素等.75显示麻醉前后气道狭窄时衰减值分布左移(低密度)。在一项双盲、随机、平行组的初步研究中,戈尔丁等.88研究了超细二丙酸倍氯米松吸入器(氢氟烷-二丙酸倍氯米松(HFA-BDP))的相对疗效;中位空气动力学直径0.8-1.2 μm)和常规的氟氯化碳制剂(CFC-BDP;对31例未行类固醇治疗的轻中度哮喘患者进行了空气动力直径中位数(3.5-4.0 μm)的研究。采用CT评价HFA-BDP和CFC-BDP对区域气陷的相对效果。治疗前分别在注射乙酰胆碱前后进行残余体积CT检查。治疗4周后,在治疗前给予相同浓度的methacholine前后重复成像。定量分析显示,HFA-BDP组的基线气体捕获量显著降低,吸入methacholine后,他们的气体捕获量比CFC-BDP组增加的少。在症状改善、肺活量测定或甲胆碱反应性方面,两组间无显著差异。结论是,HFA-BDP在治疗哮喘周围气道方面表现出更大的疗效,并且与传统的生理测试相比,功能成像CT技术更好地评估了这种效果。
另一种分析方法是通过绘制频率图来反映肺实质扩张的异质性与相邻LAA的大小。这种关系的斜率已被证明可以区分重度和轻度/中度哮喘患者,以及吸烟的哮喘患者与不吸烟者89.
未来的发展方向
哮喘患者气道尺寸的CT分析为传统的肺功能测量提供了额外的数据。尽管在图像采集和分析方法的标准化方面仍有很多工作要做,但有一些证据表明,CT可能是临床试验中更敏感的终点。由于这种常见疾病的重要问题仍有待解决,在研究环境中使用CT似乎是合理的。气道高反应性和气道壁尺寸(通过CT评估)之间的关系令人困惑,这是一个需要更多研究的主题,气道壁尺寸对气道反应性的广泛变化的贡献也需要更多的研究,这可以在正常个体中证明。在哮喘和COPD患者中,需要更多的研究将气道重塑的程度(通过组织学测量)与气道壁增厚的程度(通过CT测量)联系起来。Vignola等.90最近报道了哮喘和COPD患者的痰弹性酶和基质金属蛋白酶-9和金属蛋白酶组织抑制剂-1的比值与气道壁增厚之间的显著关系。CT气道尺寸与血液、支气管肺泡灌洗和呼气冷凝液中的炎症和修复生物标志物之间的关系是未来进一步研究的重要领域。
慢性阻塞性肺病的气道成像
慢性阻塞性肺病主要发生在吸烟者中,其定义是呼气流量异常91.COPD中的呼气流量减少与肺弹性反冲和小气道阻塞的损失的组合有关。与肺反冲损失最佳相关的病理病变是肺气肿,并且CT扫描已被广泛用于检测和量化肺气肿92-94.通过CT对气道病变的定量研究较少受到关注,但CT技术的进步使检测和量化这些患者的气道异常成为可能。导致COPD小气道阻塞的过程本质上是炎性的,其特征是细支气管壁所有层的增厚,以及气道腔内黏液的积累23.纳卡诺等.18用半最大值法测量了114例吸烟者右上叶根尖段支气管的密度和大小。94例吸烟者被阻塞(FEV)137±15%预测),20通畅(平均FEV1尽管拥有可比的吸烟历史,但仍有100±13%。纳卡诺等.18选择根尖段支气管进行测量,因为它通常是横切面,可以在CT上可靠地识别,从而可以在个体之间进行比较。他们发现,肺LAA的百分比和气道尺寸(壁厚和壁面积百分比)的变化与气流阻塞的测量独立相关。壁面积百分比与FEV有关1残余容积(RV)/总肺活量(TLC),但与肺扩散容量无关,而LAA的百分比与FEV有关1%, FEV1/FVC,以及扩散能力。有趣的是,壁面积百分比的增加与壁面积的增加和管腔面积的减少有关,这与哮喘患者形成对比,哮喘患者同一支气管壁面积百分比的增加仅与管腔面积保留的壁面积增加有关72.一些受阻的吸烟者只有壁面积的百分比增加,而其他障碍物只有增加的LAA百分比,有些人占墙面积和LAA的百分比增加。这些数据表明,个体COPD患者可能具有肺气肿或气道壁重塑作为其主要表型,并且这些表型可以通过使用CT扫描来分离。Coxson等.95测量了所有横截面的气道,并报告了一大组阻塞指数患者及其吸烟兄弟姐妹的类似结果,此外,观察到气道和实质表型表现出家族一致性,表明发生肺气肿或气道疾病的易感性是可遗传的。最近,奥兰迪等.96发现具有慢性支气管炎的COPD患者具有增加的气道壁增厚,与没有慢性支气管炎的患者更严重阻塞的患者相比。相反,没有慢性支气管炎的COPD患者在肺衰减中具有更大的显着降低。建议慢性支气管炎的COPD患者具有更严重的气道重塑,而没有慢性支气管炎的人具有更严重的肺气肿。
节段性支气管的气道尺寸与气流阻塞的测量有关,这一事实令人惊讶,因为长期以来人们一直认为COPD中气道狭窄的主要部位是内径< 2mm的膜性气道。中野最近的研究等.26可以解释这个结果;我们发现,较大气道的壁面积百分比(CT可以清楚识别并准确测量)与同一患者组织学测量的细支气管壁面积显著相关。这个结果支持了Tiddens的观察等.97,他发现软骨气道壁增厚与气流阻塞和小气道炎症有关,并提出类似的过程影响易感COPD患者的大气道和小气道。可通过CT评估的大气道增厚和狭窄,可作为治疗慢性阻塞性肺病的替代措施抗小气道炎症过程。在COPD中分离气道主要病理和实质主要病理的能力可能被证明有助于应用旨在预防或改善气道重塑或实质破坏的特定疗法。事实上,可以想象,针对其中一个过程的特异性疗法是可行的ses可能在其他过程占主导地位的个体中禁用。
囊性纤维化的气道成像
CF的气道疾病以粘液堵塞、慢性感染和过度炎症反应为特征,导致生命最初几个月的外周气道改变101-119.典型的气道异常是支气管扩张、气道壁增厚和粘液堵塞97那103那107那120-126,如图5所示⇓.
a、 b)肺功能正常的囊性纤维化(CF)患儿的计算机断层扫描(CT)显示广泛的气道异常。CF患者为15岁白人女性,1秒用力呼气量(FEV)1)预测,强制生命能力(FVC)110%PREV,强制呼气流量为81%(FEV)1/ FVC 76%。CT图像显示支气管扩张,支气管壁或厚或薄(白色箭头),舌部空气支气管征肺不张(黑色箭头),外周黏液堵塞(张开箭头)。上下叶也可见花叶灌注。
定性研究
定性CT研究从1989年开始进行,HRCT气道评分系统是评估CF气道异常最常用的方法35那37那59.那60.那99那100那102那105那127-153..所有系统都包括一个综合评分,用于主观评估CT扫描的一些特征,包括支气管扩张、气道壁增厚、粘液堵塞、,等.德容等.37比较Bhalla评分和四种改进评分系统的重现性,发现所有评分系统在观察者之间和观察者内部都具有重现性,大多数类间r值> .8。对单个组件评分的观察者之间和观察者内部的可变性没有很好的记录。布罗迪128研究表明,支气管扩张、黏液堵塞和空气滞留的一致性分别为74%、89%和61%,而de Jong等.37报告的κ值范围为0.40-0.61,适用于大多数功能。
在一些测量肺结构和功能之间关系的研究中,强迫呼气流量测量和HRCT评分系统之间有很强的相关性37那99那138那146.那147.,除了对很小的儿童的研究128那134那143.两项纵向研究的结果表明,HRCT评分在检测CF疾病进展方面可能比肺功能更敏感;在这两项研究中,肺功能测试(PFT)在2年内保持稳定 HRCT评分检测到疾病恶化36那130. 这并不是一个意外的结果,因为HRCT可以检测到局部异常,如功能上无症状的小面积肺不张和支气管扩张。以HRCT评分为终点进行了一些小型临床试验,其中一些试验未能证明有显著的治疗效果;然而,重复扫描之间的时间间隔很短132那137那140.那153.那154..
定量研究
迄今为止,未进行研究,其中患有CF患者的病理措施已经与呼吸道疾病的定量CT估计进行了比较。气道尺寸的定量评估表明,与对照相比,CF婴幼儿中的气道壁厚度和腔面积(支气管扩张)增加了。在CF婴儿中,随着年龄的增长,气道腔(支气管扩张的严重程度)的扩张增加25..在横断面研究中,de Jong等.37没有发现气道尺寸的定量测量与pft之间的相关性。在一项纵向研究中,在基线和间隔2年之后获得CT扫描和pct,气道壁厚度增加,但腔区面积没有增加;气道壁厚度的增加与强迫呼气中流量(FEF)的减少有相关性25 - 75)%pred60.. 气体捕获被认为是CF气道疾病的早期标志物150.. 在两项研究中,通过比较吸气CT扫描和呼气CT扫描的各个像素的HU分布曲线来评估气体潴留的严重程度30.那155..该测量方法可区分CF患者和对照受试者,并与RV/TLC和FEF显著相关25 - 75%pred.30.那155..
未来的发展方向
CF中的大多数HRCT研究已经使用半定量评分系统进行。除了固有的内部和观察者间变异外,这些评分系统的主要限制是缺乏在哪些系统使用的共识以及未能始终使用CT异常的定义。由于肺长增长导致的气道大小的变化以及由于粘液堵塞而导致随后的扫描,或缺乏可比较的CT部分,因此儿童呼吸道尺寸的定量研究是具有挑战性的。此外,还有关于与辐射相关的风险的真正担忧。随着CF患者的寿命增加,这些风险可能会超过早期诊断的潜在益处。
尽管存在这些问题,但越来越多的证据表明,CT可以检测到婴儿和儿童的气道结构损伤,这些婴儿和儿童年龄太小,无法接受常规PFT和/或肺功能正常。这些早期变化也可能是可逆的,因此,应在结构损伤导致不可逆转的症状之前进行治疗有越来越多的证据表明,早期和积极的治疗可以改善CF患者的生活质量和寿命102那156.-160.因此,可以对常规常规CT扫描进行合理的情况以检测气道疾病的最早指示。最终,只有随机临床试验只会回答有关常规CT扫描是否有常规CT扫描的问题。为了促进这种研究,需要一种稳健的定量技术来测量呼吸道疾病的方法,以便与已建立的CT评分系统一起使用或代替。在寻找疾病进展的早期生物标志物中,将CT与其他非肺功能障碍措施进行比较,例如氦气和硫化硫化物冲洗通风曲线是有用的161.那162.,或正电子发射断层摄影测量肺炎症的强度163..最后,需要更多的调查进入与不同CT扫描协议相关的辐射危险,以允许开发产生具有最低风险的最有益信息的协议。
评估气道的其他成像技术
许多新技术已经被开发出来,可以在不存在电离辐射相关风险的情况下对气道和/或气道狭窄的后果进行成像。支气管内超声是通过将超声探头引入气道来完成的通过纤维支气管镜,这项技术的优点是可以测量不同气道壁层的厚度164..在一个静脉受试者的一个案例研究中,抗炎治疗后,中央气道水肿的逆转165..
超极化气体磁共振成像(MRI)技术的出现为肺通气的研究开辟了全新的途径166.以及气道尺寸的测量。使用这种技术,可以对第七代气道进行气道腔的三维重建167..然而,气道壁厚度无法量化,而且超极化氦或氙-129源的有限可用性使这种方法的广泛应用存在问题167..在不久的将来,超极化气体核磁共振可能仍将是一种有限的研究工具。
结论
计算机断层扫描扫描是对对阻塞性气道疾病的理解作出重大贡献。计算断层摄影扫描技术的改进以及更快的定量算法来测量气道墙和内腔区域以及量化和定位空气捕获,并在研究努力中的频率增加,了解慢性阻塞性肺病中发生的气道的变化。现在可以获得具有各向同性体素和标准化体积的计算机断层摄影图像,允许对特定气道的纵向研究在活的有机体内. 定量计算机断层扫描已经使人们更好地了解正常人气道尺寸的变化,更好地了解哮喘、慢性阻塞性肺疾病和囊性纤维化患者的气道变化。通过这些改进,定量计算机断层扫描已准备好用于临床应用,最初用于临床试验,但最终用于个体患者的临床管理。气道的计算机断层成像具有固有的局限性:气道壁的细分无法可视化,导致气道壁变化的病理过程无法理解,气道<0.5 内腔直径mm无法直接显示。此外,计算机断层扫描的辐射剂量限制了其在纵向研究中的应用,特别是在婴儿和儿童中。然而,计算机断层扫描是唯一容易获得的、相对无创的成像方式,允许测量气道壁和管腔尺寸在活的有机体内. 随着人们对气道重塑在这些疾病功能恶化中所起作用的认识不断提高,计算机断层扫描将在研究和临床评估中发挥越来越大的作用。
- 收到2005年1月19日。
- 公认2005年3月25日。
- ©ERS期刊有限公司