摘要
支气管上皮细胞在气道宿主防御中起着重要作用,干扰素(IFN)-γ通过调节支气管上皮细胞中各种基因的表达来控制免疫反应。信号转导和转录激活因子1(STAT1)是IFN-γ信号传导的关键转录因子。维甲酸诱导基因-I(RIG-I)是DExH盒蛋白家族的成员,被认为是RNA解旋酶。RNA解旋酶在基因表达和细胞功能的调节中发挥着多种作用,RIG-I与抗病毒反应有关。
本研究的目的是在来源于人支气管上皮细胞BEAS-2B的细胞系中研究IFN-γ对RIG-I表达的影响。
在BEAS-2B细胞中发现对IFN-γ有反应的RIG-I的诱导。在另一种肺上皮细胞系NCI-H292中也证实了IFN-γ对RIG-I的诱导作用。用RIG-I互补DNA转染BEAS-2B细胞导致STAT1的上调。在过度表达RIG-I的细胞中,IFN-γ对IFN-γ诱导蛋白10的诱导作用增强。
提示维甲酸诱导基因-I可能在γ-干扰素诱导的支气管上皮细胞免疫反应的调节中起重要作用。
支气管上皮细胞通过产生多种炎症反应的因子,在宿主防御微生物感染中发挥重要作用1.. 肿瘤坏死因子-α、干扰素(IFN)-γ和白细胞介素(IL)-4等细胞因子作为支气管上皮细胞的激动剂,参与炎症性肺病的发病机制。IFN-γ通过调节各种基因的表达发挥多效性作用。在支气管上皮细胞中,IFN-γ诱导IFN-γ诱导蛋白10(IP-10)的表达2.单核细胞趋化蛋白(MCP)-13.,细胞间粘附分子-14., c-Met/肝细胞生长因子受体5.,fractalkine6.,p117.和eotaxin8..已知这些IFN-γ刺激基因的表达是通过Janus激酶(JAK) 1/2/信号传感器和转录激活因子1 (STAT1)的信号通路介导的。9.IFN-γ也可刺激STAT1的表达10.
维甲酸诱导基因-I(RIG-I)是DExH盒蛋白家族的成员,在其N端有两个半胱天冬氨酸募集结构域(CARDs)和一个C端螺旋酶结构域。RIG-I被认为是一种假定的螺旋酶,在天然抗病毒反应中发挥重要作用11IFN-γ是抗病毒反应的关键细胞因子,此前已有研究表明IFN-γ诱导血管平滑肌细胞表达RIG-I12,膀胱上皮细胞13和MCF-7乳腺癌细胞14然而,RIG-I生物学功能的细节尚不清楚,也没有关于RIG-I在支气管上皮细胞中表达的信息。
本研究旨在探讨IFN-γ对人支气管上皮细胞BEAS-2B中RIG-I表达的影响。
材料和方法
细胞
BEAS-2B细胞,一种来源于人支气管上皮细胞的细胞系15如前所述,使用Dulbecco改良的Eagle培养基(美国加利福尼亚州卡尔斯巴德市InVitrogen)进行培养,并添加10%胎牛血清(FBS)(InVitrogen)16.NCI-H292肺上皮细胞17采用含10%胎牛血清的RPMI 1640 (InVitrogen)培养。细胞与重组人(rh) IFN-γ (Roche Diagnostics, Mannheim, Germany)或rhIL-4 (R&D Systems, Minneapolis, MN, USA)孵育在指定的时间内。JAK2, JAK3和表皮生长因子受体自磷酸化α-氰基-(3,4-二羟基)-的选择性抑制剂预处理的效果N-benzylcinnamide (AG490;Calbiochem, La Jolla, CA, USA)。根据另一种肺上皮细胞的报告进行预处理18:将AG490溶解在二甲基亚砜中,在IFN-γ刺激前,用50 μM AG490预孵育30分钟。AG490及其载体对细胞活力无影响。
逆转录聚合酶链反应
使用RNEASY总RNA分离试剂盒(德国希尔登Qiagen)从细胞中分离总RNA。第一条链互补DNA(cDNA)由1 使用Moloney小鼠白血病病毒逆转录酶和引物寡核苷酸(dT)的μg总RNA12 - 18(都是在体内)。使用PCR扩增RIG-I、STAT1、IP-10、MCP-1、eotaxin和甘油醛-3-磷酸脱氢酶的cDNATaqDNA聚合酶(Qiagen)。引物序列(由Greiner Japan、Atsugi、Japan定制合成)、退火温度和产品尺寸如表所示 1.⇓.巢式PCR法扩增Eotaxin cDNA:第一轮PCR用Eotaxin正(F)和反(R)引物F1和R1进行,第二轮PCR用Eotaxin引物F2和R2对第一轮产物1:20稀释2 μL进行扩增。产物经1.0-2.0%琼脂糖凝胶电泳分析,溴化乙锭染色。
蛋白质印迹分析
用20 mM冷PBS (pH 7.4)洗涤细胞2次,用Laemmli裂解缓冲液裂解细胞。细胞裂解液在6-9% (RIG-I)或4-20% (STAT1)梯度聚丙烯酰胺凝胶上进行电泳。将蛋白转移到聚偏二氟乙烯膜上,用兔抗RIG-I抗血清(1:20 000稀释)、山萝卜过氧化物酶标记的抗兔免疫球蛋白G (Kirkegaard Perry, Gaithersburg, MD, USA)和Supersignal West Pico化学发光底物(Pierce, Rockford, IL, USA)检测RIG-I。19如前所述,使用针对STAT1和pSTAT1的兔抗体(均为细胞信号技术,美国马萨诸塞州贝弗利市)对STAT1和磷酸化STAT1(pSTAT1)进行蛋白质印迹20.
RIG-I互补DNA转染
为了研究RIG-I在BEAS-2B细胞中表达的生物学效应,用编码全长RIG-I(RIG-I(full);氨基酸1-925)或RIG-I的缺失突变体RIG-I(N)(氨基酸1-284)的cDNA转染细胞,该突变体缺乏C-末端,仅编码CARD(“ΔRIG-I”)11)和RIG-I (C)(218-925氨基酸),后者缺乏n端,仅编码解旋酶结构域。在6孔板中50-80%汇合的细胞中转染cDNA (400 ng·well)−1.),用Effectene转染试剂(Qiagen)孵育24小时。为了评估转染的效率,以类似的方式将编码绿色荧光蛋白(GFP)的cDNA转染细胞。约70%的细胞有绿色荧光蛋白表达。转染细胞用5 ng·mL处理−1.分别孵育6 h和24 h后收集IFN-γ、细胞RNA和蛋白。RT-PCR和Western blot分析如上所述。在整个实验过程中,90%以上的细胞都能存活,单独转染试剂对细胞存活率没有影响。
在NCI-H292细胞上进行了转染实验;而瞬时转染GFP cDNA的效率小于10%。
IP-10酶联免疫吸附试验
转染RIG-I(完整)cDNA的细胞用5 ng·mL−1.IFN-γ治疗24小时 h、 收集条件培养基。使用ELISA试剂盒(研发系统)测量条件培养基中的IP-10水平。
结果
RIG-I在IFN-γ刺激的BEAS-2B细胞中被诱导
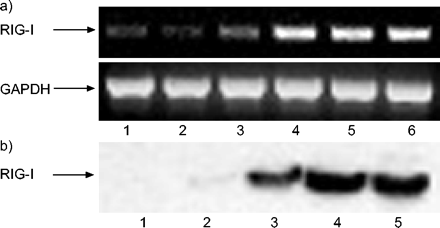
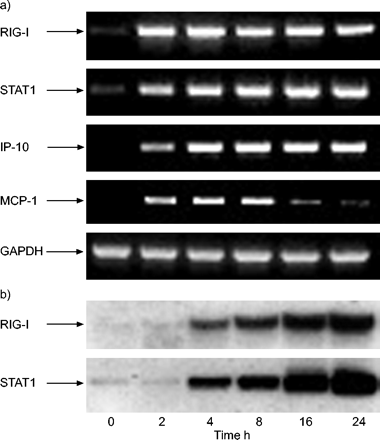
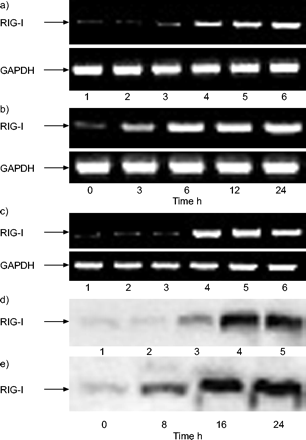
IFN-γ刺激BEAS-2B细胞表达RIG-I(图。 1b⇓)和相应的mRNA(图1a⇓)以浓度依赖的方式。RIG-I mRNA表达的时间过程如图所示 2a⇓.用5 ng·mL−1.IFN-γ在2 ~ 4 h达到最大值。IFN-γ也能诱导STAT1、IP-10和MCP-1 mRNA的表达。图2 b⇓显示IFN-γ诱导RIG-I的时间依赖性;蛋白表达滞后于mRNA表达数小时。STAT1也被IFN-γ上调。从培养基中去除胎牛血清对RIG-I的表达没有影响(数据未显示)。
干扰素(IFN)-γ诱导BEAS-2B细胞中维甲酸诱导基因-I(RIG-I)及其相应mRNA的表达。a) BEAS-2B细胞与5,4,4,4,4,4,4,4,4,4,4,4,4,4,4,5,4,4,4,5,4,4,5,4,4,4,4,5 pg·mL−1.-50 ng·毫升−1.干扰素-γ(车道1:0) pg·mL−1.;通道2:5 pg·mL−1.; 第三跑道:50 pg·mL−1.;4道:500 pg·mL−1.;第五道:5 ng·mL−1.;车道6:50 ng·mL−1.) 4 h,提取细胞总RNA。1 μg总RNA合成单链互补DNA,对RIG-I和GAPDH mRNA进行RT-PCR分析。b)用5 pg·mL刺激细胞−1.-50 ng·毫升−1.干扰素-γ(车道1:0) pg·mL−1.; 第二跑道:50 pg·mL−1.; 第3车道:500 pg·mL−1.; 泳道4:5 ng·mL−1.;第五道:50 ng·mL−1.)24小时 H然后裂解细胞并进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,将蛋白质转移到聚偏二氟乙烯膜上。RIG-I,分子质量为101 使用兔抗RIG-I抗血清和辣根过氧化物酶标记的抗兔免疫球蛋白G检测kDa。
干扰素(IFN)-γ在BEAS-2B细胞中以时间依赖性方式上调维甲酸诱导基因-I(RIG-I)和相应mRNA的表达 ng·mL−1.IFN-γ最多可用于24小时 Ha) 提取RNA并对RIG-I、信号转导子和转录激活子1(STAT1)、IFN-γ诱导蛋白10(IP-10)、单核细胞趋化蛋白(MCP)-1和甘油醛-3-磷酸脱氢酶(GAPDH)进行RT-PCR分析。b) 制备细胞裂解物并进行RIG-I和STAT1的蛋白质印迹分析。
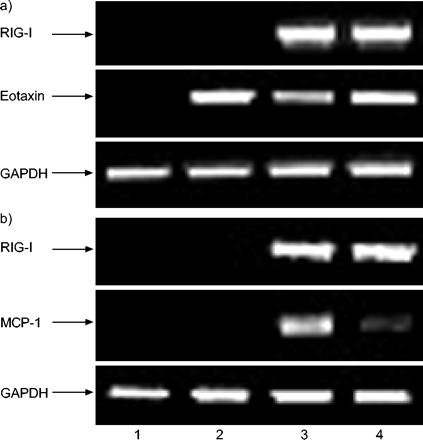
IL-4对RIG-I mRNA表达的影响见图3a⇓.IL-4诱导eotaxin mRNA的表达,但不影响RIG-I对IFN-γ的反应。用JAK2/3抑制剂AG490预处理细胞可部分抑制IFN-γ诱导的MCP-1 mRNA的表达,但对RIG-I的表达无影响(图。 3b⇓).
白介素(IL)-4和α-氰-(3,4-二羟基)-的作用N-苄基肉桂酸(AG490)对干扰素(IFN)-γ诱导维甲酸诱导基因(RIG-I) mRNA表达的影响a) 5 ng·mL共处理细胞−1.IFN-γ(泳道3和4)和5 ng·mL−1.IL-4 (lanes 2和lanes 4)处理4 h,提取RNA。对RIG-I、eotaxin和甘油醛-3-磷酸脱氢酶(GAPDH)进行RT-PCR检测。b)用50 μM AG490(第2和第4通道)预处理30 min,再用5 ng·mL处理−1.IFN-γ(第3和第4车道)治疗4个月 H从细胞中提取RNA,并对RIG-I、单核细胞趋化蛋白(MCP)-1和GAPDH进行RT-PCR。
RIG-I过表达增强STAT1表达
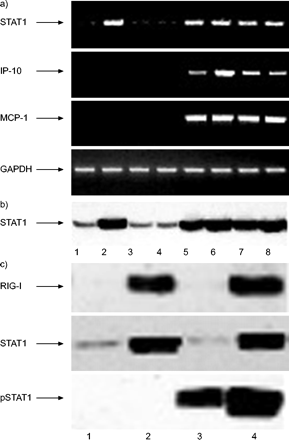
RIG-I过度表达对其他IFN-γ诱导基因表达的影响如图所示 4a⇓.RIG-I (full) cDNA转染细胞后,STAT1 mRNA表达增强,但IFN-γ诱导的STAT1上调不受影响。相反,转染RIG-I (full) cDNA未诱导IP-10 mRNA的表达,但IFN-γ诱导的IP-10 mRNA表达增强。RIG-I过表达不影响MCP-1 mRNA的表达。在转染RIG-I(完整)cDNA的细胞中,STAT1的上调被证实(图4b)⇓).转染cDNA编码缺失突变体的细胞对STAT1、IP-10和MCP-1 mrna的表达无影响。在转染RIG-I cDNA的细胞中证实了RIG-I的表达(图4c)⇓).
维甲酸诱导基因i (RIG-I)过表达对BEAS-2B细胞中其他干扰素(IFN)-γ诱导基因及信号传感器和转录激活因子1 (STAT1)表达的影响cDNA编码全长RIG-I (RIG-I (full);将缺失突变体(RIG-I(N) (lanes 3和7)或RIG-I(C) (lanes 4和8))转染至BEAS-2B细胞,24 h后,用5 ng·mL处理细胞−1.IFN-γ(通道5-8)(通道1和5:转染对照)。a)在进一步培养6小时后 h、 提取RNA并对STAT1、IFN-γ诱导蛋白10(IP-10)、单核细胞趋化蛋白(MCP)-1和甘油醛-3-磷酸脱氢酶(GAPDH)进行RT-PCR分析。b)进一步培养24小时后制备细胞裂解物,并对STAT1进行Western blot分析。c) 转染RIG-I(完整)cDNA(通道2和4)的细胞用IFN-γ(通道3和4)刺激15分钟 min和lysed。对裂解物进行RIG-I、STAT1和磷酸化STAT1(pSTAT1)的蛋白质印迹分析。
接下来,检测RIG-I对pSTAT1水平的影响(图4c)⇑).单独转染RIG-I(完整)cDNA不会诱导STAT1的磷酸化,但在过度表达RIG-I的细胞中,IFN-γ处理后pSTAT1的水平增加。
RIG-I转染对IP-10产生的影响
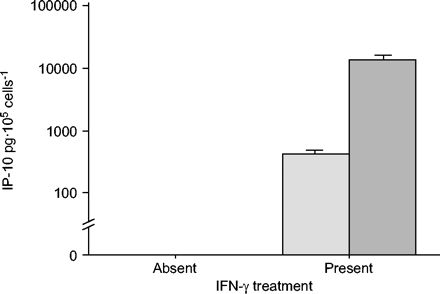
单独转染RIG-I cDNA不会诱导IP-10的表达,但在转染RIG-I cDNA的细胞中,IFN-γ诱导的IP-10分泌显著增加(图。 5.⇓).
维甲酸诱导基因-i (RIG-I)对IFN-γ处理BEAS-2B细胞产生干扰素-γ-诱导蛋白10 (IP-10)的影响用全长RIG-I互补DNA ( )(烧嘴:转染控制)。24 h后,细胞洗两次,在含5 ng·mL的新鲜培养基中再孵育24 h−1.IFN-γ。收集条件培养基并进行IP-10 ELISA。数据以平均值±表示sd(n = 3)。请注意,IP-10的浓度是以对数标度表示的。
)(烧嘴:转染控制)。24 h后,细胞洗两次,在含5 ng·mL的新鲜培养基中再孵育24 h−1.IFN-γ。收集条件培养基并进行IP-10 ELISA。数据以平均值±表示sd(n = 3)。请注意,IP-10的浓度是以对数标度表示的。
IFN-γ诱导NCI-H292细胞表达RIG-I
RIG-I mRNA在NCI-H292细胞中表达的RT-PCR分析结果如图6a-c所示⇓.IFN-γ以浓度和时间依赖性的方式诱导RIG-I mRNA的表达。IL-4和AG490均不影响IFN-γ诱导的RIG-I mRNA的表达。通过Western blot分析,IFN-γ诱导的RIG-I表达也在NCI-H292细胞中得到证实(图。 6d⇓以及(e)。
维甲酸诱导基因-I(RIG-I)在干扰素(IFN)-γ处理的NCI-H292细胞中的表达。以与图中所述类似的方式用IFN-γ处理NCI-H292细胞 1.⇑–⇑3.⇑.提取RNA,对RIG-I和甘油醛-3-磷酸脱氢酶(GAPDH)进行RT-PCR分析−1.;通道2:5 pg·mL−1.; 第三跑道:50 pg·mL−1.;4道:500 pg·mL−1.;第五道:5 ng·mL−1.;车道6:50 ng·mL−1.); RIG-imrna的时间依赖性表达;和c)白细胞介素(IL)-4(通道2和通道5)或α-氰基-(3,4-二羟基)的作用-N-苄基肉桂酰胺(AG490) (lanes 3和6)(lanes 1-3:没有IFN-γ;车道4 - 6:干扰素-γ)。d, e)对细胞裂解液进行RIG-I蛋白印迹。RIG-I诱导浓度依赖(泳道1:0 pg·mL−1.; 第二跑道:50 pg·mL−1.; 第3车道:500 pg·mL−1.; 泳道4:5 ng·mL−1.;第五道:50 ng·mL−1.) (d)和时间依赖性(e)。
讨论
t淋巴细胞通过分泌不同的细胞因子在调节免疫反应中发挥着核心作用。t辅助细胞(Th) 1型被认为参与细胞介导的免疫,Th2型被认为参与过敏反应;Th1/Th2平衡在各种病理条件下可能是重要的。IFN-γ是一种强大的细胞因子,具有多种功能,包括抗病毒和免疫调节活性,其主要来源是Th1。IL-4是由Th2表达的主要细胞因子。在支气管上皮细胞中,Th1细胞因子IFN-γ在抗病原体的免疫反应中被认为是重要的,Th2细胞因子在哮喘等过敏性疾病中发挥作用。此外,临床支气管炎症常与Th1和Th2反应的联合或不平衡有关。因此,研究和比较IFN-γ和IL-4对支气管上皮细胞功能的影响十分重要。本研究发现IFN-γ上调BEAS-2B和NCI-H292支气管上皮细胞中RIG-I的表达。相反,IL-4不诱导RIG-I表达,也不影响IFN-γ诱导的RIG-I表达。 The induction of eotaxin mRNA8.对IFN-γ和/或IL-4的反应在平行实验中得到了证实。这些结果表明RIG-I介导了IFN-γ诱导的支气管上皮细胞的免疫或炎症反应。IFN-γ激活JAK1和/或JAK2,随后是转录因子STAT1的磷酸化。用JAK2/3特异性抑制剂AG490预处理细胞,可以部分抑制IFN-γ诱导的MCP-1 mRNA的表达,但不影响RIG-I mRNA的表达;JAK2可能不参与对IFN-γ反应的RIG-I表达。
RIG-I在早幼粒细胞白血病细胞系中由维甲酸诱导21在脂多糖刺激的血管内皮细胞中19.在T24膀胱上皮细胞中发现了环氧合酶-2的表达,以响应RIG-I过表达19和IFN-γ刺激的基因15在MCF-7乳腺癌细胞中14.用RIG-I(完整)cDNA转染BEAS-2B细胞导致STAT1和相应mRNA的诱导。由于RIG-I cDNA转染不影响MCP-1 mRNA的表达,每个IFN-γ诱导基因都受到RIG-I的差异调节。
STAT1是IFN-γ信号转导的关键中介。在IFN-γ刺激的细胞中,JAK1和/或JAK2通过酪氨酸磷酸化激活STAT1。而激活的STAT1则作为一个转录因子,直接调控控制细胞反应的关键蛋白的表达22.除STAT1磷酸化状态外,调控STAT1表达的机制可能在控制细胞反应中发挥重要作用。有报道称,转录因子锌指结合蛋白89是STAT1构成性表达所必需的23,干扰素调节因子1在STAT1 mRNA的诱导中起重要作用10.目前的研究结果表明RIG-I可能是STAT1表达调控的新成员,参与IFN-γ信号通路。
IP-10是CXC趋化因子家族的成员,在激活t细胞的招募中发挥重要作用。在BEAS-2B细胞中,IP-10的表达是由IFN-γ诱导的,正如之前在其他类型细胞中报道的那样24.RIG-I cDNA转染可增强IFN-γ诱导的IP-10表达,RIG-I可能参与IFN-γ诱导的IP-10表达。然而,单独转染RIG-I cDNA并不能诱导IP-10的表达。因此,RIG-I和IP-10的表达并不是由简单的因果关系调控的,RIG-I可能参与了IP-10诱导的放大机制。RIG-I引起的STAT1表达增强导致IFN-γ刺激后pSTAT1水平升高。这可能至少部分解释了IFN-γ在转染RIG-I cDNA的细胞中诱导IP-10表达增强的原因。然而,尽管pSTAT1水平升高,但RIG-I过表达并没有改变MCP-1 mRNA的表达。这表明IFN-γ对IP-10和MCP-1表达有不同的调节机制。
RIG-I是DExH box家族的一员25在n端有两个卡,在c端有一个解旋酶结构域。DExH box蛋白参与了与核酸代谢相关的各种生物学过程,如转录、pre-mRNA剪接、核糖体生物发生、RNA转运、RNA干扰和RNA降解等26. 研究了缺失N端或C端突变体的效应。用编码这些突变体的cDNA转染细胞对STAT1的表达没有影响,STAT1是由RIG-I(完整)的过度表达诱导的。这表明CARD和螺旋酶结构域在STAT1的诱导中都是必需的。RIG-I的过度表达并不能增加pSTAT1水平,RIG-I对STAT1的诱导与STAT1磷酸化无关。RIG-I诱导STAT1表达的机制细节尚不清楚,应在未来的研究中阐明。
BEAS-2B细胞是通过引入病毒H-ras15,具有与原发支气管上皮细胞十分相似的特征。BEAS-2B和初级支气管上皮细胞对各种病原体和刺激表现出相似的反应谱27–30. BEAS-2B细胞表现出与原代支气管上皮细胞几乎相同的细胞内信号系统2.,29. 在NCI-H292(另一种来源于呼吸道上皮细胞的细胞系)中也观察到IFN-γ诱导的RIG-I表达。RIG-I可能参与气道上皮细胞的Th1型反应,应在动物模型和临床样本中检测RIG-I在气道炎症和相关疾病中的作用。
可以得出结论,干扰素-γ在BEAS-2B人支气管上皮细胞中诱导维甲酸诱导基因-I的表达,维甲酸诱导基因-I可能参与信号转导子和转录激活子1以及干扰素-γ诱导蛋白10的表达。维甲酸诱导基因-I可能至少部分参与干扰素-γ在支气管上皮细胞免疫和炎症反应中诱导的细胞反应。
致谢
作者要感谢S.M. Prescott,G.A. Zimmerman(犹他大学,盐湖城,UT,美国)和T.M. McIntyre(克利夫兰诊所基金会,克利夫兰,OH,美国)的批判性讨论,K. Munakata(弘前大学,弘前,日本)的技术帮助。
- 收到了2004年9月1日。
- 认可的2005年2月9日。
- ©ERS期刊有限公司