摘要
呼吸系统直接暴露在低水平的脂多糖(LPS)中,脂多糖是空气微粒上的一种污染物。在囊性纤维化中,主要的数据确定了气道上皮的结构改变,以及紧密连接扩张。本研究旨在确定肌球蛋白轻链激酶在LPS诱导的大鼠肺炎症反应中维持气道上皮屏障完整性的作用。
评估选择性肌球蛋白轻链激酶抑制剂5-碘萘-1-磺酰高哌嗪(ML-7)的作用:1)对肺炎症和气道上皮屏障通透性改变的影响假单胞菌铜绿假单胞菌; 和2)肌球蛋白轻链磷酸化形式的水平,在人类气道上皮细胞系(NCI-H292)和暴露于LPS后的气管组织中增加。
结果表明,LPS增加了气道上皮屏障肺膜渗透性和肺炎,并用ML-7预处理抑制了两种影响。ML-7的这种效果与NCI-H292细胞和气管组织中的磷酸化肌蛋白轻链的抑制相关。
数据,使用获得在活的有机体内和在体外方法,证明了肺炎肌菌素轻链激酶在肺炎中的关键作用,并表明肌素轻链激酶可能是用于缓解肺损伤的新药的潜在靶标。
在肺部,两个不同的上皮,气道和内皮(毛细血管)彼此恰当地邻接,构成了侵袭生物和有毒物质的连续障碍。气道上皮包括外部环境与肺部内部环境之间的界面,并且代表了可吸入分子,病毒和空气过敏原的第一次接触。平静的通道,通常由紧密结(TJ)密封,其是在上皮细胞的顶点形成邻接环的蛋白质的大分子组件1,为低水平的脂多糖(LPS)和抗原渗透提供了一条潜在途径,这些抗原作为污染物普遍存在于空气颗粒上。同样,在肠道中,上皮细胞控制过敏原、毒素和细菌从管腔到粘膜的通道。事实上,胃肠道TJ是阻止管腔化合物细胞旁通道的结构屏障1,TJ的破坏允许增加可能促进粘膜损伤的正常排除物质的上皮渗透。肌球蛋白轻链(MLC)磷酸化参与肠上皮细胞中TJ的调节。因此,在用肠致原性定植后发生MLC磷酸化大肠杆菌2和顶端细胞骨架的重组,以及TJ通透性的增加与这种磷酸化平行发生3..
最近已经鉴定了内皮细胞(EC)层的功能障碍在肺损伤或急性呼吸窘迫综合征的病理生理学中发挥了枢轴作用,这由与EC屏障功能障碍相关的轻度至严重肺部损伤的连续体组成4..内皮通透性增加可能是细胞因子释放、中性粒细胞与内皮细胞相互作用和细胞骨架改变的结果5..最近,在体外和在活的有机体内研究已经将涉及蛋白激酶的各种EC信号转导途径与EC屏障功能的生理机制联系起来6.那7..在体外通过直接磷酸化状态和细胞内细胞骨骼收缩循环的直接磷酸化状态,研究在调节EC屏障渗透率中具有暗集的MLC激酶(MLCK)和RHO激酶6..磷酸化诱导MLC的构象变化,使肌动蛋白 - 肌球蛋白相互作用和细胞收缩能够8..凝血酶和组胺等介质增加钙2+/calmodulin-dependent MLCK活性,可使MLC的苏氨酸18和丝氨酸19磷酸化9..一种细菌毒素,如LPS,可诱导MLC磷酸酶失活和增加MLC磷酸化通过ρ/ρ激酶激活5..在活的有机体内使用210-KDA MLCK的研究(MLCK210也被称为EC MLCK,因为其在ECS中的丰度)敲除小鼠说明了MLCK活性的抑制可以防止急性肺损伤7..
健康肺肺泡的上皮内层为蛋白质的传递提供了主要的屏障,>占亲水性溶质传递总阻力的90%。健康肺上皮对细胞旁溶质运输的低渗透性也是由于TJs的存在。值得注意的是,大血清蛋白(例如白蛋白、免疫球蛋白G和聚合免疫球蛋白A)通过Paracellular路线在正常肺泡上皮横跨正常肺泡上的净吸收或分泌中起着微不足道的作用。在病理条件下,由于炎症损伤由于炎症损伤而损害的病理条件,这些大蛋白质的锥虫泄漏占主导地位10.几项研究已经调查了气道上皮TJ在慢性疾病发展中的作用11那12.囊性纤维化患者进行了关于患病气道和TJ超微结构之间的相关性的研究13.这些研究确定了囊性纤维化患者的交联超微结构的差异,这些变化可能由于具有与该疾病相关的高度炎症而导致的因炎症而发生。最近,Coyne.等.14证明claudin物种负责赋予溶质通过正常人类气道组织的气道TJs的选择性流动。然而,整合有关蛋白激酶,特别是MLCK参与气道上皮通透性屏障功能的知识,直到现在还没有被认为是一个治疗靶点。
为了确定MLCK对气道上皮屏障(AEB)完整性的贡献,选择性MLCK抑制剂(5-碘萘-1-磺酰-同哌嗪(ML-7))的影响7.那15那16对LPS诱导的肺炎症和选择性AEB通透性的影响假单胞菌铜绿假单胞菌是评估在活的有机体内在老鼠身上。第二,它得到了证实在体外通过免疫印迹实验,使用原代支气管组织和人气道上皮细胞系(NCI-H292)与LPS孵育,发现MLCK是一个相关的特异性靶点大肠杆菌以及是否预先接触过ML-7。
材料和方法
在活的有机体内研究
动物护理
所有程序均按照国家农艺研究所(法国图卢兹)当地动物护理和使用委员会的相关建议进行。
手术准备
使用戊巴比妥(60 mg·Kg体重)麻醉雄性Wistar大鼠(200-225g)-1腹膜内)和麻醉以稍后的一半保持其中2小时。通过气管切开术插入配备有小导管(聚乙烯,直径0.3mm)的气管插管。
肺泡灌注剂的准备
用于实验使用LPS铜绿假单胞菌(S10;Sigma-Aldrich, l'Isle d'Abeau Chesnes,法国)或载体(无菌0.9% NaCl),在磷酸盐缓冲盐水中制备了含有5%牛血清白蛋白的等渗溶液。溶液通过0.2 μm过滤器(Nalge, Rochester, NY, USA)和0.5 μCi碘125标记的人血清白蛋白([125将白蛋白)加入到牛血清白蛋白溶液中。然后是lps铜绿假单胞菌(1μg·老鼠-1)或以恒定速率为10μl·min的恒定速率在滴注到气管之前,将载体加入滴注中-115分钟。气管输注后四小时[125白蛋白标记的肺泡灌注加LPS,测定血浆、肺空间(通过支气管肺泡灌洗(BAL))和总肺组织。在没有[125白蛋白测定BAL液中白细胞和单个白细胞的数量。
气道上皮屏障渗透率
为了评估肺通透性,大鼠每天预处理两次,持续2小时 使用选择性MLCK抑制剂ML-7(Sigma-Aldrich;在第3天首次腹腔内给药 mg·kg体重-1和连续施用1毫克·kg体重-1)或车辆(0.2 mL 10%乙醇)。最后一次给药是在气管内输注LPS前1小时铜绿假单胞菌.LPS输注4小时后,按照Pittet的描述测量上皮通透性等.17做了一些调整。评估气道上皮屏障(AEB)的通透性需要测量残留[125I]白蛋白,空气空间蛋白示踪剂,在肺中,以及[125血浆中的白蛋白。
输注LPS后四小时铜绿假单胞菌, 剩余的 [125测定BAL液、灌洗后肺组织及血浆白蛋白含量。等离子体(125测定腹主动脉血标本中的白蛋白水平。血浆分数是通过血浆体积(0.07体重(1 -红细胞压积))乘以计数得到的。所有这些残余计数(BAL液、肺组织和血浆)均表示为[125一] 气管内注射白蛋白(100%)。
细胞计数和肺髓过氧化物酶活性
在用ML-7或载体预先处理的大鼠肿瘤内输注LPS后4小时进行BAL和MECOPEROXID酶(MPO)活性测定。使用Neubauer室血液血度计计算总细胞数。使用Cytospin(Shandon,Cergy-Pontoise,France)制备BAL流体细胞的涂片,并用May-Grünwald染色染色,以检查不同的白色细胞类型。
Bradley说,肺灌洗后,在肺碎片(右上叶)中测定MPO酶的活性,MPO是多形核中性粒细胞原代颗粒的标记物等.18.使用商业改性的洛数法试剂盒测定蛋白质浓度,并且MPO活性以每克蛋白质的MPO活性为单位。
在体外研究
组织提取物
在15、30 min和1、2、3、4 h后,LPS铜绿假单胞菌-或载体灌注大鼠,无论是否预先处理ML-7,放血并收集气管远端和初级支气管组织。组织片段悬浮在RNA/DNA/蛋白质分离试剂(Tri试剂;Euromedex, Mundolsheim,法国),并使用Polytron均质器(Dremel, Breda,荷兰)在冰上均质。提取蛋白并溶于1%十二烷基硫酸钠(SDS)中进行Western免疫印迹。
细胞培养
NCI-H292人气道上皮细胞(美国弗吉尼亚州马纳萨斯市美国型培养物收集中心)在补充有2 嗯L.谷氨酰胺,100 U·毫升-1青霉素、100μg·毫升-1链霉素和10%胎牛血清(all Gibco Europe Ltd, Uxbridge, UK)。细胞生长在含有5% CO的完全湿润的空气中2在37°C时,每周转移两次。它们在5倍10升的六孔板中播种5.细胞·井-1.融合细胞在含0.1%牛血清白蛋白的RPMI 1640培养基中培养过夜。用不含血清的RPMI 1640培养基冲洗,先暴露于ML-7(0.5、10和50 μM)或载体,再暴露于LPS大肠杆菌(SO55: B5;Sigma-Aldrich 2μg·毫升-1)或15和30的车辆 最小值和1、2、3和6 H对于Western印迹,使用放射免疫沉淀缓冲液(含1%Triton X-100(法国梅兰罗氏诊断公司),150)裂解细胞 毫米氯化钠,1 mM-乙二胺四乙酸(EDTA)和10 mM-三(羟甲基)氨基甲烷(tris)(pH 7.4)、蛋白酶(罗氏诊断)和磷酸酶(西格玛-奥尔德里奇抑制剂鸡尾酒)。
Western Blotting.
通过免疫印迹,在输注LPS后,通过免疫印迹检测磷酸化的MLC(P-MLC)和20-KDA MLC(MLC-20)的形式,在大鼠气管组织提取物和NCI-H292细胞中铜绿假单胞菌或大肠杆菌分别在指示的曝光时间之后。通过15%凝胶中的Sds-聚丙烯酰胺凝胶电泳分离蛋白质,在含有25mM Tris(pH8.3),192mM甘氨酸和20%甲醇的缓冲液中,电泳转移到硝酸纤维素膜上。使用在1:100稀释或单克隆小鼠抗霉菌中的多克隆山羊抗人P-MLC抗体在1:500稀释中进行免疫印迹。将过氧化物酶标记的蛋白G(1:10,000)和蛋白La(1:20,000)用作P-MLC和MLC-20检测的二抗。使用ECL(增强化学发光)试剂(Pierce Biotechnology,Inc.,Rockford,IL,USA),通过荧光引起的免疫标具有免疫标签带。
透射电子显微镜
LPS铜绿假单胞菌或载体气管内注入4组大鼠,4组大鼠均经或未经ML-7预处理。4小时后,大鼠放血,取气管远端。标本在2%多聚甲醛/2.5%戊二醛中固定,在1%四氧化锇中后固定,用梯度乙醇溶液脱水,包埋在Epon-Araldite中。用醋酸铀酰和柠檬酸铅染色后,用HU11C日立透射电镜(Hitachi High-Technologies, Maidenhead, UK)观察超薄切片。定量分析纤毛细胞间TJs的连接扩张频率。观察人员对实验组的切片(每只大鼠4片)视而不见。每次治疗共检查30例TJs,以百分比表示TJs显示扩张的比例。
数据分析
所有数据均以平均值±表示SEM..使用方差分析进行治疗之间的比较,然后对未配对数据进行Tukey的多重比较检验。p<0.05,差异有统计学意义。
结果
在活的有机体内研究
气道肺通透性
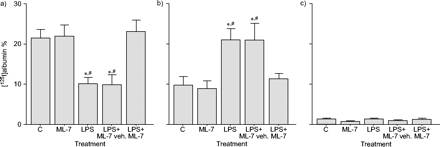
气管内注射LPS铜绿假单胞菌增强气道上皮旁细胞对大分子的渗透性,自百分率125与对照组相比,lps处理的大鼠肺组织中我收集到的肺组织中增加了(129%)(p<0.05)。相比之下125与对照组相比,LPS动物BAL液中的I显著降低(54%)(p<0.05),证实了白蛋白从空气空间到肺组织的通道增加。相反,LPS不能改变血浆中的放射性水平。ML-7预处理可降低(75%)LPS诱导的肺上皮通透性增加(p<0.05)。与此同时,ML-7也恢复了125从LPS处理的大鼠的BAL流体中的I水平对控制值(图1⇓).ML-7无影响本身观察气道通透性。
5-碘萘-1-磺基-同哌嗪(ML-7)对气道上皮旁细胞通透性的影响[125I]白蛋白回收4小时脂多糖(LPS)暴露于a)支气管肺泡灌洗(bal)液,b)肺和c)血浆。数据显示为平均值±SEM.(n = 10)。LPS显著增加了气道通透性,因为[125i] BAL流体中的白蛋白水平降低,但在肺组织中增加。用ML-7预处理预处理[125i] BAL流体和肺部的白蛋白水平与对照中检测到的人(C)。等离子体中没有发现放射性。车辆.:车辆。*:P <0.05与C;#: p < 0.05与LPS + ML-7。
肺炎
细胞计数
气管内注射LPS后4小时,BAL液中白细胞总数增加了6倍铜绿假单胞菌(p<0.05)。同样,lps处理大鼠BAL液中巨噬细胞、中性粒细胞和淋巴细胞数量显著增加。与对照组相比,ML-7预处理降低了所有白细胞数量,中性粒细胞减少了65% (p<0.05;表1⇓).
肺髓氧基酶活性
lps组大鼠肺组织中MPO活性是对照组的1.5倍(p<0.05)。ML-7预处理可抑制LPS诱导的肺MPO活性升高(图2)⇓).ML-7无影响本身发现MPO活性(数据未显示)。
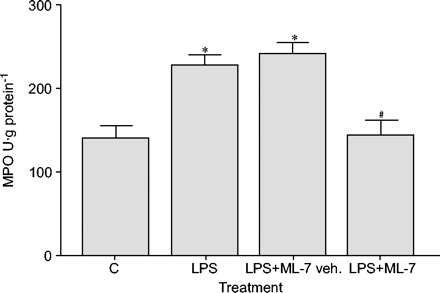
5-碘萘-1-磺酰-同哌嗪(ML-7)对脂多糖(LPS)暴露后肺中性粒细胞浸润的预防作用数据显示为平均值±SEM.(n = 10)。用ML-7预处理显着降低了髓氧化酶(MPO)活性的LPS诱导的增强。C:控制;车辆.:车辆。*:P <0.05与C;#: p < 0.05与有限合伙人。
在体外研究
组织中提取免疫印迹
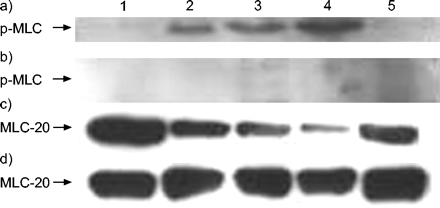
原发性支气管组织的免疫印迹显示,在输注LPS后,p-MLC呈时间依赖性增加铜绿假单胞菌.磷酸化快速开始,在LP输注后30分钟观察到最大程度。用ML-7预处理显着降低了单独的LPS后在原发性支气管组织中观察到的P-MLC水平(图3⇓).如在细胞免疫印迹中观察到的(图4⇓),在LPS输注后观察到相应的时间依赖性MLC-20下降。大鼠经ML-7预处理后,所有时间点的MLC-20水平均恢复(数据未显示)。
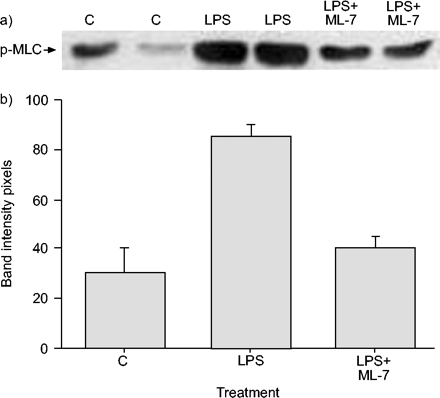
免疫印迹显示在大鼠支气管组织外植体的脂多糖(LPS)暴露后5-碘萘-1-磺酰基 - 酸碱(ML-7)30分钟的磷酸化肌蛋白轻链(P-MLC)水平的降低30分钟:a)Western印迹和B.)相应的乐队强度。数据显示为平均值±SEM..气管组织中p-MLC水平增加;ML-7预处理降低了这种效果。C:控制。
免疫印迹显示B)在NCI中通过5-碘萘-1-磺酰基 - 均外哌嗪(ML-7)和C,D)20-KDA MLC(MLC-20)水平降低磷酸化的肌球蛋白轻链(P-MLC)水平-H292在各种时间点(1:0 min; 2:30分钟; 3:1 h; 4:2 H; 5:3 h)从脂多糖(LPS)接触后大肠杆菌,A,C)没有B,D),具有50μmML-7预处理。a)在LPS曝光后2小时获得最大p-MLC水平。与ML-7剂量依赖性降低的P-MLC水平预孵育(参见表2),在50μm处具有最大效果,在50μm处未检测到浓度p-mlc。
细胞免疫印迹
在NCI-H292细胞中,在暴露于LPS后,P-MLC水平以时间依赖的方式增加大肠杆菌(图。 4a⇑). p-MLC出现在30 LPS暴露后2分钟达到最高水平 h(图。 4a⇑). 30天后观察到MLC-20水平同时降低 最小,最大影响2 LPS暴露后h(图。 4c⇑).ML-7浓度依赖性预培养(0.5-50 μM)可降低NCI-H292细胞中的p-MLC水平(表2)⇓).当细胞与ML-7 (50 μM)预孵育时,LPS暴露后的任何时间点均未检测到MLC磷酸化(图4b)⇑).同样地,在ML-7预处理NCI-H292细胞后,MLC-20水平没有变化(图4d)⇑).用另一种人支气管上皮细胞系(A549;数据未显示)观察到类似的结果。
透射电子显微镜
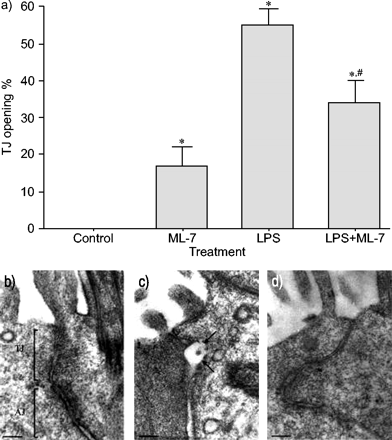
在对照组大鼠中,纤毛细胞之间观察到的所有TJ均完好无损。相比之下,4 LPS暴露h后,开放性TJs数量显著增加(53%;p<0.05与控制)。ML-7预处理显著降低了41% (p<0.05;图5⇓).
气管组织超薄切片的透射电子显微镜。a) 4小时后纤毛细胞之间紧密连接(TJ)打开的百分比在活的有机体内气管内灌注脂多糖(LPS)或对照剂。数据显示为平均值±SEM.(n = 30 tjs)。注意用5-碘萘-1-磺酰基 - 酸嗪(ML-7)预处理后TJ开口的减少。B-D)纤毛细胞之间TJ区域的显微照片:B)具有正常TJ和粘附结的控制细胞(AJ);c)细胞4小时暴露于LPS(注意TJ中的结构变形(扩张)(参见箭头));和D)来自LPS处理的大鼠的细胞,用ML-7预处理(注意TJ区域未在结构上受到影响)。秤条= 100nm。*:P <0.05与控制;#: p < 0.05与有限合伙人。
讨论
目前的结果首次证明了气道上皮细胞旁通透性在调节肺炎症反应对LPS的关键作用。此外,肌动蛋白-肌球蛋白环收缩和上皮细胞MLCK在AEB应对气道病原体的有效性中发挥了关键作用。事实上,选择性MLCK抑制剂ML-7完全抑制了气管内LPS灌注导致的AEB通透性增强和肺部炎症。
ML-7作用于MLCK活性中心的三磷酸腺苷结合位点7.那15那16,平衡解离常数(K.一世~ 300 nM,对其他激酶(>20 μM)亲和力低。在本研究中,在活的有机体内ML-7的剂量是根据在大鼠中进行的生物责任研究获得的数据选择的。静脉滴注后(1 mg·kg体重)-1),ML-7在150 ng·mL达到峰值-1在血浆中,半时间为30分钟,2-4小时后未检测到。此外,在最近公布的研究中,作者使用两次每日施用ML-7,在2mg·kg体重-1腹腔注射4小时 天19.
LPS普遍存在于空气中颗粒上的污染物,包括空气污染,有机粉尘和香烟烟雾20.. 局部暴露于LPS与肺部产生细胞因子有关,导致中性粒细胞浸润和肺损伤。在本研究中,在局部气管内暴露于1.5%的氧气后,评估肺通透性的变化 μg·大鼠-1铜绿假单胞菌有限合伙人。这是因为,每吸1根烟就会向肺部输送~ 0.2 μg的LPS20..
为了评价AEB的渗透率,Pittet之前描述了一种技术等.17是使用。这种技术可以检测肺的三个组成腔室的通透性变化,IE。空气、肺和血管组织,当动物暴露于病原体如LPS时。目前的结果表明,气管内滴注LPS可导致AEB细胞旁通透性增加,这一点可以通过显著增加[125一] 肺组织白蛋白浓度。同时,观察到明显的炎症反应,其特征是中性粒细胞流入BAL液和肺组织,如BAL液中所有类型的细胞数量增加和肺中MPO水平增加所示。但是在这个早期的时间点上,,IE。4小时在LPS暴露后,血管渗透性没有变化,同意先前的研究表明气溶病铜绿假单胞菌-衍生LPS以时间依赖性方式增加兔气道上皮细胞旁通透性(4-8) 吸入LPS后h)在早期阶段没有血管通透性变化21.参与肺损伤和肺水肿的炎症细胞包括巨噬细胞和中性粒细胞,其释放炎症介质,包括蛋白酶,氧自由基和细胞因子。然而,中性粒细胞在肺病发病机制中的作用仍然是辩论的主题。此外,只有很少的数据涉及移除的肺泡中性粒细胞在肺泡毛细血管膜损伤中的直接作用。肺泡毛细血管壁渗透性的主要因素是上皮而不是内皮屏障22.因此,已经证明中性粒细胞穿过肺泡毛细血管壁的迁移并不一定会对这一屏障造成严重损害23.然而,如果在迁移过程中没有发生伤害,病变似乎是由迁移后肺泡空间中的中性粒细胞释放的有毒产品引起的。与本声明一致,穆利根等.24证明肺泡灌注中性粒细胞蛋白酶抑制剂(分泌性白细胞蛋白酶抑制剂)对急性肺损伤大鼠模型是有益的。最近,昂等.25在气管内6小时后,BAL液中气道中性粒细胞迁移增加了5倍,但对血管通透性没有影响大肠杆菌政府在老鼠身上。
所有这些数据表明上皮细胞泄漏是免疫细胞腔积累的关键因素。选择性MLCK抑制剂ML-7降低了菌落肺细胞间渗透性和嗜中性粒细胞渗透到BAL流体和肺组织中的LPS诱导的增加,证明了MLCK在肺中炎症反应期间控制AEB渗透性的关键作用。强调这种观察结果,得到的结果在体外通过Western immunoblotting和透射电镜对人上皮细胞系(NCI-H292)和大鼠初级支气管组织进行了研究,清楚地说明了ML-7对MLCK的抑制作用。事实上,在NCI-H292或大鼠组织暴露于LPS后,p-MLC水平增加大肠杆菌或铜绿假单胞菌, 分别。通过ML-7预处理抑制p-MLC的这种增加在体外和在活的有机体内.
有什么可能的机制可以解释这种内毒素诱导的气道上皮渗透性增加通过MLCK刺激吗?
全身暴露于内毒素(LPS)导致大量炎症介质的释放,包括单核细胞/巨噬细胞和粒细胞释放的炎症介质。有两种蛋白质在刺激这些髓样细胞中非常重要:lps结合蛋白(LBP),一种血浆蛋白26CD14是巨噬细胞和粒细胞的膜蛋白27.有趣的是,血清中也存在可溶性形式的CD14(SCD14)28.研究表明,LPS对几种上皮样细胞系的激活依赖于sCD14, sCD14与LPS结合,形成LPS - sCD14复合物29.然而,目前不清楚LPS-SCD14复合物激活哪些受体,并且这些假想受体刺激了哪些第二信使。因此,LPS在气道上皮细胞中直接激活MLCK的信号通路仍有待研究,并且迄今为止,迄今为止,文献中的主要细胞内途径导致MLC磷酸化通过ρ激酶激活。推测异质三聚G蛋白偶联受体可以通过Rho鸟嘌呤核苷酸交换因子1激活Rho, Rho是鸟嘌呤三磷酸酶激活G蛋白的蛋白α.Rho的亚单位和核苷酸交换因子30..最近,有人提出异三聚体G蛋白参与cd14依赖的LPS信号通路31.此外,假设Rho介导了肌凝蛋白磷酸酶的失活,在MLCK活性存在的情况下有利于MLC磷酸化32.LPS对上皮细胞通透性的作用也可能是继发于炎症介质的释放,炎症介质可刺激肌醇1,4,5-三磷酸,调动钙2+从细胞内储存,从而增加细胞内钙2+浓度。高水平的细胞内钙2+激活钙2+/calmodulin-dependent MLCK,可磷酸化MLC的苏氨酸18和丝氨酸19残基,诱导MLC的构象变化。这些变化使肌动蛋白和肌球蛋白相互作用并激活Mg2+肌凝蛋白- atp酶活性33.无论上游机制如何,这里都证明了LPS激活MLCK,因为ML-7的选择性抑制显著减弱了LPS诱导的支气管组织和上皮细胞中的MLC磷酸化。
内毒素效应的替代机制可以是通过肺泡巨噬细胞介导的间接作用。实际上,有很好的记录,巨噬细胞的激活取决于内毒素与LPS结合蛋白的相互作用,然后与巨噬细胞的CD14受体特异性结合27. 在LPS刺激下,肺泡巨噬细胞释放多种细胞因子,如肿瘤坏死因子-α(TNF-α)和白细胞介素-134.TNF-α在肌动蛋白重排中发挥积极作用,这可能与MLCK激活有关,进而增加血管屏障功能障碍35.最近,结果表明,通过ML-7的Rho激酶和MLCK的生化抑制减少了MLC磷酸化和响应TNF-α的肌动蛋白重新排列36,表明Rho激酶和MLCK激活是TNF-α介导的细胞骨架变化机制中的关键步骤。然而,MLCK或Rho激酶抑制剂抑制MLC磷酸化并不能减弱TNF-α诱导的EC通透性,这表明MLCK单独激活不足以引起屏障功能障碍37.MLC磷酸化只是快速TJ打开的一种机制。其他可能的机制,包括TJ蛋白的磷酸化,包括紧密连接蛋白ZO-1 (ZO-1),已经被描述38.虽然这些机制具有共同的磷酸化事件,但涉及的特定激酶可能不同,因为MLC磷酸化通常发生在丝氨酸和苏氨酸残基上,而ZO-1在酪氨酸残基上磷酸化37.然而,近于激酶激活的信号系统,例如细胞内Ca的升高2+水平,可能最终导致MLC和ZO-1磷酸化。此外,尚未定义的磷酸化事件在TJ组装中可能是关键的38因此可能有助于TJ的长期监管。
总之,本研究强调了气道上皮屏障在肺损伤中的重要性,特别是在肺炎症反应的启动中。选择性肌凝蛋白轻链激酶抑制剂预处理可抑制肺组织的通透性和炎症,提示肌凝蛋白轻链激酶抑制剂可能是缓解肺损伤的新药物的相关靶点。
脚注
有关编辑意见,请参阅第776页。
- 收到了2004年6月2日。
- 公认2004年12月29日。
- ©ers Journals Ltd