摘要
内皮损伤是急性呼吸窘迫综合征(ARDS)的重要预后因素。ARDS患者血管内皮生长因子(VEGF)分泌减少可能有利于血管病变,因为VEGF通过抑制凋亡促进内皮细胞存活。
本研究旨在记录ARDS患者肺组织中的低VEGF水平,确定原因是否是肺泡II型细胞(VEGF的主要肺来源)受损,并评估血管后果。通过开放式活检或尸检,从29例严重ARDS患者(两名幸存者)和5名对照组获得肺标本。
与对照组相比,ARDS患者的肺组织匀浆含有较少的VEGF(中位数(四分位范围)ARDS 8.2(4.7–12.2)对控制28.4 (9.9-47.1)ng·g−1蛋白质)。ARDS肺表面活性剂蛋白B免疫染色增强。与对照组相比,ARDS肺组织中出现大量细胞凋亡(末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍标记染色),包括内皮细胞和肺泡II型细胞,血管床密度(CD31免疫染色)下降。VEGF水平与凋亡内皮细胞计数呈负相关。
总之,肺组织中血管内皮生长因子水平的降低可能参与了急性呼吸窘迫综合征肺灌注的降低。
急性呼吸窘迫综合征(ARDS)的详细形态学描述1包括肺毛细血管密度的降低。可以想象,由此产生的肺灌注减少可能导致肺泡死腔的增加,这已被证明是ARDS的主要预后因素2. ARDS血管病变的病理生理学是一个具有挑战性的问题,很少受到关注3..最近,Hamacher等4急性呼吸窘迫综合征(ARDS)患者的支气管肺泡灌洗液表现为体外肺微血管内皮细胞的促凋亡活性4相反,内皮细胞存活因子(抗凋亡)的降低可能是另一种假设。在早期ARDS患者的肺中发现了低水平的血管内皮生长因子(VEGF)5,6这种VEGF的减少可能有助于血管损伤的发生,因为VEGF已被证明是内皮细胞的主要生存因子7.VEGF(或VEGF- a)是一种高度保守的二聚体肝素结合糖蛋白(分子量46kda)。在人类细胞中,至少有四种不同的VEGF转录本,它们是由单一基因的交替剪接产生的。VEGF121和VEGF165以可溶的形式分泌,而VEGF189和VEGF206保留在细胞表面,或主要沉积在细胞外基质中。VEGF似乎特别影响内皮细胞的生长、存活和通透性。在肺中,VEGF主要由上皮细胞和巨噬细胞表达。VEGF也由人血小板和多形核中性粒细胞产生和储存。VEGF的生物学活性依赖于与特定受体(VEGF- r1、2和3)的相互作用,这些受体不仅在内皮细胞中表达,也在活化的巨噬细胞和肺泡II型上皮细胞中表达。内皮细胞存活是被介导的通过VEGF-R2/激酶插入结构域受体(KDR)8. 本研究的目的有两个:确定肺血管内皮生长因子的减少是否与上皮损伤有关,以及是否可能与内皮细胞凋亡增加和毛细血管密度降低有关。
材料和方法
急性呼吸窘迫综合征及对照患者的选择
ARDS定义为国际美欧共识会议推荐9. ARDS患者的肺标本在法国马赛圣玛格丽特医院通过开放式肺活检或尸检获得,并立即在-80°C下冷冻以备后续检查。开放性肺活检是出于临床原因进行的,详见其他地方10对照组为接受胸部手术治疗非小细胞肺癌的患者,这些患者的肺组织(显微镜检查的正常外观)在远离肿瘤区域的地方取样,并与ARDS患者一样进行处理。人类研究机构审查委员会(法国马赛圣玛格丽特医院)批准研究方案。
组织病理学检查
第5节 从冷冻肺组织中切取μm厚的组织。由一名组织病理学家(F.Lange)对所有肺样本进行染色(血红素/曙红/藏红花),以进行盲法标准组织病理学分析。根据肺采样时的症状持续时间(<5天或更长),ARDS患者被分为早期或晚期疾病≥5天)和存在早期或晚期ARDS的标准组织学标准11.肺泡内存在炎性渗出物和透明膜,基底膜剥蚀,肺泡壁水肿是早期渗出期的特征。晚期纤维增生期以II型肺细胞增殖与肌成纤维细胞增殖和/或纤维化为特征。采用这种基于临床和组织学标准的分类,因为它比单独使用任何一套标准更可靠;急性肺损伤及由此引起的肺泡毛细血管壁损伤可在符合ARDS标准之前发生,已知组织学病变为斑片状,相邻肺区同时存在早期和晚期特征。
肺组织匀浆蛋白表达
按照制造商(美国明尼苏达州明尼阿波利斯R和D系统公司)的建议,使用ELISA对组织样本中的VEGF和VEGF-R2/KDR蛋白表达进行定量测定。VEGF ELISA试剂盒可识别VEGF121和VEGF165(可溶性形式)。样本通过在含有20%葡萄糖的裂解缓冲液中均质溶解 mM-羟乙基哌嗪乙烷磺酸,0.5 mM-乙二醇四乙酸,1 mM二硫苏糖醇和0.32 M蔗糖(pH 7.4)用于VEGF测量,并在含有苯甲基磺酰氟和3-(3-胆氨丙基二乙基氨)-1-丙烷磺酸盐的Tris缓冲液中用于VEGF-R2测量。蛋白质含量采用Bradford(美国加利福尼亚州Richemond Bio-Rad)法测定.将每个样本中的VEGF和VEGF-R2蛋白浓度标准化为组织匀浆中的总蛋白浓度。
免疫组织化学
载脂蛋白表面活性蛋白B
使用针对表面活性蛋白(SP)-B的特异性兔多克隆抗体(Chemicon,Temecula,CA,USA)检测肺泡II型上皮细胞,并使用非免疫兔血清(Sigma,St.Louis,MI,USA)进行阴性对照目前的作者选择评估SP-B,因为该蛋白比SP-A对II型肺泡上皮细胞更具特异性,并且已知SP-C在急性肺损伤动物模型中下调。组织切片在−20°C,然后在过氧化氢(PBS中为3%)中孵育以淬灭内源性过氧化物酶。冲洗后,通过在PBS中与2%正常山羊血清(Sigma)和0.05%吐温20孵育30分钟来阻断非特异性抗原位点 然后将载玻片与抗人SP-B抗体(稀释度为1:1000)或阴性对照血清在潮湿的室内孵育2分钟 随后,将载玻片在含有0.05%吐温20的PBS中洗涤,然后在黑暗中与辣根过氧化物酶结合的山羊抗兔抗体(Catalag Laboratories,Burlingame,CA,USA)和启示底物(二氨基联苯胺(DAB)显色剂)孵育7小时 至少用苏木精对组织切片进行复染。使用光学显微镜(最终放大400倍)检查所有组织切片,并在随机抽取的10个区域中计算阳性细胞的数量。由于组织扩张的程度可能因肺标本而异,为确保所有标本的评估表面积相同,每个组织样本中评估的肺泡数量相同。
增殖细胞核抗原
用单克隆抗体PC10(PCNA染色试剂盒,ZYMED,旧金山,CA,美国)染色增殖细胞核抗原(PCNA),鉴定增殖细胞核。
血管内皮生长因子和血管内皮生长因子受体2
采用小鼠特异性单克隆抗体(MAB293;R and D Systems), VEGF-R2的检测使用针对该受体胞外结构域的小鼠单克隆抗体(KDR-1;σ)。阴性对照采用非免疫小鼠免疫球蛋白(Ig)G2B (R and D Systems)和IgG1 (Sigma)。组织切片置于1%多聚甲醛中,并在过氧化氢(3% PBS)中孵育,以熄灭内源性过氧化物酶。冲洗后,用2%正常山羊血清(Sigma)在含0.05% Tween 20的PBS中室温孵育30分钟,阻断非特异性抗原位点。玻片与抗人VEGF抗体(稀释1:160)和抗VEGF- r2抗体(稀释1:800),在1%牛血清白蛋白(BSA)或阴性对照血清的存在下,在潮湿的室内(室温)孵育2小时。组织在PBS中洗涤,用生物素化的山羊抗小鼠Ig (Sigma)作为二级连接抗体处理,并用过氧化物酶偶联链霉亲和素(Sigma)标记。用DAB显色原显示抗体,苏木精对组织进行反染色。
内皮细胞染色与凋亡检测
用末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸缺口末端标记法(TUNEL)检测细胞凋亡。简单地说,通过使用ApoptoDetect Plus过氧化物酶添加地高辛标记的核苷酸和末端脱氧核苷酸转移酶来检测凋亡片段原位凋亡检测试剂盒(Qbiogen Inc.,美国加利福尼亚州卡尔斯巴德市),符合制造商的说明。凋亡细胞的细胞核呈棕色和颗粒状。为了量化微血管内皮细胞凋亡的程度,使用抗人鼠CD31单克隆抗体(WM-59;PharMingen,San Diego,CA,USA)联合染色,识别内皮表面标记物血小板/内皮细胞粘附分子1。TUNEL切片与2%正常山羊血清(在含有0.05%吐温20的PBS中)一起孵育,随后与初级抗CD31抗体(1:100000稀释,在含有1%BSA的PBS中)在4°C下孵育过夜。使用小鼠非免疫IgG1(Sigma)作为阴性对照。应用生物素化山羊抗小鼠抗体(Sigma)30天 室温下至少30分钟,然后是亲和素-生物素-过氧化物酶(Sigma)复合物30分钟 最低温度(室温)。真蓝色过氧化物酶底物用作最终的显色剂(美国马里兰州盖瑟斯堡KPL实验室)。未使用反染色,以避免可能干扰内皮细胞表面的特定深蓝色免疫染色。当特定细胞显示棕色细胞核,周围有蓝色到黑色的膜免疫反应模式时,双重染色被认为是阳性。在10个随机选择的区域(最终放大400倍)计数阳性细胞。
图像分析
一种电荷耦合器件虹膜照相机(CDD Iris;索尼法国,巴黎,法国),加上光学显微镜(Leitz Laborlux, Wetzlar,德国),被用来查看切片,并将彩色图像数字化到PC主机。使用Perfect Image软件(ClaraVision, Orsay, France)估计CD31和TUNEL染色,该软件根据其红-绿-蓝比例(±10%)来区分颜色。每个切片至少分析了10个区域,肺泡数量大致相同。结果给出了蓝色(CD31)或棕色(TUNEL)染色表面积与总视场表面积(CD31或TUNEL染色相对于总视场表面积)的比值(%)。
统计分析
结果以中位数(四分位数范围)的形式显示在文本中。数据以箱形图的形式表示中位数和第10、25、75和90个百分位。组间差异采用Kruskal-Wallis检验事后Mann-Whitney分析。为探讨VEGF对肺微循环的可能影响,采用Spearman秩相关法评价VEGF水平与内皮定量及细胞凋亡的关系。p- value <0.05被认为有统计学意义。
结果
患者特征
共研究了29名ARDS患者(20名男性和9名女性;中位年龄64岁(50-73岁))。他们入院时的急性生理学和慢性健康评估II评分中位数为16.9(13.6-23.6)。15名患者和14名患者在死亡后立即进行开胸肺活检作为诊断程序。
肺组织取样时,22例患者动脉氧张/吸气氧比< 200mmhg, 7例患者动脉氧张/吸气氧比200 - 300mmhg。导致ARDS的原因为直接肺损伤17例(与感染有关11例,与吸入有关6例),间接肺损伤12例(非肺脓毒症7例,非感染性休克4例,胰腺炎1例)。ARDS发病5天内死亡6例为急性ARDS,其余23例为晚期ARDS;组织学结果证实了每个病例的分类。在这个选定的人群中,存活率只有7%(29人中有2人)。
对照组由5名患者组成(均为男性;中位年龄65岁(54-70))。
急性呼吸窘迫综合征及对照患者肺中血管内皮生长因子的表达
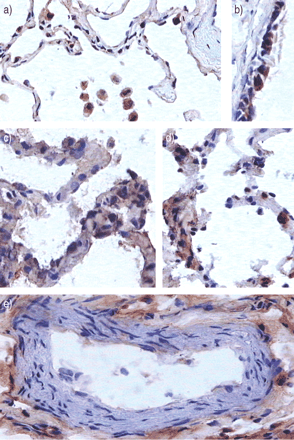
ARDS患者肺组织匀浆中的VEGF水平低于对照组:8.2(4.7–12.2)对28.4(9.9-47.1)纳克−1蛋白质,分别为(p = 0.03). 早期和晚期ARDS亚组之间没有差异(图。 1.⇓).当每克肺重量的VEGF浓度正常化时,结果相似。在对照组中,对VEGF进行免疫染色(图。 2.⇓)标记细支气管细胞和肺泡巨噬细胞,并强烈标记一些肺泡II型上皮细胞。肺泡I型上皮细胞呈阴性。在ARDS患者中,染色高度不均匀。细支气管和肺泡上皮细胞在某些区域呈阴性,在其他区域呈阳性,甚至在组织切片中也是如此。在早期ARDS组织样本中,炎性细胞也呈阳性。
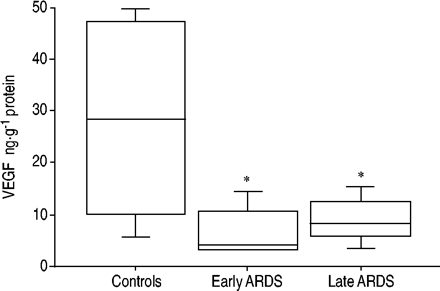
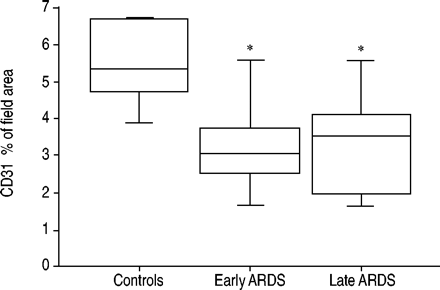
早期患者肺匀浆中的血管内皮生长因子(VEGF)浓度(<5天;n = 6) 还是晚期(≥5天;n = 23)急性呼吸窘迫综合征(ARDS)和对照组患者(n = 5) .通过免疫分析测定VEGF。方框图显示了中位数以及第10、25、75和90个百分位。*:与对照组患者相比,p<0.05。
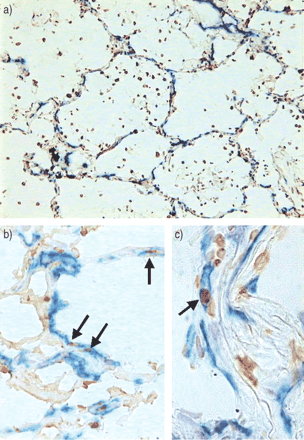
血管内皮生长因子的代表性免疫过氧化物酶染色(棕色染色)。a) 在对照组患者中,一些肺泡II型上皮细胞和一些肺泡巨噬细胞出现免疫染色。b) 气道上皮细胞呈阳性。c、 d)晚期急性呼吸窘迫综合征患者肺泡毛细血管壁明显改变;免疫染色呈异质性。某些区域的染色似乎是细胞外的,如血管周围间隙(e)。
急性呼吸窘迫综合征患者和对照组肺血管内皮生长因子受体2的表达
ELISA法测定ARDS患者肺匀浆中VEGF-R2浓度与对照组无显著差异(116(78-157))。对156 (131–191) ng·g−1蛋白质)。早期和晚期ARDS患者无明显差异。
对照组内皮细胞免疫染色可见VEGF-R2;然而,并非所有内皮细胞都呈阳性。巨噬细胞、上皮细胞和细支气管细胞均阴性。在ARDS组中,染色延伸到一些肺泡II型上皮细胞(数据未显示)。
急性呼吸窘迫综合征患者肺泡上皮Ⅱ型细胞增殖
与对照组相比,ARDS患者肺泡上皮II型细胞增生:13(11-17)对每个区域分别有7(5-8)个细胞(p = 0.003;图。 3.⇓).此外,晚期ARDS患者的肺泡上皮II型细胞数量多于早期ARDS患者:16 (12-17)对每个字段分别有11(8-12)个细胞(p = 0.02;图4⇓).尽管ARDS患者肺泡上皮II型细胞增多,但PCNA染色罕见。
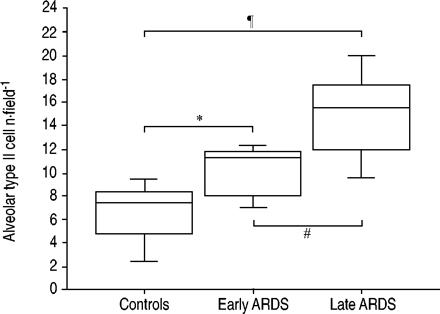
早期(<5天;n)患者肺活检中每个光场肺泡II型上皮细胞数量的量化(表面活性剂蛋白B染色) = 6) 还是晚期(≥5天;n = 23)急性呼吸窘迫综合征(ARDS)和对照组患者(n = 5) .方框图显示中位数和第10、25、75和90个百分位。*:p<0.05;#:p<0.02;¶: p < 0.005。
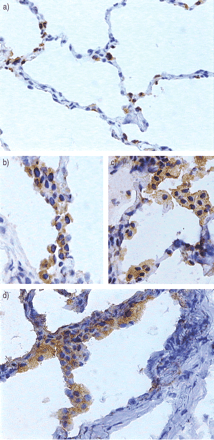
对照组患者(a)和急性呼吸窘迫综合征患者(肺泡II型上皮细胞增生覆盖肺泡屏障,导致肺泡毛细血管壁厚度增加)中表面活性蛋白B的代表性免疫过氧化物酶染色。肺泡II型上皮细胞的细胞质呈棕色。
急性呼吸窘迫综合征患者肺内皮密度降低
使用计算机辅助CD31染色定量估计内皮密度(图 5.⇓及6⇓).ARDS患者的内皮面积明显低于对照组:3.5% (2.3-4.1)对总面积的5.3%(4.7–6.7)(p = 0.01). 相反,早期和晚期ARDS之间没有差异。在超过三分之二的ARDS患者中,肺内皮的分布存在明显的异质性。
内皮染色自动定量(图像分析;见方法)早期(<5天;N = 6)或晚期(≥5天;急性呼吸窘迫综合征(ARDS) 23例,对照组5例。结果是CD31染色面积占总视野面积的百分比。箱线图显示了中位数和第10、25、75和90个百分位数。*:与对照组比较p<0.05。
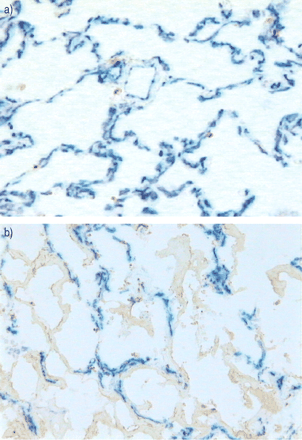
在一个对照组(a)和一个血管床密度中度下降的急性呼吸窘迫综合征(b)患者的肺组织中,使用双免疫染色检测脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍末端标记/CD31的内皮评估。内皮表面呈蓝色至深色染色blue with True Blue Peroxidase substrate (KPL Laboratories, Gaithersburg, MD, USA) as the final chromogen. No counterstaining was used.
急性呼吸窘迫综合征患者内皮细胞凋亡增加
ARDS患者的凋亡内皮细胞数量大于对照组,如TUNEL和CD31:8(6-13)双标记的细胞数量所示对每10个光场分别有4(3-4)个电池(p = 0.005;图7⇓).在早期和晚期ARDS之间,或者在ARDS患者的开放式肺活检和尸检标本之间,没有发现显著差异。肺血管内皮生长因子浓度与凋亡内皮细胞数量呈负相关(ρ = −0.40;p = 0.02).
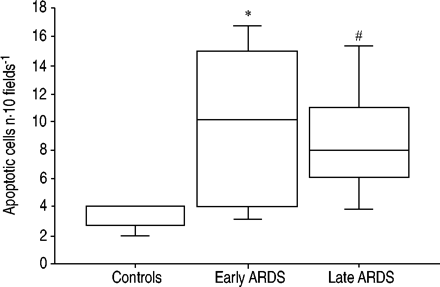
评估每10个光场中凋亡内皮细胞的数量。在早期(<5天;n = 6) 还是晚期(≥5天;n = 23)急性呼吸窘迫综合征(ARDS)和对照组(n = 5) .方框图显示了中位数以及第10、25、75和90个百分位。*:与对照组患者相比,p<0.05;#:p = 0.004,与对照组相比。
TUNEL染色的另一个结果是,与对照组相比,ARDS患者的肺部出现广泛的细胞凋亡:表面积的4.0%(3.0–4.0)对2.0% (1.0-3.2), p = 0.03。凋亡增加涉及内皮细胞,特别是炎症细胞和肺泡上皮II型细胞(图8)⇓).
具有代表性的双免疫染色显示了末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍末端标记(TUNEL)/CD31,显示了急性呼吸窘迫综合征患者肺部广泛的细胞凋亡,包括肺泡炎症细胞(a)、上皮细胞(b)和内皮细胞(c)。凋亡内皮细胞(箭头)有棕色核(TUNEL)和蓝黑色膜(CD31)。患者(b)血管床严重缺失。
讨论
本研究证实,在ARDS病程早期,肺VEGF水平较低,提示这种水平的降低可能导致内皮细胞凋亡的增加,从而使肺血管床缩小。
由于两项早期研究证明ARDS患者上皮衬里液中VEGF浓度早期降低,因此肺VEGF水平有望降低5,6. 由于上皮衬里液中VEGF浓度的降低引起了一些关注,因此有必要在肺组织中证实这一结果。目前研究的一个局限性是,对照组患者患有恶性肿瘤,即使组织取样是在远处进行的。然而,VEGF的上调在非小细胞肺癌中并不是一个恒定的发现12, VEGF表达增加与微血管密度增加有关12,这在目前的对照患者中没有得到证实。在人类其他形式的肺损伤中也发现了肺VEGF的下降,包括婴儿呼吸窘迫综合征、肺支气管发育不良和特发性纤维化13- - - - - -15.由于多种因素可能会影响受试者的肺VEGF水平,包括吸烟效应和潜在的慢性肺病,因此在本研究中不能确定VEGF水平低与ARDS有关。然而,在Thickett的研究中,ARDS患者上皮内壁液中VEGF浓度随存活时间的延长而增加,且VEGF水平持续低与生存率降低相关等6. 在目前的研究中,早期和晚期ARDS患者的VEGF水平均较低。目前患者死亡率极高(∼93%)表明低浓度的VEGF,无论处于何种阶段,都可能归因于这种选择偏倚。血管损伤程度已被证明是一个重要的预后因素,这与早期证据一致,即肺泡血管性血友病因子(内皮损伤的标志物)水平较高、肺动脉高压更严重或死亡空间更大的ARDS患者生存率降低2,11,16有趣的是,据报道急性内皮损伤在ARDS的增殖期比渗出期更为明显11尽管ARDS患者支气管肺泡灌洗液中VEGF水平较低,但有一项研究报道,血管生成活性增加主要与CXC趋化因子有关17.
尽管有文献表明,在大鼠急性肺损伤模型中,早期(第四小时)VEGF mRNA表达减少5,这些发现不排除ARDS早期VEGF释放增加、中性粒细胞迁移时中性粒细胞颗粒的胞吐以及血管床聚集的血小板释放增加。这可以解释ARDS期间血浆VEGF增加的原因18本研究部分区域细胞外VEGF免疫染色明显升高。因此,不能排除血管内皮生长因子在急性呼吸窘迫综合征特征的内皮通透性最初增加中的作用。与这种可能性一致的是,在健康动物中腺病毒诱导的VEGF过表达与水肿形成增加有关19.有趣的是,在本研究中,VEGF免疫定位标记肺泡炎症细胞,这与Thickett的发现一致等6,表明VEGF是由分离的炎症细胞释放的。
本研究的一个局限性是,目前的作者没有确定哪些VEGF亚型减少。然而,在之前的一项实验研究中,证明了细菌诱导的肺损伤与VEGF121、VEGF165和VEGF189的mrna减少有关5. 最近,佐科斯等20.已经证明,与非过敏对照组相比,死于败血症的危重患者肺组织中VEGF蛋白(使用ELISA和免疫组织化学)减少,与VEGF121和VEGF165的mRNA减少相关。
先前有人认为,ARDS相关的VEGF减少可能不是肺泡II型上皮细胞受损的结果,因为这些细胞的主要功能,即。液体清除,保存在细菌诱导的急性肺损伤模型中21其中VEGF mRNA和VEGF蛋白均出现下降5. 肺泡II型上皮细胞的数量增加,与先前ARDS的研究结果一致,这些研究表明,肺泡II型上皮细胞的数量增加,并且上皮生长因子升高1,22,23. 目前还没有证明为什么肺组织中VEGF释放减少,目前的作者先前假设,在损伤后增殖阶段,上皮细胞不分泌VEGF5.从目前的研究结果可以推测,正在凋亡的肺泡上皮II型细胞不分泌VEGF。只有一种方法(TUNEL)用于评估细胞凋亡;因此,不能明确区分坏死。然而,一些实验研究表明,在肺损伤后II型细胞增生的消退过程中,有凋亡的成分24.Bardales等25证明细胞凋亡是ARDS患者肺泡II型上皮细胞降解的主要途径。在后一项研究中,作者证明大多数患者表现为II型肺细胞凋亡(30-80%),同时伴有极为罕见的PCNA阳性25,这与目前的结果是一致的。在阿尔伯丁的研究中等26,与对照组相比,所有促凋亡标志物的抗原在ARDS患者中均增加,这进一步表明,使用尸检样本不太可能影响凋亡标志物。
本研究间接评估了肺血管内皮生长因子(VEGF)减少的原因或后果,因为VEGF减少可能导致微血管密度降低或与之相关。评估VEGF受体的表达,已知其介导抗凋亡作用。ARDS患者和对照组之间VEGF-R2的表达没有差异,这可能与血管床的减少相矛盾。这可以解释为VEGF-R2的表达并不局限于内皮细胞,因为肺泡II型上皮细胞表达VEGF-R227. ARDS患者的凋亡内皮细胞数量较多。VEGF水平与凋亡内皮细胞数量呈负相关,进一步强调了VEGF对内皮细胞存活的可能作用。必须注意的是,这种统计相关性并不意味着因果关系。VEGF可能不是参与内皮细胞凋亡的唯一因素。至少有三项研究发现ARDS患者支气管肺泡灌洗液中促凋亡可溶性因子水平升高4,26,28内皮细胞凋亡似乎导致肺血管床收缩。脓毒症动物模型的结果支持这种可能性:全身性内毒素给药可诱导肺血管内皮生长因子和内皮细胞凋亡的减少29,30..因此,改善急性呼吸窘迫综合征(ARDS)患者的肺内皮细胞存活率可能会带来临床益处。给药半胱天冬酶抑制剂已被证明可以防止内毒素诱导的急性肺损伤小鼠的致命凋亡31.Compernolle等32在新生小鼠呼吸窘迫综合征中显示了VEGF的有益作用32,和康恩等33发现在高氧诱导的肺损伤期间转染白细胞介素13的小鼠存活率增加,部分是通过VEGF合成增加介导的33.
结论
这组急性呼吸窘迫综合征患者的肺血管内皮生长因子水平较低,死亡率很高。发现内皮细胞凋亡增加,毛细血管密度降低。有必要进行进一步研究,以确定抑制内皮细胞凋亡是否可能促进肺血管内皮生长因子的表达为急性呼吸窘迫综合征患者提供临床益处。
- 收到2004年6月4日。
- 接受2004年9月20日。
- ©ERS期刊有限公司