抽象
吸入丙酸氟替卡松(FP)被广泛用于减少慢性阻塞性肺疾病肺部炎症,但对气道上皮细胞来自患者的囊性纤维化(CF)FP的潜在影响是未知的。在CF疾病,非管制炎性肺响应通过夸张核因子发生(NF)-κB的活化和升高的促炎细胞因子的生产通过气道上皮细胞。
为了确定是否FP减少支气管上皮细胞中的细胞因子产生通过NF-κB,作者nonstimulated和调查铜绿假单胞菌脂多糖(LPS)刺激的NF-κB在非CF和CF的激活沿生产NF-κB依赖性白细胞介素(IL)-6,IL-8和RANTES(调节激活,T细胞表达和分泌的)人支气管上皮细胞。
已经证实,FP的相关浓度(10-8 M) inhibited constitutive and铜绿假单胞菌LPS诱导的IL-6和IL-8产生的非CF和CF气道上皮细胞的。有趣的是,2种IκB激酶(IKK)的表达-α/β,胞质IκB-β抑制剂和NF-κB脱氧核糖核酸结合活性的降解均明显在两个CF和非CF支气管上皮细胞FP处理后减少。
它是由作者表明,丙酸氟替卡松通过阻断信号转导导致IκB-α/β激酶在支气管上皮细胞的水平降低施加的抗炎作用。在对IκB-β激酶,已知其在囊性纤维化患者的支气管上皮细胞中升高特别强的效果,进行了观察。
这项工作部分得到了INSERM的支持,它是由葛兰素史克(英国伦敦)和法国Vaincre la mucoidose协会资助的。
囊性纤维化(CF)是由在基因突变在气道上皮细胞编码CF跨膜传导调节因子(CFTR)致死遗传病症1。其中CFTR突变的主要临床表现的是中性粒细胞主导炎症2,3,这意味着CFTR缺陷检测影响气道上皮细胞的免疫功能,尤其是核转录因子的生产(NF) -κB-dependent趋化因子。越来越多的证据表明,呼吸道上皮细胞功能失调的雌性生殖道有夸张的激活NF-κB /抑制剂NF-κB复杂与调节趋化因子的表达有关4,五。目前的作者和以前的研究已经证明,上皮细胞白细胞介素(IL)-8在成人支气管上皮细胞中表达过高6。这是在两者匹配的CF和校正呼吸道上皮细胞系中观察到7,8而在CF跨膜电导regu<~?>lator纯合子缺陷小鼠(CFTR-/-)术后与正常小鼠比较铜绿假单胞菌刺激9。如何在CF气道细胞雌性生殖道功能障碍导致的激活和核本地化NF-κB尚不清楚。最近,一个在体外研究的表达ΔF508雌性生殖道CFTR(检测含有苯丙氨酸的删除位置508)中国仓鼠卵巢细胞,不表达雌性生殖道,揭示了7倍的激活增加NF-κB比野生型雌性生殖道或G551D突变。这种效应也与IL-8表达水平升高平行五。
治疗策略包括阻止转录因子如NF-κB导致炎性基因激活和抑制信号通路刺激肺部疾病。糖皮质激素的影响主要是介导的抑制NF-κB脱氧核糖核酸(DNA)绑定活动,控制基因编码炎性细胞因子,趋化因子和粘附分子在呼吸道上皮细胞10-13。丙酸氟替卡松(FP)作为一种抗炎、免疫抑制剂在临床上被广泛应用,尤其在哮喘的治疗中14和过敏性鼻炎15。最近的报告表明,体内FP的管理通过减少嗜酸性粒细胞气道活检数量能力减弱肺部炎症16并抑制中性粒细胞趋17。嗜酸性粒细胞的FP诱导细胞凋亡18并且还降低了制造几种细胞因子例如IL-1β,IL-6,IL-8和RANTES的肺泡巨噬细胞(调节激活,T细胞表达和分泌的)19和淋巴细胞20.,21。尽管有这些抗炎作用,FP在支气管上皮细胞中的分子靶点仍是未知的。了解这些机制是很有意义的,可能会导致新的治疗方法的发展,以减少气道炎症,这是早期,过度和持续的CF患者。
本研究的目的是:1)评价FP的减少构的能力和铜绿假单胞菌脂多糖(LPS)诱导培养的支气管腺上皮细胞产生促炎因子IL-6、IL-8和RANTES;和2)检查FP行动NF-κB / IκB-α通路的分子靶点。
材料和方法
细胞培养
细胞隔离和文化过程的人类支气管黏膜下腺体上皮细胞进行支气管组织收集从成人CF患者(所有ΔF508雌性生殖道突变纯合子)和non-CF控制接受肺移植的患者,如前所述22。非cf对照实验的支气管组织取自原发性肺动脉高压和肺特发性纤维化患者。用酶消化法从支气管粘膜下层分离出支气管腺上皮细胞,在I型胶原包膜上生长25 cm2在Dulbecco组织培养瓶中与Ham氏F12(50/50%,V / V),补充有1%Ultroser G(血清替代品; Sepracor公司,新城 - 拉加伦,法国)改良伊格尔培养基(DMEM),葡萄糖(10 g·L-1), sodium pyruvate (0.33 g·L-1)。青霉素G (100 U·mL-1) and streptomycin (100 µg·mL-1)还加入抗生素。
囊性纤维化和非囊性纤维化支气管上皮细胞暴露于丙酸氟替卡松
CF和非CF支气管上皮细胞(1×104细胞)在24孔培养板中生长。Prior to their exposure to FP, CF and non-CF bronchial epithelial cells were incubated for 16 h in an Ultroser G-free DMEM/Ham's F12 medium in 95% air and 5% CO2。在16小时期间结束时,CF和非CF支气管上皮细胞用DMEM / Ham氏F12培养基单独或与各种浓度的FP的介质(10预处理-9-10年-6 M) for 2 h. Afterwards the cells were activated for 4 h with DMEM/Ham's F12 containing 1.0 µg·mL-1铜绿假单胞菌有限合伙人(血清型10;美国加州圣地亚哥的Calbiochem公司)。一种FP (10-3 M) generously provided by GlaxoSmithKline was prepared in 99.5% ethanol (Merck Eurolab, Darmstadt, Germany). FP was further diluted with DMEM/Ham's F12 medium to final FP concentrations (10-9-10年-6 M) and used throughout the experiments. Immediately after each period of cell exposure, cells and culture supernatants were collected and stored at −80°C.
酶联免疫吸附法测定白细胞介素-6和白细胞介素-8,并调节活化、t细胞表达和分泌
The enzyme-linked immunoabsorbent assay (ELISAs) for IL-6, IL-8 and RANTES cytokine detection, were sensitive at 2 pg·mL-1,五 pg·mL-1和2 pg·mL-1分别是按照制造商的说明书(矿泉国际,卡马里奥,CA,USA)进行。所有试剂均为分子生物学级别,并采用无热原级水制备所有缓冲区和解决方案。In all culture supernatants, undetectable levels of endotoxin (detection limit ≥5 pg·mL-1采用定量显色性鲎试剂(LAL;比奥·惠特克,埃默里维尔,法国)。经所有实验程序后,通过台状体蓝排除测定,CF和非CF支气管上皮细胞的存活率始终超过97%。数据以ng·mL表示-1每106活细胞或作为释放细胞因子的百分比与对照组相比。
免疫荧光对IκB-α激酶表达
CF和在不存在或FP的存在下培养非CF支气管上皮细胞(10-8M, 16小时)是固定的原位in cold methanol at −20°C, air dried, and rehydrated in phosphate-buffered saline (PBS) at pH 7.2. Cells were stained for IκB-α expression using sheep antiserum to human IκB-α (Serotec Ltd, Oxford, UK) for 1 h at room temperature and a donkey anti-sheep fluorescein isothiocyanate (FITC) conjugated antibody (Ab) for 45 min at room temperature as previously described23。阴性对照通过使用非特异性免疫球蛋白(Ig)G作为主要抗体(M7769;西格玛奥德里奇Chimie公司,法国里昂)获得或FITC缀合的单独的Ab。CF和在不同条件下培养的非CF支气管腺细胞的代表性领域使用Zeiss Axiophot显微镜(Zeiss,乐Pecq,法国)记录下来。
细胞提取物和Western blot分析
CF和在不存在或FP的存在下培养非CF支气管上皮细胞(10-8 M, 16 h) were washed in PBS (pH 7.2) and cell proteins were extracted (15 min, 4°C) in radioimmunoprecipitation buffer (50×10-3 M Tris, pH 7.4, 15×10-4M NaCl, 1% Triton X100, 0.1% doo癸基硫酸钠,5×10-3 M iodoacetamide, sodium deoxycholate and 1% Nonidet P-40), which was supplemented with 1% phenylmethylsulfonyl fluoride. Cells were then harvested and the protein extracts were centrifuged (12,500×g, 10分钟,4°C)。上层清液收集并用于测定IκB-α抑制剂和两个IκB激酶(IKK-α/β)如前所述22。等量的蛋白质(µg·10毫升-1)从每个蛋白提取物使用4-15%聚丙烯酰胺凝胶变性条件(Pharmacia Biotech公司下提交电泳。,巴黎,法国)。然后将凝胶通过电转移到硝酸纤维素膜(Millipore,贝德福德,马萨诸塞州,美国)。连续洗涤后,将膜通过使用与兔的Western印迹技术分析多克隆抗人IκB-α,抗人IKK-α和抗人IKK-β抗体(Santa Cruz Biotechnology公司,CA,USA)中,用增强的化学发光试剂盒显影(Amersham公司生命科学,弗赖堡,德国)。是在Bio-Rad公司型号GS-690图像光密度进行Western印迹的密度分析。将凝胶在透射模式,分辨率为每英寸800个点设定扫描。每个条带的强度与在毫米调整体积(平均光密度×面积进行比较2)。
核蛋白提取和电泳迁移率检测
制备并在不同的条件下温育的CF和非CF支气管上皮细胞后,分析的核提取物,如先前所描述22。CF和非CF支气管上皮细胞的核提取物与中温育32磷酸盐(P)标记的NF-κB寡核苷酸。用于electophoretic迁移率变动分析(EMSA)的共有κBDNA序列是5'AGTTGAGGGGACTTTCCCAGGC3'(Promega公司,麦迪逊,WI,USA)。寡核苷酸用[α放射性标记32P]使用T4多核苷酸激酶(Pharmacia Biotech公司)。所述蛋白质-DNA复合物进行电泳上的非变性5%聚丙烯酰胺凝胶,然后在真空下干燥,并暴露在-80℃下放射自显影用胶片。In competition studies and supershift assay, a 100-fold molar excess of unlabelled oligonucleotide or 1 µg Ab was added to the binding reaction mixture, prior to the addition of the labelled κB probe. Identification of the different NF-κB heterodimeric proteins was carried out by incubating the nuclear extracts with polyclonal antibodies against the NF-κB proteins NF-κB1 (p50) and (p65) RelA (Santa Cruz Biotechnology), prior to the addition of the labelled κB probe.
统计分析
结果表示为平均值±SD。每个数据点被证实在一式三份,并进行各细胞培养实验≥3次。在细胞因子水平差异的统计显着性是通过方差分析确定。
结果
白细胞介素6的分泌丙酸氟替卡松的效果,白介素-8和调节激活,T细胞表达和囊性纤维化和非囊性纤维化支气管上皮细胞分泌
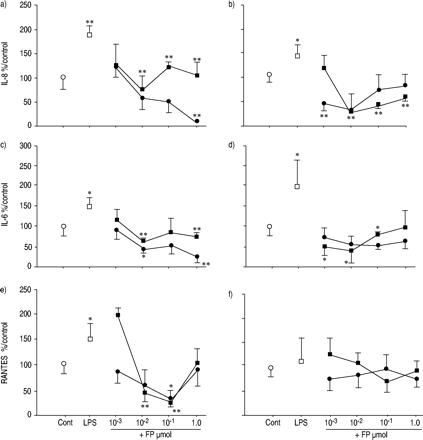
下静止培养条件(即过在未刺激状态下的4小时期间),IL-8,IL-6和RANTES的自发分泌物呈3.5,8.0-和10.0倍相比,非CF支气管上皮细胞在CF支气管上皮细胞更高,respectively (fig. 1⇓)。既CF和非CF支气管上皮细胞到FP的曝光(10-9-10年-6M, 4h时,IL-6和IL-8的分泌量明显减少(p<0.05),呈剂量依赖性(图2a-d)⇓)。观察RANTES的显著减少(p <0.05)仅在非CF支气管上皮细胞与FP 10-7 M and 10-8有趣的是,用FP (10-8M)显著降低(p<0.05)铜绿假单胞菌LPS诱导的IL-8和IL-6生产的CF和非CF支气管细胞。RANTES产量显著(P <0.01)降低铜绿假单胞菌LPS用FP刺激非cf支气管上皮细胞10-8 M. There was no significant effect of FP on unstimulated and铜绿假单胞菌LPS刺激RANTES分泌CF支气管上皮细胞(图2C和d⇓)。
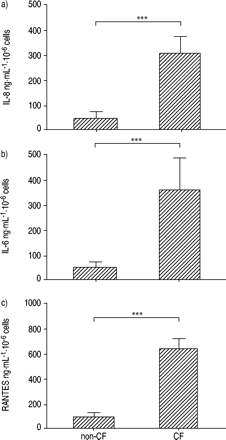
自发性水平的细胞因子白介素(IL) 8、IL - 6和监管激活后,正常t细胞表达和分泌(咆哮)发布的培养non-cystic纤维化(non-CF)和ΔF508纯合子的囊性纤维化(CF)如果支气管上皮细胞(4 h-period)状态。数据以三个独立实验的平均值±标准差表示。* * *:p < 0.001。
丙酸氟替卡松(FP)对体外培养的人非囊性纤维化(non-囊性纤维化)白细胞介素(IL)-8 (a, b)、IL-6 (c, d)释放的浓度影响及激活后正常t细胞表达和分泌(RANTES) (e, f)的调控(a, c, e)与ΔF508 homozygous cystic fibrosis (CF) bronchial epithelial cells incubated for 2 h (b, d, f). Control (Cont.) non-CF and CF bronchial epithelial cells were maintained either in basal growth medium alone (○) or with铜绿假单胞菌脂多糖(LPS)(1.0µg·毫升-1;□)。Non-CF and CF bronchial cells were pretreated with FP for 2 h with (•) or without (▪) the addition of铜绿假单胞菌LPS (1.0 µg·mL-1) 4小时。数据分别以对照组和非对照组支气管上皮细胞的百分比表示。数据代表三个独立实验的平均值±标准差,每个实验条件重复进行。*:p < 0.05;**:与单独或合用基础生长培养基相比,p<0.01铜绿假单胞菌LPS增加。
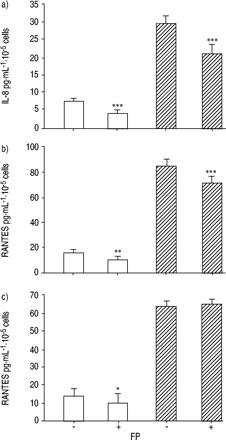
CF和非CF支气管上皮细胞暴露于FP的时间为10-8 M for a 16-h incubation period resulted in a significant decrease of IL-6 and IL-8 production (fig. 3a and b⇓)。与非CF支气管上皮细胞相比,CF支气管上皮细胞中RANTES分泌未见明显减少(图3c)⇓)。
细胞因子白细胞介素的水平(IL)-8,IL-6和调节活化作用,表达和分泌由非囊性纤维化释放(RANTES)正常T细胞(非CF:□)和纯合的ΔF508囊性纤维化(CF:└它们暴露于丙酸氟替卡松(FP)之后)支气管上皮细胞(10-8 M ) for 16 h (+). Data are presented as mean±sd of three separate experiments in which each condition was carried out in duplicate. *: p<0.05; **: p<0.01; ***: p<0.001, compared with the medium without FP (−).
丙酸,一种本构的有效抑制剂囊性纤维化支气管上皮细胞的核factor-κB激活
因为大多数促炎细胞因子基因包括il - 6和引发包含κB-binding图案在基因的启动子区域,作者调查了是否抑制细胞因子表达的FP (10-8米,16 h)是由于减少NF-κB激活。
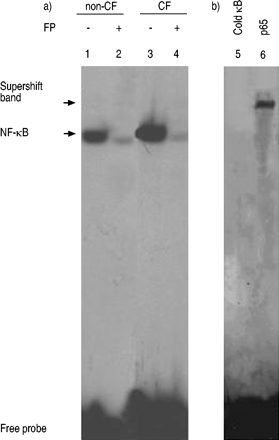
电泳迁移率变动分析从未经刺激-CF支气管上皮细胞中收获的核提取物的(EMSAs)证明活化的NF-κB(图的高的组成水平。图4a⇓(3)进铜绿假单胞菌LPS刺激非CF支气管其中观察到(图4A NF-κB的激活上皮细胞⇓,泳道1),FP治疗显着降低铜绿假单胞菌LPS诱导的NF-κB结合活性(图4A⇓,泳道2相比泳道1)。无内源性的NF-κB结合活性在未受刺激的,非CF发现支气管上皮细胞,如先前报道24(数据没有显示)。暴露的CF支气管上皮细胞FP的差别导致了强烈的对这些NF-κB(图4⇓,泳道4)。的NF-κBDNA结合竞争试验中被证实的特异性。从静息CF支气管细胞与100倍过量的未标记的(冷κB)的NF-κB寡核苷酸导致的结合活性(图完全抑制核提取物温育。图4b⇓,泳道1)。该NF-κBDNA结合蛋白复合物的组分通过用抗体对NF-κB的p65亚基执行超迁移测定法来确定。正如图4b所示⇓, p65抗体的加入引起了超移(图4b)⇓,泳道2)。
核因子(NF)-κB结合活性铜绿假单胞菌lipopolysacharide (LPS)刺激non-cystic纤维化(non-CF)支气管细胞(a,车道1),如果ΔF508纯合子的囊性纤维化(CF)支气管上皮细胞(a,巷3)孵化卡松丙酸(FP) (10-8 M) for 16 h (a, lanes 2 and 4, respectively). To demonstrate the specificity of binding of the NF-κB oligonucleotide, a 100-fold M excess of unlabelled NF-κB (b, lane 5, cold κB) was used to compete with the labelled NF-κB probe. The addition of antibody to RelA (p65 subunit) component (b, lane 6, p65) caused a supershift, as indicated. This figure is representative of three experiments.
丙酸氟替卡松诱导核因子抑制剂-κB-α表达
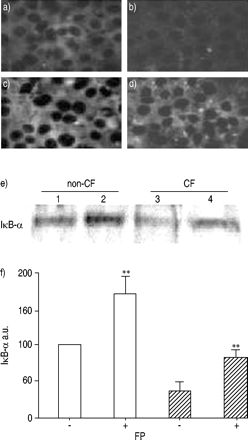
IκB-α的表达缺失或FP (10-8M, 16 h)分别在CF和非CF支气管上皮细胞中分析。结果表明:增加IκB-α发生在non-CF支气管上皮细胞的细胞质FP治疗后(图5所示⇓)。与未经处理的CF支气管上皮细胞相比,没有检测到免疫反应性观察IκB-α,FP治疗允许的感应和维护IκB-α表达CF支气管上皮细胞(图5⇓)。这些结果通过显示该IκB-α水平在FP处理的CF支气管上皮细胞,通过光密度分析评价升高到IκB-α水平的60%的未治疗的非CF支气管上皮细胞(图发现Western印迹进一步证实。5E⇓)。These results, which agree with the EMSA data (fig. 4·),表明本构NF-κB激活检测与FP CF减少支气管上皮细胞治疗通过诱导和胞质IκB-α的维护。
在非囊性纤维化核因子κB(IκB-α)蛋白的胞质抑制剂的表达(非CF:□)和ΔF508纯合囊性纤维化(CF:└)之前(A,B)和它们的曝光后支气管上皮细胞到丙酸氟替卡松(FP)(10-8M) 16 h (c, d),免疫荧光显示。等量的蛋白质提取从non-CFΔF508纯合子CF细胞治疗与FP与否进行分析水平的IκB-α西方墨点法使用特定抗体IκB-α(e)。光密度分析数据结合三个类似的研究(f),表示在任意单位(a.u)。密度测量结果报告为IκB-α水平相比的百分比从未经处理的non-CF支气管腺体细胞(e,巷1)。一个代表三个独立实验的实验。* *:p < 0.01。
丙酸减少IκB-α/β激酶蛋白表达
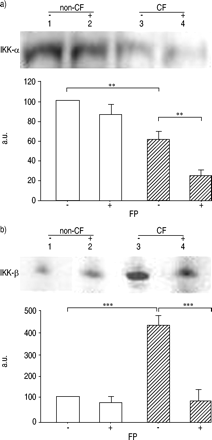
确定的IκB-αCF和non-CF支气管腺体细胞FP治疗前后相关的水平IKK-αIKK-β表示,西方能够从CF进行细胞提取物和non-CF支气管腺体细胞培养在没有或FP (10-8米,16 h)。IKK-α水平相比,基础水平的升高IKK-β被发现在CF支气管上皮细胞(增加4.5倍)与观察non-CF支气管上皮细胞。一致的增加水平IκB-α抑制剂FP治疗后(图6所示⇓),FP诱导显著减少IKK-α和IKK-β激酶在CF和non-CF支气管上皮细胞(图6 a和b⇓)。有趣的是,在CF IKK-β水平的数字化的Western印迹的图像分析FP处理后支气管上皮细胞显示IKK-β(降低80%),以类似的水平的显着降低在未处理的非CF支气管上皮细胞中发现(图6B⇓,泳道4相比泳道1)。
的抑制剂的表达核因子κB激酶(IKK)-α和非囊性纤维化(非CF:□)IKK-β蛋白的水平和ΔF508纯合囊性纤维化(CF:└)它们暴露于10后支气管上皮细胞-8 M fluticasone propionate (FP) for 16 h, as demonstrated by Western blotting (a and b). Equal amounts of protein extract from non-CF and ΔF508 homozygous CF cells treated with or without FP were analysed for the levels of IKK-α and IKK-β kinases. Densitometric analyses of the data combined with three similar studies, are expressed in arbitrary units (a.u.). Densitometric results are reported as percentage of IKK-α and IKK-β protein levels compared with those obtained from untreated non-CF bronchial epithelial cells (a and b, lane 1), respectively. The figure shows one representative experiment of three independent experiments. **: p<0.01; ***: p<0.001.
讨论
目前的研究结果表明,FP降低了未刺激和刺激后IL-6和IL-8的产生铜绿假单胞菌LPS刺激非CF和CF患者的支气管上皮细胞。在CF支气管上皮细胞,这减少FP il - 6和引发生产与强烈的本构NF-κB激活,减少胞质IκB-α抑制剂积累的增加和减少IKK-α和IKK-β激酶表达,IKK-β特别明显。
在这项研究中铜绿假单胞菌LPS用作炎症刺激,以增加所述促炎细胞因子的释放,并模仿气道上皮的炎症反应。近日,Escotte等。25已经描述了一个体内轻度炎症的异种移植模型中,并表明,FP减少LPS诱导的IL-8释放。很少有研究侧重于IκB蛋白在LPS刺激后肺调节。Mizgerd等。26最近报道说,LPS诱导IκB-α和IκB-β的时间依赖性一个显著的损失,但他们并没有研究抗炎药物的效果。
相反,IL-6和IL-8的非CF和CF气道上皮细胞的降低后的FP,在FP处理后的CF支气管上皮细胞中观察到RANTES生产的弱还原。一些作者已表明RANTES表达的诱导要求在初级上皮细胞NF-κB的活化27的,而其他人已经表明RANTES和IL-8基因表达被不同地通过NF-κB调节的28。在目前的研究中,缺乏FP影响咆哮CF上皮细胞的表达表明,NF-κB以外的信号通路可能牵涉其中。Dhawan等。29最近鉴定了新的NF-κB诱导丝裂原活化蛋白激酶(MAPK),其参与IKKs和NF-κB的活化信号转导途径。在本研究中,MAPK信号传导可能在休息状态和FP处理后调节在CF支气管上皮细胞中的NF-κB依赖性方式表达RANTES。进一步的调查是必要的,以证实这一假说。
在CF患者中,支气管上皮细胞产生大量趋化因子IL-8的,甚至在不存在细菌感染的6,24和抗炎性细胞因子IL-10的生产的较低水平的30.因此,支气管上皮细胞是抗炎分子,尤其是吸入类固醇的一个重要靶点。如前所述,FP是一种具有抗炎活性的甾体,其特点是对甾体结合位点的高亲和力31。它被描述为比其他糖皮质激素更有效,如丁烯酮和倍氯米松。在压抑NF-κB激活肺泡上皮细胞32,33。在本研究中,我们证明了FP在一定浓度的FP(10)下具有最大的抗炎作用-8 M) in both non-CF and CF bronchial epithelial cells. Previously the authors had reported that dexamethasone (DEX) used at higher concentrations (10-7-10年-5M)不能显著降低CF中IL-8的产生,但不能显著降低非CF支气管上皮细胞中IL-8的产生24。FP比DEX更强的原因可能与FP的亲脂性和其糖皮质激素受体(GR)的高亲和力有关。
为了进一步鉴定,通过该FP发挥其抗炎作用的潜在分子靶点,所述NF-κB/IκB-α途径,已知可用于大多数促炎症细胞因子的基因的表达的主要信号传导途径,进行了调查。据证实,在本研究的第一个时间,即CF支气管上皮细胞内,FP大大降低NF-κB活化,其与平行胞质IκB-α抑制剂的水平升高。此外,还表明FP减少两者IKK-α和IKK-β的表达水平,特别是用于CF IKK-β(由4.5倍的减少),但不能在非CF支气管上皮细胞。进一步的研究将需要在基因表达水平来表征IKK-α/β激酶和IκB-α的电位变化,提高的分子机制上CF FP动作的理解(前和/或转录后机制)和正常的支气管上皮细胞。
在这项研究结果表明,基底的IKK-βCF支气管上皮细胞过度升高,支持的假设机制导致IKK-β表达改变在CF的规定,这一现象可能与持续的炎症过程描述CF气道疾病。缺乏胞质IκB-β抑制剂以前报告的作者在CF支气管上皮细胞体内和在体外24部分可能是介导内生IKK-β水平升高。众所周知,NF-κB激活的关键步骤之一是由两个IκB IκB-α抑制剂的磷酸化激酶,IKK-αIKK-β,导致其退化34。通过促炎性刺激物激活IKK的机制仍然定义不清35。介导其激活响应不同刺激的生理IKK激酶的身份是紧张调查的主题36。这已经很好地认识到,只有体内IKK-β而不是IKK-α需要NF-κB的活化35。迄今为止,尚不清楚为什么CF支气管上皮细胞表现出升高内源性IKK-β表达式,仍有待确定FP如何减少IKK-βCF支气管上皮细胞中表达。IKK激酶可能被上游水平的受体激活,导致IKK磷酸化。一些潜在的IKK激酶可能参与了这种激活35。进一步的研究是必要的,以澄清是否IKKs的上游,即NF-κB-inducing激酶和MAP激酶可能FP行动的分子靶点。
本资料显示,丙酸氟替卡松作为核因子κB活化的两个非囊性纤维化和囊性纤维化支气管上皮细胞的负调节物。该数据还表明,升高的囊性纤维化支气管上皮细胞可能参与这种调节的内源性核因子抑制剂-κB-β激酶表达找到。作者假设的支气管上皮细胞中改变的核因子抑制剂-κB-β激酶表达可能代表负责异常炎症反应,囊性纤维化的特征的可能机制。可能是作为核因子κB活性的部分还原的负调节和白介素-6和-8生产的后续失调的结果。患者bronchectasis,它已经表明,吸入丙酸氟替卡松降低痰炎性介质的水平37。在囊性纤维化患者中,丙酸氟替卡松没有引起大多数肺部炎症参数(痰白细胞计数、髓过氧化物酶活性和超氧阴离子释放)的显著变化。这可能与丙酸氟替卡松未能穿透囊性纤维化气道黏液衬里有关38。在活的有机体内,concentrations of inhaled fluticasone propionate (1 mg·day-1)估计在人肺组织> 17h的纳米级范围内39。在本研究中,丙酸氟替卡松的相关浓度为10-8 M for 16 h) reduced the negative regulator of the nuclear factor-κB activation and subsequent interleukin-6 and -8 production, by bronchial epithelial cells of cystic fibrosis patients. Further work is now required to determine whether the在体外本研究的观察结果可以转化为囊性纤维化患者的临床意义。
致谢
笔者衷心感谢S.伯努瓦优秀的技术援助。
- 收到了2002年4月17日。
- 公认2002年12月17日。
- ©ERS期刊有限公司