摘要gydF4y2Ba
本研究旨在观察超敏性肺炎(HP)患者肺泡淋巴细胞的凋亡情况。研究了HP患者和正常未暴露对照。gydF4y2Ba
HP患者的淋巴细胞凋亡百分率明显低于正常患者(37.4±3.4)gydF4y2Ba与gydF4y2BaAnnexin V和丙啶碘检测方法为56.5±5.5%,0.4±0.1gydF4y2Ba与gydF4y2Ba1.0±0.2%的dUTP切口末端标记技术(TUNEL))。HP患者的支气管肺泡灌洗(BAL)淋巴细胞Fas抗原阳性的比例明显高于正常人(71.7±5.4)gydF4y2Ba与gydF4y2Ba50.4±9.0%)。而两组间Fas配体(FasL)阳性的BAL淋巴细胞比例差异无统计学意义。患者和正常人BAL液中可溶性Fas (sFas)水平分别为80.5±8.5 pg·mLgydF4y2Ba−1gydF4y2Ba和23.2±3.1 pg·毫升gydF4y2Ba−1gydF4y2Ba,分别。在所有受试者中,BAL淋巴细胞的百分比和sFas水平之间存在正相关,但在单独的研究组中没有发现。HP患者肺淋巴细胞中诱导的抗凋亡基因Bcl-xL产物的胞内数量明显高于对照组,而构成性抗凋亡蛋白(Bcl-2)的胞内数量无差异。gydF4y2Ba
综上所述,超敏性肺炎患者肺淋巴细胞凋亡较正常人低。这至少可以部分解释为可溶性Fas(抗凋亡基因)和Bcl-xL的增加。gydF4y2Ba
过敏性肺炎(HP)是一种由抗原引起的肺部炎症性疾病,表现为免疫调节被破坏,导致大量淋巴细胞在肺部积聚gydF4y2Ba1gydF4y2Ba.有三种可能的机制(不是相互排斥的),淋巴细胞在HP肺部积聚:1)增加募集gydF4y2Ba2gydF4y2Ba;2)本地扩散gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba4gydF4y2Ba;3)生存率增加(细胞凋亡减少)。本研究探讨HP患者肺淋巴细胞凋亡减少的问题。gydF4y2Ba
在对抗外来抗原的免疫反应中,免疫活性细胞的克隆扩增是有效保护的必要条件。为了维持组织内环境的稳定,这些细胞最终必须死亡gydF4y2Ba5gydF4y2Ba.因此,细胞存活的调节对于限制潜在有害细胞在肺部的积累至关重要。细胞凋亡是一种生理的、基因控制的细胞对外界和内部刺激的反应,其目的是消除不需要的细胞,同时防止对周围细胞或组织的损害gydF4y2Ba6gydF4y2Ba.细胞凋亡通常与Fas抗原(Fas或CD95)及其生理配体(FasL或CD95L)通过细胞间相互作用的交联有关gydF4y2Ba7gydF4y2Ba.这一途径可被可溶性Fas (sFas)抑制。gydF4y2Ba8gydF4y2Ba.这些相互作用通常涉及炎性细胞死亡的调节,特别是淋巴细胞gydF4y2Ba9gydF4y2Ba.CD4+ t细胞凋亡主要由Fas引起,CD8+ t细胞死亡主要由肿瘤坏死因子1型受体(TNFR1)和2型受体(TNFR2)引起。gydF4y2Ba10gydF4y2Ba.gydF4y2Ba
Bcl-2基因家族通过促凋亡(Bax, Bcl-xS)和抗凋亡产物(Bcl-2, Bcl-xL)的平衡调控凋亡过程gydF4y2Ba11gydF4y2Ba.一些细胞因子也能影响细胞凋亡。例如,白介素-2可以抑制炎症细胞凋亡gydF4y2Ba12gydF4y2Ba.这种细胞因子在HP中上调gydF4y2Ba13gydF4y2Ba.gydF4y2Ba
涉及淋巴细胞存活的另一个机制是B7-CD28共刺激途径。CD28是淋巴细胞携带的分子,是抗原提呈细胞(APC)上B7-1和B7-2受体的配体,如肺泡巨噬细胞gydF4y2Ba14gydF4y2Ba.CD28刺激可通过淋巴细胞增加Bcl-xL的表达和IL-2的产生gydF4y2Ba15gydF4y2Ba.最近的研究表明,B7-CD28共刺激通路参与HPgydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba.因此,这一途径可能通过上调某些淋巴细胞特异性抗凋亡因子来促进淋巴细胞在HP中的积累。gydF4y2Ba
假设HP患者肺部淋巴细胞的聚集可能是由细胞凋亡减少引起的,本研究对正常人和HP患者通过支气管肺泡灌洗(BAL)恢复的肺淋巴细胞凋亡进行了量化和表征。gydF4y2Ba
材料和方法gydF4y2Ba
主题gydF4y2Ba
我们研究了39名新诊断的HP患者(均为非吸烟者)和40名未暴露于HP抗原的非吸烟者。其中32例为农民肺(gydF4y2BaSaccharopolyspora rectivergulagydF4y2Ba),三名加湿器发热(gydF4y2Ba青霉菌gydF4y2Basp.),两份含有鸟肺(鸟类蛋白),一份含有泥炭苔HP (gydF4y2Ba青霉菌gydF4y2BaSp)及一名有锯木厂粉尘暴露者(gydF4y2Ba拟青霉属gydF4y2Ba).所有病人在灌洗前都与抗原有接触,没有人在手术前接受过皮质类固醇。此外,没有患者有潜在的肺部或其他疾病。在本研究中,每个实验对象至少参加了一次测试。HP的诊断是基于以前发表的标准gydF4y2Ba1gydF4y2Ba.拉瓦尔医院(魁北克,加拿大)伦理委员会批准了这项研究,所有受试者都签署了知情同意书。gydF4y2Ba
支气管肺泡灌洗gydF4y2Ba
标准纤维镜检查获得BAL。HP患者取0.9%无菌生理盐水300 mL, 50 mL等量滴注于肺叶中部或舌部。由于正常受试者的BAL淋巴细胞数量较低,他们接受了双重灌洗(右中叶240ml,舌部240ml)。依次抽吸每个等份,测量恢复的体积。BAL细胞用Hank平衡盐溶液洗涤,在roswell Park Memorial Institute 1640培养基(Canadian Life Technology, Burlington, ON, Canada)中重悬,补充10%胎牛血清和1%青霉素-链霉素,并用血细胞计计数。BAL细胞存活率(台台蓝除外)为90-99%(平均95.9%)。对不同的炎症细胞(淋巴细胞、巨噬细胞、中性粒细胞和嗜酸性粒细胞)进行鉴别计数,用Diff-Quik染色的细胞旋制剂(Baxter Diagnostics, Mississauga, on, Canada)。采用标准方法,采用尼龙-羊毛柱分离BAL淋巴细胞gydF4y2Ba18gydF4y2Ba.使用这种技术,平均92%的纯淋巴细胞被回收(范围85-95%)。gydF4y2Ba
膜联蛋白V和丙啶碘gydF4y2Ba
根据制造商的说明,使用凋亡检测试剂盒(R&D System, Minneapolis, MN, USA)对BAL细胞进行染色。使用EPICS®ELITE ESP流式细胞仪(Beckman-coulter, Miami, FL, USA)对细胞进行细胞分析。每次试验至少计数10,000个细胞。采取了适当的控制措施。膜联蛋白阳性和碘丙啶阴性的细胞被认为是早期凋亡细胞。gydF4y2Ba
实验室建设gydF4y2Bainsitu公司gydF4y2Badeoxyribonucleicacid碎片gydF4y2Ba
采用末端脱氧核苷转移酶(TdT)介导的dUTP刻痕末端标记技术(TUNEL),重组TdT (rTdT)对多聚甲醛固定的风干细胞自旋制剂进行染色。gydF4y2Ba19gydF4y2Ba.在检测中,细胞旋制剂在4%多聚甲醛的磷酸盐缓冲溶液(pH 7.4)的新鲜溶液中固定30分钟。然后用PBS洗涤玻片两次,并在渗透溶液(0.1% Triton X-100和0.1%柠檬酸钠)中置于冰上(4°C)孵育2分钟。用PBS再次洗涤后,样品周围的区域干燥和20µL酶溶液(0.3 U rTdT (Canadian Life Technology), 6×10gydF4y2Ba−10gydF4y2BaM生物素-16- dutp (Roche Diagnostics Canada, Laval, QUE, Canada), 0.1 M卡可迪酸钾(pH 7.2), 2×10gydF4y2Ba−3gydF4y2BaM CoClgydF4y2Ba2gydF4y2Ba、2×10gydF4y2Ba−4gydF4y2BaM二硫苏糖醇),并在样品上放置盖玻片。在37°C的湿室中孵育60分钟。在PBS洗涤三次后,13.5 nM的共轭荧光染料streptavidine-Alexa 488gydF4y2BaTMgydF4y2Ba(Molecular probes, Eugene, OR, USA)加入20µL滴液中,4°C避光保存20分钟。延长gydF4y2BaTMgydF4y2Ba使用抗褪色试剂盒(分子探针)(根据制造商的协议)安装载玻片,以避免荧光猝灭。阴性对照用酶缓冲液代替rTdT,阳性对照在酶液孵育前立即用5U的Dnase 1 (Amersham Pharmacia Biotech, Piscataway, NJ, USA)预孵育。使用表面荧光显微镜(尼康Eclipse 6600;尼康加拿大公司,魁北克,QE,加拿大)与适当的过滤器(尼康过滤器B2-A,例如:450-490,em: 505)。每张幻灯片上至少有300个细胞被计数。采用两种标准鉴定阳性细胞(凋亡晚期):1)细胞核上明亮的绿色荧光;2)凋亡细胞的形态特征。gydF4y2Ba
抗体gydF4y2Ba
异硫氰酸荧光素标记的Bcl-2/100gydF4y2Ba1gydF4y2Ba抗人Bcl-2-FITC), D×2(小鼠IgGgydF4y2Ba1gydF4y2Ba、抗人CD95-PE (Fas)、NOK-1(小鼠IgG)gydF4y2Ba1gydF4y2Ba抗人CD95L-PE (FasL))、2H12(小鼠抗人Bcl-xL)、HIT3a(小鼠IgGgydF4y2Ba1gydF4y2Ba抗人CD3-PerCP)和同型对照(小鼠IgG)gydF4y2Ba1gydF4y2Ba-FITC,老鼠免疫球蛋白gydF4y2Ba1gydF4y2Ba-PE和小鼠IgGgydF4y2Ba1gydF4y2Ba- perp)购自Pharmingen (San Diego, CA, USA)。gydF4y2Ba
流式细胞术检测Fas、FasL和Bcl-2gydF4y2Ba
总共2.0×10gydF4y2Ba6gydF4y2Ba用200µL PBS+1%牛血清白蛋白重悬BAL细胞。一批细胞(5×10gydF4y2Ba5gydF4y2Ba细胞·50gydF4y2Ba−1gydF4y2Ba用抗cd3的2µL或同型对照的2µL标记,置于冰(4℃)保存45 min。同样的方法用于标记细胞样本1.0×10gydF4y2Ba6gydF4y2Ba用cd95(2µL)、cd95l(2µL)和特异性同型对照。其余单元格(5×10gydF4y2Ba5gydF4y2Ba使用商业试剂盒(Perm kit;在与抗bcl -2抗体及其特异性同型对照(2µL抗体,置于冰上45分钟)孵育前。gydF4y2Ba
支气管肺泡灌洗液中可溶性Fas的测定gydF4y2Ba
根据制造商提供的方案,使用OptEIA Human Fas试剂盒(Pharmingen),采用夹心式酶联免疫吸附试验(ELISA)对BAL液中的sFas进行定量。gydF4y2Ba
Western blot样品的制备gydF4y2Ba
总共1×10gydF4y2Ba6gydF4y2BaBAL淋巴细胞纯化nylon-wool列和resuspended 20µL(裂解缓冲(10毫米Tris-HCl (pH值7.4)),150毫米氯化钠,2毫米乙二胺四乙酸(EDTA), 2% triton x - 100、1%的混合物的蛋白酶抑制剂(2毫米EDTA, 2毫米polymethylsulfonyl氟化物,1µg·毫升gydF4y2Ba−1gydF4y2Ba抑肽酶1µg·mLgydF4y2Ba−1gydF4y2Ba20µL的2×上样缓冲液(200mm Tris HCl (pH 6.8), 20%甘油,2%十二烷基硫酸钠(SDS), 0.0005%溴酚蓝,10% 2-巯基乙醇)。100℃加热5 min使混合物变性,10000 ×离心gydF4y2BaggydF4y2Ba1分钟,以沉淀样品中的磷脂。取上清液(40µL) -70℃冷冻备用。gydF4y2Ba
Western blot检测Bcl-xLgydF4y2Ba
样品(1×10gydF4y2Ba6gydF4y2Ba用12%聚丙烯酰胺凝胶(sds -全氟碳相关气体交换(PAGE))分离并转移到聚偏二氟乙烯膜上。在室温下用阻断缓冲液(5%脱脂奶粉,0.05% tween 20在tris缓冲盐水中)阻断印迹1小时,用1:100稀释的Bcl-xL单克隆抗体检测1小时。次级探针(阻断缓冲液1:100),与山羊IgG抗鼠IgG辣根过氧化物酶(Cedarlane, ON,美国),采用增强化学发光(Amersham Pharmacia Biotech)化学发光检测。以肺泡BAL巨噬细胞为阳性对照。密度分析使用Scion Image (Scion cooperation, MO, USA)进行。gydF4y2Ba
统计分析gydF4y2Ba
除非另有说明,结果以平均值±sem表示。除以下情况外,所有数据均采用t检验进行分析:1)发现BAL淋巴细胞百分比与sFAS分子浓度之间存在相关性,使用Spearman秩相关检验;2) Mann-Whitney u检验阳性淋巴细胞比例。p值<0.05被认为是显著的。gydF4y2Ba
结果gydF4y2Ba
在两组受试者中,男性和女性的比例没有差异。HP受试者的平均年龄高于正常受试者。各组受试者各种BAL炎症细胞的百分比和数量与之前发表的相似gydF4y2Ba16gydF4y2Ba(表1gydF4y2Ba⇓gydF4y2Ba).分别测定39例HP患者中28例和40例正常对照组中14例的淋巴细胞CD4:CD8比值。HP患者的比值范围为0.1 ~ 10.6均值±sd(2.0±2.8),正常对照组的比值范围为0.3 ~ 5.1(1.7±1.2)。两组间无显著差异。这一结果与安藤的发现相一致gydF4y2Ba等gydF4y2Ba.gydF4y2Ba20.gydF4y2BaCD4:CD8比值不是描述HP患者BAL淋巴细胞群的良好参数。gydF4y2Ba
过敏性肺炎(HP)患者与正常对照的特征及支气管肺泡灌洗gydF4y2Ba
HP组的BAL淋巴细胞Annexin+/PI-明显低于正常组(37.4±3.4%,n=18)。gydF4y2Ba与gydF4y2Ba56.5±5.5 (n=15), p=0.004;图1一个gydF4y2Ba⇓gydF4y2Ba).为了证实这一结果,我们用TUNEL法检测了一组被试的BAL细胞的胞旋。HP患者的BAL淋巴细胞TUNEL阳性较健康者少(0.4±0.1%,n=9)。gydF4y2Ba与gydF4y2Ba1.0±0.2 (n = 7), p = 0.033;图1 bgydF4y2Ba⇓gydF4y2Ba).每项实验均包括阳性和阴性对照。阳性对照(用脱氧核糖核酸(DNA)预培养的细胞)给予100%的阳性细胞。阴性对照(无TdT的TUNEL试验)给予0%的阳性细胞。gydF4y2Ba
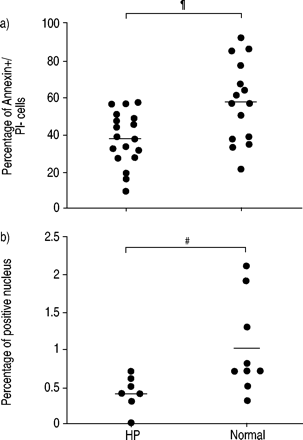
超敏性肺炎(HP)患者和正常人支气管肺泡灌洗及淋巴细胞凋亡的评价。a)采用Annexin V和碘化丙啶(PI)双探针技术检测早期凋亡细胞数量。b) dUTP刻痕和标记技术用于评估凋亡的最后阶段。实线表示平均值。gydF4y2Ba#gydF4y2Ba: p = 0.033;gydF4y2Ba¶gydF4y2Ba: p = 0.004。gydF4y2Ba
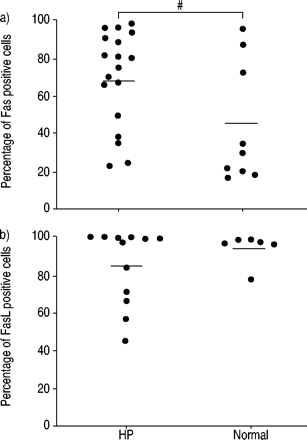
如图2a所示gydF4y2Ba⇓gydF4y2Ba其中,HP患者的Fas阳性淋巴细胞百分率比正常人高约50%(68±5.4% (n=18), 46.7±9.0 (n=9), p=0.004)。这一结果与Agostini的数据一致gydF4y2Baet al。gydF4y2Ba21gydF4y2Ba.测定FasL阳性淋巴细胞的比例。如图2b所示gydF4y2Ba⇓gydF4y2Ba结果表明,HP患者与正常对照组的FasL阳性淋巴细胞比例分别为84.9±5.7 (n=12)和95.6±3.2 (n=6),差异无统计学意义(p=0.23)。gydF4y2Ba
超敏性肺炎(HP)患者和正常人支气管肺泡灌洗淋巴细胞a) Fas和b) Fas配体表面受体阳性的百分比。实线表示平均值。gydF4y2Ba#gydF4y2Ba: p = 0.004。gydF4y2Ba
HP患者BAL液中sFas的含量是正常人的3倍多(80.5±8.5 pg·mL)gydF4y2Ba−1gydF4y2Ba(n = 23)gydF4y2Ba与gydF4y2Ba23.2±3.1 (n = 14), p = 0.0001;图3gydF4y2Ba⇓gydF4y2Ba).BAL液中sFas浓度与fas阳性淋巴细胞比例无相关性(数据未显示)。在所有受试者(HP +正常)中,观察到BAL淋巴细胞百分比与sFas浓度呈正相关(RgydF4y2Ba2gydF4y2Ba= 0.38, p = 0.0001;图4gydF4y2Ba⇓gydF4y2Ba).随着BAL淋巴细胞数量的增加,sFas分子的增加是可以预期的,因为这些细胞是这种分子的主要生产者。负相关(RgydF4y2Ba2gydF4y2Ba= 0.24, p = 0.0058;图4 bgydF4y2Ba⇓gydF4y2Ba)在淋巴细胞百分比和细胞凋亡百分比之间(Annexin/PI试验)。然而,在单独的研究组中,相关性并不显著。此外,sFas浓度与细胞凋亡百分率无相关性(数据未显示)(Annexin/PI检测)。gydF4y2Ba
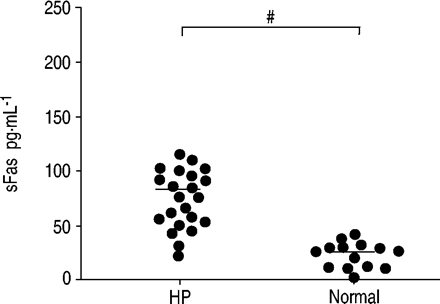
超敏性肺炎(HP)患者和正常人支气管肺泡灌洗液中可溶性Fas的定量分析。实线表示平均值。gydF4y2Ba#gydF4y2Ba: p = 0.0001。gydF4y2Ba
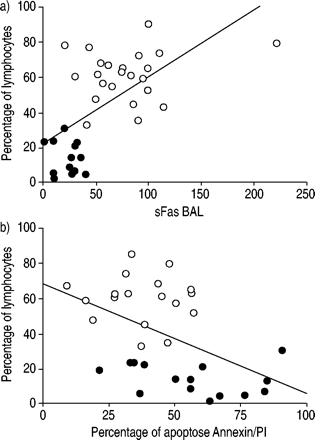
支气管肺泡灌洗(BAL)淋巴细胞增多与a)可溶性Fas (sFas)浓度和b)膜联蛋白V (Annexin V)和碘丙啶(PI)细胞百分率的相关性。〇过敏性肺炎(HP)患者;•:正常。实线表示平均值。gydF4y2Ba
Bcl-2蛋白阳性淋巴细胞比例(74.4±7.71%)无统计学差异(n=6)。gydF4y2Ba与gydF4y2Ba93.1±2.8 (n = 5), p = 0.066;图5gydF4y2Ba⇓gydF4y2Ba).然而,细胞内Bcl-xL水平(图。6 a和bgydF4y2Ba⇓gydF4y2Ba)比正常人增加2.5倍以上(9.9±3.3 (n=6))。gydF4y2Ba与gydF4y2Ba3.8±1.9 (n = 7), p = 0.03;图6 bgydF4y2Ba⇓gydF4y2Ba).图6gydF4y2Ba⇓gydF4y2BaWestern blotting结果具有代表性。测量采用Scion Image密度测量软件,单位任意。gydF4y2Ba
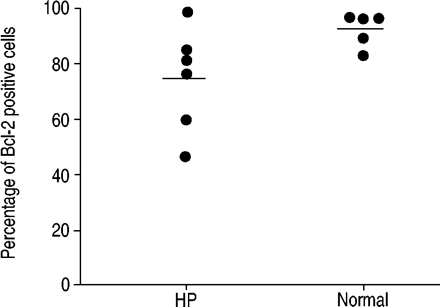
超敏性肺炎(HP)患者与正常人支气管肺泡灌洗淋巴细胞Bcl-2阳性的比例实线表示平均值。gydF4y2Ba
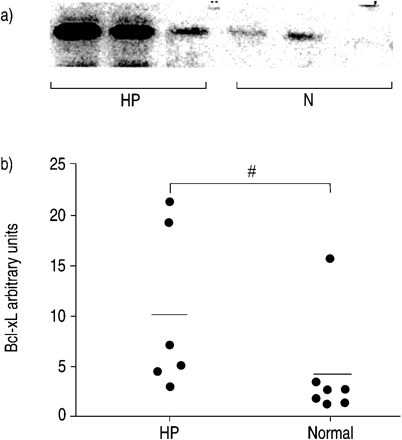
定量测定超敏性肺炎(HP)患者和正常人支气管肺泡灌洗淋巴细胞中Bcl-xL蛋白。a) Western blot检测Bcl-xL蛋白条带的代表性结果显示,3例HP患者的Bcl-xL蛋白表达高于3例正常对照组。b)采用密度测量软件(Scion Image)对条带进行定量。gydF4y2Ba
讨论gydF4y2Ba
本研究表明,通过两种不同的技术,与正常人相比,HP患者的BAL淋巴细胞凋亡减少。因此,HP的淋巴细胞增多特征至少部分可以通过减少肺淋巴细胞的凋亡来解释。gydF4y2Ba
该结果不能量化细胞凋亡在HP肺炎症维持中的相对重要性,但提示它可能是一个重要的因素。虽然所有的测试都没有对每组所有受试者的BAL细胞进行,但所进行的研究清楚地显示了组间的显著差异。gydF4y2Ba
凋亡淋巴细胞的减少和Fas阳性细胞数量的增加起初似乎是矛盾的。与Fas表达相关的预期较高的凋亡百分比可能被可溶性Fas浓度的增加和细胞内Bcl-xL的增加所掩盖。Fas/FasL的结扎是一种细胞间的相互作用,通常涉及细胞凋亡的开始。sFas与FasL结合,因此限制了活化淋巴细胞上促凋亡受体的数量gydF4y2Ba22gydF4y2Ba.sFas的脱落是一种炎症机制,通过免疫系统可以延长肺淋巴细胞的生存能力,这似乎是HP发生的情况。Fas/FasL启动细胞凋亡失败的可能性不能消除。例如,在培养的淋巴细胞(Jurkat型)中过度生产Bcl-2蛋白可抑制fas诱导的细胞凋亡gydF4y2Ba23gydF4y2Ba.此外,在表达Fas的MCF7细胞(体液上皮细胞)中过量产生Bcl-xL,使这些细胞能够抵抗Fas诱导的凋亡gydF4y2Ba24gydF4y2Ba.gydF4y2Ba
虽然本研究证实HP患者肺淋巴细胞表达的Bcl-xL高于正常人,但细胞内Bcl-2水平是否升高尚不清楚。阳性细胞可能含有未知数量的Bcl-2(检测限为最大浓度)。需要Western blot技术进一步评估Bcl-2蛋白在减少HP细胞凋亡中的作用。gydF4y2Ba
HP患者BAL淋巴细胞内Bcl-xL水平升高可能与共刺激增加有关gydF4y2Ba通过gydF4y2BaB7-CD28通路。事实上,如前所述,HP中这一通路是不受调控的。已知共刺激B7-CD28的增加可增加对淋巴细胞凋亡介导的抵抗力gydF4y2Ba通过gydF4y2Ba细胞内Bcl-xL蛋白的增加和IL-2的表达增加,IL-2是这些细胞的生存因子gydF4y2Ba15gydF4y2Ba.gydF4y2Ba
本研究结果提出了一个有趣的问题,即HP中BAL淋巴细胞凋亡的减少是否由于细胞本身的内在调节和/或由于收集它们的肺微环境。肺环境中除Bcl-xL和sFas外,可能存在其他抗凋亡因子参与淋巴细胞凋亡的降低。gydF4y2Ba
需要进一步的研究来阐明HP控制淋巴细胞存活的机制。微环境的影响将需要gydF4y2Ba在体外gydF4y2Ba研究抗凋亡细胞因子对BAL淋巴细胞的影响。例如,纯化的HP患者和对照组的BAL淋巴细胞可以用Fas激动剂和IL-2培养,以及时评估这些不同刺激对淋巴细胞凋亡的影响。还需要进一步的工作来调查这些发现与HP发展的相关性,因为已经表明,淋巴细胞增多也会发生在没有症状的暴露个体的肺部gydF4y2Ba25gydF4y2Ba.gydF4y2Ba
结论gydF4y2Ba
本研究表明,淋巴细胞凋亡的减少可能与过敏性肺炎肺泡淋巴细胞增多有关。这些淋巴细胞增加存活率的潜在机制包括高水平的可溶性Fas,增强的Bcl-xL,以及肺中存在抗凋亡细胞因子。gydF4y2Ba
致谢gydF4y2Ba
作者谨向G. Tremblay和M. Laviolette表示感谢,感谢他们的有益讨论。gydF4y2Ba
- 收到了gydF4y2Ba2001年10月2日。gydF4y2Ba
- 接受gydF4y2Ba2002年10月2日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba