抽象的
睡眠呼吸暂停综合征(SAS)是血管疾病和中风的已知风险因素。结构性脑损伤,作为公开神经功能缺陷或更巧妙的是认知功能障碍,是SAS的常见症状。脑损伤的生化标志物的存在在SAS中对于筛选甚至小脑损伤并监测治疗的效率,对SAS具有很大的益处。
因此,在10名轻度SAS患者(50.8±9.9 YRS,呼吸扰动指数(RDI)18±3.6,动脉氧饱和度最低(minS.啊,一个2)80.5±4.06%)和9例严重SAS(50.3±11.5 YRS,RDI 75.4±21.7,minS.啊,一个256.56±14.58%),使用市售的测定以前和睡眠地测量血清特异性烯醇酶(NSE),S-100β蛋白和β-痕量的血清浓度。
只能发现正常范围内的血清水平,与血液何时或SAS的程度无关。
由于无神经症状或先前脑血管事件的患者睡眠呼吸暂停综合征引起的结构脑损伤可能太小而无法产生S-100β的可测量增加,神经元特异性烯醇酶和β-痕量血清浓度或亚临床脑损伤可能在较低的范围内使用的分析方法的检测限。需要生化标志物和更灵敏的方法,用于检测睡眠呼吸暂停综合征的小脑损伤。
睡眠呼吸暂停综合征(SAS)的特征是,由于上呼吸道间歇性狭窄或阻塞,在睡眠期间反复出现呼吸障碍,伴有重复的低通气和呼吸暂停阶段以及打鼾。除了心血管并发症的发病率增加外,伴有连续缺血性卒中的血栓栓塞和血流动力学事件也是SAS的可能后果1,脑缺血是SAS患者的主要风险之一2.
结构脑损伤,表现为明显的神经缺陷或微妙的神经心理功能障碍,是SA的常见症状3..尽管可以通过临床检查和放射性成像技术容易地确定中风的解剖和功能程度,但大多数大脑都是智力沉默的,并且在检测更细微的脑损伤如认知缺陷的情况下存在固有的困难。研究基础上采用的神经心理学测试的电池需要专家员工来执行它们,这是持续的,不适合临床实践。因此,脑损伤的生化标志物的存在将在SAS中具有很大的好处。
已经基于各种蛋白质的测量水平开发了几种监测技术,包括神经元特异性烯醇酶(NSE),肌酸激酶BB,髓鞘碱性蛋白质,胶质纤维酸性蛋白质,白细胞介素-6,转化生长因子-β和S-100β蛋白质4.-9..然而,在大多数研究中,这些物质只能在脑脊液中测定10并且仅通过腰椎穿刺收集CSF样品仅针对严重病例中的诊断目的表明,与并发症的风险有关。由于采样程序引起的污染也可能影响CSF中所有标记的浓度11.因此,反映了轻微缺血性损伤的潜在的非血清血清标志物引起了关注。测量脑血管胁迫或脑损伤的蛋白质标记物的血液水平可以允许在相对较低的风险下进行频繁测试,因此在SAS中可用于估算脑损伤的可能程度,检测脑卒中的高危患者,选择此类患者更积极的治疗和监测治疗效率。
血浆腺苷以前曾用于SAS患者作为低氧血症的标志物12后来发现,在颈动脉内膜切除术中,它也是脑缺血的敏感指标13.然而,在腺苷水平和局灶性脑损伤之间没有发现相关性,并且腺苷的血管舒张抑制作用也可能参与脑血流量的爆发波动。此外,方法论困难限制了其在常规临床实践中的使用。其他生物化学标志物的低氧血症或诸如胆红素等氧自由基反应的指标14或循环鸟苷一单磷酸盐15可能对脑损伤过度特异性或直接受SAS相关扰动的直接影响,例如右侧心力衰竭或肾功能不全15.目前,据报道,血液中的S-100β蛋白和NSE的测量是最合适的非侵入性方法16.
术语“S-100”描述了由两个亚单位组成的二聚体蛋白质家族,称为α和β。已知三种异构体。S-100a(αβ)存在于神经胶质细胞和黑素细胞中,S-100b(ββ)存在于中枢和周围神经系统的神经胶质细胞和雪旺细胞以及郎格罕细胞和垂体前叶细胞中。S-100a0(αα)占大脑S-100蛋白的5%,主要存在于慢抽搐骨骼肌、心脏和肾脏的神经系统之外17.
在头部创伤,脑缺氧,脑出血和缺血性卒中后,已在各种形式的急性脑损伤中观察到CSF和血清中S-100的升高5.那7.那8.那10那18-20.以及颅内肿瘤和传染性损伤21-23.因为只有低水平的这种蛋白质通常存在于血清中,所以在对大脑的结构损伤后血清中S-100的存在可能是由于被坏死胶质细胞的选择性泄漏到CSF中,通过受损的脑血液障碍。因此,S-100ββ异构体的升高血清浓度与经过验证的脑损伤相关4.那20..
脑细胞含有大量糖酵解酶烯醇化酶,NSE被定义为γ-γ同工酶亚单位。NSE构成∼总烯醇化酶亚单位的75%。它主要存在于神经元中,位于细胞质中,在神经内分泌细胞中浓度较低。然而,它也存在于其他几种组织中24那25并作为神经母细胞瘤和燕麦细胞癌的肿瘤标记物25.在头部损伤,人类,人类全身缺氧之后增加血清NSE和对中枢神经系统的各种侮辱(CNS)7.-9.那19那26.此外,因为红细胞和血小板含有相当大量的NSE,所以通过样品收集诱导的溶解可能会干扰NSE测量24.
β-痕量是主要的CSF蛋白,显示在结构上,酶促和免疫学相同,与前列腺素-D合酶(PGD)27.PGD已在覆盖脑表面,脊髓和大型脑内血管以及动物和人类中的脉络丛和少偶突胶质细胞的裂缝中28.它用作诸如睡眠唤醒循环,体温和神经递质释放等几种中央动作的神经调节剂28最近发现,它还与健康人类的睡眠调节有关29. 脑卒中发病后患者脑脊液中β-trace水平升高30.,也可以在脑血管疾病患者的血清中检测β-痕迹31.,可能指示修复过程。
在这项研究中,对血液中S-100β蛋白、NSE和β-trace蛋白水平的系列测量进行了评估,以确定它们是否可用于检测神经系统检查正常且既往无神经脑血管事件史的SAS患者的轻微脑损伤。
材料和方法
研究科目
19名男性患者的年龄范围为32-64 YRS(平均50.6 YRS)。参加该研究的每位患者接受大脑的神经学检查和计算断层扫描(CT)。患有脑梗塞,出血,头部创伤或CNS感染的患者,入院前6个月或CNS肿瘤的患者被排除在研究中。患者均未具有先前神经事件的明确历史,如短暂性缺血性发作(TIA),长期可逆缺血性神经缺陷(PRIND)或中风。所有人都有正常的肾功能。所有受试者都在精神病学和心理治疗部门,大学·哥廷根或普通医院普通医院普及医院的睡眠实验室进行了研究。
本研究由当地研究道德委员会批准,并从每位患者获得书面同意。
方法
睡眠分析
通过使用标准方法的国际指南,通过隔夜多核园诊断SAS诊断出夜间。32.那33.:标准多导睡眠图监测脑电图、左右眼电图、心电图、颏下肌电图和胫前肌肌电图。通过测量通过热敏电阻的鼻腔和口腔气流来评估呼吸参数。用两条电感式容积描记带同时测定由呼吸力引起的胸部和腹部呼吸偏移。手指脉搏血氧仪(Biox 37003;Ohmeda,东京,日本)用于连续测量动脉血氧血红蛋白饱和度。通过红外视频监控检测身体位置和运动。所有记录都记录在多导睡眠描记器(日本东京,日本)上,并存储在个人计算机系统中。
实验室方法
在睡前不久的晚上23:00,在睡前23:00,在醒来后立即获得血样两次,然后在06:00 H觉醒后立即。在血清中进行以下分析:S-100β,NSE和β-痕量蛋白。在包括标准的批量中进行测定,并测量所有样品两次。考虑了进一步分析的平均值。对于S-100β蛋白,NSE和β-痕量测量,使用了足够敏感以检测健康对照受试者的S-100β,NSE和β-痕量的方法。
使用免疫溶胶测定试剂盒(Lia-Mat®SangtecTeCl100; Bromma,Sweden)测量S-100β蛋白的血清浓度。Sangtec100测量由三种单克隆抗体SMST 12,SMSK 25和SMSK 28所定义的蛋白质S-100的β-亚基。用于检测和计算,使用了一个发光分析仪(BYK Sangtec,Diezenbach,德国)。该测定的检测限为20 pg·mL-1.在280 pg·ml-1,定义的分析内变异系数(CV)为5.5%,分析间变异系数为10.1% (LIA‐mat®Sangtec100产品信息)。正常健康对照组血清中S‐100β水平≤0.11µg·L-1(LIA‐mat®Sangtec100产品信息),该信息与作者实验室建立的截止值相对应34..
血清NSE水平由COBAS核心NSE酶免疫测定(EIA)试剂盒测定Hoffmann-La Roche Ag(瑞士巴塞尔)。这种固相三明治EIA使用单克隆和多克隆抗NSE。健康志愿者身上的血清NSE的正常范围为3.3-13.3 ng·ml-1,平均值±SD为6.9±2.2 ng·mL-135..
血清中的β-痕量由自动Behry Nephelometer分析仪上的免疫晶骨测定(Behringwerke Ag,Marburg)测定。测试试剂盒采用与胶乳颗粒偶联的亲和纯化的多克隆兔抗体,足够敏感(分析敏感性为0.05 mg·l-1)可靠地测量血清浓度。之前已经报告了β-微量分析的有效性数据36..
分析
手动确定睡眠阶段和唤醒数据并附上个人计算机系统存储的数据。对心肺功能障碍的评估包括RDI,MinS.啊,一个2,去饱和指数(S.啊,一个2-i)对于整个夜晚和晨动血压(BP)。
数据表示为算术平均值±SD。对组和时间差异的统计分析基于对各方差(ANOVA)的分析,对每个获得的参数重复测量。两组之间的统计学比较也使用0.05水平的T检验进行。
结果
所有患者的NSE血清浓度范围在3.7-33.6 ng·mL之间-1.两名患者,每组中的一个患者在健康志愿者的正常范围内始终增加NSE血清浓度。只有两名轻度SAS患者在睡眠前的值相比,早上显示出来。
在15名患者中,S-100β蛋白的血清浓度低于测定的检测限(0.02μg·l-1).在所有患者中,S-100β的血清水平在正常范围内。只有两名严重SAS患者在早晨S-100β中略有升高。
SAS中的血清β-痕量的范围为0.29-1.32 mg·l-1.在4例轻度SA患者中,早晨增加了血清β-痕量浓度> 10%,而3例严重SAS的患者在睡眠前的价值观(表2)比较的情况下会降低> 10%(表2⇓).
NSE的血清浓度(ng·ml-1),S-100β(μg·l-1)和β-痕量(mg·l-1)没有显着差异,与血液(B之前或睡眠(a))或SAS的程度(表2)无关(表2⇑).与RDI (rNSE / B.=−0.0028 rNSE / A.=−0.3081,rβTrace/ B.= 0.1982,rβTrace/ A.= 0.1517)。NSE和β -痕量血清浓度与RDI之间的关系如图1所示⇓.
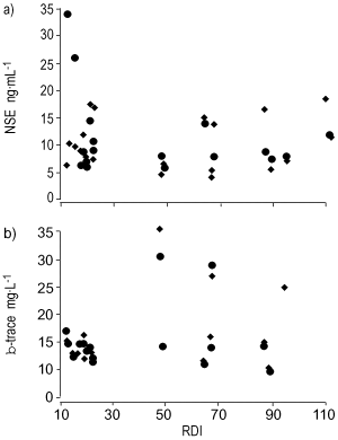
脑损伤生化指标的关系。a)神经元特异性烯醇化酶(NSE)和b)根据血液采样时间的呼吸紊乱指数(RDI)测定睡眠呼吸暂停综合征β‐trace和严重程度。♦:睡觉前;•:在睡眠。
然而,两次温和和严重SAS之间的β-痕量血清浓度的统计比较显示严重SAS中较高水平的趋势:严重SAS 0.62±0.33 mg·L.-1,在轻度SAS 0.45±0.06 mg·L.-1(在单侧t‐测试中p=0.06)。
讨论
在没有神经系统症状或先前脑血管事件的轻度和严重的SAS患者中,可以发现神经元标记NSE的血清浓度,星形痛标记S-100β蛋白或脑膜标记物β-痕量蛋白质没有升高。这些患者中的SAS引起的结构脑脑损伤可能太小,不能产生可测量的这些标记物的血清浓度或亚临床脑损伤的血清浓度可以定位在这里使用的分析方法的较低检测限范围之外。然而,需要SAS中脑损伤的生化标记,因此进一步调查需要更敏感的方法。
几种脑脊液标志物,包括S-100β蛋白和NSE,可以作为脑损伤程度的敏感标志物。对神经病变患者脑脊液中S-100β蛋白和NSE浓度的研究表明,中枢神经系统细胞损伤程度与脑脊液中这些蛋白浓度之间存在定量关系8.那10那18. 临床上,在缺血性卒中后不久发现脑脊液和血液中NSE水平升高,大多数缺血性卒中、脑内出血和蛛网膜下腔出血患者的脑脊液和血清中S-100蛋白浓度升高7.那8.那20.那37..还有报道称,血清中较高的NSE水平与大梗塞体积相关联9..与对照受试者相比,患有急性脑梗死的患者显然升高了S-100和NSE的血液水平。
关于小型结构脑损伤,只有小梗塞患者的CSF S-100β略微增加4.或短暂性脑缺血发作和轻微卒中后脑脊液S‐100水平无升高8.已报告。此外,在任何患有小的皮层下梗死的患者中,血清中的S‐100蛋白都无法测量6..然而,在从患者患者患者患者患者患者患者患者中汲取的20%样品中,已经检测到血清浓度的血清浓度增加38.在健康对照组中测定了血清S‐100蛋白7.那39..这些不同的结果可能是由于用于测定血液中S - 100蛋白的分析方法的低检出限不同。小梗死和短暂性缺血发作后NSE升高8..在轻微的头部受伤的患者中也发现了NSE的增加9..没有证据表明卒中的其他危险因素,例如糖尿病或高血压以及主体年龄或性别,影响S-100或NSE的血液水平7..
由于脑梗死缺乏规定,所研究的生化标志物不能被分开被视为脑缺血的诊断工具,但它们确实表明CNS中的任何细胞损伤。因此,目前的作者认为,两个或更多标记结果的组合可以提高其有用性和可靠性。分析这些标志物的另一个原因是灰色和白质损伤之间的可能性,因为S-100β主要存在于主要在神经元中的胶质细胞和NSE中23,而β-痕迹用作脑膜标记。
虽然睡眠呼吸暂停增加了几种机制,但最重要的是具有潜水脑血管疾病的动脉粥样硬化的患病率越来越多,并且血液灌注的栓塞风险增加和显着的血液动力学变化。假设TIA只代表一种温和的可识别脑缺血形式,这项研究的一个目的是调查在没有先前TIA的历史中发生结构脑损伤,使用缺血局灶性脑损伤的外周标记发生。SAS患有持续性神经心理学缺陷的患者,尽管存在适当的非连续正气道压力处理,但也被排除在本研究之外,以避免与任何其他原始的可能脑损伤混合而不是SAS。
由于连续低氧血症和可能的脑损伤,在未治疗的严重SAS患者中,星形胶质细胞或神经元的完整性无法恢复。特别是,早晨快速眼动睡眠的比例增加通常与呼吸障碍的增加相对应。因此,在标记物的生物半衰期内,在睡眠后的早晨立即采血似乎是检测脑组织损伤的合适方法。据报道,NSE在血清中的半衰期为~ 48小时40因此,只要梗塞损伤继续和脑组织就会洗掉梗塞损伤,就预期NSE的血液水平将会上升。肾脏通过肾脏消除血浆S-100ao,其生物半衰期为2小时41..因此,必须通过持续释放来维持升高的血清浓度。随着时间的推移,随着时间的推移,S-100β蛋白的增加表明,通过血脑屏障的不可逆转破坏,S-100的逐步释放到循环中。
尿液收集和生化标记的测量可能是检测细微变化的有用方法,但由于肾功能障碍,SAS的限制15.S-100蛋白的原发性肾脏排泄将允许从过夜或晨尿中取出测量,但首先必须建立这种方法。
本研究中SAS患者的血清生化指标仅在正常范围内,与采血时间无关。这些标志物在SAS中也不占优势,而这些标志物可以区分灰质和白质或脑膜损伤。因此,可以预期,只有明确的神经元梗死,包括至少部分半暗带的破坏,才会导致细胞外S‐100β、NSE或β‐trace的增加。胶质细胞或神经元的渗漏必须伴随着血液- CSF屏障的功能损害,以允许S - 100β和NSE从脑组织运输到血管腔室。梗死面积也显著影响S‐100β和NSE的释放,可能是SAS引起的结构性脑损伤太小,无法产生可测量的血清S‐100β蛋白或NSE的增加。亚临床脑损伤也可能位于所使用的分析方法的检测下限之外。相反,由于所研究的患者没有神经学上的迹象或症状,他们可能没有小的结构性脑损伤。
本研究的另一个方面是严重SAS患者的血清PGDS有增加的趋势,已知这与睡眠过度有关。PGDS参与人类睡眠调节29,以及一些嗜睡性疾病,如锥虫引起的昏睡病、全身肥大细胞增多症、抑郁症或细菌性脑膜炎,表明PGDS酶或其产物前列腺素D发生变化2在不同的体液中28那36..因此,有必要进一步研究PGDS在睡眠过度中的作用。
独立于低检测限,血液中S-100β,神经元特异性烯醇酶和β-痕量蛋白质浓度的测量并未似乎是检测卒中个体风险和监测治疗在睡眠呼吸暂停中的影响的有用方法耐心。需要进一步调查,特别是在具有不可否认的小脑损伤的受试者中,例如短暂性缺血性攻击或血管痴呆以及睡眠呼吸暂停综合征,通过其他可能更敏感的方法,例如氧化应激或泌尿指数等索引。然而,睡眠呼吸暂停综合征中存在小脑损伤的生化标志。非侵入性生化标记对于临床实践中的特定价值,以筛选小弥漫性脑损伤,表明脑损伤的最终程度和监测治疗的进展和/或效率。
- 已收到2001年6月20日。
- 公认2002年2月11日。
- ©ers Journals Ltd














