抽象的
电子显微镜揭示肺泡上皮细胞死亡,基底覆盖,肺泡在Covid-19患者中的塌陷,塌陷和密封,暗集纤维化引发中的表面活性剂功能障碍和肺泡不稳定性https://bit.ly/38yEX2g
致编辑:
脆弱的肺泡血-气屏障是2019冠状病毒病(COVID-19)的主要靶点。其微结构为由I型和II型细胞组成的肺泡上皮,表面覆盖表面活性剂、薄间质和毛细血管内皮。与严重COVID-19发病机制特别相关的是II型肺泡上皮细胞感染[1.].基于它们作为表面活性剂的生产者和作为两种上皮细胞类型的前体的双重功能,表面活性剂的改变和异常上皮细胞的再生是可以预期的。
尽管已经有一些关于新冠病毒19的病理生理学是急性呼吸窘迫综合征(ARDS)的典型形式还是肺损伤的独特形式的讨论,但作为急性肺损伤和ARDS的组织病理学相关性的弥漫性肺泡损伤(DAD)在新冠病毒19中是一个常见的发现[2.–4.].DAD包括肺泡上皮损伤、水肿形成和表面活性剂改变的早期渗出期(或急性期),以及II型肺泡上皮细胞立方化生和肺泡间隔增厚的晚期增殖期(或组织期),最终导致恢复或纤维化[5.].在爸爸的背景下,强调了崩溃(或Ateelectatic)崩溃的概念,作为纤维化肺肺进展的重要事件[6.–8.].最初的肺泡上皮损伤伴表面活性物质改变,导致肺泡不稳定和塌陷,由于折叠和剥离的肺泡上皮基板“粘连”和折叠的肺泡上的再上皮化而变得不可逆。
崩溃的形态学证据强加沉重,特别是薄肺泡上皮基底层薄膜的追踪需要甚至只能通过透射电子显微镜(TEM)提供的分辨率[8.].在这里,我们报告TEM水平的更改,证明崩溃紧急后验尸来自一名新冠病毒-19患者的样本。该62岁男性患者SARS-CoV-2检测呈阳性,因新发呼吸困难和发热入院,并于1月1日插管 第二天。他接受儿茶酚胺、抗生素、肾脏替代治疗,但没有抗病毒或抗炎治疗。在肺保护性机械通气(呼气末正压16-21)下 潮气量∼6. mL/kg体重;动脉氧张力/吸入氧分数(120–150)和间歇性俯卧位,肺浸润部分消失。13 经过数天的机械通气,患者因突发性感染性休克死亡。
尸检是关于§1sregg的法律依据进行的,是柏林尸检法和德国感染保护法的§25(4)。本研究由Charité - Universitätsmedizin柏林(EA 1/144/927 13)的伦理委员会批准,并符合赫尔辛基的宣言。
灭活潜在传染性的病毒,两大组织样本从右边下叶与3%甲醛固定(从刚准备depolymerised多聚甲醛)在0.1 M甲次砷酸盐缓冲12 h后通过改变固着12 h(建议由罗伯特·科赫研究所后,柏林,德国)。在透射电镜下,26个较小的组织样本被切割,用1.5%戊二醛/1.5%多聚甲醛在0.15 M Hepes缓冲液中固定过夜,然后用1%的OsO后固定4.用0.1%单宁酸浸泡0.5 h,用1%硫酸钠洗涤(均用0.05 M Hepes)。最后样品在乙醇中脱水,环氧丙烷浸渍,Epon包埋。超薄切片(约70 nm)的五个不同的TEM块,用柠檬酸铅反染色,并用Leo 906 TEM(蔡司,Oberkochen,德国)检查。
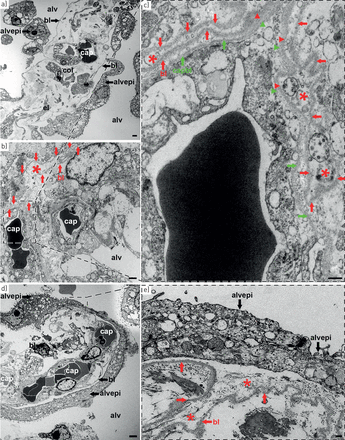
超微结构所见见图1.肺泡间隔因间质水肿而增厚。肺泡上皮被II型细胞覆盖,表明增生试图修复上皮损伤区域。在某些地方,II型细胞向I型细胞表型过渡。肺泡上皮细胞部分肿胀或坏死,游离细胞或相连细胞层脱屑进入肺泡腔内。结果,肺泡上皮基底层在很大程度上被剥蚀。在所研究的5个TEM块体中,均能观察到剥蚀的基底纹层的内褶皱。这些内摺与塌陷的肺泡腔毗邻。在其入口处,这些内折部分被增殖的肺泡上皮细胞所覆盖。
a) 肺泡间隔膜含有毛细血管(cap)和间质,间质含有胶原纤维(col)和弹性纤维(el)。由于间质水肿,隔膜增厚。隔膜两侧的肺泡上皮(alvepi)向肺泡腔(alv)部分分离在脱落部位,肺泡上皮基底层(bl)被剥落。比例尺:2 µm.b)血增厚的肺泡间隔-肺泡腔(alv)中的空气和毛细血管(cap)中的血液之间的空气屏障。注意到剥落的肺泡上皮基底层(bl;红色箭头)内折,肺泡腔塌陷(红色星号)。比例尺:1 µm.c)盒状区域(b)的高倍放大,显示折叠的肺泡上皮(bl;红色箭头)以及部分融合的毛细血管内皮基底层(capbl;绿色箭头)(红色和绿色箭头).毛细血管内皮基底层继续包围毛细血管内皮,而肺泡上皮基底层转向内折的起点,从而与塌陷的肺泡腔接壤(红色星号)。比例尺:250 肺泡间隔带毛细血管(cap)。肺泡上皮(alvepi)显示具有微绒毛的厚细胞延伸,这是II型和I型肺泡上皮细胞表型之间的过渡细胞的特征,因此表明上皮细胞增殖。alv:肺泡腔;bl:肺泡上皮基底层。比例尺:2.5 µm.e)盒状区域的高倍放大(d中)。进入肺泡内折处,肺泡腔塌陷(红色星号),周围有一层剥落的肺泡上皮基底层(bl;红色箭头)。注意两个过度生长的肺泡上皮细胞(alvepi)对入口的“密封”。比例尺:250 纳米。
这个后验尸这里呈现的Covid-19患者的超微结构发现类似于爸爸的先前描述[6.]及特发性闭塞性细支气管炎性肺炎[9],以及在大鼠博莱霉素损伤模型和特发性肺纤维化患者接受肺移植的外植体中发现[8.,10,提示它们是肺泡上皮损伤的共同反应模式。博莱霉素模型在COVID-19的背景下特别有价值,因为它在急性肺损伤后诱导纤维化反应,可以可追踪、可重复和可修订的方式跟踪[11].这些结果可以解释为一系列的事件:肺泡上皮细胞的损伤导致表面活性物质功能障碍和肺泡不稳定,随后出现微肺不张。塌陷的肺泡基板脱落,塌陷的肺泡入口被增生的肺泡上皮细胞封闭,形成增厚的隔膜。其结果是肺泡空气体积的损失和肺泡气体交换面的损失。
在此发现的超微结构改变后验尸患者样本提供了新冠病毒-19肺损伤后可能转变为肺纤维化的形态学证据。尽管患者的机械通气可能有助于DAD的进展[12],急性DAD也见于不依赖机械通气的COVID-19肺炎[2.,4.].如果没有脓毒性休克的发展,这个病人可能存活下来,但发展成纤维化。在博莱霉素肺损伤和纤维化动物模型中,外源性表面活性剂治疗可减弱这种向肺纤维化的转变[13].这表明表面活性剂系统的恢复,例如通过外源性表面活性物质治疗,可能被认为是对新冠病毒-19患者的早期治疗干预。其他人也提出了类似的概念[14,15],符合COVID-19预防性抗纤维化治疗的总体思路[11].
总之,后验尸Covid-19患者的超微结构发现显示肺泡上皮细胞死亡,肺泡上皮基底层膜的剥落,肺泡塌陷和崩溃的损伤。这些改变表明了早期的表面活性剂功能障碍是Covid-19病理生理学中的重要事件。
可共享PDF
确认
由Petra Schrade(电子显微镜核心设施,Charité)提供的专家技术援助得到了高度认可。
脚注
作者贡献:概念和设计:M. Ochs和M. Witzenrath。材料和数据收集:S. Elezkurtaj, D. Horst, J. Meinhardt, F.L. Heppner, S. Weber-Carstens, A.C. Hocke和M. Witzenrath。数据的获取、分析和解释:M. Ochs和S. Timm。手稿起草和/或修改:M. Ochs, S. Timm和M. Witzenrath。最终审定稿:M. Ochs, S. Timm, S. Elezkurtaj, D. Horst, J. Meinhardt, F.L. Heppner, S. Weber-Carstens, A.C. Hocke和M. Witzenrath。
利益冲突:M.Ochs没有什么要披露的。
利益冲突:蒂姆没有什么可披露的。
利益冲突:S. Elezkurtaj没有什么可披露的。
利益冲突:D.霍斯特没有什么可透露的。
利益冲突:J.迈因哈特没有什么可披露的。
利益冲突:F.L.Heppner无需披露。
兴趣冲突:S. Weber-Carstens无需披露。
利益冲突:A.C. Hocke没什么可透露的。
利益冲突:M.Witzenrath报告来自Actelion、Noxon和Quark Pharma的拨款,来自拜耳医疗、Biotest、勃林格·英格尔海姆、Pantherna和Vaxxilon的拨款和个人费用,来自Actelion、Aptarion、阿斯利康、柏林化学、Chiesi、葛兰素史克和诺华的个人费用,在提交的工作之外。
支持声明:M. Ochs获得了德国教育和研究部(BMBF: 01DG14009)和柏林大学联盟(BUA: 501_Elektronenmikroskopie)的支持。A.C. Hocke得到了柏林大学联盟(BUA) GC2全球卫生(冠状病毒前期探索项目)、德国教育和研究部(BMBF: RAPID, Organo-Strat, alvbarrie - covid)、德国研究基金会(DFG: SFB-TR84;B6, Z1a),柏林卫生研究所(BIH), Charité 3R, Charité-Zeiss MultiDim。M. Witzenrath项目由德国研究基金会(DFG: SFB-TR84 C6和C9)和德国教育与研究部(BMBF: CAPSyS (01ZX1304B), SYMPATH (01ZX1906A), PROVID (01KI20160A))资助。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2020年11月12日。
- 认可的2020年12月23日。
- 版权所有©作者2021。
这个版本是在知识共享署名非商业许可4.0的条款下发布的。有关商业复制权利和许可,请联系权限在}{ersnet.org