摘要
肺动脉高压(PH)的定义是平均肺动脉压大于20mmhg,分为五个不同的组,具有相似的病理生理机制、血流动力学特征和治疗管理。放射科医生在PH的多学科评估和管理中发挥着关键作用。基于PH患者成像和/或管理方面的专业知识,以及系统评价方法的经验,弗莱希纳学会内部成立了一个工作组。工作组确定了CT、MRI和核医学在PH评估中的应用的关键问题:一)非侵入性成像能够识别PH值吗?b)成像在确定PH的原因中起什么作用?c)影像学如何确定PH的严重程度和并发症?d)治疗前如何使用影像学来评估慢性血栓栓塞的PH值?e)PH治疗后是否应进行影像学检查?这篇系统综述和立场论文强调了影像学在PH的识别、检查、治疗计划和随访中的关键作用。
摘要
来自Fleischner学会:这篇系统综述和立场论文强调了影像学在成人肺动脉高压的识别、检查、治疗计划和随访中的关键作用https://bit.ly/343kgbN
简介
肺动脉高压(PH)是一种由平均肺动脉压(PAP)大于20mmhg定义的血流动力学疾病,并被分为具有相似病理生理机制、血流动力学特征和治疗管理的不同组[1- - - - - -6) (表1).诊断过程从临床怀疑PH和超声心动图与PH相吻合开始,接着确定临床比较常见的PH组(如2组为慢性左心疾病,3组为慢性肺部疾病),然后区分4组为慢性血栓栓塞性PH (chronic thromboembolic PH, CTEPH),最后诊断为1组肺动脉高压(pulmonary arterial hypertension, PAH),属于排除诊断。
PH分类概述强调了患者管理每个阶段优化方法的必要性。这需要整合成像方式和最新的技术进步。放射学界在PH值评估方面面临着新的挑战。本立场文件的一个重要目标是与PH临床医生共享当前的成像选择,以最佳地利用现有资源。虽然诊断和治疗最好在专门的中心进行,但所有放射科医生都可以在这种疾病的早期识别中发挥更积极的作用,有助于减少诊断的延误。为了达到这些目标,本立场文件着重于一系列与非专家和专家中心相关的问题,强调非侵入性成像(如.CT, MRI和核医学)方法在PH (表2).特别关注慢性毛细血管前PH的成像(第1、3、4和5组)。专家中心可以定义为满足PH转诊中心标准的中心,根据欧洲心脏病学会和欧洲呼吸学会指南(188bet官网地址附录E1中的表E1) [7].
BOX 1缩写
BPA球囊肺血管成形术
慢性血栓栓塞性肺动脉高压
间质性肺疾病
肺动脉
PAH肺动脉高压
肺动脉压
PCH肺毛细血管瘤病
PEA肺内膜切除术
PH型肺动脉高压
PVOD肺静脉闭塞性疾病
右心室
V / Q ventilation-perfusion
框2主要结果
平均肺动脉压大于20mmhg定义为肺动脉高压(PH)。
肺动脉直径不足以作为PH值的独立标准
根据目前的指南,通气灌注肺扫描是PH患者的推荐调查,以排除慢性血栓栓塞性PH
单能CT可提供PH病因的诊断信息,应在诊断策略中发挥更重要的作用
双能CT结合形态学信息和肺灌注(即。碘图),具有提高CT诊断能力的潜力
除终身抗凝外,肺内膜切除术是近端梗阻性病变患者的首选治疗方法;对于不能手术的病例,建议采用或不采用球囊肺血管成形术的药物治疗
心脏MRI已成为判断各种病因PH患者右心室功能的参考标准;一些mri衍生变量,如右心室射血分数,提供独立的预后信息
材料与方法
在Fleischner学会内部成立了一个工作小组,基于成像方面的专业知识(M. Remy-Jardin, M.L. Schiebler, A.N.C. Leung, J.M. Wild, M.M. Hoeper, P.O. Alderson, L.R. Goodman, J. Mayo, L.B. Haramati, Y. Ohno, E.J.R. van Beek, D.A. Lynch和G.D. Rubin)和/或PH患者管理(M.M. Hoeper, M. Humbert和P. Thistlethwaite)以及系统评价方法的经验(C.J. Ryerson)。图书管理员也包括在内(S.L.奈特)。工作组确定了五个关键问题,这些问题集中在CT、MRI和核医学在PH评估中的应用上(附录E2).
PH成像方式概述
用于评估疑似或确诊PH患者的无创成像方式包括经胸多普勒超声心动图、胸部x线摄影、CT、放射性核素通气灌注(V/Q)肺显像和MRI。表2,由A修改而来schaet al。[8],总结了它们的相对优势和劣势。经胸多普勒超声心动图是PH中最广泛使用的无创筛查工具,本立场文件将不进行综述,因为它已在最近的国际指南和PH世界研讨会论文集中得到了讨论[7,9].
尽管胸部x线摄影在本文中没有特别回顾,但它在晚期PH中的作用值得特别提及。在大多数特发性PAH患者中,诊断时胸片异常,显示中心肺动脉扩张,与周围血管修剪形成对照[7].在较晚期的病例中可看到右心房和右心室增大[7].胸部x线摄影可以通过显示肺部疾病或左心疾病引起的肺静脉充血的迹象来帮助鉴别诊断PH。它还可以通过分别显示动静脉比增加和减少来帮助区分动脉和静脉PH值[7].总的来说,任何特定患者的PH值与影像学异常的程度无关。至于心电图,正常的胸片并不排除PH值[7].
问题1:非侵入性成像是否能够识别PH值?
在PH患者中,PAP升高可导致影像学评估的结构、功能和血流动力学改变。大量CT [10- - - - - -14]和核磁共振研究[15- - - - - -18]的研究表明,肺动脉(PA)的绝对或相对大小可以与右心导管测量的PAP直接相关。然而,静态PA尺寸在常规胸部CT研究中用于识别PH值的诊断性能产生了不一致的结果,受试者工作特征曲线下面积(auc)分别为PA直径的0.55 - 0.93和PA直径-主动脉比(以下简称PA比)的0.73-0.95 [10- - - - - -13,19- - - - - -22].
这种可变性可能反映了用于确定PH值存在的诊断标准和参考标准的差异、血管测量技术和应用临界值缺乏标准化所引起的异质性。以及不均匀的患者选择实践,导致研究人群在PH的慢性和严重程度上存在差异。对PA大小截断值的优化选择,以区分PH的存在或不存在,理想情况下将结合健康人群中值分布的知识。年龄越大,性别为男性,体表面积越大,PA大小越大,PA比例随年龄增加而降低[23,24].此外,PA比值不适用于主动脉扩张的情况。基于706名健康美国人的心电图门控胸部CT扫描的测量结果,正常PA直径的90百分位截断值男性为28.9 mm,女性为26.9 mm;男女的PA比值对应的第90个百分位截断值为0.91 [23].在813名健康韩国人中观察到的90百分位PA直径和PA比值截断值,男性分别为31.3 mm和1.05,女性分别为29.6 mm和1.03 [24].
PAP升高的持续时间和严重程度都可能影响相关PA扩张的程度[15].在急性呼吸窘迫综合征(如PAP升高持续时间相对较短)等疾病中,PA直径对PH的检测不可靠[19].慢性轻度PAP升高,如间质性肺疾病(ILD)和慢性阻塞性肺疾病等肺部疾病通常发生在PH中,也可能难以准确诊断,因为正常人群和这些患病人群之间的PA大小测量有重叠[25- - - - - -29].在一项对134名疑似PH患者的前瞻性研究中[30.], PA直径和PA比值对晚期ILD和非晚期ILD患者PH的检测分别表现为较差(auc分别为0.65和0.64)和一般(aus分别为0.73和0.78)。在这项对轻度至中度PH患者的前瞻性研究中(平均PAP, ILD组为32.3 mmHg,非ILD组为37.9 mmHg),血管测量的鉴别性能明显低于一项对489例平均PAP较高患者的回顾性研究(整个队列的平均PAP, 41 mmHg;ILD患者的平均PAP为41 mmHg;非ild患者的平均PAP, 43 mmHg)指的是PH中心[16].在本研究中,ILD组PA直径和PA比值的auc分别为0.87和0.80,非ILD组为0.83和0.79。在ILD组和非ILD组中,PA直径大于29 mm和大于30 mm的应用截断值分别产生了相应的75%和76%的敏感性和89%和73%的特异性。在增强胸部CT检查中增加心室测量,如左右心室内径大于或等于1.2,可提高诊断性能,特别是在PH值为中重度的患者中[21].
Truonget al。[31]推导并验证了一个基于ct的PA直径和PA比率的四级严重程度分类系统(每个测量细分为正常、轻度、中度和严重),用于PH诊断,旨在分别在低和高临界值时最大化测试的敏感性和特异性。使用男性(≤29 mm)和女性(≤27 mm) PA直径的性别特异性正常截断值和性别中性PA比值(0.9),推导队列中正常层的敏感性分别为99%和93%,对应的特异性分别为57%和65%,阴性预测值分别为96%和86%。在最严重的层中,PA直径和PA比率截断值大于34 mm和大于1.1时,特异性分别为98%和100%,相应的敏感性分别为65%和50%,阳性预测值分别为98%和100%。重要的是要认识到,使用四级分类系统的截止值,这些结果是在高危人群中发现的,回顾性登记的228名患者在三级医疗中心接受了疑似PH评估,最终发现有高患病率(60%);PH值明显升高的患者平均PAP (45 mmHg)。在实际情况下,在疾病的患病率和严重程度可能较低的情况下,胸部CT测量这些PA大小以诊断PH值的诊断准确性将受益于前瞻性研究的进一步验证。表3显示了一个经验性指南,当发现PA扩张是一个偶然发现时,根据PH风险的不同阈值。图E1和E2说明在临床实践中对PA直径的解释需要结合临床背景。
在MRI中,动态PA大小测量(PA直径、PA比值、PA面积和PA相对面积变化)在诊断PH时表现出与基于ct的测量相当的性能,auc范围为0.71至0.93 [15- - - - - -18,32].总的来说,MRI的诊断性能优于非心电图门控CT,因为它能够评估和量化额外的心血管结构和功能指标,表明PAP和肺血管阻力增加。这些指标包括室间隔角、右心室射血分数、心室质量指数和PA搏动,据报道,这些指标在有PH值和无PH值的患者之间表现出良好到极好的辨别能力(auc, 0.87-0.99) [32- - - - - -37].所有这些测量也可以通过心电图门控CT实现,但除了在小队列中研究外,尚未对其用于评估PH值进行研究[38].据报道,MRI肺血流动力学定量也具有诊断价值[39- - - - - -42];在一项对233名疑似PH患者的研究中(PH亚组的平均PAP, 45 mmHg),使用心电图门控自旋回波双反转恢复“黑血”序列成像的肺血流异常缓慢引起的伪影的简单视觉评分优于PA直径和PA比率(AUC为0.86)与0.81和0.75)在PH诊断中的作用[35].通过回归分析,Johnet al。[43]已经开发并验证了两种性能相似的多参数心脏MRI模型(auc分别为0.95和0.93),包括室间隔角、心室质量指数、黑血慢流程度(模型1)或舒张PA面积(模型2)。在303例疑似PH患者的验证队列中,模型1诊断PH的敏感性、特异性、阳性预测值和阴性预测值(疾病患病率,85%;平均PAP, 42 mmHg)分别为93%、79%、96%和67%。在临床中评估PH值的实际考虑,详见附录E3.
问题2:成像在确定PH的原因中起什么作用?
在PH潜在原因的分层中,V/Q肺显像在筛查CTEPH中起着关键作用,而CT是主要的成像工具,传统上用于进一步评估PH的潜在原因[7,9].本节提供了一个更新的方法,技术发展和目前的临床方法,PH值管理在常规临床实践。
V / Q闪烁扫描法
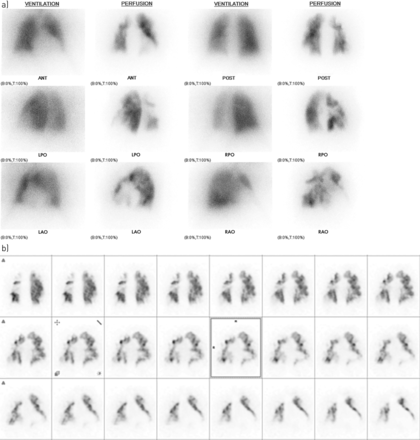
目前的指南规定,应对PH患者进行V/Q肺扫描,以排除CTEPH [7,44].Other than this one indication, V/Q lung scanning is rarely useful in elucidating a cause of PH. The recognition of CTEPH is based on approaches similar to those used for the detection of acute pulmonary embolism, utilising chest radiography with combined V/Q lung scanning techniques.The identification of lung segments and/or subsegments without perfusion but preserved ventilation (即。不匹配)高度提示PE [45].对于有PH且胸片清晰的患者,正常或接近正常的V/Q肺扫描几乎排除了CTEPH,其敏感性为90%-100%,特异性为94%-100% [46,47].不匹配灌注缺陷的存在与CTEPH相容,需要在专家中心进一步检查(图1) [6,7,44].
78岁女性,胸片正常,临床怀疑慢性血栓栓塞性肺动脉高压(CTEPH)。a)平面通气(81m-氪)和灌注(99m-锝大团聚白蛋白)成像显示正常通气肺多节段和亚节段缺损,高度提示CTEPH。b) SPECT灌注图像详细分析冠状面灌注缺损。蚂蚁:前;LAO:左前斜;LPO:左后斜肌;职位:后;RAO:右前斜;RPO:右侧后斜。
PH值的明确终点的重要性需要明确的肺扫描解释。最近,年代爱因斯坦et al。[48]和埃特尔et al。[49]研究了一般患者人群中疑似急性肺栓塞的肺显像,并主张用更明确的方法取代基于概率的V/Q肺扫描解释,即PE的正常、非诊断或异常。同样的策略也被推荐用于ph值患者的诊断工作。与平面肺显像相比,SPECT灌注肺显像可提高检测急性肺栓塞的敏感性[50- - - - - -52].SPECT对PE的敏感性增加主要与检测较小的灌注缺陷有关,如亚节段急性栓塞引起的灌注缺陷。与平面扫描相比,不确定的结果较少。最近一项研究[53]发现SPECT灌注扫描在识别CTEPH阻塞血管段方面比平面V/Q扫描更敏感。在10%的PAH和7.1%的肺静脉和毛细血管高压(肺静脉闭塞性疾病(PVOD)/肺毛细血管瘤病(PCH)患者中,V/Q SPECT扫描报告了与CTEPH中所见相似的不匹配灌注缺陷[54].在大多数PAH患者中,V/Q闪烁是正常的或没有明显异常,并不能帮助区分PVOD/PCH与特发性PAH [55].PVOD/PCH患者异常时最常见的模式为斑块状灌注缺损,其灌注特征与双能CT肺灌注图像相似[56].对74例PH患者的SPECT肺显像与对比增强灌注MRI进行比较:其中30例为CTEPH, 10例为无PH的慢性血栓栓塞性疾病[57].SPECT和MRI对PE的敏感性几乎相同(97% SPECT, 100% MRI)。唯一未被SPECT灌注显像检查的患者为远端CTEPH。SPECT/CT在PE的显像评估中得到了广泛的评价,但在CTEPH的诊断方法中尚未得到广泛的应用。
值得注意的是,如果灌注剂(即。在横膈膜下检测到人白蛋白大团聚物(Tc-99m MAA)的锝标记颗粒,这可能表明存在从右到左的心脏分流。显然,心内分流是引起PAH的重要原因。如果心脏缺陷有从右向左流动的成分,一些Tc-99m MAA颗粒会绕过肺并定位于其他器官(如.肝脏,肾脏,大脑)。这种分流的更明确的诊断是通过获得颅骨侧位视图,这将显示Tc-99m脑内活动。膈下Tc-99m MAA活性也见于有宏观肺内分流的肝衰竭患者(肝肺综合征)、先天性肺动静脉畸形患者(Osler-Weber-Rendu病)以及接受了穴肺吻合手术的患者。
单能CT的作用
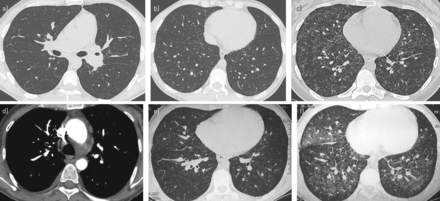
CT扫描速度快,具有良好的时空分辨率,能够全面评价心肺结构,是其显著的特点。根据临床情况,可以考虑CT平扫和增强检查。非对比胸部CT是一种强大的无创检查,适用于肺部疾病(如。慢性阻塞性肺疾病(ILD)是导致血流动力学综合征(即。第3组PH)。在PH亚组中描述的一些不清楚和/或多因素机制的全身和代谢疾病(第5组)也可以从胸部CT无对比检查中获益,如结节病、肺朗格汉斯细胞组织细胞增多症和神经纤维瘤病。在PAH中,肺微血管病变可导致CT上的细微变化,包括小叶中心小结节、周围新生血管和小叶区毛玻璃样衰减。结节性毛玻璃样影、间隔线和腺病高度提示PAH,伴明显的静脉和毛细血管(PVOD/PCH)受累(图2) [58,59].
肺静脉闭塞性疾病(PVOD)/肺毛细血管瘤病(PCH)所致肺动脉高压的CT表现。a) 45岁女性,非对比检查,左右主支气管水平的CT横断面显示双肺小叶中心肺结节,因淋巴结肿大导致左肺门肿大。b)同(a)所示检查,下叶水平CT横断面可见双侧小叶中心结节,右下叶中隔细线。c) 51岁女性,CT平扫下叶水平横断面显示大量结节性磨玻璃样混浊。d) 35岁女性胸部CT血管造影显示纵隔淋巴结肿大。e) 61岁女性患者治疗前无对比检查下叶水平的横切面CT。双肺可见小叶中心结节。f) CT横切面与(e)所示水平相同(同一患者);使用内皮素受体拮抗剂6周后胸部CT平扫显示肺水肿。
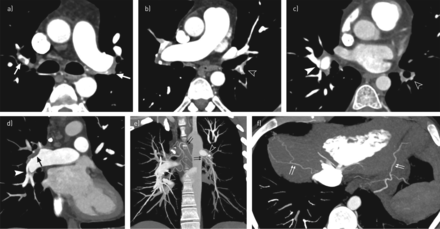
胸部增强CT是第二种基于CT的方法,可用于阐明PH病因。虽然前面引用的PH病因中可描述的形态学变化也可以类似地识别,但增强CT的主要好处是用于检测CTEPH(第4组),其诊断不仅依赖于PAs慢性梗阻的血管征象的描述(图3),也可用于诊断较不常见的疾病,例如纤维性纵隔炎(第5组)(图4)、心内分流、动脉导管未闭、肺静脉回流异常,超声心动图可能会漏诊(组1)。在心血管结构水平上缺乏形态学异常和可评估的PAs,增加了PAH的可能性(组1 PH)。
胸部CT血管造影显示一名25岁男性,双侧急性肺栓塞(PE)后持续呼吸困难1年,提示慢性血栓栓塞性肺动脉高压的中期发展。a-c) CT横切面和d和e)冠状位斜位最大强度投影,f)横切面显示慢性PE的大量血管特征,包括部分充盈缺损(单个白色箭头和单个黑色箭头),腔内带和腔内网(白色箭头),肺动脉严重狭窄(黑色箭头)。存在支气管动脉(图e中黑色双箭头所示)和膈下动脉(图f中白色双箭头所示)的全身侧支供应。左肺叶间动脉再灌注超出梗阻(图(e)中黑色箭头),同侧支气管动脉肿大。
Images show chest CT angiography in a 69-year-old woman with previous history of silicosis, responsible for fibrosing mediastinitis and subsequent development of pulmonary hypertension (PH) (group 5 PH).a and b) Transverse CT sections and c) coronal oblique reformation shows severe stenosis of right and left interlobar pulmonary arteries (arrowheads) by silicotic hilar adenopathy.Diameter of both arterial sections does not exceed 5 mm, responsible for pulmonary hypertension with marked dilatation of mediastinal pulmonary arteries.
在现行指引中[7], CT血管造影与高分辨率CT (即。前者适用于CTEPH患者的检查,后者适用于所有PH患者。该指南承认,一旦确定PH的原因,CT在患者管理中的重要作用,但在CTEPH和非CTEPH患者的分类中,CT没有发挥重要作用。这种情况反映了Tunariuet al。[46],其中比较了早期多探测器CT技术与V/Q扫描技术的准确性。在现在被认为是次优和过时的CT技术中,CT血管造影表现出高特异性(99.3%),但灵敏度低(即。, 51.3%)。最近的元分析[60]评估了CT对CTEPH的诊断准确性,记录了四排和八排多排CT技术与64排多排CT到320排CT或双源CT等最新发展的扫描仪相比的有限诊断价值[47,61,62].在后一类设备中,合并敏感性为99%,特异性为97%,这使得作者得出结论,CT可以成为CTEPH筛查的标准。除了技术方面的考虑,目前CT血管造影在PH诊断方法上的局限性是基于放射科医生在识别慢性血栓栓塞性疾病的CT特征方面的不同专业知识,因此,这一领域显然需要教育和培训。如在表4,对特定的影像学表现进行结构化检查有助于识别CTEPH。在最近的一项研究中,调查了潜在的CTEPH诊断与急性肺栓塞的关系濒死经历- - - - - -Verhaaret al。[63]强调了动脉直径减小、血管内网和镶嵌灌注以及支气管动脉扩张的重要性。
双能CT血管造影的作用
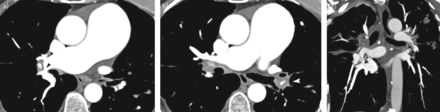
与单能CT相比,双能CT血管造影通过生成碘图提供了额外的诊断能力,碘图被认为是肺灌注的替代标记物。在PH的临床背景下,双能CT肺灌注主要在CTEPH中进行研究,在灌注缺陷的检测上与闪烁成像有很好的一致性[64].双能ct描绘的灌注缺陷也显示出与PH严重程度的血流动力学估计有良好的相关性[65,66].最近,双能CT灌注与V/Q闪烁的诊断价值进行了比较,其敏感性和特异性分别为97% ~ 100%和86% ~ 92% (图5) [61,62].尽管在患者水平上,两种成像方式之间有极好的一致性,但在节段水平上,两种成像方式之间的一致性从中等到中等不等[61,62,64,67],因为它们对远端肺循环的描述不同。灌注闪烁显像显示了标记微球在小动脉水平的分布,而双能CT灌注捕捉到肺实质增强的全体性阶段,因为系统-肺分流有助于灌注闭塞肺动脉段远端的动脉床[68,69].当碘图分析与肺动脉形态的标准CT图像相结合时,双能CT诊断CTEPH的敏感性和特异性为100% [61,62,70].这些有希望的结果需要更大规模的验证,但加强了现代CT技术在CTEPH诊断中的日益重要的作用[71,72].此外,双能CT显示的肺灌注模式可以将PAH与外周形式的CTEPH区分开来,与V/Q显像一致[56].在PH病因的诊断方法中,对不断发展的CT作用的考虑总结在附录E4.
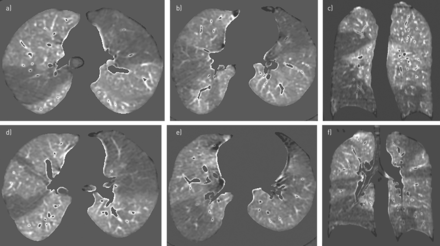
图像显示双源双能CT肺灌注成像,51岁女性慢性血栓栓塞性肺动脉高压(CTEPH)。a-d) CT横切面和e、f)双能CT肺灌注图像冠状面重构(窗口设置:400 HU/40 HU)显示双肺多个不同程度的三角形灌注缺损,高度提示肺血栓栓塞性疾病。
PH患者获取CT血管造影的实际考虑
胸部CT血管造影通常不需要心电图同步,包括薄层容积CT采集。时间分辨率最高的短屏气(1-4秒)采集(即。最短的旋转时间)避免呼吸运动伪象,同时尽量减少心脏运动伪象。整个胸腔应采用单次体积采集扫描,并重建为连续的薄片(≤1mm)。肺部和纵隔图像均应复查。
注射方案基于丸跟踪,有两种选择:一)传统CT肺血管造影检查,感兴趣的区域位于肺干(触发数据采集的阈值,120 HU);或b)并发肺循环和体循环混浊,有一感兴趣区域位于升主动脉(阈值,100 HU)。体积和流速与标准胸部CT血管造影检查所选的相似(即。60-80 mL,流速为4 mL·s−1).当已知肺血管阻力较大时,血流速率(即。2毫升·s−1而不是4ml·s−1),由于造影剂在PAs中进展缓慢,建议采用此方法。在高心输出量、低千伏峰值扫描和高血流率(即。4 - 6毫升·年代−1depending on the patient venous access) are recommended to ensure adequate vascular opacification.
The iodine concentration of the contrast material used usually ranges between 300 mg I per mL and 350 mg I per mL;双能CT扫描时可增加至370-400 mg I / mL,以确保后处理碘图上肺微循环有充分的混浊。Scan acquisition during a systemic arterial phase (即。升主动脉内感兴趣的区域)可能会掩盖由于增强而造成的灌注缺陷通过支气管及/或非支气管全身侧支[68].这种扫描条件可能会影响治疗前对灌注缺陷的评估,但不排除在碘图上充分识别肺栓塞型缺陷[61,62,70].
问题3:影像学如何确定PH的严重程度和并发症?
PH对RV后果的评估
在PH的发展过程中,右心室体积和收缩末期和舒张末期压力有重要的变化。在进行性发展至肺心病(本病的终末期)时,右心室舒张末期容积较大,充盈压力增加,壁厚增加,壁刚度增加,舒张功能障碍加重,打开肺动脉瓣所需的压力最终变为系统上压力,室间隔变平,然后向左心室腔弯曲;这进一步限制了左心室的充血。随着时间的推移,RV应对体积和压力过载的能力被超过。肺心病是一种非常困难的疾病,如果没有积极的治疗,会导致快速死亡。即使使用磷酸二酯酶抑制剂进行最大静脉肺小动脉扩张治疗(如.西地那非),肺心病的致命性只能暂时得到改善。
PAH患者的PH严重程度应结合临床资料进行评估,包括运动试验、生化标志物、影像学(超声心动图或MRI)和血流动力学评估[7].心脏MRI在评估右心室形态和功能方面比超声心动图更准确,还可以测量每搏量和一氧化碳。以下心脏mri测量可预测PH治疗后的预期寿命:右心室收缩末期容积,右心室舒张末期容积指数(合并风险比,1.06;95% ci: 1.00, 1.12;p=0.049),右心室射血分数(合并危险比,1.23;95% ci: 1.07, 1.41;p=0.003)、每搏容积指数、右心室收缩末期容积指数(合并风险比,1.05;95% ci: 1.01, 1.09;P =0.013)、全局纵向应变率、全局周向应变率和左室舒张末期指数(合并风险比,1.16;95% ci: 1.00, 1.34; p=0.045) (附录E1中的表E2) [73- - - - - -80].There is variability in these measures partly due to the wide range of individuals studied and a lack of grouping by disease severity.Obviously, individuals with PH with very mild disease found incidentally will differ markedly from those with severe long-standing PH.
疾病严重程度(轻度、中度或重度)与不同程度的影像学生物标志物紊乱有关。心肌T1映射在PH中可能是唯一的特征。在一项对490名连续患者的研究中,右心室插入点的T1将PH患者与健康个体区分开来,并与室间隔角密切相关[81].
小血管疾病的评估
小血管疾病或肺微血管病变是指ph存在时肺循环的远端改变。而特发性或遗传性PAH的特征是毛细血管前PAs (<500 μm)的重大重塑伴丛状病变,PVOD/PCH优先影响肺小静脉,并可能与肺毛细血管扩张和增生有关[2].In CTEPH, there is growing evidence that, in addition to mechanical obstruction of proximal arteries, some patients develop a pulmonary microvasculopathy affecting the wall of distal muscular PAs out to arterioles and venules [82,83].他们在CTEPH治疗前评估中的描述将在下一节中讨论,题为“问题4:治疗前如何使用影像学评估CTEPH ?”
如前所述,在PAH中,肺微血管病变可导致CT图像的细微变化。在大多数PAH患者中,V/Q闪烁不会显示明显异常,可能是正常的。它不能区分PVOD和特发性PAH [54].异常时,最常见的模式为斑块状灌注缺损,双能CT肺灌注图像也可见[56].数字血管造影、CT血管造影和MR血管造影对肺动脉树的后处理可用于确定分形几何。随着PH值的增加,肺动脉树简化,这种简化可以通过使用三维分形几何来枚举。分形维数计算采用三维盒数距离度量时(如.血管弯曲度的读数),发现它与平均PAP (Spearmanr= 0.60) (84].远端小PA相对于主PA的损失是血管修剪的标志。
PH患者显著PA增大的并发症有哪些?
PAH患者的PA增大可压迫冠状动脉左主干或左前降支,导致冠状动脉血流减少(图6).在一项对765名PAH患者的研究中[85],有心绞痛或类似心绞痛症状121例,根据左主冠状动脉与PA的关系,有94例CT血管造影异常。94例患者中48例左主冠状动脉狭窄大于或等于50%。左主冠状动脉狭窄大于或等于50%的最佳预测因子是PA直径大于或等于40mm。当它发生时,左冠状动脉主动脉压迫对PAH患者来说是一个非常严重的问题。所使用的治疗方案将根据当地的专业知识而有所不同。可选择的方法包括:置入支架、心脏搭桥手术、医疗管理以显著降低pap,偶尔进行肺移植。任何手术都必须仔细考虑,因为ph患者的手术死亡率会增加。对于这个关键问题,没有一种单一的治疗方案总是有效的。
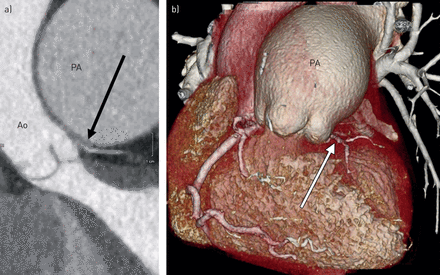
图像显示结缔组织病(硬皮病)所致长期肺动脉高压伴左冠状动脉受压。a)起源于Valsalva左窦的左冠状动脉主动脉多平面重构显示肺动脉块状动脉(PA)压迫(箭头)。b)冠状动脉CT容积成像显示肺动脉干(PA)肿大,左冠状动脉主干(箭头)非常小。Ao:主动脉。
主PA剥离少见,但死亡率高。在最近的系统回顾中[86在1842年以来报道的150例病例中,平均诊断年龄为45岁,男性略占优势(1.1:1)。PA夹层最常见的临床表现为呼吸困难伴胸痛。报道的病因有酸碱度、先天性心脏病(动脉导管未闭等过度循环病变)和后天性心脏病。肺干是73%病例的解剖部位。PA夹层最严重的并发症是心包积血造成的心包填塞,84.2%的病例在尸检时观察到[86].
问题4:治疗前如何使用影像学来评估CTEPH ?
上下文
在0.6%至4.4%的急性肺栓塞中,残余有组织的血栓对PAs的异常持续阻塞,并结合不同程度的显微血管病变,可能导致CTEPH [6,44,63,82].如果不及时治疗,CTEPH会导致右心衰和过早死亡[6,7].近年来,环卫组织的医疗武器库取得了显著进展。正如第六届世界PH研讨会论文集所述,CTEPH管理是一个快速发展的肺血管医学领域,在多学科团队的专家中心进行多模式、个性化的治疗是强制性的[6,7].
目前的CTEPH管理
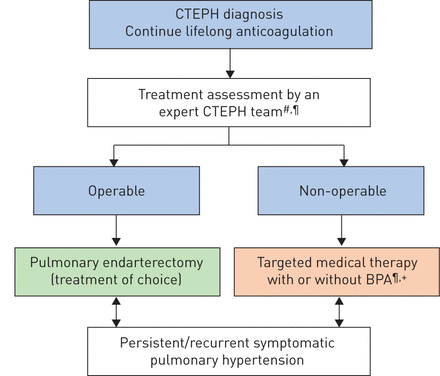
第六届世界PH研讨会(图7) [6].专家中心的CTEPH治疗决策涉及多学科团队,包括经验丰富的肺动脉内膜切除术(PEA)外科医生、球囊肺血管成形术(BPA)介入放射科医生/心脏科医生、肺血管成像经验丰富的放射科医生,以及具有PH专业知识的肺科医生/心脏科医生[6].除了无限期抗凝外,PEA也是因主动脉、大叶动脉、节段动脉和亚节段动脉梗阻性病变而被视为手术候选的患者的首选治疗方法[6,7].然而,大约一半的CTEPH患者在成像时肺血管阻力与血管梗阻程度不成比例,可能表现为严重的远端微血管病变,被认为不适合手术[6].对于技术上无法手术的病例,建议使用PH药物治疗,加或不加BPA [6].口服riociguat(一种鸟苷酸环化酶刺激剂)和皮下treprostinil是目前批准用于不能手术的CTEPH的唯一药物[6,7].
流程图显示了修订的治疗算法管理患者的慢性血栓栓塞性肺动脉高压(CTEPH)。#:多学科(肺内膜剥脱外科医生、肺动脉高压专家、球囊肺血管成形术(BPA)介入专家、放射科医生);¶:治疗评估视乎专业水平而定;+:在某些情况下,可考虑使用无药物治疗的双酚a。转载,经允许,来自参考文献[6].
PEA可操作性评估
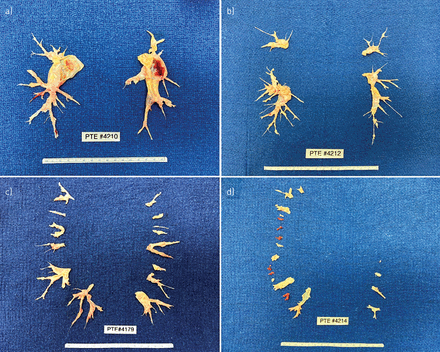
在这种治疗方法中,明确CTEPH病变的解剖分布是至关重要的,某些特征更有可能预测良好的手术结果[6].最重要的外科进展是重新定义了动脉内膜切除术的远端范围[87,88].然而,重要的是要强调,在PEA操作性的适用性方面,手术中心之间不可避免地存在差异[89].不能操作性的标准通常包括远端PA梗阻,肺血管阻力增加与提示微血管疾病的可及闭塞数量之间的不平衡,肺血管阻力大于1500dyn·s·cm5,以及共病[6].CTEPH病变类型和位置可根据最新的加州大学圣地亚哥分校CTEPH手术分类进行分类,包括以下四个级别(图8): 0级(两肺均无血栓栓塞性疾病的证据),I级(病变始于主要PA, IC级对应于一个主要PA完全闭塞),II级(病变始于大叶动脉或主要下行PA), III级(病变始于节段动脉水平)和IV级(病变始于亚节段动脉水平)[87].
图片显示最新的加州大学圣地亚哥分校慢性血栓栓塞性肺动脉高压(CTEPH)手术分类。该图显示了肺动脉内有组织的血栓栓塞物质的位置,影响了其手术可及性:1-3级为可及病变,4级为不可手术。a) 1级疾病累及一条或两条主要肺动脉。b) 2级疾病始于大叶分支或超过上叶动脉起落。c) 3级疾病始于节段性血管。d) 4级疾病始于亚节段血管。
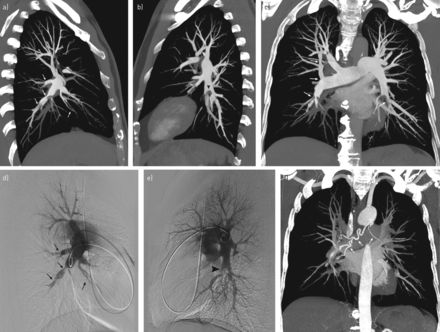
一旦CTEPH确诊,CT血管造影可用于评估可操作性(图9而且10) [6].CT可以为手术规划提供血管路线图,是描述有组织血栓栓塞物质近端范围的最佳方式,具有良好的PEA平面相关性[87].然而,必须强调的是,使用CT来评估手术适宜性需要相当多的影像学专业知识,通常最好由大量和经验丰富的机构进行[6,7,90].由于疾病在一般人群中相对罕见,在CTEPH的CT解释方面,成像界存在很大的知识差距[6].扫描方案遵循胸部CT血管造影的建议。PAs的分析需要结合使用横断面成像和多平面重构,以提高薄腹板和带的检测,局灶狭窄和亚节段血管的显示。数字减影血管造影,以前被认为是参考标准,已在很大程度上被非侵入性方式所取代。随着远端PEA的进步,BPA的出现,以及对远端血管评估的普遍关注,传统的数字减影血管造影可能并不总是适合精细解剖分析。为此,选择性节段血管造影、锥束CT和心电图门控CT也可考虑用于精确勾画远端肺血管[90,91].
a - f)图像显示57岁中枢性和外周性慢性血栓栓塞性肺动脉高压(CTEPH)患者肺内膜切除术前的CT血管造影和肺血管造影评估。CT图像和相应肺血管造影的右肺动脉(a、b)和左肺动脉(c、d)矢状位显示中央和外周动脉CTEPH的大量血管特征。在右肺,箭头指向狭窄和狭窄后扩张、腹膜和血管修剪;在左肺,箭头指向一个大的壁内缺损和下方的腔内网。最大强度投影(冠状面)显示肺动脉期双侧CTEPH血管病变(箭头指向狭窄和狭窄后扩张、腹网和腔内缺损(e))和数据采集后期右侧支气管动脉扩张(箭头(f))。
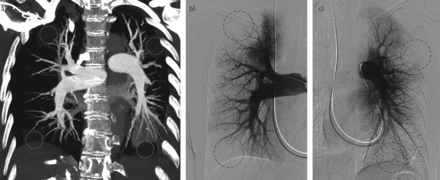
a - c)图像显示一名28岁的周围性慢性血栓栓塞性肺动脉高压患者的CT血管造影和肺血管造影评估。最大强度投影(冠状面)(a)及对应的右(b)、左(c)数字肺血管造影研究正位图。CT血管造影重成像显示周围肺动脉血管修剪,远端灌注不良(虚线圈),血管造影视图显示相应的灌注缺陷(虚线圈)。
成像时发现的机械性梗阻程度与右心导管测量的血流动力学损害严重程度之间通常没有明确的相关性[6].这种差异是由于肺小血管的重塑程度不同[82].在干预前识别肺小血管疾病是非常重要的,因为它会转化为更严重的疾病和更糟糕的结果。不能手术的CTEPH患者有明显的小肺血管疾病,可选择使用或不使用BPA进行药物治疗[6].
支气管动脉肥厚的发展是CTEPH的一个众所周知的特征,反映了体循环和肺动脉循环之间的侧支[6,82,83,92].支气管动脉与毛细血管前肺小动脉之间存在吻合,毛细血管后小静脉与小静脉之间也存在吻合[82].来自体循环的侧支吻合在维持近端PA梗阻下游缺血肺实质的灌注和生存能力方面具有重要作用。一些作者提出,当支气管动脉和吻合口不能发育时,远端血栓形成可能是弥漫性的,危及肺小动脉的开放[83].年代himizuet al。[92]从CTEPH患者的CT血管造影分析中报道了支气管动脉的横截面积与血栓栓塞物质的中心范围相关。在该研究中,近端型CTEPH的支气管动脉总面积明显大于远端型。数字减影血管造影毛细血管期胸膜下灌注差预示可手术CTEPH患者PEA后预后较差[93].胸膜下灌注不良的定义是指,在数字减影血管造影毛细血管期,胸膜侧侧距离胸膜小于或等于1.5 cm(约一根肋骨宽度)。图11).在这种情况下,V/Q肺扫描也显示保留通气的胸膜下灌注减少[94].
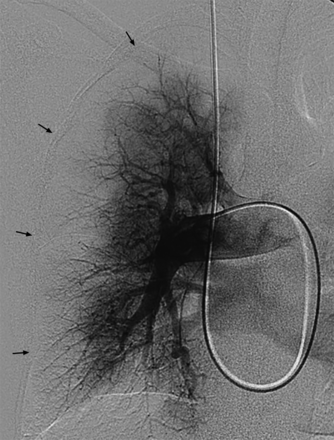
图像显示数字减影肺血管造影(右侧注射),55岁女性,患有不能手术的慢性血栓栓塞性肺动脉高压。血管造影毛细血管期的正位视图,可见胸膜下灌注不良(箭头)。
BPA的评估
双酚a是无法手术的CTEPH患者的替代疗法[95,96].Kawakamiet al。[91他们最近回顾了97例CTEPH患者的500个连续的BPA手术(1936个病变)。病变分布及特征评价如下:A型,环形狭窄病变;B型,腹膜病变;C型,病变次全;D型,完全闭塞病变;E型,病变弯曲。环状狭窄和腹膜病变的成功率较高,并发症发生率较低。全闭塞病变的成功率最低。扭曲病变与高并发症率相关。在诊断不明确的情况下,光学相干断层扫描可能有助于更好地描述血管内病变。 However, experts in BPA rarely use this technique because of the need for high contrast agent volume and the concern for renal toxicity, as well as the requirement for forceful injection that may increase perfusion pressure in the peripheral pulmonary vasculature and cause pulmonary injury [97].
肺血管造影毛细血管期胸膜下灌注不良,提示存在小血管疾病伴弥漫性远端血栓形成,是BPA失败的一个预测因素[94].Taniguchiet al。[94]的结果显示,在不能手术的CTEPH患者中,正常灌注组的支气管动脉总面积大于灌注不良组。支气管动脉发育不良可能与CTEPH患者远端弥漫性血栓形成有关[83].
问题5:PH治疗后是否需要影像学检查?
CTEPH在PEA或BPA之后
CTEPH的所有治疗方式,特别是PEA和BPA的主要目标是改善症状(理想情况下,患者已从CTEPH相关的物理限制中恢复),并改善肺血流动力学,以使静时肺血流动力学正常化或接近正常化。因此,对接受PEA或BPA的患者进行术后评估的最初重点是他们的运动能力(如.6分钟步行试验),休息时血流动力学,右心室功能。PEA手术后,约50%的患者在休息时PA压力降低至小于或等于25 mmHg;另有30%的患者平均PA压在25 mmHg至30 mmHg之间,肺血流动力学基本恢复正常[98].对于BPA,还没有大规模的长期数据,但患者在休息时肺血流动力学达到正常或接近正常的比例低于PEA手术[95,99- - - - - -101].然而,BPA的结果在初始学习曲线后有所改善[96].此外,最近的数据表明,不同的治疗方案可能是互补的;联合治疗方案可显著降低肺血管阻力,最近的Riociguat研究证明了这一点与Balloon Pulmonary Angioplasty in Non-operable Chronic Thrombo-embolic Pulmonary Hypertension, or RACE, study showing added benefit of BPA on top of initial riociguat therapy and反之亦然[102].
PEA或BPA后肺血流动力学的正常化或接近正常化通常伴随显著的症状改善。在达到这些治疗目标的患者中,除了超声心动图外,通常不需要临床随访成像。对于PEA后仍有症状或PH残留或两者都有的患者,需要影像学来确定进一步的治疗方案,如对PEA后周围性CTEPH残留的患者使用BPA [103].传统的数字减影血管造影仍然是最广泛使用的成像工具,用于在首次CTEPH干预后将患者分类为重复PEA或BPA。然而,新型成像工具如锥束CT可以提供更详细的血管结构和梗阻性病变信息[104- - - - - -106].二维数字减影血管造影可定量BPA前后区域肺碘浓度[107].
除了这些临床考虑外,有大量的文献关于CT和MRI评价PEA或BPA后肺灌注、血流量和残余肺血管疾病的程度。
磁共振相位对比成像(phase contrast MRI)已被用于展示BPA前后PA内血流的变化[108].灌注闪烁显像可用于检测PEA或BPA后的残余灌注缺陷,但不足以指导进一步治疗。SPECT肺显像已被描述用于评估BPA后区域肺灌注变化[108].与SPECT相比,双能量CT可以提供更详细的信息和更高的空间分辨率,同时提供血管形态信息。日本的初步研究发现,双能CT对BPA前后区域肺血容量的评估比SPECT成像更可靠[109,110].用双能CT确定区域肺血容量的自动量化也可能是评估区域血流量变化和显示血容量(碘)图中任何新的或残留缺陷的一种选择[111].动态增强MRI灌注成像可提供肺灌注的定性和半定量评估,并有望在CTEPH中定量绘制肺灌注图[112].动态对比增强灌注方法已被用于证明双酚a治疗CTEPH患者的区域灌注参数、区域血流量、区域血容量和平均肺传输时间的改善[113].当与气体通气MRI结合时,延迟增强灌注MRI也被用于评估CTEPH患者PEA前后肺V/Q匹配的改善[114].
在PEA成功后,电影MRI可以显示左右心室收缩末期和舒张末期容积的正常化,心室间期同步的重新建立,心室间隔“向左”弯曲的恢复,以及右心室质量的减少[115- - - - - -117].系列MRI研究表明,PEA术后4周内发生逆转心脏重构,术后3个月和6个月变化不大[118].最近,Maschkeet al。[119]通过MRI证明,PEA后整体右心室功能和左右心室同步性得到改善,但周向和径向功能的恢复存在区域差异。这些发现的临床意义尚不清楚。
双酚a后连续MRI观察Satoet al。[120显示了左、右心室射血分数的改善。在Fukuiet al。[117], mri显示双酚a后右心室功能明显改善,而左心室功能基本不变。右心室收缩末期和舒张末期容积的下降与使用右心导管测量的肺血管阻力的下降密切相关(r= 0.74,r分别为= 0.72;两者p<0.001),再次表明右心室功能的改善紧随后负荷的降低。心脏MRI也被用于证明BPA后心室同步性改善和室间隔心肌T1值增加(恢复到正常心肌T1值)[121,122].
BPA后,结合区域肺实质灌注测量和心脏MRI的MRI研究显示,经BPA处理的肺叶的肺血流量改善,而未经BPA处理的肺叶的肺血流量改善程度较低,与血流动力学和心室质量指数的变化相关[113].心脏MRI研究也被用于预测CTEPH中哪些患者在PEA后会恢复运动能力。MRI显示脑卒中容量反应受损的患者运动受限[123].
Patients with PAH and CTEPH undergoing medical treatments
影像学作为接受药物治疗的PAH或CTEPH患者随访评估的一部分,目前主要集中在心脏。经胸超声心动图是临床应用最广泛的影像学工具,但不是本文的重点。MRI通常被认为是心脏成像的参考标准,因为它提供了高分辨率的三维成像,并允许可靠地量化腔室容量、肌肉质量和血流量,以及心脏的功能评估[124].闪烁显像和CT目前在接受药物治疗的PAH或CTEPH患者的常规随访评估中都没有确定的作用。因此,本节将重点讨论在接受药物治疗的PAH或CTEPH患者中使用MRI作为随访工具。这一节没有得到专门的系统文献综述的支持。
几种MRI测量可用于确定右心室功能。连续心脏门控连续屏息短轴平衡稳态自由进动电影图像后处理以计算舒张末期和收缩期末期腔室容积[125].值得注意的是,右心室每搏量是射入肺循环的血量和三尖瓣返流量的总和。对肺动脉瓣水平的二维相位对比图像和/或四维流量图像进行后处理后,可以确定有效的肺血流(以及有效的冲程量)。
核磁共振成像已用于确定接受多环芳烃治疗的患者的心功能[126].At baseline, MRI volumetry-derived RV stroke volume indexed to body surface area, RV ejection fraction, and RV end-diastolic volume index are independent predictors of survival in patients with PAH [74,75,127].经年龄、性别、体表面积校正后,右心室舒张末期容积指数和PA僵硬度也有相同结果[80,128].随访期间,右心室卒中容量指数下降、右心室容量增加和左心室充盈减少与高死亡风险相关[74].Notably, changes in RV ejection fraction were more predictive of outcome than were changes in pulmonary vascular resistance assessed with right heart catheterisation [75].连续MRI显示,在右心室破坏初期,右心室纵向和周向应变平行下降;随着时间的推移,纵向应变的恶化最终停止,而周向应变继续下降。室间隔进行性向左移位加重了这种情况[116].MRI也被用于显示PH患者PA硬度增加,RV和PA耦合减少,这些测量也可能在随访评估中有用[129- - - - - -131].根据2015年4月发表的文章的元分析[78],最强的mri衍生预后预测因子是右心室射血分数(合并危险比,1.23;95% ci: 1.07, 1.41;p=0.003),右心室舒张末期容积指数(合并危险比,1.06;95% ci: 1.00, 1.12;p=0.049),右心室收缩末期容积指数(合并风险比,1.05;95% ci: 1.01, 1.09;P =0.013),左室舒张末期容积指数(合并危险比,1.16;95% ci: 1.00, 1.34;p = 0.045)。右心室和左心室质量与预后无关[78].
尽管一些研究试图用MRI估计平均PAP和肺血管阻力[132,133], mri衍生的压力估计值对于ph治疗患者的随访评估仍然不够可靠。较小的临床试验已经使用mri衍生的终点,如右心室质量和右心室射血分数[134- - - - - -136但MRI尚未用于大型多中心研究,主要是由于后勤原因和简单的事实,监管机构尚未批准基于MRI衍生变量的药物。PVOD/PCH患者通常对多环芳烃治疗反应较差,使用多环芳烃药物可能与危及生命的肺水肿的潜在风险相关(图2 ef) [137,138].
结论
过去十年的研究表明,非侵入性成像在肺动脉高压(PH)诊断方法、预后分类和治疗监测中的重要性。除了目前各中心的指导方针和实践所承认的这一重要作用外,成像方式也在不断发展,人工智能已经进入医学成像领域。附录E5提供了新兴技术和/或方法的概述,这些技术和/或方法可以推动当前成像的一些限制,并在PH管理中开辟新的应用领域。重点介绍了几个临床相关领域。附录E6总结本文每个部分的关键信息。工作小组遵循详细的搜索策略附录E7(表E3 - e15)及图E3.
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充附录E1至E7,包括所有补充表格erj - 04455 - 2020。补充
补充图E1至E3erj - 04455 - 2020。数据
可共享的PDF
脚注
Author contributions: Guarantors of integrity of entire study, M. Remy-Jardin, Y. Ohno, M. Humbert;研究概念/研究设计或数据采集或数据分析/解释,所有作者;重要知识内容的稿件起草或修改,全体作者;审定稿稿,所有作者;同意确保与工作有关的任何问题得到适当解决,所有作者;literature research, all authors;clinical studies, L.R. Goodman, G.D. Rubin;statistical analysis, C.J. Ryerson, P.O. Alderson, L.R. Goodman, P. Thistlethwaite;and manuscript editing, all authors.
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:M. Humbert得到了法国国家研究机构根据资助合同anr -18- rhhs -0006 (DESTINATION 2024)管理的avenir投资项目的支持。
利益冲突:M. Remy-Jardin在提交的工作之外,从Siemens Healthineers, Boehringer Ingelheim, Roche和MSD收取讲座费用,包括在演讲者局的服务。
利益冲突:C.J. Ryerson未披露任何相关关系。
利益冲突:M.L. Schiebler未披露任何相关关系。
利益冲突:梁安琪未披露任何相关关系。
利益冲突:J.M. Wild没有披露相关关系。
利益冲突:M.M. Hoeper是Acceleron、Actelion、拜耳、Janssen、MSD和辉瑞的董事会成员和顾问,在提交的工作之外,他接受了Acceleron、Actelion、拜耳、Janssen、MSD和辉瑞的讲座费用,包括在演讲者局的服务。
利益冲突:奥德森检察官没有披露相关关系。
利益冲突:L.R. Goodman未披露任何相关关系。
利益冲突:J. Mayo在提交的工作之外,还收到了来自加拿大西门子医疗公司的讲座费用,包括演讲者办公室的服务费用。
利益冲突:L.B. Haramati未披露任何相关关系。
利益冲突:Y. Ohno在进行研究期间获得了Canon Medical Systems的研究经费;在提交的工作之外,有拜耳制药的补助金/补助金悬而未决;获得日本文部科学省的科学研究补助金;获吸烟研究基金资助;获得了Daiichi Sankyo的研究资助
利益冲突:P. Thistlethwaite未披露相关关系。
利益冲突:E.J.R. van Beek是ai丹斯、Imbio和QCTIS的董事会成员,是InHealth和曼秀雷敦的顾问,在提交的工作之外;是QCTIS的所有者和创始人;作者及其配偶为董事。
利益冲突:S.L. Knight未披露相关关系。
利益冲突:D.A. Lynch是Parexel Imaging, Boehringer Ingelheim, Veracyte, Daiichi Sankyo和AstraZeneca的顾问,在提交的工作之外,从Boehringer Ingelheim获得了讲座的报酬,包括对演讲者局的服务。
利益冲突:G.D. Rubin未披露任何相关关系。
利益冲突:M. Humbert是Acceleron, Actelion, Bayer, GSK和Merck的董事会成员和顾问;与Acceleron、Actelion和Bayer的资助/资助正在等待中;从Actelion、拜耳(Bayer)、葛兰素史克(GSK)和默克公司(Merck)获得讲座费用,包括在提交作品之外的演讲服务。
- 收到了July 15, 2020.
- 接受2020年10月28日。
- ©2021欧洲188bet官网地址呼吸学会和RSNA。这篇文章是同时联合发表在欧洲呼吸杂志而且放射学.这些文章都是相同的,除了风格上的变化,以保持每个期刊的风格。任何一个版本都可以用来引用这篇文章。