文摘
微阵列是一种强大而有效的工具,允许全基因组基因表达差异的检测控制和疾病之间的条件。他们被广泛应用于研究不同形式的肺动脉高压的病理学,即组1,包括特发性肺动脉高血压患者,和组3,包括肺动脉高压与慢性肺部疾病,如慢性阻塞性肺疾病和特发性肺纤维化。到目前为止,许多人类微阵列研究进行分析全球(肺匀浆样品),compartment-specific(激光捕获显微解剖),细胞特定类型(孤立主细胞)和循环细胞(外周血)表达谱。组合,他们在发展提供重要信息,发展和晚期疾病。在未来,系统生物学方法,非编码rna的表达,调节编码rna和动物模型与人类疾病之间的直接比较可能是重要的。
文摘
全面的概述compartment-specific微阵列研究肺动脉高压患者的材料http://ow.ly/YEFO2
介绍
肺动脉高压(PH)包括一个大范围的疾病与肺动脉压力升高≥25毫米汞柱。PH值的特点是肺血管重塑和与高阻肺血流量,最终导致右心衰和死亡(1]。PH值可以表现为:肺动脉高血压(PAH)(组1);PH值由于左心脏病(组2)、慢性肺疾病(CLD)和/或缺氧(组3);慢性血栓栓塞的PH值(4组);和PH值不清楚多因子的机制(5)组(1]。PH值是一个频繁的患病率(60%)和CLD的严重并发症2]。PH值的出现疾病进展的指标和预测患者的结果2- - - - - -4]。多环芳烃的主要病理生理特点和PH值CLD是肺血管重塑的小肺动脉。这包括,最重要的是,内膜的增生,内增厚由于肺动脉平滑肌细胞(PASMC)扩散,在某种程度上,外膜改造(5,6]。PH值的另一个特点是内部和血管周的炎症导致生长因子信号通路的激活和PASMCs扩散,进而强化动脉重塑(7]。循环细胞及其介质也被假定参与疾病进展,因为他们能够促进招聘、保留和分化的循环单核细胞的细胞群,导致血管重塑8,9]。虽然PH值的理解病理学大幅增加,近年来仍有迫切需要完全理解底层机制如何驱动血管重塑。
RNA表达的研究
基因表达研究,如微阵列和RNA序列,提供了访问和快速筛选技术来检测基因,重新组基因或通路参与改造过程。他们允许广泛而公正的看微分博士全基因组基因表达模式迄今为止,RNA表达的研究被用来识别基因和通路,以前没有与PH值相关发病机制(10),2)发现新的潜在生物标记物(11),3)识别个体的风险发展中PH值(12),4)确定药物在疾病进展的影响13]。
除了识别编码rna (mRNA),非编码rna的表达,如小分子核糖核酸(microrna)也可以分析。与编码mrna,非编码rna不翻译成蛋白质14,15),但可以调节mrna的表达在转录和转录后水平(14]。非编码rna参与表观遗传过程可分为两个主要团体:短非编码(如。microrna < 30元)和长非编码rna(> 200元)16]。而短的非编码rna吸引了一些关注在最近的研究(11,17)、信息表达、功能和作用长非编码rna在PH值仍然是有限的。
微阵列技术和数据分析
微阵列技术已经被用于超过二十年,今天,是良好的和高度标准化水平的仪器和生物化学18,19]。此外,大多数研究使用微阵列基因表达研究。由于这些原因,本文着重于研究利用微阵列技术。
微阵列是工具来测量大量的不同的核酸序列在一个复杂的混合物。RNA样本会被放大,标签和杂交斑点寡核苷酸的数组。图像分析识别,量化信号和构造数据表包括现货注释可以进一步处理和分析。数据处理包括背景减法和正常化调整强度资料不同的数组。确定候选基因,可能是组间差异表达或条件下,基因可以通过他们的平均排名(对数转换)褶皱变化或t统计量(可能放缓),和一流的基因可以被识别。也是惯例创建列表的候选基因与给定的错误发现率(预期的假阳性的比例实际上拒绝零假设)(20.]。后来,基因可以通过聚类分析co-expression模式,多维标度和主成分分析来识别基因集,可能参与类似的生理过程。外部定义的基因集,例如,基因属于一个特定的信号通路,可以为统计分析浓缩在顶级基因(基因片段的浓缩分析)或统计代表候选基因(代表分析)(21]。
微阵列研究的挑战
学习困难的基因可能参与肺血管重塑困惑了几个可以影响结果的因素,如标本采集和存储的方法,RNA质量(22],pre-amplification [23),标签协议(24),微阵列平台(25应用[],和数据分析26- - - - - -29日]。此外,数据的解释是容易产生偏见。选择标准是主观的,和一个不错的选择取决于上下文,设计和实验的目的。许多基因通常确认为不同监管。选择基因相关疾病发病机理是具有挑战性的。通常,最强的不同调节基因被选中作进一步分析。是否这些也是生物相关的基因是不可预测的。监管较少但病理生理重要基因可能很容易被忽略。因此,聚类等方法,基因设置或网络分析并行使用信息从许多基因,因此对偶然变异的个体基因更健壮。额外的集成、外部知识的生物学的基因可以生成假设有关生物过程,通过表达谱的变化反映出来。
差异基因表达的相关性检测到只能估计,结合微阵列芯片分析结果与验证通过免疫印迹或流式细胞仪检测蛋白质含量。确认发现的蛋白质水平是至关重要的管制并不会自动导致基因变化的蛋白质水平由于microrna指纹控制蛋白质组和非编码rna。
选择标准
本文试图总结当前和相关文献专注于基于微阵列的高通量转录组分析特发性肺动脉高压(IPAH)(如原型疾病),家族性肺动脉高血压(FPAH)和PH值与CLD如慢性阻塞性肺疾病(COPD)和特发性肺纤维化(IPF)。人类微阵列研究PH值组2、4和5是有限的(30.),不包括综述。微阵列数据的分析可以从不同的隔间的肺癌,我们总结了当前状态的数据收集的微阵列分析人类的肺匀浆样本,激光捕获microdissected肺动脉,孤立或循环细胞(表1)。
微阵列研究的具体细节发表在肺匀浆(LH),激光捕获显微解剖(LCM)和孤立的或循环细胞自2001年以来,专注于肺动脉高血压(PAH)或肺动脉高压(PH)与慢性肺部疾病相关,按时间顺序显示
研究包括在本文的选择标准是文章类型(研究文章发表,直到2015年11月),物种(人类),技术(微阵列或基因阵列)和疾病(组1和3的PH值或多环芳烃)。短简介微阵列研究PH值的啮齿动物模型提供了本文的末尾。
微阵列研究人类的肺部组织
肺移植(代表终末期疾病)或活检材料(代表一个时间点在疾病进展但通常不是临床显示,因此,很少有)提供一个独特的机会来识别分子机制和潜在的新的治疗靶点病变的肺。虽然进入人类外植体是相当有限的,这是一个更大的挑战来获得必要的健康供体材料的比较。控制组织的来源可以来自裁员移植肺,肺nontransplanted或切除肿瘤。这可以偏见微阵列分析的结果。同样,其他混杂因素如疾病的严重程度、并发症、药物和群体的年龄/性别可能会影响研究结果。
最简单但至少精制方法在分析基因表达在PH值的分析样本总肺匀浆。在肺内的动脉只代表一小部分肺组织(< 10%),这个舱的表达谱可能主要蒙面,甚至失去了在分析肺匀浆(50]。不可避免的是,整个组织的平均结果的使用各种来自不同细胞类型的表达谱。此外,肺部分可能包含船只大小不同,可能有不同的细胞成分,这使得它难以解释的结果相关的生物过程。此外,严重的实质CLD的改造可能掩盖相关结果。然而,利用肺匀浆可以提供基因表达的见解,通过进一步免疫组织化学验证,可能会导致新发现的潜在目标参与血管重塑。为了具体分析基因表达在肺血管,几项研究已经应用激光捕获显微解剖(LCM)孤立小肺动脉(51,52]。另一种方法来克服组织异质性是主要分析孤立的人类细胞,如肺动脉内皮细胞,PASMCs或成纤维细胞。然而,在这里,几个方面必须考虑作为基因表达的变化可以影响隔离和细胞培养条件。使培养细胞基因表达的影响是众所周知的53- - - - - -55]。生长因子的培养基可以改变旁分泌激素信号和细胞生长,从而可以影响基因表达(56,57]。最后,分析循环细胞可以提供一个有用的工具来检测疾病进展或监控个性化药物的新型生物标志物。由于其临床的可访问性,血液细胞代表最方便的细胞来源评估基因表达改变的PH值。
肺匀浆样品
用人类肺匀浆样品IPAH FPAH, Geraciet al。(31日]显示编码激酶和磷酸酶基因的表达减少,upregulation致癌基因和基因编码离子通道蛋白,与控制。他们还发现了基因IPAH与FPAH区分开来。其中包括改变生长factor-β受体III (TGFRB3),骨形态发生蛋白2 (BMP2),增殖蛋白激酶激酶5 (MAPKK5C),激活受体激酶1 (RACK1)、载脂蛋白C-III (APOC3)和基因编码核糖体蛋白SA /层粘连蛋白受体1 (RPSA/LAMR1),这只是IPAH患者样本中发现的。在另一项研究中,一个特定的基因签名包括基因相关的监管actin-based能动性,蛋白质泛素化,和营地,把增长factor-β增殖蛋白激酶,雌激素受体、一氧化氮和血小板源生长因子(PDGF)信号中确定PAH相比健康的肺组织。重要的是,骨形态形成蛋白受体二世(BMPR2)表达下调,甚至在受试者没有这种基因的突变(32]。这两个研究[31日,32)带来的光不仅突变BMPR2FPAH的基因,这是最突出的原因(58的差别,但也对这些BMPR2noncarrier患者可能导致PH发病机理。此外,女性与IPAH显示高表达雌激素受体1 (ESR1)。令人惊讶的是,基因表达谱的肺匀浆PH-IPF病人像比PAH样品与正常对照组,表明缺乏一般的PH值签名(32]。多环芳烃的另一个微阵列研究样本集中在代谢异质性。该基因编码细胞色素P450 7 b1 (CYP7B1),胆汁酸合成的同工酶,多环芳烃肺中高度表达与控制(34]。H苏et al。(33)相比,基因表达谱的系统性硬化症(SSc)相关的肺纤维化和IPF和IPAH SSc-PAH子集。他们发现基因参与炎症和激活先天免疫等CXCL10(interferon-γ-inducible蛋白10)作为调节PH值发生的所有组独立。与上述研究中,发现了这里,一个特定的PAH签名,包括基因抗原表达和趋化因子的活动。这个签名是PAH表型的程度成正比。米ura所言et al。(12]调查IPF样品有无共存博士发现的PH值基因签名主要与细胞外基质(ECM)改造和PASMC和纤维母细胞增殖/迁移,而non-PH表型主要是与促炎的相关基因。综上所述,大部分的基因表达研究肺匀浆样本多环芳烃和肺纤维化与酸碱显示一个共同的基因表达特征,包括基因参与细胞增殖、炎症、免疫和ECM重塑。参与炎症与PH值相关联的基因;然而,他们同样被证明参与non-PH样品,揭示全球影响力的炎症基因PH值而不是一个签名。
激光捕获microdissected肺动脉
2009年,李奥曼et al。(35)执行第一个transcriptome-wide表达式分析阻力LCM的肺血管来源于外植IPAH和nontransplanted供体肺组织。作者发现高表达平面细胞极性介质如无翼成员11 (WNT11),蓬乱的(深潜器)和ρ激酶(岩石)。本研究指向发展WNT信号通路激活在肺内的血管重塑。Patelet al。(36]相比肺动脉的基因表达IPF患者健康的捐赠者和没有共存的PH值,并显示介质的PASMC内皮细胞增殖,WNT信号、补体系统激活和细胞凋亡在IPF小动脉差异表达。IPF的基因表达谱和PH-IPF相似,表明可比血管IPF患者群体的变化,没有明显的博士这一发现可能促使转录组的猜测,重组前进行博士的外观比较基因表达谱在肺内的动脉IPF和慢性阻塞性肺病的PH值显示多个基因属于视黄醇新陈代谢和ECM途径区分这两个肺疾病的血管重塑与PH值(6]。综上所述,使用LCM肺动脉最近的研究表明,许多识别基因参与WNT信号、扩散或ECM重塑。LCM方法强调,发育的信号通路在血管重塑和重新激活,他们可以协调增殖和ECM沉积过程。
孤立的主细胞
到目前为止,一些研究调查扩散的机制,单一细胞的迁移和贡献肺动脉壁的改造。然而,这些过程的分子司机在很大程度上仍未知。
尽管内皮功能障碍的发病机制的研究中是一个关键的功能多环芳烃(59),迄今为止,只有一项研究分析了基因表达在人类微血管内皮细胞(HMVECs)通过微阵列分析。Costelloet al。(38]相比主要HMVECs来源于肺组织的基因表达谱与心脏的来源和分析基因表达在低氧暴露。90个基因被确定为不同肺内皮的监管。小精灵(GREM1),CXCR7被验证的具体调节肺细胞对缺氧的反应。GREM1是骨形成拮抗剂(60),本研究指向一个监管的重要性BMPR2和这个轴的重要性在博士的识别CXCR7强调发展趋化因子及其受体的贡献的PH值(38]。目前,比较健康的基因表达谱芯片研究HMVECs和PH HMVECs缺乏。因此,内皮细胞有必要的额外的分析洞察到基因表达的观察内皮功能障碍在博士符合这个概念,在最近的一项研究中,R赫德et al。(61年]研究内皮细胞转录组的健康和IPAH病人使用RNA序列,提出了一个替代或补充微阵列分析方法。小说BMPR2功能障碍之间的关系,减少表达内皮胶原IV (COL4)和ephrin A1 (EFNA1)提出,这可能是在PAH内皮损伤的基础。
与内皮细胞相比,几项研究已经调查人类PASMCs的基因表达谱。这些细胞构成的主要细胞类型的内侧层肺血管壁和被认为做出显著贡献的肺动脉的改造。Yu等。(40)相比,基因表达模式在人类PASMCs IPAH和遗传多环芳烃(HPAH)的控制。表现出类似的趋势的差异表达基因的表达在HPAH和IPAH PASMCs。许多基因参与细胞增长/增殖和细胞周期的调控。此外,某些血管活性的受体如缓激肽B2受体(BKB2RHPAH和IPAH细胞)表达下调。除了编码rna,非编码rna已经受到了越来越多的认可但他们参与改造过程仍然是难以捉摸的。在最近的一项研究中,G欧等。(39]分析了PASMCs microrna基因表达和识别凋亡mir - 210作为主要的microrna的缺氧引起的。Fantozziet al。(37)检查是否BMP2不同调节基因表达在PASMCs正常受试者和IPAH病人。外生的骨形成蛋白(BMP)可能弥补功能障碍的BMP信号由于突变IPAH骨形态发生蛋白受体的差别和/或对这些病人。他们观察到> 1000个基因是相对的监管IPAH PASMCs。IPAH细胞基因调节包括那些与生长因子和相关配体、膜受体、转录因子信号转导蛋白激酶(如。c-Fos、原癌基因结合蛋白和核因子κB),和酶(如。白三烯C4合成酶和ATP合酶)。IPAH细胞凋亡诱导的基因表达下调或proapoptotic因素,膜受体、离子通道和转运蛋白、转录因子(如。滑雪,转录因子E2F1 TFE3,乳腺癌转录因子ZABC1),和细胞质酶激酶。总之,增长和转录因子的调控指向的参与PASMC增殖,从而导致内侧增厚和血管重塑驾驶疾病的恶化和加速度。
最外层的肺动脉(动脉外膜)是由成纤维细胞(62年和炎症细胞63年]。成纤维细胞,血管重塑的贡献是有争议的62年,64年]。尽管他们增殖在不同刺激如PDGF-BB [65年)或缺氧(66年),动脉外膜的厚度从PH患者肺动脉不是大大不同于船只从健康受试者6,62年]。目前一个非常有限的研究处理基因被监管的外膜层博士H苏et al。(33)基因表达相比不仅在肺匀浆IPAH和SSc-PAH还在孤立主要从这些患者成纤维细胞。成纤维细胞来源于SSc-PAH和IPAH共同签名基因(24);然而,一些基因区分这两个实体。基因在IPAH强烈调节成纤维细胞包括趋化因子和白细胞介素(ILs)如白介素、引发和IL-13受体。本研究强调炎症组件外膜层的重要性,这表明这些细胞在PH发病机制中的作用。
循环细胞
在过去的十年中,大量的微阵列研究解决mRNA和microrna的表达在细胞从循环PH患者(表1)。除了一个,所有这些研究分析循环外周血单核细胞(PBMCs),包括多个细胞如淋巴细胞、单核细胞和自然杀伤细胞。
2004年,乙妳et al。(41]相比,基因表达的PBMCs IPAH和二级PAH (sPAH)(包括门静脉高压、钙质沉着、雷诺氏现象,食管蠕动障碍指硬皮病、间质性肺疾病、接触anorexigens芬特明/氟苯丙胺和慢性肺血栓栓塞疾病)患者控制,并发现该基因本体类“炎症反应”和“对压力的反应”在IPAH调制与健康对照组相比。IPAH和sPAH有类似的表达谱。同样的,你lrichet al。(42]发现基因参与炎症机制、宿主防御或内皮功能影响IPAH PBMCs。比较研究从SSc-PAH PBMCs IPAH PBMCs表明PBMC两疾病组和相关基因表达相似的生存与已知的预测多环芳烃。另外本研究支持这样的看法,即血管生成和趋化性/炎症与多环芳烃的严重程度相关联(43]。一项研究在2010年由Pendergrasset al。(45)研究多环芳烃在有限的共存是否PBMCs系统性硬化症(lSSc)基因表达的影响。健康对照组的基因表达分析杰出lSSc样本和分离lSSc-PAH lSSc没有PAH,指向一个特定的PAH签名。Cheadleet al。(47]分析了成绩单的PBMCs IPAH和SSc-PAH相比健康的捐赠者。多个基因表达特征被发现,杰出的各种疾病组的控制。其中一个基因集,红细胞成熟,丰富具体的多环芳烃和与血液动力学的相关措施增加IPAH患者的疾病严重程度。Risbanoet al。(46)相比,基因表达谱的PBMCs SSc患者没有共存的多环芳烃,并确定IL-7受体(IL7R)显著降低样本PAH患者。Chesne等。(48)PBMC基因表达与健康对照组相比,多环芳烃和囊性纤维化患者以识别终末期慢性呼吸道疾病相关基因签名。微阵列研究结果验证了在第二个独立队列和慢性阻塞性肺病患者添加到验证共同签名。共同签名组t细胞因子7 (TCF7),IL7R早期相关的两个基因激活,表达下调。综上所述,两项研究强调的重要性IL7R博士H的潜在生物标志物人物et al。(13从vasodilator-responsive]相比PBMCs (VR)多环芳烃vasodilator-nonresponsive PAH患者。差异基因表达微阵列分析模式包括信息粘附因子,细胞骨架和ρGTPase基因。DSG2编码一个desmosomal钙粘着蛋白参与WNT /β-catenin信号,和Ras同系物家庭成员Q (RHOQ),它编码一个细胞骨架蛋白参与insulin-mediated信号,是足以正确区分五VR-PAH病人验证队列的队列,这意味着这些基因的预后潜力。
在循环PBMCs, microrna的概要文件也进行了分析。R赫德et al。(11)表明,mir - 150等离子体中表达下调IPAH病人和与2年期这些患者的生存。另一项研究的PBMCs PH患者相比健康温和(平均平均肺动脉压(肺动脉平均)29毫米汞柱)和严重的PH值(平均肺动脉平均46毫米汞柱),并发现几个microrna是表达下调(mir - 451和mir - 1246)或调节(miR-23b, mir - 130 - a和mir - 191),和其表达水平与PH值的程度成正比(17]。最近的一项研究arrionet al。(49)强调的潜在相关性在IPAH miR-23a与患者的肺功能,因此可能作为一种潜在的生物标志物。
到目前为止,只有一项研究分析PBMCs的族群,即淋巴细胞。W美国东部时间et al。(44从患者FPAH]生成淋巴细胞中被永久地传颂BMPR2突变突变阳性,但无病家庭成员,和由此产生的lymphoblastoid细胞系进行微阵列分析。疾病状态BMPR2突变携带者在增殖,基因差异表达与三磷酸鸟苷信号和压力反应通路。雌激素代谢基因CYP1B1(细胞色素P450 1 b1)被发现女性PAH患者显著下调。这个基因的低表达与疾病严重程度相关。重要的是,这项研究说明BMPR2突变影响炎症细胞的基因表达谱。在未来,进一步的微阵列分析PBMC亚种群应得到更深的洞察改变基因在特定的人群和描绘他们的个人贡献博士此外,血液中发现的其他细胞表达谱,如多形核中性粒细胞,没有分析到目前为止。然而,这可能是相关的,因为据报道,中性粒细胞淋巴细胞比率是PAH患者显著增加(67年]。
综上所述,简单的可访问性和识别等提出了循环标记microrna(特别是miR-23)提供了一个机会去应用作为IPAH预后工具或PH值与肺部疾病和决心的疾病进展和治疗评估。然而,检测不同调控基因签名在疾病条件下必须在一个单独的队列验证确认预后的潜力。这个迄今为止只执行在一个非常有限的研究。从癌症研究的经验证明,批准的验证等关键是如何可靠的生物标记物(68年]。
总结微阵列研究啮齿动物的肺部组织
在平行于研究人类样本,进行了微阵列研究缺氧,野百合碱(MCT)在啮齿动物全身的PH值。虽然动物模型只能概括人类血管重塑的某些方面,如PASMC增殖或炎症,他们不仅代表了一个非常好的工具调查晚期疾病,而且疾病发病,进展或逆转。
古典和接受轻微的酸度是低氧诱导模型在老鼠和老鼠69年]。调查人员集中在不同疾病阶段和分析基因表达在不同的疾病发展(短跨度为缺氧暴露(70年,71年)、终末期疾病(长期缺氧暴露(50,72年])或逆转重塑(复氧(73年,74年])。日积月累,这些研究表明,疾病发作期间,多个转录和生长因子,如内皮素(EDN1)[70年)和神经营养酪氨酸激酶受体2型(NTRK2)[71年),被激活。在疾病晚期,已经观察到显著的结构性变化,如在原骨胶原,tenascin C (过渡委员会),S100钙结合蛋白A4 (S100A4)、集群分化36 (CD361)和吸收FK506结合蛋白(FKBP1A)[50]。反向改造方法可以揭示基因参与的逆转重塑过程,其中包括腺苷甲硫氨酸脱羧酶1 (AMD1)[74年),Ras GTPase-activating-like蛋白(IQGAP1)、胰岛素样生长因子结合蛋白3 (IGFBP3)和乳铁蛋白(LTF)[73年]。
人类炎症组件的酸度由MCT-induced最佳相似模型大鼠(75年]。PH值在这个模型中,大量研究分析信使rna或microrna的表达变化和显示病变的基因参与应对伤害和炎症,血管形态发生和基因编码蛋白酶(76年- - - - - -78年),以及miR-22、miR-30 let-7f, mir - 322和mir - 451, miR-21, let-7a [79年]。
此外,不同的研究考察了PH值的影响药物测试(80年],应变差异[81年],间歇性或持续暴露于低氧(82年和性别差异83年]在开发过程中基因表达变化的PH值在不同的啮齿动物模型。
结论、局限和展望
到目前为止,超过25人类微阵列研究提供大量的基因表达数据,从单个基因表达复杂的路径分析,已执行。在过去的15年里,更方便的隔间,如循环细胞,研究了更频繁(图1)。
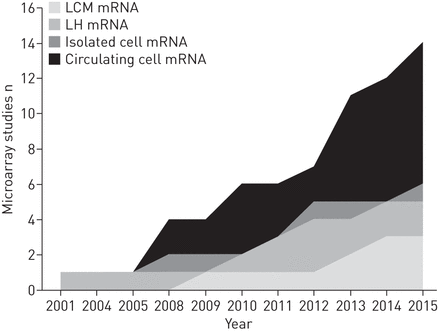
人类的数量自2001年以来发表的微阵列研究在肺匀浆(LH),激光捕获显微解剖(LCM)和孤立的或循环细胞专注于肺动脉高血压或肺动脉高压与慢性肺部疾病相关。
ECM基因表达变化,血管增生,炎症过程和WNT通路现在越来越认可过程潜在的PH值是重要的(表1和图2)。WNT信号之间的直接联系和发育过程中,细胞增殖和迁移84年指向对血管重塑。尽管个人指纹是观察不同细胞类型和隔间,许多监管共享途径。这表明类似的信号模式参与发病机理在不同PH值肺隔间(图2)。这些是否适应或病理反应,精确的机制和动力学的监管尚未阐明。进一步理解底层机制可以帮助开发PAH患者有效的治疗方案和PH值与CLD相关联。
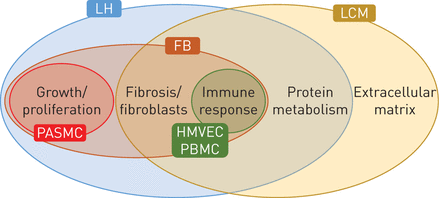
维恩图描绘重叠和发散的微阵列分析讨论研究的结果。韩:肺匀浆、LCM:激光捕获显微解剖,FB:孤立的纤维母细胞,PASMC:肺动脉平滑肌细胞;HMVEC:人类微血管内皮细胞;PBMC:外周血单核细胞。
每个讨论的研究都集中在一个特定的方面疾病的发病机理。可以设想,识别常见的信号特征和当地的基因调控网络可能导致检测重要的监管机构管理更基本的生物过程和途径或特定部分,参与发病的博士此外,大量的数据仍有待探讨。缺少一致性的样本收集、贮存和准备以及微阵列平台和生物信息学分析阻碍直接比较,防止一般的结论。然而,可用的数据仍然是一种有价值的新假说的产生来源的分子机制推动博士芯片结果的效用可以增强标准化的数据采集和分析,从而保持承诺,他们可能显著提高我们理解pathomechanisms PH值。
在不久的将来,新技术将补充微阵列平台。作为模范地,下一代RNA序列将被应用到显示的快照RNA的存在和数量、可变剪接、转录后修饰、基因融合、和突变/单核苷酸多态性。因此,它将有助于产生一个更全面的印象的疾病发病机制85年]。事实上,最近的一项研究已经利用这种技术来调查IPAH患者的内皮细胞转录组(61年]。
总之,在未来的RNA表达的研究,这将是重要的1)比较和协调从动物模型和人类疾病的基因表达,2)用系统生物学的方法来识别复杂疾病发展签名和理解疾病的动态发展水平的监管网络,和3)分析非编码基因表达可能影响编码的基因的表达。
确认
我们要感谢李马什(路德维希玻耳兹曼肺血管研究所,格拉茨,奥地利)的批判阅读手稿。
脚注
利益冲突:披露可以找到与这篇文章www.qdcxjkg.com
- 收到了2015年12月3日。
- 接受2016年2月15日。
- 版权©2016人队















