摘要
肺动脉高压是一种致命的肺压力升高,并发右心衰。肺动脉高压表现形式多样;其中之一是肺动脉高压(PAH),其特别特征是渐进式重构和小肺血管阻塞。多环芳烃患者的神经激素失衡与较差的预后和生存有关。在这篇关于多环芳烃中神经激素调节的回归基础文章中,我们提供了一个已经在临床前和临床中测试过的药理学和非药理学策略的概述。由于缺乏对神经激素系统在整个疾病过程中如何变化的了解,以及从动物模型转化为人体试验的困难,多环芳烃患者的神经激素调节策略的益处受到了限制。我们建议,需要对神经激素状态进行纵向和个体评估,以提高神经激素调节策略的时机和特异性。正在发展的成像技术,如正电子发射断层扫描,可能有助于确定不同疾病阶段的多环芳烃患者的神经激素状态,并优化个人治疗反应。
摘要
为了进行有效的干预,需要更好地了解肺动脉高压和相关右心衰发展过程中的神经激素变化http://bit.ly/2NCV0nO
简介
肺动脉高压是一种致命的肺压力升高,并发右心室衰竭。肺动脉高压可分为五组。第一组是肺动脉高压(PAH),其特征是肺小血管进行性重塑及阻塞[1].由此导致的动脉直径减小可使肺循环中的血压升高至正常压力的五倍[2].然后,肺循环从低循环变为高压循环,增加薄壁右心室的负荷。这最终导致右心室衰竭和死亡[3.,4].目前尚无治愈多环芳烃的方法,治疗选择也有限。
神经激素失衡是各种形式肺动脉高压的疾病调节剂之一,它一再被认为与PAH患者的不良临床结果和生存期有关[5- - - - - -7].因此,许多对神经激素系统的药物和非药物干预已经在临床前和少数临床研究中进行了研究[8].然而,从临床前研究到临床研究的转化是困难的,而且经常缺乏。
最近的两篇综述广泛描述了神经激素激活有害影响的分子途径[9以及针对多环芳烃神经激素系统的药理学或侵入性策略[8].我们希望在此基础上进一步研究,为多环芳烃神经激素系统的研究提供未来的方向。因此,在这篇回归基础的文章中,我们将概述神经激素系统如何确保心血管内稳态;2)描述人类多环芳烃中神经激素系统是如何发生全身性和局部性变化的;3)探讨神经激素变化对PAH和右心衰进展的影响;4)对干预多环芳烃神经激素系统的临床前和临床研究进行了全面综述。
值得注意的是,神经激素的变化可能在各种形式的肺动脉高压中起作用。因为大多数临床数据都是在多环芳烃中收集的,所以这是我们综述的重点。此外,其他形式的肺动脉高压的特征是常见的共病(如。左心衰或其他肺部疾病),使神经激素系统的观点复杂化。因此,下文所述的神经激素变化和干预措施的效果主要集中于在多环芳烃患者中获得的证据。
回归基本
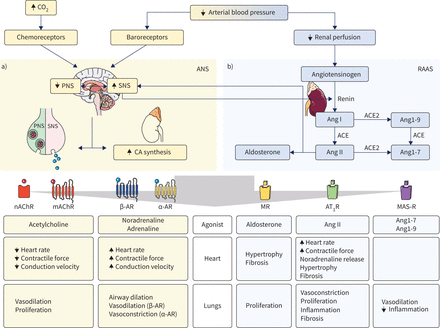
神经激素系统的一个重要功能是维持心血管内稳态。神经激素系统的两个支柱是自主神经系统(ANS)和肾素血管紧张素醛固酮系统(RAAS)。两个系统的不同组成部分和功能见图1.
短期和长期控制血压通过神经激素信号:a)自主神经系统(ANS)和b)肾素-血管紧张素-醛固酮系统(RAAS)。PNS:副交感神经系统;SNS:交感神经系统;Ang:血管紧张素;血管紧张素转换酶;CA:儿茶酚胺;nAChR:尼古丁乙酰胆碱受体;mAChR:毒蕈碱乙酰胆碱受体;AR:肾上腺素受体;MR:矿物皮质激素受体; AT1R: Ang II型1受体;MAS- r: MAS受体。
ANS可以细分为两个具有相反作用的系统:交感神经系统(SNS)和副交感神经系统(PNS),如图所示图1一个.SNS拥有肾上腺素能突触,通常在(生理)压力下被激活,为身体准备行动,而PNS有胆碱能突触,在休息时流行。然而,这两个系统都在基础水平上持续活跃,净生理效应取决于SNS和PNS活性之间的平衡。
ANS保证了心血管稳态的短期控制。血压和动脉CO2主动脉弓和颈动脉窦中的压力和化学感受器持续监测其水平。当动脉血压下降时,压力感受器被灭活,压力感受器控制的SNS抑制被解除。同时,PNS活性被抑制,向SNS平衡。当CO增加时,SNS也被激活2血液中的水平由化学感受器检测。
SNS的激活导致去甲肾上腺素从突触直接释放到心肌细胞和血管上。此外,交感神经刺激肾上腺合成和释放肾上腺素和去甲肾上腺素[10到达心脏和肺部通过血液中。肾上腺素随后会与α-和β-肾上腺受体结合。增加信号通过肾上腺受体和来自副交感神经烟碱和毒蕈碱乙酰胆碱受体(nAChR和mAChR)的信号减弱导致心肌收缩速率和力度的净增加。此外,刺激血管中高表达的α-肾上腺受体可引起血管收缩,从而恢复动脉压。
与ANS一样,RAAS被细分为两个反活性系统:经典和替代RAAS系统,如图图1 b.经典的RAAS由来已久,涉及血管紧张素转换酶(ACE)、血管紧张素(Ang)、Ang II型1受体(AT)1R),醛固酮和矿物皮质激素受体。替代RAAS系统的研究较少,涉及ACE2、Ang1-7、Ang1-9和MAS受体。
RAAS确保长期控制血压和血容量。当动脉血压下降时,肾脏灌注压降低。因此,肾素从肾脏释放到血液中,促进血管紧张素原转化为Ang i。后者在肺中被ACE进一步转化为Ang II [11].Ang II是一种强血管收缩剂通过在1但也可增加心肌收缩的速度和力量[12].此外,Ang II促进肾上腺醛固酮的释放通过矿物质皮质激素受体,诱导钠和水滞留在肾脏和增加血容量。然而,醛固酮也直接作用于心脏,导致心脏肥厚和纤维化[13].醛固酮对心脏的这些作用与血压升高无关。在(肺)血管系统中,醛固酮的病理水平与氧化应激和血管炎症相关[13].
在相反的RAAS途径中,Ang I转化为Ang1-9, Ang II转化为Ang1-7,均通过ACE2进行。Ang1-7和Ang1-9在很大程度上反对经典RAAS通路的血管效应通过MAS受体[14,15].Ang1-7和Ang1-9对心脏的直接影响尚不清楚。
神经激素系统影响全身和局部
ANS和RAAS不是孤立运行的。一些相互作用已经被证实,在中心和局部,并主要研究慢性心力衰竭患者或实验性心力衰竭。系统水平的相互作用包括sns诱导肾素从肾脏释放[16,17以及大脑中Ang II的中枢活动。例如,ACE抑制剂或AT对经典RAAS信号的抑制1R受体阻滞剂增加PNS活性[18,减少社交网络活动[19].后者也发生在AT时1R阻断只应用于大脑[20.,表明Ang II直接作用于中枢神经系统。此外,Ang II增强化学受体的激活[21,22]并抑制对心率的压力感受器反射控制[20.,23,两者都导致了社交网络活动的增加。相比之下,SNS活性可以通过替代RAAS途径降低通过抑制下丘脑去甲肾上腺素释放[24].
ANS和RAAS之间的相互作用也在局部发生。例如,Ang II通过增强交感神经末梢去甲肾上腺素的释放来增加肾上腺素能信号传递[20.],并抑制心脏去甲肾上腺素的再摄取[25].此外,基因表达的AT1心脏中的R受Ang II和β的调节1肾上腺素能受体(26,27],提示局部SNS和经典RAAS的平衡决定了AT的基因表达1R在心里。β-肾上腺受体和RAAS信号之间的交叉信号在肺血管系统中也有描述[6].
PAH患者神经激素系统的全身性和局部性变化
ANS的系统性变化
多环芳烃反复与系统性SNS活动增加有关。社交网络活动,直接测量通过PAH患者周围神经的肌肉交感神经活动增加[28,29].此外,大多数PAH患者的血浆肾上腺素水平升高。30.- - - - - -33但并非所有的研究[34].
SNS和PNS之间的联系是这样的,SNS活动的增加会导致PNS活动的减少。运动后的心率变异性和心率恢复指标可间接评价中枢神经系统活性。正如预期的那样,PNS活动的心率变异性指数[28,35,36和心率恢复[37,38]在多环芳烃患者中减少。自主神经系统对SNS活动的不平衡和对PNS活动的不平衡与运动能力的降低有关[39,40],较差纽约心脏协会功能类[29,41多环芳烃的死亡率增加[30.,32].
ANS的局部变化
在多环芳烃中,SNS不仅被全身激活,而且在心肌中也被局部激活[33,35,42].SNS激活的重要触发因素是心房和心室拉伸:在多环芳心病患者中,β-肾上腺受体表达在右心室特异下调,而在左心室无下调[43],与心室壁应力有关[44].心房拉伸对SNS激活的作用在研究球囊性心房间隔造口的研究中得到证实。尽管房间隔造口术设计时没有干扰神经激素系统,但它部分减少了肌肉交感神经的活动[45].这种肌肉交感神经活动的减少与心房压的降低有关,这表明心房拉伸在SNS激活中发挥了额外的作用[45].
SNS的急性增加对于增强心脏收缩的速度和力度非常重要,从而使右心室能够应对增强的负荷。然而,持续的心脏SNS激活导致β选择性下调1-肾上腺受体和下游信号通路中剩余β-肾上腺受体的解耦[43].β-肾上腺受体表达和信号的减少至少通过两种方式损害右心室功能。首先,尽管PAH患者右心室心肌细胞的收缩力(收缩末端弹性)和发力能力增强[3.], β-肾上腺受体信号的丧失会降低右心室收缩储备[43,46].运动中收缩储备的丧失导致动室解耦和急性右心室扩张[47],并与运动能力降低和生存能力降低有关[48].第二,β-肾上腺受体表达减少在PAH舒张功能受损中也起重要作用。β-肾上腺受体的下游靶点之一是蛋白激酶A (PKA),它调节心肌细胞硬度通过巨大肌肉瘤蛋白肌提蛋白的磷酸化[49].因此,β-肾上腺受体表达减少导致PKA活性和PKA介导的肌素磷酸化降低,从而增加右心室心肌细胞的硬度[50].在实验性多环芳烃中,持续的肾上腺素能激活进一步与心脏肥厚、纤维化、凋亡和毛细血管密度降低有关[51,52].
持续的肾上腺素能激活也与肺血管重构有关。β-肾上腺受体信号通路受损导致肺动脉内皮细胞产生的一氧化氮减少,导致肺血管收缩[6].肾上腺素能直接刺激肺动脉平滑肌细胞可进一步加强这一点,并共同导致慢性肺血管收缩[6].此外,持续的肾上腺素能刺激可引起肺动脉平滑肌细胞肥大和增殖[53,54].
与已知的SNS的局部变化相反,到目前为止,只有一项研究报道了右心室的反活性PNS信号的变化。D一个年代ilvaGoncalvesB操作系统等.[36]显示PAH末期患者右心室nAChR表达增加,突触间隙内乙酰胆碱酯酶降解乙酰胆碱可能减少。在很大程度上,尚不清楚PNS是否以及如何在肺部发生变化。
RAAS的系统性变化
在多环芳烃中也描述了RAAS激活的不平衡。与健康对照组相比,多环芳烃患者血浆Ang I和Ang II水平升高[55,56].然而,Ang I和Ang II水平只在进行性多环芳烃中升高,而在稳定期多环芳烃中没有升高,且与疾病进展和死亡率相关[57].多环芳烃患者血浆醛固酮浓度高于无多环芳烃但原因不明的呼吸困难对照组[58].在本研究中treatment-naïve例患者的亚组中,醛固酮水平与肺血管阻力呈正相关,与心排血量呈负相关[58].然而,在一个更大的多环芳烃患者队列中,醛固酮浓度与心排血量、6分钟步行距离(6MWD)或生存率没有直接关系[59].
在多环芳烃中,除了经典的RAAS激活外,替代性RAAS激活也可能减少。一项研究报道患者血浆中Ang1-7和Ang1-9水平降低[56,而另一项研究报告的Ang1-7水平没有变化[55].在后一项研究中,较高的Ang II/Ang1-7比值表明ACE2减少了Ang II向Ang1-7的转化[55].与对照组相比,PAH患者的血浆ACE2浓度并不低,但提示自身抗体可能降低ACE2活性[56].总的来说,RAAS内部的平衡似乎有利于经典RAAS激活,这与更糟糕的疾病进展和生存有关。
RAAS中的局部更改
除了PAH患者的经典RAAS信号的全身性改变外,局部的改变也有报道。ACE从Ang I向Ang II的转化主要发生在肺部,发现肺部ACE活性整体下降[60].然而,这种减少可能部分是因为内皮表面面积的减少。相比之下,PAH患者分离的肺动脉内皮细胞中ACE活性增加[57而ACE表达在较小的肺血管(腺泡内动脉到毛细血管)中上调[61]及丛状病变[61,62]。这些发现暗示Ang II的形成在多环芳烃肺血管系统局部增加。此外,PAH患者远端肺动脉AT增加1R表达式[57].持续接触Ang II可导致离体患者肺动脉平滑肌细胞肥大和增殖通过在1R信号[57],并与血管炎症、纤维化和内皮功能受损有关[12].
此外,在肺血管系统中也可能合成局部醛固酮[63].多环芳烃肺中醛固酮水平或矿物皮质激素受体表达的变化尚未见报道。然而,在实验性多环芳烃以及分离的人肺动脉平滑肌细胞和肺动脉内皮细胞中,醛固酮与血管重塑的增加有关[63- - - - - -65].
持续的经典RAAS活性对心脏也有不利影响,包括心肌细胞肥大、纤维化和传导系统紊乱[12].人的心脏有一个局部RAAS系统,独立于循环RAAS系统,但与之相关[66].只有一项研究报道了多环芳烃患者心脏RAAS活性的局部变化[67].与肺相反,AT1R的表达在右心室下降,尽管ACE的表达和Ang II的形成增加[67].多环芳烃中心脏醛固酮信号转导的局部变化尚未见报道。
对替代RAAS活动的局部变化知之甚少。随着人们对严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)的入口点ACE2重新产生兴趣,最近的研究表明,在外植的PAH肺中,可溶性但非膜结合的ACE2的mRNA增加了[68].尽管ACE2的上调在PAH中被认为是有益的,但这种向可溶性ACE2的转变对PAH患者的意义尚不清楚。在心脏中,ACE2活性可能增加,表现为Ang II中Ang1-7的形成增加[69].
多环芳烃的神经激素调节策略
综上所述,我们可以清楚地看到,多环芳烃中的神经激素系统在全身和局部都处于失衡状态。这两个水平的不平衡与更糟糕的疾病进展、生存或心脏和血管重构相关。尽管在心排血量下降的情况下,增加SNS和经典RAAS活性是维持心血管稳态所必需的,但人们认为SNS和RAAS的慢性激活最终会导致不适应。这可能导致心脏进一步恶化和神经激素平衡增加的恶性循环,并因进行性肺血管重构而加剧。因此,神经激素系统一直是一些实验性治疗的目标。治疗策略可分为药理学方法和非药理学方法。概述了ANS和RAAS的治疗策略图2而且3.,分别。
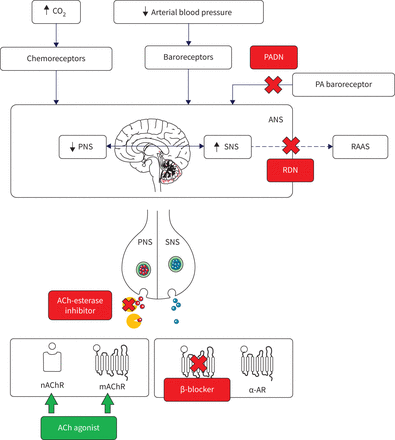
自主神经系统(ANS)的药理和外科干预靶点。PADN:肺动脉去神经;PA:肺动脉;PNS:副交感神经系统;SNS:交感神经系统;肾素-血管紧张素-醛固酮系统;RDN:肾去神经;课时:乙酰胆碱;nAChR:尼古丁乙酰胆碱受体;mAChR:毒蕈碱乙酰胆碱受体; AR: adrenergic receptor.
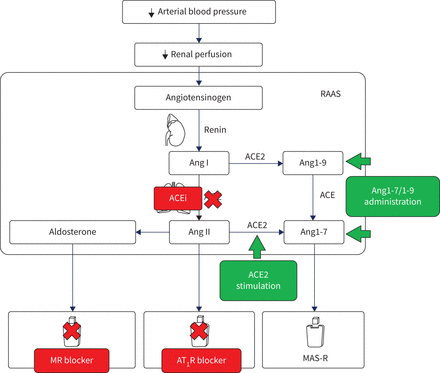
肾素-血管紧张素-醛固酮系统(RAAS)的药理和外科干预靶点。Ang:血管紧张素;血管紧张素转换酶;ACEi: ACE抑制剂;MR:矿物皮质激素受体;在1R: Ang II型1受体;MAS- r: MAS受体。
药物治疗
针对不同神经激素系统的药理学治疗的效果总结在表1.在这里,我们将讨论一些已经在患者中测试过的方法。
β受体阻滞剂以SNS为靶点,是左心衰治疗的基石,但目前的指南不建议在PAH中使用β受体阻滞剂[2].一项小型试点研究证实了非选择性β受体阻滞剂卡维地洛在患者中的安全性[79].然而,在一项更大的随机对照试验中,卡维地洛并没有改善右心室功能和6MWD [81],尽管静息心率较低,β-肾上腺受体表达增加。为了防止可能的外周血管舒张和运动诱导的骨骼肌血流钝化,β1-肾上腺受体选择性β受体阻滞剂比索洛尔检测[80].在这项研究中,心脏指数的下降引起了人们对心脏功能实际上恶化的担忧[80].虽然没有发现进行性心力衰竭的其他指标,但心功能和6MWD缺乏改善,没有迹象表明给PAH患者开比索洛尔。β的遗传变异1-肾上腺受体可引起卡维地洛过敏,但对美托洛尔和比索洛尔不敏感[116可能导致对β受体阻滞剂的不同个体反应。
对经典RAAS的药理干预包括ACE抑制、AT1阻滞剂和矿物皮质激素受体拮抗剂。ACE抑制肺动脉高压的临床研究始于20世纪80年代,当时人们观察到卡托普利可以降低充血性心力衰竭患者的全身和肺血管阻力[92].两项早期研究表明,卡托普利可降低多环芳烃患者全身血管阻力,但不能降低肺血管阻力[91,92].相比之下,I发现肺血管阻力显著降低kramet al。[93服用卡托普利4天后。在这项5名患者的小型研究中,两名最年轻的患者在3周的维持治疗中出现了临床改善[93].总的来说,这些非常小的研究没有表明卡托普利抑制ACE在PAH治疗中的作用。事实上,ACE抑制剂的全身血管舒张作用可能会夸大SNS和经典RAAS活性。虽然没有进行进一步的试验,但ACE抑制可能在亚组患者中仍有益处。
在1阻断剂尚未在多环芳烃中进行临床试验。相反,两项临床研究调查了氯沙坦在慢性阻塞性肺疾病继发肺动脉高压中的应用[One hundred.]以及继发于肺部疾病或左心室衰竭的肺动脉高压[99].治疗8周后观察到氯沙坦的有益作用,包括降低平均肺动脉压(mPAP)和增加运动能力[99].然而,在慢性阻塞性肺病继发性肺动脉高压中,氯沙坦导致了心功能和运动能力改善的早期趋势,但在整个12个月的治疗过程中没有保持这种趋势[One hundred.].因此,在1氯沙坦阻断对肺动脉高压患者可能有短期而非长期的影响。
由于其利尿作用,矿物皮质激素受体拮抗剂被用于处理多环芳香型右心室衰竭的症状。然而,矿物皮质激素受体拮抗剂可能对心脏和肺有额外的影响。两项研究调查了矿物皮质激素受体拮抗剂螺内酯在多环芳烃中的应用。一项回顾性分析了在内皮素受体拮抗剂氨布里森坦的ARIES-1和-2试验中使用螺旋内酯的患者[117]揭示了使用螺内酯增强了氨布森坦在6分钟步行和多环芳烃严重程度上的益处[107].然而,使用螺内酯的患者在基线时通常有更严重的多环芳烃。因此,在这些患者中,氨布里森坦的治疗潜力可能更高,这将错误地提示螺内酯的作用。最近在42例1组多环芳烃患者中单独使用螺内酯进行了研究,其中19例为特发性多环芳烃[106].虽然没有发现螺内酯对纤维化标志物、运动能力、疾病进展或心功能的影响,但使用螺内酯是安全的,耐受性良好。正在进行的临床试验(ClinicalTrials.gov:NCT01712620)的目的是确定较长治疗时间和较早起药的螺内酯的临床潜力。
激活具有反作用的替代RAAS,而不是降低经典RAAS活性,也可能有助于恢复RAAS内部的平衡。我们才刚刚开始认识到替代RAAS系统在多环芳烃发展中的作用。因此,迄今为止,只有一项临床试点研究存在,调查重组人ACE2对5例特发性多环芳烃或遗传性多环芳烃患者的影响[55].重要的是,没有提出安全问题,ACE2的耐受性良好。此外,观察到肺血流动力学和炎症状态的短期改善,为进一步的ACE2给药试验铺平了道路。
非药物治疗则
神经激素调节的非药理策略的临床前和临床研究的结果总结在表2.在多环芳烃患者中,只有肺动脉去神经(PADN)被研究过。
肺动脉压力感受器激活反射性引起肺血管收缩[132,133),可能通过肾上腺素能神经[134].这为PADN作为一种逆转肺血管收缩的方法提供了理论依据。事实上,在13例接受PADN的PAH患者中观察到mPAP的急性下降[127].在3个月的随访中,即使患者完全停用多环芳烃药物,mPAP仍保持下降。此外,在padn后6个月,血流动力学、6分钟行走距离和临床状态均有逐步改善。这些改善在长达1年的随访后得以维持[129].血流动力学状态和6MWD的改善最近在一项多中心开放标签试验中得到证实,尽管该研究中的益处没有那么显著[128].重要的是,R奥斯玛et al。[128结果显示,在接受PADN的患者中,个体反应差异很大。当mPAP和肺血管阻力平均降低时,有3例患者肺血管阻力实际上增加了。然而,有趣的是,在本研究或另一病例报告中,没有观察到mPAP的急性降低[130],这表明除了缓解反射性血管收缩外,其他机制也可能起作用。
其中一个机制可能是社交活动的普遍减少。伸展的肺动脉压力感受器有助于增加健康个体的肌肉交感神经活动[135].考虑到肺动脉压的急剧增加,多环芳烃患者很可能也是如此。此外,肺动脉压力感受器刺激增加了动脉压力感受器设定点和阈值[136],导致动脉压力感受器失活,从而增加SNS活性。然而,padn术后4或6个月随访时心率保持不变[128,表明社交网络活动在手术后并没有减少。
神经激素调节策略在临床应用的局限性
到目前为止,我们已经描述了多环芳烃患者的全身和局部神经激素失衡和恢复策略。转译困难和缺乏对多环芳烃患者神经激素失衡发展的机制认识限制了神经激素调节疗法的使用。
在这篇综述中描述的所有研究中,有四分之三是在多环芳烃的各种动物模型中进行的,主要是大鼠、小鼠和猪。然而,β受体阻滞剂或血管紧张素转换酶抑制剂在动物研究中所看到的有希望的结果还没有转化为人体试验。显然,这些动物模型的有用性是有争议的。首先,常用的啮齿动物模型在某些方面与多环芳烃相似,但不是所有方面。实验性多环芳烃通常在几周而不是几年的过程中发展,就像人类多环芳烃的情况一样。这可能会限制补偿机制的发展[137].第二,临床研究总是在多环芳烃特异性治疗的背景下进行,而动物只接受研究药物。
多环芳烃神经激素调节的临床研究有其自身的局限性。重要的是,在终末期多环芳烃中,任何治疗的治疗窗口都很小,因此通常提倡早期干预[138].然而,应该强调的是,神经激素的变化并不仅仅是适应不良。事实上,神经激素活性的急性变化对维持心血管内稳态至关重要,因此对抗神经激素系统有时可能是有害的。在多环芳烃进展的某一时刻,持续的神经激素激活变得不适应。在这一阶段,神经激素调节可能是有益的。关于右心衰或左心衰患者神经激素变化的纵向数据很少。慢性充血性心力衰竭患者血浆去甲肾上腺素和肾素水平进行性升高[139,表明渐进式神经激素失衡。此外,在衰竭的心脏中发现的去甲肾上腺素、Ang II和醛固酮水平已被证明对心脏和血管系统产生有害影响,如其他文献所述[140,表明神经激素的剂量依赖性效应。因此,似乎有一个针对神经激素系统的最佳治疗窗口,介于病理水平的急性激活和慢性激活之间。因此,结合血流动力学和右心室功能数据,获得神经激素活性的纵向数据是至关重要的。
必须解决两个重要的限制,它们阻碍了对神经激素随时间变化的研究。首先,用于研究的人体组织几乎没有,只能从终末期多环芳烃中获得。因此,不太适合研究纵向变化。其次,多环芳烃是一种罕见的疾病,大多数临床研究最多只能包括几十名患者。这使得很难达到足够的统计能力,更不用说测试亚组患者或不同的药物剂量和时间。患者数量少与左心室衰竭中神经激素调节的研究有重要区别,在左心室衰竭中神经激素调节策略已被实施,尽管对神经激素随时间的变化缺乏类似的了解。这从两个方面影响了临床研究。首先,可以对左心室衰竭患者的大量队列进行回顾性分析,以确定影响神经激素调节策略疗效的因素。这在多环芳烃中是不可能的。其次,迄今为止,具有广泛纳入标准的小型临床研究几乎没有显示神经激素调节对多环芳烃的任何有益作用。 Failure to enrol large numbers of patients requires diligent patient selection to prove smaller, yet clinically significant treatment effects.
可供研究的人体组织和临床试验中有限的患者数量都不会改变。对神经激素变化的纵向评估可以告诉我们在疾病过程中何时何地神经激素脱轨变得明显,从而帮助选择患者采用特定的神经激素调节策略。此外,它将告诉神经激素调节策略是否如预期的那样及时和有针对性。因此,我们提倡开发、验证和使用非侵入性和微创性工具来监测多环芳烃的神经激素变化。在下一节中,我们将讨论可能的工具,在不同的发展阶段,这可能有助于提高我们对多环芳烃神经激素变化的理解。
多环芳烃神经激素变化的纵向评估策略
测量自主神经活动的黄金标准是直接测量(对)交感神经运动的肌肉微神经摄影,通常是在浅表骨骼肌。或者,区域去甲肾上腺素溢出的测定允许对SNS激活的器官特异性测定。使用微透析,可测定局部乙酰胆碱浓度以测定PNS活性[141].然而,这些测量都是高侵入性的,因此不适合重复测试。相反,血浆(或)肾上腺素水平已被用于研究SNS激活,但并不是一个可靠的标记[29].另外,外周血细胞中的β-肾上腺受体密度可作为SNS(过度)激活的标志[142].传统上,β-肾上腺受体密度的测定依赖于耗时的配体结合测定。然而,流式细胞术定量β-肾上腺受体密度最近有报道[143,允许进行简单、高通量的测试。使用该技术,研究表明与健康对照相比,多环芳烃患者血细胞中的β-肾上腺受体密度较低[144β受体阻滞剂卡维地洛可剂量依赖性增加[81].因此,外周血细胞的变化似乎与心脏的变化相似。使用流式细胞术定量β-肾上腺受体表达作为PAH患者SNS的标记物,还需要进一步的研究来验证。
测量PNS活性通过由于突触间隙中乙酰胆碱降解和清除率高,血浆乙酰胆碱浓度不可行[141].相反,血浆乙酰胆碱酯酶活性可能作为PNS活性降低的生物标志物[145],但这需要在多环芳烃患者中验证。
从心电参数中可以得出PNS和SNS活性的非侵入性间接测量方法。连续心跳之间的时间有自然变化,称为心率变异性。在频域上表示时,可区分高频(HF)、低频(LF)和甚低频谱功率[146].低频/高频比值通常用于确定交感神经-迷走神经平衡,假设低频功率由SNS产生,高频功率由PNS产生。然而,这种假设并不成立[146].因此,大多数研究都没有发现低频/高频比值与SNS和PNS活性的直接测量之间的相关性[141].在多环芳烃中尤其如此,在多环芳烃中,已观察到LF/HF比值与肌肉交感神经活动呈负相关[28].此外,在标准化实验室设置之外,适当测量和分析心率变异性变量是复杂的[141].尽管如此,已经描述了用于推导源自心跳的自主测量的改进方法[147智能手表和活动追踪器等可穿戴设备的出现,允许在现实环境中进行动态记录。
另一种确定中枢神经系统功能的非侵入性方法是测量最大运动后的心率恢复。多环芳烃患者心率恢复降低,并与变时功能障碍和临床恶化有关[36- - - - - -38,148,149].心肺运动试验(CPET)可方便、常规地评估心率恢复。然而,更简单的方法是在6分钟步行测试(6MWT)后进行心率恢复,这种测试在临床上更为常见。在心力衰竭患者中,心率恢复预测生存的预测价值与试验是在最大强度还是次最大强度下进行无关[150].在PAH患者中,6MWT后的心率恢复甚至比测试距离本身更能预测临床恶化[38].然而,对于从6MWT或最大CPET恢复的心率的使用,还没有在心衰或多环芳心病患者中进行直接比较。一项研究表明,与CPET相比,PAH患者在6MWT期间表现出相对较高的有氧能力,尽管心率较低,但没有将心率恢复作为PNS活动的标记进行比较[151].值得进一步研究的是,这些非侵入性测量(可能很容易从门诊测量或简单测试中获得)是否有助于确定和监测PAH患者的自主神经状态。
神经激素的变化也可以用成像技术来研究。正电子发射断层扫描(PET)可能成为一个额外的强大的工具,以研究神经激素激活在临床设置。许多PET示踪剂现已可用于研究ANS的不同方面,包括突触前神经递质循环、β-肾上腺受体密度、PNS末梢神经和mAChR表达[152].
PET示踪剂也用于研究RAAS活性,通过ACE和AT1R表达式[60,153].由于ACE示踪剂通常聚集在ACE高表达的器官中,因此特别适合用于观察肺中的ACE活性[153].对血浆水平和几种RAAS成分的活性的评估,虽然组织特异性较低,但速度更快、成本更低。如前所述,在进行性多环芳烃中,血浆Ang I和Ang II水平升高,而在稳定型多环芳烃中则没有升高[57].此外,血浆肾素水平是多环芳烃患者死亡率的独立预测因子[154].
总的来说,心率变异性算法和成像技术的不断发展为神经激素活动的测量和分离带来了希望。与血浆水平和CPET一起,它们可能为神经激素系统的纵向评估提供工具,并研究不同器官局部神经激素系统之间的相互关系。
结论
现在很清楚,神经激素失衡参与了多环芳烃的发展和进展。然而,神经激素系统对心血管内稳态至关重要。因此,为了成功的临床实施,神经激素干预的时机和特异性需要提高。由于可用于临床试验的患者数量限制了亚组的使用,因此需要对神经激素活性进行纵向评估。非侵入性技术,如成像技术,可能有助于确定哪些患者可能受益于神经激素调节,以及在疾病进展的哪个阶段。
可共享的PDF
确认
作者感谢Denielli da Silva Gonçalves Bos (São Paulo大学医学院肺脏部-心脏研究所,São Paulo, Brazil)的讨论。
脚注
利益冲突:H.J. Bogaard报告来自Janssen、Ferrer和Novartis的拨款和个人费用,在提交的作品之外。
利益冲突:A. Vonk Noordegraaf报告了来自Actelion和MSD的个人费用,来自拜耳的个人费用和其他(顾问委员会),来自强生和MSD Morphogen-IX的其他(顾问委员会),在提交的工作之外。
利益冲突:F.S.德曼没有什么可透露的。
利益冲突:e·l·彼得斯没有什么可透露的。
支持声明:H.J. Bogaard、A. Vonk Noordegraaf和F.S. de Man得到了荷兰心血管研究计划:荷兰心脏基金会、荷兰大学医学中心联合会、荷兰健康研究与发展组织和荷兰皇家科学院(CVON-2012-08 PHAEDRA、CVON-2018-29 PHAEDRA- impact、CVON-2017-10 Dolphin-Genesis)的支持。H.J. Bogaard和A. Vonk Noordegraaf获得了Actelion、GSK和Ferrer (Therabel)的研究资助。E.L.彼得斯、冯克·诺德格拉夫和F.S.德曼得到了荷兰科学研究组织(NWO-VICI: 918.16.610, NWO-VIDI: 917.18.338)的进一步支持。荷兰心脏基金会Dekker高级博士后资助项目(2018T059)。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2020年12月24日。
- 接受2021年3月13日。
- 版权所有©作者2021。
本版本按照创作共用署名非商业性许可4.0的条款发布。商业复制权利及许可请联系权限在}{ersnet.org