摘要
在儿童LRTI机械通气过程中,呼吸菌群从嗜血杆菌-和莫拉克斯氏菌属-以抗生素耐药为主的基因型到以抗生素耐药为主的基因型肠杆菌科,和葡萄球菌和链球菌物种。https://bit.ly/3pGfvhQ
给编辑:
下呼吸道(LRT)拥有独特的、动态的低密度微生物群落,这些群落是通过上呼吸道(URT)微吸入建立的[1- - - - - -3.].然而,在插管和机械通气过程中,气管内管暂时改变了上呼吸道和下呼吸道之间的解剖连续性,可能为空气中微生物提供了桥梁,为微吸痰提供了屏障。儿童严重LRTI插管后不久,鼻咽和LRT的微生物区系显示非常相似[4].然而,尚不清楚患儿在接受机械通气和抗生素治疗后康复时,呼吸道微生物群落是如何发展的。因此,我们分析了参与我们研究的急性LRTIs患儿的呼吸菌群变化,这些患儿入院于儿科重症监护病房(PICU)进行机械通气[4].
在2013年9月至2016年9月期间招募了29名需要插管和通气的社区获得性LRTI婴儿。队列的平均年龄为3.4个月(范围为1.0-12.8个月),其中48%为女性。所有患儿均诊断为毛细支气管炎。21例儿童的常规微生物检查结果可用。28/29名儿童接受了抗生素治疗(25卡莫昔拉夫,2种头孢菌素,1种阿奇霉素),其中5名在PICU入院前不久已经开始接受治疗。我们在插管时(29 NP, 27唾液,25 ETA)和拔管前(16 NP, 15唾液,14 ETA)获得鼻咽拭子、唾液和气管内抽吸物(ETA),平均值±sd插管后5.9±2.6天。收集唾液的方法是将吸水海绵放置在颊袋和舌下,直到唾液饱和,立即用无菌注射器将唾液转移到甘油DEPC培养基中。在常规气管插管抽吸时收集ETA,不灌注生理盐水。在PICU出院后51.9±13.5天随访期间,我们获得了20份NP拭子和19份唾液样本。
通过对16S rRNA V4高变区测序,生成微生物群谱。序列数据保存在NCBI Sequence Read Archive数据库(BioProject ID PRJNA669463)中。研究方法的详细资料已于先前发表[4].总体而言,插管时29 NP、27唾液和24个ETA样本,拔管时12 NP、14唾液和11个ETA样本,随访时20 NP和19个唾液样本通过了质量控制(可用样本的94.5%),符合进一步分析的条件。在基线菌群组成、年龄或性别方面,拔管样本缺失的婴儿与有样本的婴儿没有显著差异(数据未显示)。以16S rRNA基因为靶点,采用定量(q)PCR检测细菌载量[5,6].肺炎球菌的存在和丰度由lytAqPCR。
阿尔法多样性分别使用Chao1和Shannon丰富度和多样性指数进行评估。细菌负荷和α多样性总结为中位数(四分位间距(IQR)),并使用线性混合效应模型(包括受试者随机效应)评估各时间点的差异。在受试者内部限制排列的情况下,通过Bray–Curtis不相似矩阵上的排列多元方差分析评估总体微生物组成的差异。使用无监督分层聚类法将微生物群群分配给每个样本。如前所述,使用随机森林分类分析确定每个集群的生物标记物种[7].聚类和时间点之间的关联用Fisher的精确测试进行了测试。为了评估生态位之间的微生物群落一致性,我们计算了学科内的Bray-Curtis相似性(1 - Bray-Curtis dissimilarity)和个体操作分类单元(OTU)丰度之间的Spearman相关性。
我们的结果显示,在插管和拔管期间,所有生态位的细菌载量都显著下降,但对于唾液,这一差异不显著(NP:从92.2 (43.9-309.6)pg·µL−1至4.0 (1.6-24.0)pg·µL−1, p = 0.024;唾液:从270.3 (80.5-771.8)pg·µL−1至113.0 (20.1 ~ 290.6)pg·µL−1, p = 0.158;ETA从126.8 (31.6-708.2)pg·µL−1至3.9 (2.8-13.4)pg·µL−1, p = 0.039)。恢复后,NP菌载量仅略有增加(39.6 (13.9-144.6)pg·µL)−1, p=0.459),在唾液中的表达更强烈(达到364.8 (200.5-775.5)pg·µL−1, p = 0.014)。同时,插管和拔管的NP丰富度和多样性具有可同性(Chao1:从47.5(34.6-62.3)到46.8 (34.3-54.2),p=0.840;Shannon:从1.17(0.81-1.87)到1.53 (0.81-1.75),p=0.945。唾液的丰富度和多样性在插管和拔管时有所下降,但差异仅为显著(Chao1:从55.0(43.1-62.6)到46.8 (39.4-50.9),p=0.443;Shannon:从2.1(1.8-2.6)到1.5 (0.9-1.8),p<0.001,恢复后再次显著增加(至2.3 (1.8-2.6),p<0.001)。在ETA中,我们观察到插管和拔管之间的丰富度和多样性有轻微的不显著增加,这似乎主要是由于均匀度的增加而不是物种丰富度的增加(Shannon:从0.14(0.07-0.76)到0.99 (0.45-1.63),p=0.112;Chao1:从32.8 (29.4 - -42.8),51.0 (40.5 - -62.3),p = 0.065)。此外,插管和拔管期间,NP (R2=5.8%, p<0.001)和唾液(R2=7.6%, p<0.001),在ETA样本中甚至更高(R2= 11.2%, p = 0.002) (图1一个- c)。因此,与回收样品相比,NP和唾液菌群组成更不同于拔管前(NP: R2= 12.8%, p = 0.020;唾液:R2=10.2%, p=0.012)2= 7.0%, p = 0.001;唾液:R2=3.5%, p=0.038),表明由于在狭窄的时间范围内进行抗生素治疗和/或机械通气,对生态造成了显著的影响,并偏离了健康的微生物群。
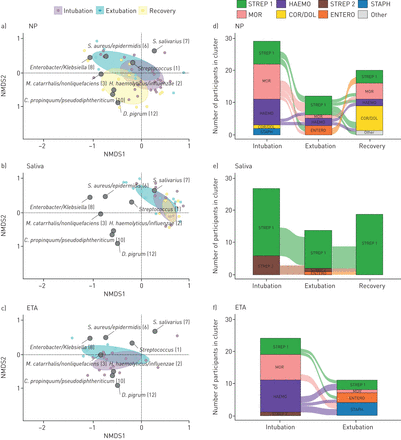
a–c)基于Bray–Curtis不相似矩阵的非计量多维标度(NMDS)双标图,显示a)鼻咽(NP)、b)唾液和c)气管内吸出物(ETA)在插管、拔管和2小时后的总体微生物群组成 恢复时间为个月,以及八个生物标记物操作分类单位。椭圆代表每个亚组数据点的标准偏差。d)NP,e)唾液和f)ETA在插管时间、拔管时间和2个月后的聚类转换冲积图 月恢复时间。基于Bray–Curtis不相似矩阵对所有样本进行分层聚类,确定了七个不同的聚类,其特征为链球菌(1)(链锁状球菌1),莫拉克斯氏菌属复活/ nonliquefaciens(铁道部)流感嗜血杆菌/溶血性嗜血杆菌(HAEMO),棒状杆菌属propinquum / pseudodiphtheriticum与Dolosigranulum pigrum(软木/痛单位)、唾液链球菌(7)(喉炎的症状2),肠杆菌/克雷伯菌(ENTERO),或金黄色葡萄球菌/表皮球菌(金黄色葡萄球菌)。堆叠的条形图表示每个时间点每个集群中的样本数量,条形图之间的连接表示在时间点之间有两个连续样本可用的参与者的过渡。
然后,我们对NP、唾液和ETA菌群进行了聚类,并区分了7个聚类,它们的特征分别是链球菌(1)(链锁状球菌1),莫拉克斯氏菌属复活/ nonliquefaciens(铁道部)流感嗜血杆菌/ haemolyticus(HAEMO),棒状杆菌propinquum / pseudodiphtheriticum与Dolosigranulum pigrum(软木/痛单位)、唾液链球菌(7)(喉炎的症状2),肠杆菌/克雷伯菌(ENTERO),或金黄色葡萄球菌/表皮球菌(金黄色葡萄球菌)(图1 d- f)。在NP和ETA中,MOR和HAEMO群集在插管时占优势,在通气和抗生素治疗后减少。COR/DOL谱只在NP样本中发现,且大多在恢复后观察到(p<0.05)。拔管时,仅在未接受抗生素治疗的单个婴儿中观察到mor群集。相比之下,在唾液中,插管时strep1和strep2簇均占主导地位,拔管时strep2簇减少,恢复后完全消失(不显著)。
总的来说,在拔管时,STREP 1、葡萄球菌和ENTERO聚集是最普遍的,这与接触抗生素后的预期变化一致。在strep1群集中,观察到从插管时肺炎球菌优势向拔管前非肺炎球菌链球菌优势的转变(Spearman相关性)lytACt-values与链球菌(1)插管时的丰度:ρ=−0.68,p<0.001;拔管时:ρ=−有趣的是,葡萄球菌谱在插管时仅出现在两个NP样本中,但在拔管时主要出现在ETA中(p=0.006)。肠簇在拔管时被发现(p<0.05)。肠杆菌/克雷伯菌在四名儿童中(2-8岁)成为最主要的OTU 插管和通气天数(平均NP丰度:50.8%,范围0.03-99.4%;唾液:11.9%,范围0.0-45.1%;ETA:64.5%,范围30.0-99.7%),尽管该OTU在插管时几乎不存在,但有一名儿童的NP丰度非常低,为0.008%。为了在物种水平上鉴定这种OTU,我们尝试重新培养相应的样本,并在其中三种被鉴定为肠杆菌属下水道MALDI-TOF质谱分析。总之,这些发现暗示了典型的医院获得性和耐抗生素的病原体大肠下水道在PICU期间,在这些儿童的呼吸道中定植和/或占主导地位。同样地,我们观察到a的优势寡养单胞菌在一例拔管前患者中,尽管在插管时几乎不存在埃塔菌群(0.002%),但仍有一例患者存在埃塔菌群(埃塔菌群的77.7%),再次提示在通气期间选择或生长。一般来说,入院时进行的常规培养证实了在12/21儿童的NP和/或ETA谱中观察到的主要病原体。培养结果在5/21儿童中为阴性,证实了非主要革兰氏阳性,但缺乏对主要病原体的检测在四名儿童中观察到t(革兰氏阴性)病原体。这些发现强调了培养结果,尤其是在接受抗生素治疗的儿童中,往往缺乏了解呼吸道病原体存在和/或占优势的能力。
我们之前在该队列中证明了插管时NP和ETA菌群的高度一致性,表明NP是幼儿LRTI的源群体[4].然而,有趣的是,插管时NP-ETA的一致性(受试者内中位数Bray-Curtis相似性0.66,IQR 0.44-0.81)在拔管前下降了(0.53,IQR 0.31-0.63),尽管这种差异没有显著性(Wilcoxon秩和检验,p=0.188)。此外,拔管前NP和ETA样本之间只有36个OTUs(联合相对丰度为36.6%)仍然存在显著相关性,而插管时为74个OTUs(联合相对丰度为84.2%),这表明非NP微生物可能已经在LRT群落中安顿下来。因此,我们研究了微滴吸是否可以解释这些结果,并研究了插管和拔管前唾液和ETA样本之间的一致性。我们观察到,在插管和拔管前(0.17,IQR 0.04-0.61)时,唾液和ETA之间的微生物群落组成的一致性都很低。此外,两小位相关的otu数量从插管时的70个(联合相对丰度57.0%)下降到拔管时的52个(联合相对丰度14.7%)。总的来说,我们的数据表明,与儿童口腔菌群相比,鼻咽菌群是呼吸道微生物更重要的来源,而且鼻咽菌群、唾液和ETA菌群在机械通气过程中相对独立进化,这导致上呼吸道和呼吸道微生物群落之间的分离增加。
综上所述,我们观察到,在插管和通气期间,在社区获得性LRTI危重患儿联合抗生素治疗期间,呼吸菌群组成明显改变,甚至进一步偏离“健康”状态。细菌负荷下降,优势病原体的相对丰度下降,同时允许耐抗生素细菌,包括葡萄球菌种类,非肺炎链球菌,和肠杆菌/克雷伯菌物种,殖民和/或过度生长各自的生态位。此外,我们的数据表明,插管/通气和/或抗生素使用对各自生态位的微生物群落有不同的影响。我们的研究结果与之前在成人身上的研究结果一致[8].然而,与成人不同的是,患有严重LRTI的幼儿的LRT菌群比插管前的口腔菌群更能反映NP,而后者在通气过程中没有改变。本研究的主要局限性是样本量小。未来,需要更大规模的研究来解开(不同)抗生素治疗和机械通气插管对呼吸菌群动力学的独立影响。进一步的研究尤其重要,因为插管期间的呼吸菌群组成最近与成人的临床结果有关。例如,维icksonet al。[9报道了重症成人肺中肠杆菌科菌种的检测与急性呼吸窘迫综合征和机械通气时间延长有关。类似地,在一个大型机械通气患者队列中,较差的临床结局与低α多样性合并LRT中病原体过度生长有关,而与典型口腔类群占优势的高α多样性相比[10].与这些发现一致,W面向对象et al。[11,发现口腔科物种丰度增加,包括链球菌插管期间和通气与成功拔管有关。因此,本文的研究结果证明了对危重患儿气管插管和通气期间呼吸微生物群变化与恢复的关系进行类似研究的必要性,以及探索方法,以防止在这一已经脆弱的患者群体中快速获得和/或富集抗生素耐药病原菌。
可共享的PDF
确认
我们感谢参与的孩子和他们的家人。我们还要感谢乌得勒支大学医学中心威廉敏娜儿童医院PICU的所有护士和儿科医生。
脚注
利益冲突:E.M.de Koff无需披露任何信息。
利益冲突:W.H. Man没有什么可披露的。
利益冲突:M.A. van Houten没什么可透露的。
利益冲突:nj.g. Jansen没有什么可披露的。
利益冲突:K. Arp没有什么可披露的。
利益冲突:哈斯拉特没有什么可披露的。
利益冲突:E.A.M.桑德斯没什么可透露的。
利益冲突:D.Bogaert无需披露任何信息。
支持声明:这项工作部分得到了荷兰科学研究组织(NWO-VIDI;CSO/NRS苏格兰高级临床研究奖学金(SCAF/16/03)。这项研究是由哈勒姆斯帕恩医院和荷兰乌得勒支大学联合发起的。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年7月6日。
- 接受2020年11月14日。
- 版权©2021人队。
这个版本是在知识共享署名许可证4.0的条款下发布的。