摘要
IFCT-0504 II期试验评估了厄洛替尼的疗效与卡铂-紫杉醇(CP)作为130例晚期鳞状突出腺癌(ADC)的一线治疗。
该研究的主要目标是治疗效果,基于16周的疾病控制终点进行评估。
主要目标得到满足,66例CP治疗患者中35例(53%)疾病得到控制,64例厄洛替尼治疗患者中25例(39.1%)疾病得到控制。全人群的中位无进展生存期(PFS)为3.6个月。疾病控制率在治疗组和病理亚型之间没有差异,而在PFS治疗组和肿瘤病理亚型之间有很强的相互作用(p=0.009)。用厄洛替尼治疗的粘液性肿瘤患者进展风险增加(危险比3.4,95% CI 1.7-6.5;p≤0.001)。两组非粘液性肿瘤患者的PFS相似。中位总生存期为20.1个月,不同治疗组间无差异。这些发现没有通过分子分析进一步阐明,毒性特征与预期一致。
我们的研究表明CP和厄洛替尼在晚期lepidic ADC的治疗中起主导作用。基于这些发现,厄洛替尼不应作为无表皮生长因子受体突变的鳞状ADC患者的一线治疗药物。
摘要
晚期鳞腺癌病理亚型与治疗(厄洛替尼/化疗)的相互作用http://ow.ly/QHA2q
简介
细支气管肺泡癌(BAC)术语在国际肺癌研究协会(IASLC)/美国胸科学会(ATS)/欧洲呼吸学会(ERS) 2011年指南中进行了回顾[188bet官网地址1].具有BAC特征的前腺癌(ADC)被归类为侵袭性非粘液性(NM)鳞状优势ADC (L-ADC)及其粘液性变体。
晚期L-ADC(前身为ADC-BAC)曾被广泛认为是耐化疗的,但在较早的回顾性研究中报告了相互矛盾的结果[2,3.],而对最佳治疗方法所知甚少,因此有理由启动一项特定试验[2,3.].此前只有两项非随机II期试验调查了紫杉醇单药疗法的疗效,每3周给药一次[4,5],但西南肿瘤小组(SWOG) 9714试验报告的低反应率和不可接受的毒性将这种方法定义为不适应[5].培美曲塞单药治疗最近取得了很好的效果法语组间de Cancérologie胸(法国胸科联合组间(IFCT)) 0401试验[6]以及在一项过早结束的II期试验中[7].三个II期试验评估了表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKIs)作为晚期ADC-BAC的一线或二线治疗的使用[8- - - - - -10],显示出令人鼓舞的疗效和良好的毒性特征。使用抗egfr抗体单药治疗也有类似结果的报道[11].
区分NM和粘液性L-ADC似乎越来越重要[1- - - - - -3.].在IFCT中-0401试验中,与EGFR-TKIs早期进展的粘液性患者相比,NM患者在吉非替尼治疗下表现出明显改善的无进展生存期(PFS) [10].然而,直到第22个月,患者组之间的总生存期(OS)没有差异,这表明在吉非替尼后给予卡铂-紫杉醇(CP)或培美曲塞作为“挽救”治疗对粘液性患者有效[6,10].因此,我们认为有必要评估CP方案在晚期L-ADC一线治疗中的效果,在IFCT-0504试验设计时,CP是用于非小细胞肺癌(NSCLC)的四种最有效的铂双联剂之一[12].最后,与厄洛替尼相比,为了最大限度地减少这种化疗的毒性,并使其在耐受性方面更易于接受,我们选择在每周方案中给予紫杉醇与卡铂,并维持紫杉醇,直到在疾病控制的患者中观察到进展,正如B先前建议的那样elaniet al。[13].
我们设计了一项随机、II期平行组试验,评估一侧厄洛替尼,另一侧卡铂加每周紫杉醇作为晚期L-ADC患者(原晚期BAC)的一线治疗。两个兵种之间的交叉是计划好的。病理亚型(NM型和粘液型)对治疗效果的影响也进行了评估,同时还评估了生物标志物的探索性小组。
材料与方法
研究设计
IFCT-0504是一项开放标签、随机、多中心、II期平行组试验,评估一线厄洛替尼和CP治疗晚期L-ADC的疗效。主要目标是治疗效果,终点为16周的疾病控制。次要终点为PFS和OS。我们的次要目标是安全性和生活质量,后者是未来文章的主题,以及病理肿瘤亚型对疗效的影响。探索性目标包括集中的生物标志物分析表皮生长因子受体及柯尔斯顿·拉斯(喀斯特)突变状态,以及微管蛋白-β III类(TUBB3)蛋白和MutS蛋白同源物2 (MSH2)在肿瘤标本中的表达。
该方案得到了Comité法兰西岛人身保护第十该试验由法国国家卫生局(www.clinicaltrials.gov标识符号码NCT00384826),并由所有病人提供书面知情同意书。
合格标准
为了纳入,所有患者必须在组织学或细胞学上被诊断为晚期BAC (IIIB/IV期),不能手术的I-IIIA期患者也符合条件[14].具有细胞学ADC特征且缺乏任何可用的组织学标本的患者,如果他们有弥漫性或肺炎型放射学表现提示BAC,则符合条件[1,15].病理诊断最初是根据2004年世界卫生组织(WHO)病理分类所作的局部病理评估[14] IFCT病理小组随后审查了所有肿瘤样本,并使用IASLC/ATS/ERS 2011 BAC术语将其重新分类为L-ADC和相应的病理亚型[1].进行抗disastase周期性酸- schiff染色以更清楚地区分NM与粘液性肿瘤[1,16].
年龄≥18岁,东方肿瘤合作组表现状态(PS)为0、1或2的患者符合条件。既往接受过肺癌全身治疗的患者被排除在外。
治疗
患者随机1:1接受厄洛替尼(E组)或CP (CP组),采用最小化方法,按性别分层,PS (0-1)与2)和吸烟状况(从不吸烟或戒烟未满5包年与≥5包年的前吸烟者或积极吸烟者)。厄洛替尼(150 mg / d)口服,CP静脉输注(第1天卡铂在曲线下6处,紫杉醇90 mg·m)−2第1、8和15天),最多6个28天周期,随后每周服用紫杉醇(90 mg·m)−2)维护。患者接受治疗,直到疾病恶化、无法忍受的毒性或死亡。进一步的治疗包括两种治疗在两个手臂的交叉。三线治疗为培美曲塞(500 mg·m−2),每21天重复一次。
评估
年龄、性别、吸烟状况及呼吸症状评分[10]在纳入时进行记录。在纳入研究前4周内,患者需要在计算机断层扫描(CT)和正常的纤维支气管镜上显示肺部病变,才能纳入研究。胸外检查包括脑CT或磁共振成像和上腹部CT或超声检查。
采用世卫组织标准评估反应[17],并在4周后进行CT扫描,然后每12周进行一次。由于在之前的IFCT-0401试验中观察到BAC患者亚群的早期进展,我们纳入了4周的早期评估[10].WHO标准优于RECIST(实体瘤反应评价标准),因为后者倾向于延迟疾病进展诊断[18,19].IFCT-0504指导委员会进行了独立审查,对治疗分配不透明。
毒性分级使用国家癌症研究所通用毒性标准(3.0版)。
统计方法
采用Fleming两阶段优化设计。我们测试的假设是16周的控制率是否至少达到50% (H1)与每只手臂内30% (H0)。在第一阶段,30例患者被累算。如果在这30例患者中观察到9例或更少的非进展性疾病病例,则该手臂将因无效而停止使用。如果观察到的非进展性疾病病例≥14例,则停止试验组并拒绝原假设。否则,将增加30名患者,使每组患者总数达到60名。如果在60例患者中观察到≥21例非进展性疾病,则原假设将被拒绝。这种设计提供了10%的I型错误率(单侧)和95%的功率。根据指导委员会的回顾性评估,考虑到可能有10%的患者不合格,该设计将使每组65名患者随机分配。
在所有分析中检测了治疗臂(E和CP)和病理亚型(粘液和NM)之间的成对相互作用。当相互作用显著时,进行分层,并以地层为单位进行单变量和多变量分析。logistic回归分析[23],目的是探讨与疾病控制和反应相关的人口统计学和临床因素。将单因素分析中p<0.2的变量纳入多因素logistic回归,然后采用逆向程序选择,保持显著性水平为0.05。采用Kaplan-Meier方法估计OS和PFS [24]和中位生存时间,使用Brookmeyer和C罗利[25].对于总生存期和PFS, Cox模型[26]用于计算风险比(HR),并对每个变量使用Wald检验。应用Cox模型来确定与生存显著相关的因素。P <0.05为差异有统计学意义。所有分析均使用SAS软件9.3版(SAS Institute Inc., Cary, NC, USA)进行。
结果
病人的特点
入组时间为2006年9月至2009年7月,133名患者注册,130名符合条件(组E: n=64;臂CP: n=66)。其中96例(73.8%)能够进行集中分子肿瘤分析(图1而且表1).除12例患者外,其余患者诊断时均为IIIB-IV期(表1).在诊断时的12例I-IIIA期患者中,11例在纳入试验前出现了手术后复发的晚期疾病,1例仍处于IB期但发展为不能手术的疾病。
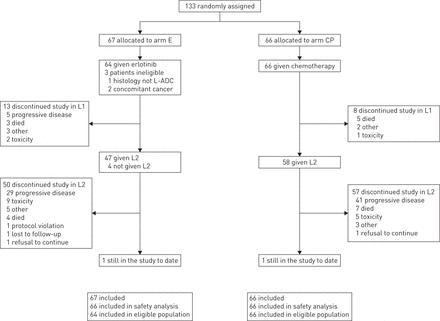
研究资料。艾凡:埃罗替尼;CP: carboplatin-paclitaxel;L-ADC:鳞片为主的腺癌;L1:第一行;L2:第二行。
其中67例为NM肿瘤,53例为粘液性肿瘤。总共有12名患者无法评估病理亚型(细胞学诊断),最后一名患者因缺乏L-ADC诊断而不符合条件。除了排除细胞学诊断为L-ADC的患者外,不同治疗组之间的临床和病理特征没有差异(表1)或在总体试验和分子群体之间(在线补充表S1)。
疾病控制和应对
总体而言,109例患者在16周时进行了反应评估:E组52例,CP组57例。共有21例患者因死亡(n=15)、毒性导致早期停药(n=3)、失去随访(n=1)、拒绝改变治疗(n=1)或其他原因(n=1)而无法评估。在4周评估时,由于疾病进展,42例患者(32.3%)应用早期治疗交叉(E组和CP组分别为24例和18例)。
根据两阶段弗莱明设计(见方法部分),主要终点达到,25例患者接受厄洛替尼治疗(疾病控制率(DCR) 39.1%, 95% CI 27.1-51.0%), 35例患者接受CP治疗(DCR 53.0%, 95% CI 42.0-65.0%)。此外,在整个人群中,60例患者在16周时实现了疾病控制(DCR 46.2%, 95% CI 37.6-54.7%),其中2例(1.5%)表现出完全缓解,24例(18.5%)表现出部分缓解,34例(26.2%)疾病稳定。在一项探索性分析中,DCR在两组之间没有统计学差异(E组和CP组分别为39.1%和53%;P =0.11)或病理亚型(表2).
DCR治疗效果与病理特征之间无交互作用。低RSS、女性性别或年龄> ~ 70岁的患者在16周时DCR明显升高(在线补充表S2)。
治疗依从性和毒性
两组患者的治疗依从性同样良好.两组28天周期的中位数为3次(四分位数范围:E组,1-6.5;臂CP, 1-9)。前六个周期给药的中位剂量强度厄洛替尼和紫杉醇分别为100%(范围526 - 100%)和81.3%(范围0-103%),卡铂为99.7%(范围0-135%)。
无意外不良事件发生(表3).E组3例(4.5%)患者和CP组16例(24.2%)患者因治疗相关不良事件停止治疗(p=0.001)。
总体而言,105例(80.8%)患者接受二线治疗(厄洛替尼后CP: n=47;CP后厄洛替尼:n=58)和77(59.2%)三线治疗(培美曲塞87.0%)。有112人死亡,其中一人可能归因于E组的治疗毒性。
PFS和OS
中位随访时间为69.4个月(范围53.0-87.4个月),1例患者在3个月后失访。中位PFS和OS分别为3.6个月和20.1个月(图2).1年、2年和3年OS率分别为63.9% (95% CI 55.7-72.1%)、43.6% (95% CI 35.2-52.0%)和30.8% (95% CI 23.0-38.7%)。
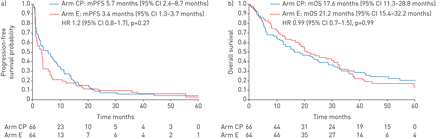
a)无进展和b)总人群中治疗组的总生存期。Arm CP(卡铂-紫杉醇)作为计算危险比(HRs)的参考。艾凡:埃罗替尼;mPFS:中位无进展生存期;mOS:中位总生存率。
治疗组和病理亚型对PFS的影响
而PFS在不同治疗组间无差异(表2而且图2),治疗效果之间存在较强的交互作用(E与CP)对PFS亚型、粘液型和NM型的影响(p=0.009) (图3).因此,分析按病理亚型进行分层。
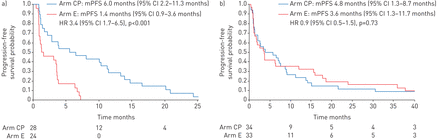
总体人群中按治疗组和病理亚型划分的无进展生存期。a)卡铂-紫杉醇(CP)和厄洛替尼(E)组黏液性肿瘤无进展生存期。b)臂CP和e中非粘液性肿瘤的无进展生存期以臂CP作为计算危险比(HRs)的参考。交互作用的p值:p=0.009。mPFS:中位无进展生存期。
在粘液性L-ADC患者中,在单变量和多变量分析中,只有治疗组与PFS改善相关(在线补充表S3)。以手臂CP为参考,使用厄洛替尼治疗的粘液性患者进展或死亡的风险显著增加(HR 3.4, 95% CI 1.70-6.50;p < 0.001)。使用厄洛替尼治疗粘液性患者的中位PFS仅为1.4个月(95% CI 0.9-3.6个月),而使用CP治疗的中位PFS为6.0个月(95% CI 2.2-11.3个月)(图3).在多变量分析中,年龄为> ~ 70岁且不吸烟的NM L-ADC患者PFS改善。诊断时为I-IIIA期但术后复发的患者PFS较差(在线补充表S4)。两组NM患者的中位PFS相似(E: 3.6个月,95% CI 1.3-11.7个月;CP: 4.8个月,95% CI 1.3-8.7个月)(图3).
分子群体的探索性分析
在分子人群中,DCR为50.0% (95% CI 40.0-60.0%),中位PFS和OS分别为3.6个月(95% CI 1.9-6.5个月)和23.0个月(95% CI 15.2-30.0个月)(表2).
生物标志物分析结果
总的来说,96个肿瘤标本中的76个(79.2%)进行了所有四种生物标志物分析(表2).表皮生长因子受体突变(外显子19:n=3;21外显子;在5例(5.6%)病例中观察到n=2),所有病例均为NM肿瘤(100%)(黏液肿瘤与NM肿瘤之间的p=0.03)。喀斯特24例(27.3%)发生突变,其中粘液性肿瘤19例(44.2%),NM性肿瘤5例(9.4%)(p=0.0003)。
表皮生长因子受体突变状态、MSH2和TUBB3表达在两组间平衡良好。喀斯特E组的突变频率低于CP组(17.1%)与36.2%, p=0.04)(在线补充表S6), 24个肿瘤中只有7个含有喀斯特MSH2和TUBB3的表达在粘液和NM患者之间没有差异(数据未显示)。
生物标志物分析对DCR、PFS和OS的影响
在分子群体中未发现治疗臂效应对DCR的影响与病理特征之间的相互作用。L-ADC的存在表皮生长因子受体突变(OR 10.3, 95% CI 1.3 -未确定;p=0.025)和年龄>70岁(OR 3.5, 95% CI 1.3-9.9;多变量分析显示,p=0.01)与16周时DCR显著增加相关(数据未显示)。
在分子群体中发现PFS治疗组和肿瘤病理亚型之间存在显著的相互作用(p=0.04)(在线补充图S1)。因此,分析按病理亚型进行分层。然而,没有分子测试能够为粘液和NM患者提供额外的预测疗效信息。
与一般人群一样,在多变量分析中,只有治疗组与粘液性L-ADC患者PFS改善相关。以CP组为参考,使用厄洛替尼治疗的粘液性患者进展或死亡风险显著增加(HR 4.1, 95% CI 1.9-9.0;p<0.001)(在线补充表S7)。在NM - L-ADC患者中,在多变量分析中,不吸烟状态与PFS改善相关,而诊断时的I-IIIA期与PFS恶化相关。两组NM患者的PFS相似(在线补充表S8)。
在多变量分析中,发现生物标志物数据对OS无影响,尽管NM - L-ADC患者(p=0.09)或表皮生长因子受体突变(p=0.05)倾向于提高生存率(表2).
讨论
IFCT-0504试验是自2011年IASLC/ATS/ERS指南发布以来首次评估晚期L-ADC管理的试验,并实现了其主要目标,两组患者16周DCR均超过30%。其次要目标所产生的调查结果也令人感兴趣。厄洛替尼和CP疗效与L-ADC病理亚型之间存在强相互作用。然而,这一发现并没有通过分子分析来阐明。最后,根据一线治疗选择(厄洛替尼),OS没有差异与CP)。
我们的研究人群与先前评估晚期BAC的试验相似,特别是在NM肿瘤(51%)和粘液性肿瘤(42%)的相对比例方面[5,7,8,9,10,11].与之前的报道一致,表皮生长因子受体而且喀斯特5.6%(6-22%)检测到突变[9,10,11]及27% (10-30%)[2,3.]的个案。表皮生长因子受体突变只在NM肿瘤中发现,而喀斯特突变与粘液性肿瘤或吸烟的NM肿瘤患者有关。我们的结果与未明确TUBB3阳性表达的肺部ADC病例的结果相似(67.5%)[27,28]和MSH2高表达(40.5%)[29],但未发现蛋白表达与临床特征及L-ADC病理亚型有明显相关性。
我们的DCR和PFS结果与先前报道的晚期BAC人群相似[4,5,7- - - - - -11].DCR在治疗组和病理亚型之间没有差异,尽管治疗效果之间有很强的相互作用(组E与CP)对PFS亚型、粘液型和NM型的影响(p=0.009) (图3),正如先前的研究所显示的[10].以CP组为参考,使用厄洛替尼治疗的粘液性患者的疾病进展或死亡风险显著增加(HR 3.4, 95% CI 1.7-6.5;p≤0.001),厄洛替尼治疗的粘液性患者的中位PFS比cp治疗的粘液性患者低4倍。然而,治疗臂的选择不影响NM L-ADC患者的PFS。
这些发现在分子群体中得到了证实。表皮生长因子受体突变与DCR的改善(100%与为46.2%表皮生长因子受体分别为突变型和野生型;p=0.02)和PFS (18.5 .与3.5个月,p=0.08) (表2) [9- - - - - -11].然而,低表皮生长因子受体突变率(n= 5,5.6%)表明这种分子改变对治疗效果的影响很小,即使在e组,DCR和PFS也不受肿瘤的影响喀斯特突变状态(表2).考虑到喀斯特在E组患者的41个肿瘤中,仅在7个肿瘤中观察到突变,这一发现不能解释厄洛替尼在粘液性患者中的低疗效[30.].TUBB3和MSH2是先前被发现在腺癌中呈阳性表达的标志物[21,22].之前的报道也表明,TUBB3 [27,28]及MSH2 [29]蛋白水平,通过免疫组化评估,可预测NSCLC中顺铂和紫杉烷反应。然而,MSH2和TUBB3肿瘤表达对DCR或PFS均无影响(表2),即使在CP组中也是如此,这与最近发表的一项关于接受紫杉烷/长春瑞滨化疗的NSCLC患者的荟萃分析形成了鲜明对比[31].
我们的结果表明,对于晚期L-ADC患者,一线治疗的选择似乎更依赖于病理亚型,而不是假定的预测生物标志物,除了少数NM L-ADC患者表皮生长因子受体突变。然而,我们没有探索野生型EGFR-TKI耐药相关的其他生物标志物表皮生长因子受体非小细胞肺癌(32].表皮生长因子受体信号通路的其他分子异常(一种蛋白激酶,的兵(细胞外信号调节激酶)和PTEN(磷酸酶和张力同源物)损失)在晚期BAC中观察到[33,34].HER2(人EGFR2) [33,35]或肝细胞生长因子/c-met过表达/扩增在粘液性BAC中更为常见[36],可能与EGFR-TKI耐药有关。最近发现,与NM肿瘤相比,粘液性肿瘤过表达胰岛素样生长因子-1受体(IGF1R)和双调节蛋白[33,34],在吉非替尼治疗下,IGF1R较高的表达与疾病进展相关[37,38].
尽管在紫杉醇单一疗法治疗的粘液性患者中有改善OS的报道[5]以及接受EGFR-TKIs治疗的NM患者[8,10],这些观察结果并没有得到我们数据的支持。我们发现在整个人群中病理亚型与治疗效果之间的强相关性对OS没有影响,这也是出乎意料的,尤其是在粘液亚型中。最后,无论是表皮生长因子受体而且喀斯特突变状态或MSH2和TUBB3表达与长期生存明显相关,这可能是我们试验设计的结果。鉴于我们的试验缺乏这种子集分析的能力,IFCT-0504试验设计可以解释这些发现。首先,厄洛替尼可能比吉非替尼更有效表皮生长因子受体-突变群体,如前所述[39].其次,我们在每周计划中应用紫杉醇作为铂基双联剂,目前已证明与单药治疗相比,紫杉醇可改善ADC患者的OS [40].第三,我们的交叉治疗阶段旨在让所有患者接受目前在晚期BAC中评估的两种最佳治疗方案(EGFR-TKI和基于紫杉醇的化疗)[2,3.].我们预先定义的三线培美曲塞方案是基于IFCT-0401试验的先前数据,这些数据表明吉西他滨的效果较差[6],而培美曲塞单药疗法最近已被证明在晚期BAC中具有出色的活性[7].最后,我们纳入了早期评估(4周),以检测野生型患者早期进展的风险表皮生长因子受体L-ADC接受EGFR-TKIs作为一线治疗[41,42].
因此,我们的研究证实了铂盐、紫杉醇和培美曲塞等常规化疗在晚期L-ADC治疗中的作用。我们的研究结果也敦促医生不要将TKIs作为急性脑缺血患者的一线治疗表皮生长因子受体野生型肿瘤。病理结果证明比非成瘾性分子生物标记物更有价值(喀斯特, MSH2和TUBB3)选择最佳治疗方案,我们的数据证实,对于粘液性L-ADC患者,化疗应优于EGFR-TKIs。然而,一些新的体细胞基因融合可能为晚期粘液性L-ADC提供了治疗机会,这种肿瘤除了化疗外没有有效的治疗方法,经常表现为多灶性不可切除疾病[43,44].
确认
这项工作之前在2011年6月美国伊利诺伊州芝加哥举行的美国临床肿瘤学会年会上部分发表[45].
IFCT研究人员(按他们对研究贡献的顺序)是Nathalie Baize (CHU,昂热,法国),Jean-François Morere (APHP, CHU Avicenne,博比尼,法国),Dominique Paillotin (CHU, Bois-Guillaume,法国),Pierre Mourlanette (Clinique des Cèdres, Cornebarrieu,法国),Laure Gautier-Felizot (CH, Dax,法国),Chrystèle Locher (CH, Meaux,法国),Michel Poudenx (CRLCC,法国),Daniel Coëtmeur (CHG,圣布里尤,法国),Pierre Fournel (ICL, Saint-Priest en Jarez,法国),法国),Youcef Douadi (CH、Saint-Quentin、法国),她Audigier-Valette(气、土伦、法国),菲利普·布朗(CH、价、法国),迪迪埃Debieuvre(气、Vesoul、法国),帕特里克Chatellain (CH、Annemasse、法国),让-吕克·布列塔尼人(CHG、贝尔福、法国),弗朗索瓦Guichard (Polyclinique,波尔多,法国),阿兰Vergnenegre(医院du Cluzeau、里摩日、法国),莫里斯Perol(克罗伊Rousse,里昂,法国),帕特里斯·雷(CHU,尼姆,法国),伯纳德Lebeau(安东尼APHP、巴黎、法国),Gislaine Fraboulet (CH, Pontoise, France), Lidia Petit (CHU, Reims, France), Alain Prevost (CRLCC, Reims, France), Marielle Sabatini (Polyclinique, Saint-Jean-de-Luz, France), Philippe Richard (CHR, Saint-Omer, France)和Eric Pichon (CHU, France, Tours)。
作者要感谢Marie Paule Lebitasy, Elodie Amour, Quân Tran, Jérémy Monchaux, Ahmed Slimani和Rébecca Rouveau(法国巴黎IFCT临床研究部)。
脚注
编辑评论:呼吸呼吸J2015;46: 1259-1261 [doi:10.1183/13993003.01563 -2015]
这篇文章有补充资料可从www.qdcxjkg.com
临床试验:本研究注册于www.clinicaltrials.gov标识符编号NCT00384826.
支持声明:这项工作得到了IFCT的支持,得到了Roche SA France的无限制赠款(Roche SA France也提供了厄洛替尼)和法国抗癌联盟(法国抗癌联盟).罗氏没有参与试验设计、数据收集或解释、讨论或手稿撰写。本文的资助信息已存入FundRef.
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2014年12月24日
- 接受2015年7月8日。
- 版权所有©ERS 2015














