文摘
流行病学研究表明,香烟烟雾暴露的危险因素增加了敏化作用和哮喘的发展。本研究的目的是检查香烟烟雾对敏化作用的影响和过敏性气道炎症反应低剂量的屋尘螨(HDM),并获得潜在机械的见解。
老鼠被暴露于低剂量的HDM提取结合空气或香烟烟雾暴露,在过敏原敏化作用或在过敏性呼吸道疾病的发展。
老鼠与此同时暴露于低剂量的HDM,加上吸烟3周,演示了一个哮喘表型显著增加气道嗜酸性粒细胞,杯状细胞化生,气道高反应性和HDM-specific血清免疫球蛋白G1,相比唯一HDM或香烟烟雾暴露。此外,香烟烟雾吸入,在最初接触HDM过敏原,足以促进哮喘表型的敏化作用和发展一个完整后重新HDM。树突细胞介导运输机械化、香烟烟雾暴露短放大荧光素isothiocyanate-labelled HDM过敏原的胸内淋巴结和生成本地辅助细胞2型反应。
短的香烟烟雾暴露足以促进过敏敏化作用和低剂量HDM-induced过敏性哮喘的发展,可能通过影响树突细胞的功能。
大多数哮喘开始于儿童早期敏化作用后,他们再次暴露在无处不在的环境过敏原,如屋尘螨(hdm)、模具、植物花粉、动物皮屑。敏化作用强烈依赖的风险水平的过敏原接触(1]。在过去的几十年,哮喘的发病率增加了在世界范围内,尤其是在工业化国家。这强烈的哮喘患病率上升强调环境和社会经济条件的一个重要作用[2]。
的一个主要与哮喘有关的环境危险因素暴露于香烟烟雾中(3]。流行病学研究表明,吸烟负责高哮喘严重程度评分(4,5),减少肺功能(5,6)和贫穷的哮喘控制(7,8]。吸烟甚至与敏化作用增加有关HDM过敏原(9),似乎是在儿童和成人哮喘发作的危险因素10- - - - - -12]。调解机制的副作用吸烟对哮喘发病机制有待阐明。大多数小鼠模型,旨在描述吸烟和过敏性气道炎症之间的复杂的相互作用,依靠“代孕”的敏化作用过敏原卵清蛋白(OVA) (13- - - - - -18]。当卵子本质上是一个惰性蛋白质,香烟的作用可能被高估了。此外,生化卵子之间性格的差异和现实生活中的过敏原是一个不可否认的限制以前卵巢模型。
解释观察到的哮喘患病率增加由于香烟烟雾暴露,我们提出对敏化作用,吸烟可以降低阈值HDM过敏原。我们开发了一个临床相关的过敏性哮喘小鼠模型,使用低剂量的HDM作为现实生活中的高空过敏症,加上吸烟。我们检查了香烟烟雾的影响在敏化作用和随后的哮喘发展和检查接触几天烟是否足以'局部淋巴结的敏化作用。最后,我们寻找潜在的机械的见解。
方法
老鼠
雄性BALB / c小鼠(6 - 8周大)购买的哈伦(泽斯特、荷兰)。所有在活的有机体内动物伦理委员会批准的操作是根特大学医学和健康科学学院(比利时根特)。
香烟烟雾暴露和HDM管理
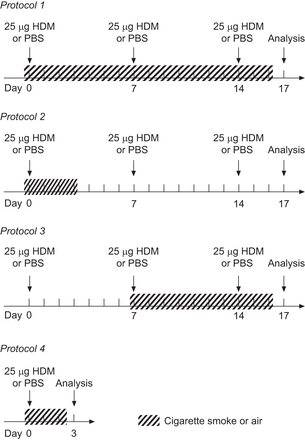
老鼠每组(n = 10)受到全身香烟(3 r4f肯塔基引用香烟;美国肯塔基州列克星敦市肯塔基大学)如前所述19]。控制老鼠暴露在空气中。30分钟后烟雾暴露,25μg HDM提取(Dermatophagoides pteronyssinus;爱格里尔实验室、美国NC) (Der p 1 25.27μg·毫克−1蛋白质;内毒素8.43 U·毫克−1)或PBS鼻内接种isoflurane-anaesthetised老鼠在天0,7和14和老鼠在17天分析。评估的影响香烟的发展HDM-induced过敏性哮喘,我们执行协议1 (图1)。为了揭开香烟烟雾的影响在敏化作用阶段,老鼠受到HDM并根据协议2或4(香烟图1)。香烟烟雾的影响在挑战阶段是评估使用协议3 (图1)。
投资协议。四组都包含在我们的试验装置:PBS /空气,PBS /香烟(唯一的香烟),屋尘螨(HDM) /空气唯一(HDM)和HDM /香烟。控制老鼠暴露在空气中。
支气管肺泡灌洗和cytospins
最后烟雾暴露和72 h后24 h后HDM应用程序中,老鼠实施安乐死的过量戊巴比妥(Sanofi-Ceva、巴黎、法国)。支气管肺泡灌洗(BAL), cytospins和细胞分化进行了如前所述[19]。剩余的细胞用于fluorescence-activated细胞分选仪分析。
肺癌和纵隔淋巴结单细胞悬浮体
肺灌注生理盐水+ EDTA通过肺动脉去除污染血液细胞。肺、纵隔淋巴结(mln)被移除和消化如前所述20.]。
流式细胞术
染色程序、数据采集和分析进行了如前所述[19]。单克隆抗体(mab)用来确定小鼠树突状细胞(DC)人口anti-CD11c(克隆HL3) anti-major组织相容性复合体(anti-MHC)二类(我/我,克隆M5/114.15.2)和anti-CD11b(克隆M1/70)。CD11b+DCs被定义为CD11c-bright、低autofluorescent细胞强烈表达MHC II类和CD11b表面。以下马伯被用来染色小鼠t细胞亚类:anti-CD3(克隆145 - 2 - c11), anti-CD4(克隆GK1.5) anti-CD8(克隆53 - 6.7)和anti-CD69(克隆H1.2F3)(所有从BD Pharmingen马伯,圣地亚哥,美国)。
mLN细胞培养
Paratracheal和胸内淋巴结parathymic收集到无菌试管中冷(4°C)组织培养基(中医)和消化(如上所述)来获取单个细胞悬液。中医是准备使用RPMI 1640补充10%胎牛血清,l谷氨酰胺、青霉素、链霉素和β-mercaptoethanol(所有从Gibco BRL;英杰公司集团;Merelbeke、比利时)。细胞被一式三份转移到圆底,96 -孔板(美国加利福尼亚州圣何塞,正欲)有或没有HDM提取μg·15毫升−1培养基,在2×10的密度5细胞每口井,湿润37°C孵化器孵化有限公司为5%2。5天之后,上层的收获和冷冻细胞因子的测量。
组织学
左肺在4%多聚甲醛固定,嵌在石蜡中。横向部分3μm与刚果红染色(Klinipath,克拉,比利时)突出嗜酸性粒细胞,周期性acid-Schiff识别杯状细胞,或应用α-smooth肌肉肌动蛋白评价气管平滑肌的内容。使用蔡司KS400图像分析仪定量测量进行平台(从、德国)如前所述21]。确定肥大细胞,肺沾toluidin蓝色。肥大细胞的数量统计每个字段(整个左肺叶)。只有那些位于气道壁包括进行分析。
蛋白质测量
总免疫球蛋白(Ig) E测定使用涂布microtitre盘子和生物素化的多克隆兔anti-mouse IgE(大学(Universite libre de Bruxelles) s Florquin,布鲁塞尔,比利时)。的检测HDM-specific IgG1, microtitre盘子被涂上一层HDM提取。血清添加,辣根peroxidase-conjugated多克隆山羊anti-mouse IgG1抗体(美国Bethyl实验室、蒙哥马利、TX)。水平的HDM-specific IgG1发表在光学密度。mLN上层的化验了白介素(IL) 4, IL-5, IL-13, IL - 10和干扰素(IFN) -γ通过多路复用(默克密理博,布鲁塞尔,比利时)。碎的上层清液肺、IL-25 IL-33,胸腺基质淋巴细胞生成素(TSLP) granulocyte-macrophage集落刺激因子(gm - csf)和IL-1β用ELISA(研发系统,阿宾顿,英国)制造商的指示。
气道反应性的评估
气道反应性测定,曝露在tracheostomised老鼠使用FlexiVent系统(Scireq,蒙特利尔,加拿大)。注射引起的神经肌肉阻滞是泮库溴铵(1毫克公斤−1)静脉注射。检查气道高反应性,老鼠的挑战随着剂量的碳酰胆碱(0、5、10、20、40、80、160和320年μg·公斤−1)。“快照摄动”策略实施的阻力(动态)整个呼吸系统(航空公司、肺癌和胸壁)。对于每一个鼠标,剂量反应曲线生成和计算曲线下的面积。
评估DC迁移的气管内的荧光HDM滴注法
获得荧光标记HDM HDM提取分离反对carbonate-bicarbonate缓冲区(pH值9.5)一夜之间在4°C。10 mg·毫升−1异硫氰酸荧光素(FITC)在二甲亚砜(DMSO溶液;西格玛奥德里奇,Bornem,比利时)添加到HDM溶液在室温下和旋转1 h。在黑暗下,执行整个过程无菌条件。经过4天的香烟烟雾暴露,犀牛老鼠(i.p。氯胺酮(80 mg·公斤1;氯胺酮1000切瓦;切瓦桑特Animale,比利时布鲁塞尔)和甲苯噻嗪(8毫克公斤−1;Rompun 2%;拜耳公司、勒沃库森、德国)垂直和50μL FITC-conjugated HDM举行(100μg)或PBS是用移液器吸取略高于他们的声带。老鼠牺牲0,24和48 h后滴注法。mln被移除,如上所述进行处理。歧视之间的mLN气道(AW) (CD11c派生而来int-high/ MHC II高)和non-airway派生DCs (CD11c(算了)+/ MHC IIintV)进行发布的使用方法ermaelenet al。(20.]。的百分比HDM-bearing AW-DCs决心通过流式细胞术FITC的分数+MHC II高CD11cint-high细胞。结果表示为FITC的百分比+DCs相对于直流总人口。
统计分析
统计分析与执行PASW统计18(美国芝加哥,IL)使用非参数测试。不同实验小组使用Kruskall-Wallis测试比较多比较。两两比较了使用Mann-Whitney紫外线测试。一个假定值≤0.05被认为是显著的。报道值表示为±扫描电镜。
结果
吸烟促进最近诊断为过敏性哮喘的发展
评估吸烟的作用HDM-induced过敏性哮喘的发病机理,BALB / c小鼠暴露于香烟烟雾或空气3周和灌输HDM(25μg)或PBS一周一次(图1、协议1)。相比之下,我们先前描述模型(22),我们灌输这位少HDM为了限制HDM的生物效应。
接触HDM和香烟烟雾加剧BAL流体和肺组织的过敏反应
唯一的鼻内交付HDM引起微弱与嗜酸性粒细胞增加哮喘表型,CD11b+DCs和CD4+和CD8+T淋巴细胞相比PBS-exposed控制老鼠(图2)。香烟烟雾暴露增强总细胞和巨噬细胞的数量(数据未显示),中性粒细胞,CD11b+DCs和CD4+和CD8+球流体相比air-exposed小鼠T淋巴细胞(图2)。随之而来的接触HDM和香烟烟雾过敏表型显著放大。这反映的嗜酸性粒细胞数量增加10倍和CD11b上升+DCs和CD4+和CD8+T淋巴细胞与其他组相比,BAL流体。没有进一步增加巨噬细胞(数据未显示)或观察中性粒细胞(图2)。同样,肺单细胞悬浮液CD11b+DCs和激活CD4+CD69+和CD8+CD69+t细胞相比,唯一的HDM或香烟(图3)。组织学分析显示支气管血管周围嗜酸性炎症和mucin-producing HDM-exposed老鼠的杯状细胞,而天真的控制老鼠(图3 b和c)。然而,暴露于香烟烟雾和HDM导致嗜酸性粒细胞的进一步增加,杯状细胞和肥大细胞(图3 b, c和d)。气道壁改造的其他特性,如量化气管平滑肌的内容,显示四组之间不存在差异(数据没有显示)。
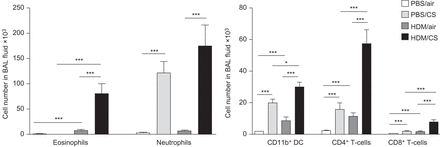
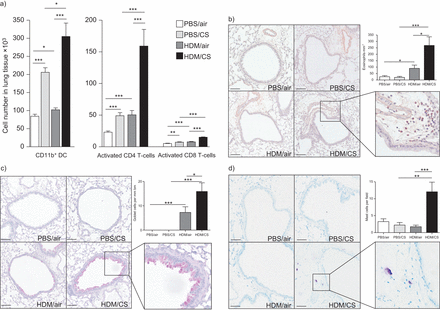
细胞分化在支气管肺泡灌洗(BAL)流体从老鼠同时暴露在PBS或屋尘螨(HDM),加上空气或香烟(CS)为3周。数据意味着±扫描电镜;n = 10动物/组。DC:树突状细胞。*:p < 0.05;* * *:p < 0.001。
从小鼠肺组织细胞分化和组织病理学评价同时暴露在PBS或屋尘螨(HDM),加上空气或香烟(CS)为3周。一)细胞分化;b)嗜酸性支气管旁浸润的显微照片;c)杯状细胞;肥大细胞和d)。细节显示细胞放大框和量化的数字图表所示。数据意味着±扫描电镜;n = 10动物/组。直流:树突细胞;bm:基底膜。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
结合接触HDM和香烟烟雾增加HDM-specific IgG1生产血清中
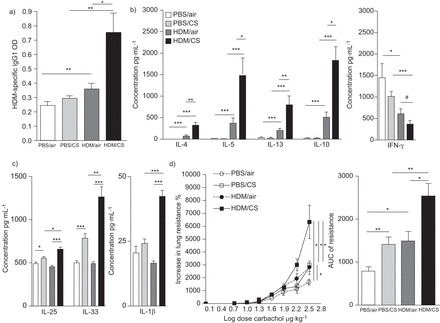
四组之间血清总IgE没有差别(数据未显示),但HDM-exposed老鼠显示显著升高有浓度过敏原特异性IgG1滴定度血清,而天真的控制老鼠。这个级别后进一步增加接触HDM和香烟烟雾(图4)。HDM-specific IgE测量低于检测极限。
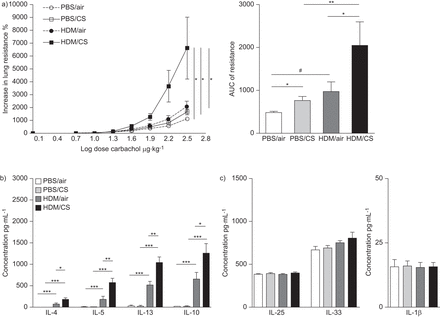
免疫球蛋白(Ig),细胞因子和小鼠气道高反应同时暴露在PBS或屋尘螨(HDM)结合空气或香烟(CS)为3周。一)HDM-specific IgG1;b)蛋白水平的白介素(IL) 4, IL-5, IL-13, IL - 10和干扰素(IFN) -γHDM-restimulated淋巴结细胞的上清液;c)的测量IL-25, IL-33 IL-1β浮在表面的碎肺;和d)碳酰胆碱剂量反应曲线和气道高反应曲线下面积(AUC)。数据意味着±扫描电镜;n = 10动物/组。OD:光密度;*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;#:p = 0.072。
香烟烟雾暴露在敏化作用,而不是在对后续哮喘过敏原的挑战是重要发展
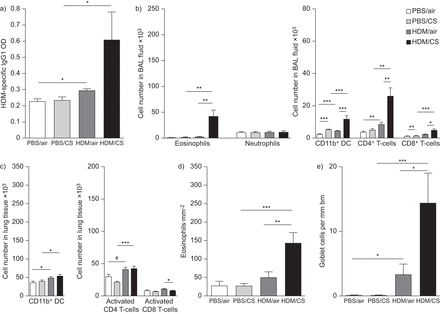
探讨香烟烟雾的假定的角色在敏化作用,BALB / c小鼠短暂暴露于香烟烟雾(连续4天)和灌输HDM(25μg)在连续3周(每周图1、协议2)。在HDM /香烟smoke-exposed小鼠的血清,增强有浓度过敏原特异性IgG1滴定度检测(图5)。在协议1相比,小鼠3周收到了香烟,没有观察到中性粒细胞在协议限制香烟烟雾暴露后2 (图5 b)。老鼠与此同时暴露于HDM只有4天的烟表明BAL CD11b+DCs, CD4+和CD8+t淋巴球相比其他组和的人数增加了20倍BAL嗜酸性粒细胞(图5 b)。协议1相比,炎症BAL流体不明显,甚至在肺单一细胞悬浊液,DCs和t淋巴球不再增加的数量总和HDM /香烟烟雾暴露(图5度)。然而,组织学检查发现更多嗜酸性粒细胞(图5 d)和杯状细胞在气道壁(图5 e),以及增加与此同时暴露小鼠气道高反应(图6)。完全,这些Th2-associated气道反应伴随着增加il - 4, IL-5 IL-13和重振mLN文化的上层清液中il - 10的HDM /香烟smoke-exposed老鼠(图6 b),但在IL-25没有差异,IL-33 IL-1β生产可以观察到所有四组之间(图6 c)。
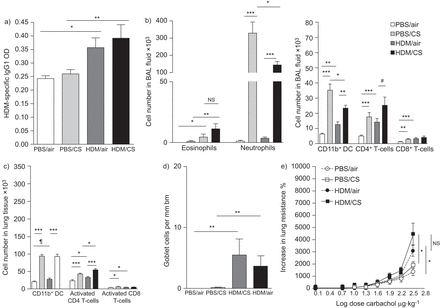
免疫球蛋白(Ig),同时炎症反应和组织病理学评价小鼠暴露在PBS或屋尘螨(HDM)和4天的空气或香烟(CS)。一)HDM-specific IgG1;b)细胞分化的支气管肺泡灌洗(BAL)流体;c)肺消化;嗜酸性粒细胞的d)量化;和e)测量的杯状细胞。数据意味着±扫描电镜;n = 10动物/组。OD:光密度;直流:树突细胞;bm:基底膜。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;#:p = 0.059。
氯化氨甲酰胆碱和细胞因子反应的小鼠气道高反应同时暴露在PBS或屋尘螨(HDM)和4天的空气或香烟(CS)。氯化氨甲酰胆碱)剂量反应曲线,曲线下面积(AUC);b)蛋白水平的白介素(IL) 4, IL-5, IL-13和IL - 10在HDM-restimulated淋巴结细胞的上清液;c)测量IL-25、IL-33 IL-1β碎上层清液的肺。数据意味着±扫描电镜;n = 10动物/组。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;#:p = 0.051。
相反,暴露于香烟烟雾中只在HDM-challenge阶段(图1、协议3)没能引起过敏的表现型和没有显示增加HDM-specific IgG1 (图7),或数量的嗜酸性粒细胞升高,CD11b+DCs或平衡液中T淋巴细胞(图7 b)和肺组织,除了CD4的崛起+CD69+肺的t细胞(图7 c)。另外,我们没有发现杯状细胞的数量增加(图7 d)或在这些小鼠气道高反应(图7 e)。
免疫球蛋白(Ig)、炎症反应、组织病理学评价和小鼠气道高反应同时暴露在PBS或屋尘螨(HDM)和空气或香烟(CS)在过敏原挑战阶段。一)HDM-specific IgG1;b)细胞分化的支气管肺泡灌洗(BAL)流体c)肺消化;d)量化的杯状细胞;和e)气道高反应性碳酰胆碱。数据意味着±扫描电镜;n = 10动物/组。OD:光密度;直流:树突细胞;bm:ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;#:p = 0.076;¶:p = 0.07。
短期暴露于香烟烟雾中提高HDM吸收和mLN DC迁移,促进共同的高空过敏症的敏化作用
调查是否4天吸入的烟已经影响气道直流贩运和排水LNs抗原运输,我们交付荧光标记的HDM气管内的香烟——或者air-exposed老鼠。FITC+DCs中只发现CD11c人口int-high/ MHC II高AW-DCs。在不同跨度为HDM滴剂后(24小时和48小时),香烟smoke-exposed老鼠显著增加排水LNs DC-mediated HDM运输,相比之下,air-exposed老鼠(图8)。
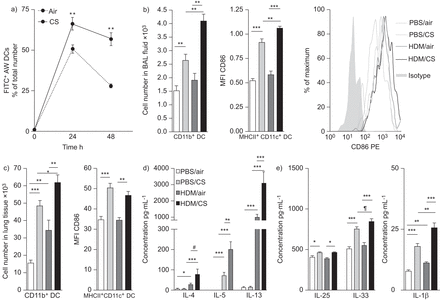
迁移,招聘和肺部树突状细胞(dc)的成熟细胞因子和相应的配置文件在PBS或屋尘螨(HDM)和急性空气或香烟(CS)曝光。纵隔淋巴结)DC迁移;b)集群的区别(CD) 11 b+DCs和CD86表达支气管肺泡灌洗(BAL) DCs;c)肺DCs(在低autofluorescent的人口计算,CD11c+和主要组织相容性复合体(MHC) II+DCs);d)蛋白水平的白介素(IL) 4, IL-5和IL-13 HDM-restimulated淋巴结细胞;e)测量IL-25、IL-33 IL-1β上层清液的肺。数据意味着±扫描电镜;n = 10动物/组。FITC:异硫氰酸荧光素;亚历山大-伍尔兹:气道派生;小额信贷机构:平均荧光强度;体育:藻红蛋白。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;#:p = 0.07;¶:p = 0.059。
描述香烟的作用在最初的敏化作用对常见的气源性致敏原,我们BALB / c小鼠暴露于香烟烟雾中连续三天,灌输HDM过敏原(25μg)(第一天图1、协议4)。这个简短的香烟烟雾和之间的交互HDM过敏原CD11b的数量显著增加+DCs在BAL流体和肺组织(图8 b和c),证明下增强激活BAL DCs CD86的表达(图8 b)。在功能层面上,我们发现短暂暴露于香烟烟雾中第一次接触HDM过敏原足以诱发mLN的敏化作用,特点是明显的Th2细胞因子在HDM /香烟smoke-exposed老鼠(图8 d)。解释这个高度有浓度过敏原特异性敏化作用的状态,我们测量典型DC-activating细胞因子释放的支气管上皮细胞在敏化作用过程的早期。TSLP和gm - csf低于检出限,但IL-25 IL-33和IL-1β高架在香烟smoke-exposed老鼠(图8 e)。IL-1β进一步增加后相伴接触HDM和香烟烟雾。
讨论
在本文中,我们证明了香烟烟雾暴露在过敏敏化作用可以发挥决定作用和哮喘的发展。我们表明,伴随的暴露于香烟烟雾和低剂量的HDM导致明显的Th2-related哮喘表型,这几乎是现在的HDM独处时使用。此外,我们表明,在过敏原,急性香烟烟雾暴露就足以引发敏感和随后的哮喘发展,放大可能的过敏原运输向mln气道DCs。
哮喘发展最有力的预测因子的敏化作用是常见的环境过敏原,如hdm、草花粉或动物的皮屑。临床流行病学研究提供了间接的证据表明吸烟与增加敏化作用有关HDM过敏原。烟雾暴露甚至与更高的哮喘疾病的发生率和严重程度。特别是儿童变得更容易接触,由于烟,在图中以喘息和哮喘发病率增加儿童和青少年在被动吸烟吸入(23]。
在我们的实验室,我们创建了一个小鼠模型,支持从流行病学研究发现,使用HDM作为临床相关的过敏原。HDM室内过敏原的最重要来源,负责过敏性症状,10%的个体。它是一个复杂的混合各种过敏原蛋白质和非蛋白的化合物,与某些过敏原的自然能力诱导通过呼吸道粘膜敏化作用[24]。尽管商业化的内容准备HDM提取广泛不同的25),这些提取的可能是一个不错的表示室内HDM过敏原出现在我们的家庭。检查是否吸烟可以降低哮喘发展的门槛,我们首先创建了一个温和的小鼠哮喘模型的down-titration HDM蛋白质含量,直到几乎没有可以引起哮喘表型(数据没有显示)。这样的模型相关评估潜在的协同效应在香烟烟雾吸入。
在本文中,我们证明了香烟烟雾暴露促进和加剧哮喘疾病,在图中以增加嗜酸性粒细胞,中性粒细胞在落下帷幕。这些研究结果与我们之前的协议工作,调查吸烟的哮喘发展中的作用与卵子“代孕”过敏原(14,26]。然而,卵子不是天然过敏原和长期暴露引发吸入宽容,而非过敏性炎症,在老鼠27]。
我们的研究的一个重要创新,利用青少年年龄在6 - 8周的老鼠,是引人注目的结果,只有3天的香烟烟雾暴露在最初的过敏原接触足以' HDM-specific LNs Th2细胞。这个过程可能是由增强的HDM气道DCs的运输。我们的研究表明,青少年吸烟,年幼的孩子可能会变得更容易过敏敏化作用和随后的哮喘发展,由于(短)吸入香烟烟雾。在我们看来,这些结果可以外推到人类,因为我们的小鼠香烟烟雾暴露协议达到碳氧血红蛋白(COHb)水平与那些在人类吸烟者(28,29日)和自COHb水平儿童(1 - 2岁)父母的烟是类似以成人吸烟者(30.]。
此外,我们专注于先天pro-allergic细胞因子的释放,以指示DCs山Th2-mediated肺部细胞反应(31日]。3周的HDM和香烟烟雾暴露导致更多IL-25 IL-33 IL-1β。相反,当停止香烟烟雾暴露在最初的敏化作用之后,没有发现这些细胞因子的差异2周后停止吸烟。这表明香烟的协同作用,特别是在持续的过敏反应,并说明了吸烟的直接影响在气道上皮细胞和先天pro-Th2细胞因子的释放,在激活DCs和随后的哮喘发展的驱动力。IL-1βIL-33甚至后增加一个HDM管理局相伴3天的烟雾暴露,表明这些细胞因子的作用在敏化作用阶段和在促进敏化作用过程由于香烟。支持了这个观点illartet al。(32)最近证实这些细胞因子的作用在哮喘的早期发展。通过阻断IL-1βIL-33信号在HDM敏化作用,他们证明了IL-1βTh2细胞因子参与生产,对BAL炎症而IL-33是至关重要的。
据我们所知,这是第一个在活的有机体内模型显示香烟之间明确的协同作用和HDM过敏原。符合我们的观察,Rusznaket al。(33从初级]发现炎性介质释放增加在体外人类支气管上皮细胞的培养,在暴露于香烟烟雾和Der p过敏原。Blacquiereet al。(34)检查怀孕期间母亲吸烟的影响。HDM曝光后,老鼠的后代吸烟母亲显示增加气道壁改造和气道高反应性,但没有增加炎症反应或高架Th2细胞因子可以在HDM演示/香烟smoke-exposed老鼠。米itchell和同事(35,36]研究孕激素的作用,结合或没有香烟,加剧过敏性呼吸道疾病。虽然在实验设置不同,他们发现了一些迹象增加过敏炎症由于吸烟;然而,这些不太明显比我们的模型。与我们目前的结果,最近的一项研究otelhoet al。(37使用小鼠模型的建立过敏性哮喘,报道中嗜酸性粒细胞明显减毒BAL流体的老鼠暴露HDM和香烟,减少粘液一起生产,CD4的病例中没有区别+t细胞活化和HDM与气道高反应,或者香烟smoke-exposed老鼠。
差距我们的数据,上述研究基本的差异可能与过敏原和香烟烟雾暴露协议,如明矾作为Th2扭曲佐剂的使用(35,36]或时间、持续时间和强度的烟雾暴露。此外,商用制剂之间的可变性HDM提取(如。内毒素内容)可能影响潜在的发展Th2反应肺(37]。
与先前的研究相比,我们的模型是创新的,因为我们展示协同使用轻度哮喘模型和一个简短的香烟烟雾暴露协议。明确区分的敏化作用和过敏原挑战阶段能检查吸烟对哮喘发病机制的不同阶段的影响。因为哮喘表型的多样性,结合临床前小鼠模型的接触过敏原和环境污染物在未来将变得更加重要。结合模型模拟更接近人类的真实情况,因此更可靠的测试提供机械的见解和潜在的治疗策略。
与流行病学研究结论和协议,我们提供生物机械的数据,支持假设的环境因素,如吸烟,敏化作用和随后的哮喘的危险因素的发展。我们发现,即使是短期的香烟烟雾接触过敏原敏化作用可以降低阈值,使个人更容易未来哮喘发展。
确认
我们要感谢迎接巴比尔,依莲Castrique,因陀罗•德•Borle菲利普·德Gryze Katleen De Saedeleer Anouck高堡,玛丽玫瑰羊皮,Ann Neessen Christelle Snauwaert和伊芙琳Spruyt(所有实验室转化研究阻塞性肺疾病,根特大学根特,比利时)为他们的优秀的技术援助。
脚注
支持声明
本研究支持的协同行动研究根特大学(转炉/果阿01251504)和大学间的吸引力波兰人(IUAP)计划,比利时,比利时科学政策、项目P6/35。kg。Tournoy高级临床研究员FWO-Vlaanderen格兰特。
感兴趣的语句
没有宣布。
- 收到了2012年6月18日。
- 接受2012年8月8日。
- ©2013人队