摘要
在进行实时荧光定量PCR时,管家基因(HKGs)的稳定性至关重要。到目前为止,普通HKGs的稳定性还没有在正常和特应性受试者的人气道上皮细胞(AEC)中进行系统的比较。
在AECS中,来自30个健康的Atopic anthmatic或Atopic哮喘儿童队列的AECS中测量了12 HKG的表达水平。使用三种不同的Visual Basic用于应用程序小程序(Genorm,Normfinder和Bestkeeper)测定基因表达稳定性。
所有12厂门都在AECS中表达。然而,由于低表达水平,排除了次黄嘌呤罗基转移酶和塔塔结合蛋白基因的进一步分析。基因对基因的环旋蛋白被所有三种方法排名最稳定。三组患者之间的β-肌动蛋白和甘油蛋白和甘油醛-3-磷酸脱氢酶基因的表达水平显着差异,具有特应性哮喘,显示出两种基因的最高表达水平。
结果表明,Cellophilin A基因是利用来自健康和哮喘儿童的未培养支气管气道上皮细胞的表达研究分析的最合适的内脏基因,并突出了每个实验模型验证内务基因的重要性。
气道上皮是一种特别有吸引力的组织,用于识别哮喘发病机制和新的治疗策略的新机制1.上皮是重要的屏障和/或分泌生物分子的来源。越来越多的证据表明,哮喘上皮细胞和非哮喘上皮细胞在生物化学和功能上存在内在差异2.这些内在变化可能影响哮喘的易感性。仔细比较正常上皮和哮喘上皮的基因表达谱,可以进一步阐明哮喘发生的分子基础。
实时定量PCR (Real-time quantitative PCR, qPCR)是比较不同生物条件下基因表达谱的一种非常有效的技术。当比较正常和疾病细胞和组织中的基因表达谱时,重要的是考虑影响表达水平的因素,如起始物质的不同数量和质量,以及RNA提取和逆转录效率。在提出的几种标准化方法中3.,管家基因(HKGs)被接受并经常用于规范qPCR,从而减少在基因表达量化中可能产生的错误。理想的HKG应在感兴趣的细胞和组织中稳定表达,而不受实验条件或疾病状况的影响。然而,这样一个理想的香港kg目前并不存在4.常用的HKGS在不同组织和/或疾病状态下表达水平的可变性5- - - - - -8,强调在开始任何qPCR研究之前,进行评估研究以识别不同组织和/或疾病状态中最稳定的hkg的重要性。
先前的研究报告称,两种常用的HKG的mRNA表达的降低,即编码β-肌动蛋白(ACTB)和甘油醛-3-磷酸脱氢酶(GAPDH)的基因,在支气管肺泡灌洗液细胞和来自哮喘的活组织检查组织未使用吸入皮质类固醇与使用吸入皮质类固醇的正常对照和哮喘受试者相比7.这提供了直接证据,证明HKGs在用于哮喘患者的定量mRNA检测前需要仔细验证。然而,目前还没有系统比较正常和特应性人气道上皮细胞(AECs)中常见HKGs的稳定性的研究。
在本研究中,测量了12hKG的表达水平,并在衍生自健康的非含量非发育健康健康儿童和特应性哮喘儿童的未培养人AEC中分析了它们的表达的稳定性。在使用三种不同的统计方法进行分析和比较之后,本作者建议细胞苷(或肽基脯氨酰异构酶A基因)建议PPIA)作为研究哮喘AECs基因表达的hk。
方法
样品收集
本研究预计普罗维登斯医疗研究伦理委员会(Providence卫生保健研究所,温哥华,BC,加拿大)以及儿童玛格丽特医院儿童伦理委员会(Perth,Australia)的批准。主题选择(表1⇓)和AEC集合已在前面详细描述2,9.哮喘被定义为在抽样前12个月内由医生记录的医生诊断的哮喘加喘息。采用普通过敏原的面板,包括草粉,牛奶,模具,花生,蛋清和动物毛发,通过阳性放射性气流测压试验结果确定了特应性状态。所有特征性哮喘患儿童都表现出轻度疾病,因此没有吸入或口服糖皮质激素治疗。对于目前的研究,AECs是从接受选修手术的30名儿童获得,用于代表三组患者的非血清疾病。简而言之,在手术前立即进行细胞学刷(BC 25105; Olympus,North Ryde,Australia)直接穿过气管管,并摩擦上皮表面以进行样品。然后将刷子取出并将尖端切断到5ml培养基中(含有20%(体积/体积)的热灭活胎牛血清的RPMI 1640)。将细胞悬浮液立即放在冰上,并且该过程至少重复一次。然后将收集培养基汇集,离心并重悬于5ml收集介质中,并通过阳性选择除去巨噬细胞。在收集的15分钟内,使用Neubauer Heococytometer(Boeco,Hamburg,Germany)测定细胞数。 Each sample of epithelial cells obtained by nonbronchoscopic brushing contained a mean±SD.3.41±140万个细胞,这在表型组之间没有显著差异(数据未显示)。在5ml细胞悬液中,2ml(约140万个细胞)用于RNA提取。
RNA提取和互补DNA合成
使用制造商描述的RNEasy迷你提取试剂盒(Qiagen,Hilden,德国)从细胞中提取总RNA。在隔离过程中,通过RNase-Fair DNase I消化(QIAGEN)消除了基因组DNA。随机选择的提取的RNA样品的质量和数量使用安捷伦生物分析仪系统(Agilent Technologies,Inc.,Santa Clara,CA,USA)进行测定。使用光谱仪量化所有样品。使用六核苷酸引物合成互补DNA(cDNA)并多指TM值在含有1×逆转录酶缓冲液的最终反应体积的最终反应体积的逆转录酶(应用生物系统,福斯特城,USA),5.5mm MgCl2,每个脱氧核糖核苷三磷酸0.5 mM, 2.5 μM随机六聚体,0.4 U RNase抑制剂,1.25 U Multiscribe逆转录酶和200 ng RNA。所有反应均在以下条件下进行:初始引物在25°C孵育10分钟,随后逆转录酶在48°C孵育1小时,最后在95°C灭活逆转录酶5分钟,冷却至4°C,然后在-80°C保存。
内参基因选择和实时荧光定量PCR
从常用的参考基因中选择了12个HKG;表2中列出了它们的全名,缩写和函数⇓.前11个基因是应用生物系统推荐的内源性对照组基因。鸟嘌呤核苷酸结合蛋白,β-肽2状1基因(GNB2L1)也包括在分离的人中性粒细胞中显示出稳定表达10..在慢性阻塞性肺疾病患者中,无论疾病严重程度如何,它也被确定为巨噬细胞的可靠检测指标11..
所有12个基因的表达研究在384孔板上进行,使用ABI Prism 7900HT序列检测系统(Applied Biosystems),使用预先制备的引物和探针(Applied Biosystems)。鉴定结果列于表2⇑.根据制造商的指示进行反应,细微修饰。简而言之,在最终PCR反应体积为10μl的最终PCR反应体积(20倍稀释),含有1×Taqman PCR主混合物(Applied Biosystems),0.9μm的每个正向和反向引物和0.25μm探针。PCR的条件包括在95℃下10分钟的放大仪金激活(施加的生物系统),然后在95℃下在95℃下循环,在60℃下1分钟。所有反应一式三份进行,每种基因的非模板对照。电子方法12.用于调整各种基因的扩增效率的差异。使用以下系列稀释液的每种基因产生标准曲线,所述串联CDNA的串联CDNA:1.33-,4-,12-,36-,108-和324倍。使用SDS 2.1软件(Applied Biosystems),在0.2的固定值下手动确定阈值循环(CT)。随后使用CT来计算线性回归线来通过对对应的CT绘制模板量的对数来计算线性回归线。使用一对引物检查基因组DNA污染,所述引物扩增基因的内肾区域。
统计分析
为了确定所选参考基因的稳定性,使用了三种不同的应用程序(VBA)小程序(vBA)小程序(Genorm,Bestkeeper和Narmfinder)。Genorm applet提供了基因表达稳定性(m)的量度,单个基因与所有其他测试对照基因之间的平均成对变异(v)4.BestKeeper应用程序通过对所有候选基因对进行两两相关分析,确定最优HKGs,并计算最适合的HKGs的几何平均值13..常常法仪专注于发现具有最低内部和组间表达式变化的基因14..
数据显示为平均值±SD..当表达水平为正态分布时,三组受试者之间的基因表达水平比较采用单因素方差分析(双尾),当表达水平非正态分布时采用非参数(Wilcoxon)检验。使用Bonferroni校正对多次比较进行调整。
结果
质量控制和放大效率
采用安捷伦生物分析仪系统,随机抽取8例哮喘儿童和健康儿童的上皮细胞,测定其RNA的质量和数量。特应性病人的样本不包括在本分析中。安捷伦生物分析仪的结果以电泳图的形式生成。均值±SD.RNA提取量为2.7±0.67 μg。以RNA完整性数(RIN)测定的总RNA质量为7.93±0.60。28S与18S RNA之比为1.85。在电泳图上观察到的高RIN和完整的28S和18S核糖体RNA亚基表明,RNA的降解发生在可接受的水平(图1)⇓).使用内含子特异性引物随机扩增10个CDNA;所有10个cDNA样品都产生了阴性结果,而基因组DNA对照是阳性的。
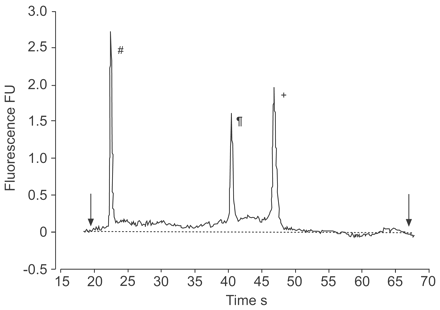
使用安捷伦生物分析仪(安捷伦技术公司,Santa Clara, CA, USA)进行RNA分析。显示了三个RNA峰(#: 50 bp分子质量标记物;¶: 18S核糖体RNA;+:28s核糖体RNA)。箭头表示RNA浓度计算的集合开始和结束时间(░:计算基线)。福:荧光单位。
标准曲线是通过绘制稀释倍数的股票cDNA对每个基因的Ct。线性相关系数(R2)的范围为0.994 ~ 0.999。根据标准曲线的斜率,从公式E = 10推导出标准的放大效率−1 /坡- 1,范围89-109%。样本中12个基因的Ct均覆盖在标准曲线范围内。然后利用e -法对不同基因的扩增效率差异进行调整,根据每个研究基因的标准曲线对样本Ct计算调整后的表达量12..
候选HKGs的表达水平
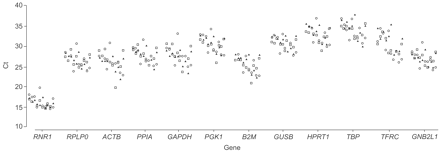
12个HKGs显示了广泛的表达水平,18S rRNA基因中位数Ct最低为15.8 (RNR1)对于TATA结合蛋白基因的最高中值CT为34.4(真沸点)(图。2⇓).在对30名队列研究对象进行的三次重复试验中SD.11例次黄嘌呤核糖基转移酶基因(HPRT1)和16个样品真沸点.因此,对于这两个基因,数据的准确性是可疑的。这可以通过中位CT为33.2和34.4来解释HPRT1和真沸点, 分别。这些高CT表明目标cDNA数量接近单拷贝水平。所以,HPRT1和真沸点被排除在进一步的分析之外。对于剩下的10 hkgs,只有一个来自健康的Atopic组的样品很高SD.在一个基因的三份测定中,该样品还具有四种基因的最低CT。来自健康的非植物性非易熟的另一个样品具有非型高CT,其导致了两种HKG的测定中的异常值。因此,这两个样品被排除在进一步的分析之外,并且最终分析包含28个样品10 HKG。
原始定量RT-PCR周期阈值(Ct)检测30例气道上皮样本中的12个候选管家基因(□:健康、非特应性、非哮喘;○:健康的特异反应性;▴:过敏性哮喘)。RNR1:18s核糖体RNA基因;rplp0.:酸性核糖体蛋白基因;ACTB.:β-肌动蛋白基因;PPIA:Cyclophilin A(或肽基脯氨基异构酶A)基因;GAPDH.:甘油醛-3-磷酸脱氢酶基因;PGK1: phosphoglycerokinase基因;B2M.:β2微球蛋白基因;GUSB:β-葡糖醛酸酶基因;HPRT1:次黄嘌呤核转移酶基因;真沸点: tata结合蛋白基因;TFRC:转移素受体基因;GNB2L1:鸟嘌呤核苷酸结合蛋白,β-肽2-like 1,基因。
HKGs表达稳定性的测定
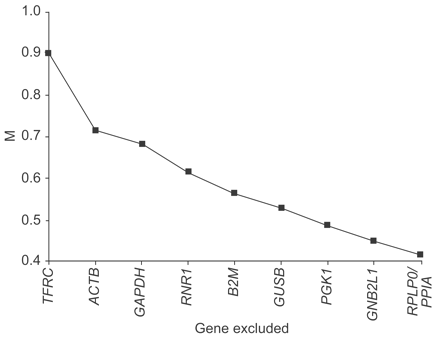
采用geNorm、BestKeeper和NormFinder三种不同的VBA applet评估HKG的稳定性。geNorm程序基于所有研究基因之间的平均V来计算一个基因的M。研究的10个基因均达到高表达稳定性,M值低,即。低于1.5的默认限制,除转铁蛋白受体基因外(TFRC)其中m为1.7。图3.⇓表示候选HKGs的M的平均值。曲线表示逐步排除最不稳定的hkg。最初排除了TFRC,酸性核糖体蛋白基因(rplp0.),PPIA被鉴定为两个最稳定的基因(表3⇓).geNorm程序还用于计算标准化因子(NF),并评估产生该因子的最佳内参基因数量(图4)⇓).从两个最稳定的基因首先计算NF,V在NF之间量化n和NFn + 1.将第三基因添加到最稳定的两个HKG,rplp0.和PPIA,产生的V值为0.125,低于0.15的临界值,这表明不需要加入额外的内参基因进行归一化,尽管包括6个HKGs的变异最小,添加第7个基因产生的V值最小,为0.082。
使用Genorm程序确定管家基因的表达稳定性(M)。从分析中连续排除该基因,M表示单个基因与所有其他测试对照基因之间的平均成对变化。在X轴上的每个点处所示的基因是从以下步骤中排除的基因。最稳定的基因是那些仍然存在的基因,即。那些展示最低米的人TFRC:转移素受体基因;ACTB.:β-肌动蛋白基因;GAPDH.:甘油醛-3-磷酸脱氢酶基因;RNR1:18s核糖体RNA基因;B2M.:β2微球蛋白基因;GUSB:β-葡糖醛酸酶基因;PGK1: phosphoglycerokinase基因;GNB2L1:鸟嘌呤核苷酸结合蛋白,β-肽2状1,基因;rplp0.:酸性核糖体蛋白基因;PPIA:Cyclophilin A(或肽基脯氨基异构酶A)基因。
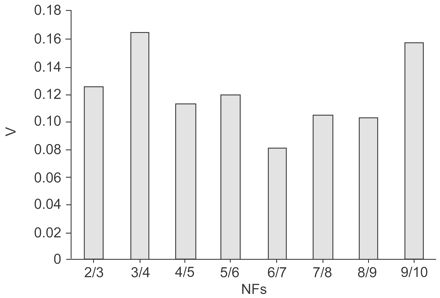
确定标准化的最佳参考基因数。Genorm从至少两个基因计算归一化因子(NF),并确定两个顺序NF之间的平均成型变化(V),如。2/3表示分别对来自两种基因的NFS的比较。
BestKeeper程序被用来评分候选者香港的稳定性。这种方法允许对香港gs进行比较分析。所有10个候选hkg均高度相关,并合并为一个指数。然后,计算每个HKG与指标之间的相关性。HKGs与BestKeeper指数之间的最佳相关性为PPIA(r = 0.988;表3⇑).
最后,使用NormFinder程序对候选者HKG的稳定性进行评分。该方法将组内和组间的表达变化结合为一个稳定性值,使基因按表达稳定性进行排序。该程序识别的最稳定和最不稳定的基因是PPIA和TFRC,与geNorm和BestKeeper分析得到的结果相同,但其他基因的稳定性排序在三个不同的程序中略有不同(表3)⇑).
三组受试者中候选HKG的表达水平
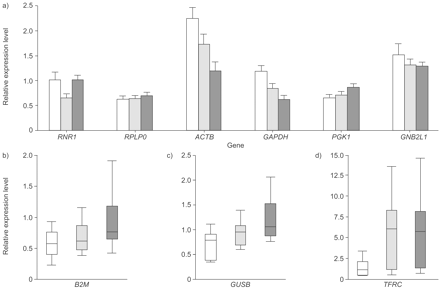
PPIA是三种不同的分析方法所发现的两个最稳定的香港天文台中唯一的香港天文台。以该基因为参照,比较了其他候选HKGs在三组表型不同的儿童、健康的非特应性非数学儿童、健康的特应性儿童和特应性哮喘患者中的表达水平(图5)⇓).结果表明,在纠正多种比较之前,三组基因的三组患者之间的表达水平无关紧要(rplp0.,GNB2L1和β2-microglobulin基因(B2M.)).其中一个基因(甘油激酶磷酸基因(PGK1), p = 0.07), 3个基因(β-葡萄糖醛酸酶基因(GUSB), p = 0.026;TFRC,p = 0.021;RNR1,p = 0.037),对两个基因的显着差异(ACTB.,p = 0.0047;GAPDH.,p = 0.0008)。Bonferroni校正(九次比较)之后,表达水平ACTB.和GAPDH.仍有显著差异;特应性哮喘患者两种基因的表达水平最高,而健康的非特应性非哮喘患者两种基因的表达水平最低(调整后的p值分别为0.042和0.007)。
三组内政机基因相对表达水平的比较(□:特应哮喘;Ⅳ:健康的Atopic;▒:健康的非植物性非发电机)。通过使用环孔A(或肽基丙烯酸异构酶A)基因作为参考,计算每个基因的相对表达水平。a)通过单向ANOVA(两尾)对六种基因的表达水平的比较。数据显示为平均值±扫描电镜.b-d)使用非参数Wilcoxon检验比较三个基因表达的箱线图。盒子代表中位数和四分位数范围;竖条表示范围。RNR1:18S核糖体RNA基因(P = 0.037);rplp0.:酸性核糖体蛋白基因(p = 0.677);ACTB.β-肌动蛋白基因(p = 0.0047);GAPDH.:甘油醛-3-磷酸脱氢酶基因(p = 0.0008);PGK1:磷酸甘油激酶基因(P = 0.07);GNB2L1:鸟嘌呤核苷酸结合蛋白,β-肽2状1,基因(P = 0.543);B2M.:β2-microglobulin基因(p = 0.129);GUSB:β-葡糖醛酸酶基因(P = 0.026);TFRC:转铁蛋白受体基因(p = 0.021)。
虽然三个不同VBA小程序的HKG表达稳定性的顺序略有不同,但三个程序中最稳定的7个HKG是相同的。此外,geNorm程序还发现6个最稳定的HKGs产生的变异最小。根据这6个基因的表达水平计算NF,比较三组患者中所有10个研究的HKGs的表达水平,得到的结果与单一hkkg的结果相似,即PPIA.经Bonferroni校正(10次比较)后ACTB.和GAPDH.在组之间仍然显着差异(分别校正p值,分别为0.011和0.006)。即使是最保守的Bonferroni纠正,即。校正19比较,结果仍然显着(调整为0.021和0.011的p值)。然而,由于从六个基因的表达水平计算的NF和来自单个基因的表达水平高度相关,因此用R20.89,使用的测试PPIA作为HKG和使用六个基因的测试,因为HKGS不是独立的。因此,使用Bonferroni校正非常保守。
共同调节研究的HKGs
当使用成对比较方法确定HKG稳定性,例如Genorm或Bestkeeper,所研究的基因之间的共调节可能影响结果,因为这些算法选择了任何共调节基因。为了检查研究的基因之间的潜在共调控,使用巧妙的途径分析进行网络分析(Ingenuity Systems,Inc.,Redwood City,CA,USA)进行15..基于来自已发布文章的已知关系,基于Web的应用程序允许发现,可视化和探索交互网络。
目前的分析表明,除了两个基因,即rplp0.和GNB2L1,被评估的基因之间没有相关性。一项更深入的分析显示,在炎症介质肿瘤坏死因子激活组织的情况下,或在癌症的情况下,癌基因髓细胞瘤病病毒癌基因同源物(MYC).然而,发现这些基因的启动子区域不与刺激肿瘤坏死因子或刺激期间的刺激以外MYC在美国,这些基因的表达在很大程度上是独立的。
讨论
理想的HKG应在所有受试者中保持稳定的RNA转录水平,无论疾病状态如何。因此,本研究的目的是评估正常、特应性和特应性哮喘儿童AECs中12个潜在HKGs的表达差异。文献检索表明,在气道上皮的研究中,没有单一基因被一致地用作参考基因16.- - - - - -20..此外,用作正常情况的HKG在本研究中没有系统地评估。
本研究的特征在于:1)同时调查12个常见的HKG。2)使用Taqman探针测定的基因表达量化(除了RNR1分析,探针跨越了该基因的内含子);3)使用三种不同的applet进行数据分析;4)各种细胞标记物免疫染色显示,AECs占总细胞的主要成分(96.6%)2,9.这些功能对于数据可靠性和对结果的有意义的解释很重要。
所有HKGS除外GNB2L1从TaqMan人内源性控制面板(应用生物系统)中选择。被调查的香港基因一般可分为八组:与糖酵解有关的基因(PGK1和GAPDH.)、转录相关基因(真沸点),与翻译相关基因(RNR1),结构/细胞骨架相关基因(ACTB.),参与蛋白质合成的基因(rplp0.),编码溶酶体酶的基因(GUSB),核苷酸 - 代谢相关基因(HPRT1),最后,不能明确分类为其中一个分组的基因,包括PPIA,B2M.,TFRC和GNB2L1(表2⇑).研究显示功能多样化的HKGs,可成功选择不同细胞、组织和疾病状态的内参基因。
TaqMan测定法比其他实时检测方法(如SYBR Green)提供了更大的特异性、准确性和重现性。21..此外,跨越内含子的探针的设计避免了因污染基因组DNA而产生的误差,这是影响基因表达量化的重要因素。
三个不同的VBA applet所确定的HKG稳定性顺序并不完全相同,这可以通过每个applet所采用的不同原则来解释。geNorm和BestKeeper都使用两两比较的方法4,13..geNorm根据几何平均表达水平选择合适的内参基因。其原理是,无论实验条件和疾病状况如何,两种理想HKGs在所有样品中的表达比例都是相同的。两个HKGs基因表达比例的变化可能是由于其中一个或两个基因的表达变化造成的;因此,随着表达稳定性的降低,比值的变化也会增加4.Genorm方法的设计不适用于鉴定单一最佳的HKG,而是,相反,至少两个最佳代表几何平均值的基因的组合4.BestKeeper也使用几何平均值选择变量最小的基因,但使用原始Ct数据而不是转换到相对表达水平的数据,如geNorm中使用的13..Bestkeeper还识别评估所有HKG的最稳定的基因13..该成对比较方法存在问题,即它倾向于选择具有类似表达谱的基因。randfinder使用基于模型的方法14..该方法分别分别分析亚组,估计群体和族族表达式变化,并计算候选基因稳定性值14..最佳的HKG组间和组内联合表达变异最小。与两两比较方法相比,该方法具有考虑样本亚组间系统差异的优点,受候选HKG共调节的影响较小14..理论上,这种基于模型的方法更适合当前的研究设计。在本研究中,PPIA基于双向比较方法或基于模型的方法,被三个程序被识别为最稳定的基因。rplp0.和GNB2L1,这些基因在geNorm分析中处于最稳定的前三名,尽管它们仍然位于之后PPIA.结论是,即使某些香港特区之间存在潜在的共同调控,这在本研究中并不明显。Bionaz和Loor也得到了类似的结果22..此外,若干个体研究使用了Genorm,Bestkeeper和Normfinder程序,以确定最稳定的HKG和给定的可变结果,对某些但不在其他方面的所有三个程序一致14.,23.- - - - - -25..在确定了不一致结果的研究中,确定了常规程序的常规计划优于其他方案14..因此,本文作者推荐使用NormFinder程序在与本研究类似的实验设计的研究中选择HKGs。
PPIA编码免疫蛋白类别的蛋白质的成员,其所有具有肽基丙醇顺式CIS /反式异构酶活性,因此被认为参与蛋白质折叠和/或细胞内蛋白质转运26..PPIA被用作HKG,因为其具有显着的进化守恒和宽的细胞和组织分布27..在最近的一份报告中,PPIA在AECs的表达研究中作为HKG,因为它不受变应原刺激的显著影响19..在本研究中,PPIA被所有三种方法列为最稳定的基因。另外,三种方法检测的6个最稳定基因和4个最不稳定基因相同;的利用率PPIA所有6个排名靠前的基因作为参照基因都产生了非常相似的结果。总的来说,目前的结果是一致的PPIA作为研究哮喘AECs基因表达的首选HKG基因。
值得一提的是,变异总是存在于任何一个HKG,基因表达的标准化与一个单一的HKG可能会导致结果偏倚。因此,建议使用多个hkg4.目前研究的结果表明,使用三个(PPIA,PGK1和rplp0.)到六个HKGS(PPIA,PGK1,rplp0.GNB2L1,GUSB和B2M.),如果实验资源可用。
本研究还表明,在表达水平上存在显著差异ACTB.和GAPDH.在正常、特应性和特应性哮喘患儿之间,哮喘患儿表达量最高,正常患儿表达量最低。经过多次比较后,差异仍然显著。这个结果表明ACTB.和GAPDH.,两种最常用的HKG,不能用作哮喘症AECS基因表达研究中的HKG。以前通过眩光报道了类似的结果等等。7.然而,在眩光的研究中等等。7不使用吸入的皮质类固醇的哮喘受试者表现出使用吸入皮质类固醇的正常对照和哮喘受试者显着低的GAPDH和β-肌动蛋白mRNA的水平。这可以通过两项研究中的细胞类型不同的事实来解释。在目前的研究中,AECS是主要的(> 96.6%)细胞类型,而在眩光的研究中等等。7,上皮细胞占少数(<1.4%),巨噬细胞和淋巴细胞占多数(>92.5%)。此外,在本研究中,研究对象是儿童,而眩光等等。7学习成年人。这两项研究之间观察到的差异仅用于进一步突出研究人员对所使用的每个实验模型进行验证的研究人员的重要性。
综上所述,嗜环蛋白A基因被确定为来自正常、特应性和哮喘儿童的人类气道上皮细胞的基因表达研究中最合适的正常化剂。此外,由于β-肌动蛋白和甘油醛-3-磷酸脱氢酶基因在哮喘上皮细胞中的显著高表达水平,目前的研究结果质疑编码基因作为此类研究的管家基因的适用性。
支持声明
本研究得到了澳大利亚国家卫生和医学研究委员会(堪培拉; 303145和458513),儿童卫生研究基金会(珀斯),西澳大利亚哮喘基金会(珀斯),过敏原(汉密尔顿,加拿大),加拿大国家卓越网络和不列颠哥伦比亚省龙结构(加拿大卑诗省)。J-Q。他是迈克尔史密斯卫生研究基金会的收件人(温哥华)奖学金和Izaak Walton Killam纪念奖学金(哈利法克斯,NS,加拿大)。
感兴趣的语句
警方Paré的利益声明可以在这里找到www.www.qdcxjkg.com/misc/statements.shtml
- 已收到2007年10月1日。
- 接受2008年4月2日。
- ©ERS期刊有限公司