摘要
除了经典的同种免疫外,还有其他的机制参与了毛细支气管炎闭塞综合征(BOS)的发病过程。人们推测,作为先天免疫反应的组成部分的抗菌肽(AMPs)在BOS发病机制中起着一定的作用。
neutrophil-derived安培人类的肺表达抗菌肽(hCAP) -18 / LL-37α-defensins(人类嗜中性粒细胞肽(版)1 - 3),和人类上皮细胞衍生安培β-defensin (hBD) 2、抑弹性酶蛋白和分泌leukoprotease抑制剂(SLPI)以稳定的肺移植受者和BOS。检测呼吸道病原体与AMP水平的关系。
已于44名肺移植受者(30稳定,14 BOS)进行支气管肺泡灌洗(BAL)。BAL是为病原体培养并进行ELISA为安培。气道病原体的存在用显著增加嗜中性粒细胞衍生的细胞和上皮来源的AMP的水平相关。当患者没有在BAL流体的病原体进行了分析,8个接收方与BOS具有升高HCAP-18 / LL-37和HNP 1-3用25页稳定的收件人进行比较。β防御素2和蛋白酶蛋白水平在BOS和稳定的接受者相媲美,但SLPI水平BOS减少。
支气管炎闭塞性综合征与气道气道疏通素18/LL-37升高和人中性粒细胞肽1-3活化的中性粒细胞相关,即使没有病原体。同时伴有气道分泌性白蛋白酶抑制剂的减少,这可能有利于非同种免疫气道损伤,降低抗蛋白酶防御和增加中性粒细胞脱颗粒。
肺移植为选择的终末期肺部疾病患者提供了一种现实的治疗方法;然而,5年的长期存活率仅为49%。肺移植术后存活1年的主要死亡原因是闭塞性细支气管炎1,2。这在组织学上表现为中小气道的慢性炎症和纤维增生修复,最终导致腔内闭塞。临床相关,闭塞性细支气管炎综合征(BOS)表现为进行性、不可逆的气流阻塞,通过一秒钟用力呼气量的下降来诊断(FEV)1)在没有其他原因导致移植物功能障碍的情况下,移植后获得的最佳结果的80%以下。频繁的急性排斥反应是BOS的一个危险因素3.- - - - - -5并且,迄今为止,它已被归因于慢性排斥反应的发生的体现通过同种免疫机制。然而,BOS与嗜中性粒细胞在两种支气管肺泡灌洗(BAL)流体和支气管活检相关联6- - - - - -9而不是单纯的淋巴细胞浸润。尽管出现了更有效的免疫抑制,但急性排斥反应频率的降低并没有反映在BOS患病率的降低上10。这引起了人们的怀疑:在BOS发病机制中,同种免疫是否是唯一的,甚至是主要的机制?
移植的肺暴露在环境中,具有高度发达的先天免疫系统,以防止微生物。先天免疫应答可以直接地通过吸引炎性细胞或通过编排充当“危险信号”,它可诱导alloimmunity后续适应性免疫应答诱导损伤11。
抗菌肽(AMPs)是形成先天免疫系统基本要素的阳离子肽。安培发现在人类的航空公司包括人类抗菌肽(hCAP) -18 / LL-37α-和β-defensins,蛋白酶抑制剂分泌leukoprotease抑制剂(SLPI)和弹力素12,13。它们的释放是由炎症细胞因子和微生物产物刺激的,它们作为内源性抗生素直接作用于一系列微生物14- - - - - -16。AMPs还调节炎症和免疫,影响修复过程。它们对中性粒细胞、嗜酸性粒细胞、单核细胞、树突状细胞和t细胞具有趋化作用。此外,它们还影响成熟,上调树突状细胞的内吞能力和共刺激分子的表达,并通过细胞增殖和抑制细胞凋亡来促进上皮表面的修复17- - - - - -21。AMPs在随后的适应细胞或体液对损伤的反应中起关键作用,有利于修复反应。
作者假设,在存在气道病原体和BOS的情况下,肺移植受者气道中AMPs的表达会增加。这将有助于免疫细胞募集、促炎性趋化因子释放和创造有利于气道损伤和随后的上皮损伤或修复的环境。作者的目的是研究来自中性粒细胞和上皮细胞的AMPs在稳定肺移植受者和BOS受者气道中的水平,并确定气道病原体和AMP水平之间的关系。
材料和方法
研究人群
我们招募了在心肺移植中心(英国泰恩河畔纽卡斯尔的弗里曼医院)进行随访的肺移植受者。BOS是根据国际心脏和肺移植(ISHLT)标准诊断的22。接受监视性或研究性支气管镜检查的患者符合纳入研究的条件。接受活检证实急性排斥反应的患者(主要表现为淋巴细胞性排斥反应)被排除在外。
常规的免疫抑制剂包括泼尼松龙、环孢素和硫唑嘌呤。他克莫司和/或霉酚酸酯分别代替环孢霉素和硫唑嘌呤,临床表明。部分BOS受者根据当地协议接受全淋巴照射和/或长期阿奇霉素治疗。根据移植前及供体微生物学,局部方案:氟氯西林/甲硝唑/克林霉素≤1周;可洛霉素喷雾剂铜绿假单胞菌移植前和/或BAL阳性铜绿假单胞菌;复方磺胺甲恶唑的卡氏肺孢子虫1周后预防。
本研究的伦理批准由当地研究伦理委员会(纽卡斯尔和北泰恩赛德伦理委员会,纽卡斯尔)授予,并从所有研究的患者接受了知情同意书。
抽样
支气管镜检查(Olympus FB 45.5;奥林匹斯,日本东京)是在病人预先用药注射。咪达唑仑。使用180毫升生理盐水注入移植肺的右中叶或舌骨进行BAL。用温和的吸力回收液体,然后汇集。通过标准化微生物培养方法,使用选择性琼脂糖和延长培养时间,对一部分进行了细菌、病毒和真菌的存在评估。任何细菌的生长都被认为是阳性的。总共进行了6-8次经支气管活检,以排除基于ISHLT标准的急性排斥反应。
用纱布过滤并离心。脱细胞部分在-80℃保存,ELISA和Western blot检测。使用Nebhauer血细胞计和giemsa染色的胞质酶制剂进行细胞总数和差异计数。在测定BAL成分时,准确确定稀释因子的方法目前尚无共识。遵循欧洲188bet官网地址呼吸协会特别工作组的建议,采用了一种不校正蛋白质水平的标准化方法23。
ELISA
建立三明治elisa法测定无细胞BAL上清液中AMP水平。商用工具被用于人类嗜中性粒细胞α-defensins(人类嗜中性粒细胞肽(版)1 - 3)和弹力素Hycult生物技术(Uden、荷兰)和白介素8 (IL) Biosource国际(尼,比利时)。ELISAs是按照制造商的说明进行的。
人类β-defensin (hBD-2) ELISA是使用定义良好的执行方法24。采用荷兰莱顿大学医学中心(Leiden University Medical Centre)开发的ELISA系统检测SLPI、hCAP18/ lr -37和人中性粒细胞弹性酶(human neutrophil elastase) ELISA试剂盒。25,26。
hCAP-18/LL-37和SLPI的凝胶电泳和Western blotting
选择具有代表性的样品(8个稳定样品和8个BOS样品)进行电泳和Western blotting。这是为了确定完整的hCAP-18的存在及其与LL-37的裂解,以及SLPI及其降解产物的存在。样品经16.5% Tris/Tricine凝胶SDS-PAGE处理。分离的蛋白被转移到聚偏二氟乙烯膜上(Bio-Rad, Hercules, CA, USA)。非特异性结合位点一夜之间被阻断。用小鼠单克隆抗LL-37抗体1.1 c12孵育1 h,孵育至LL-3727并用多克隆兔抗SLPI免疫球蛋白G为SLPI26。二抗分别为辣根过氧化物酶标记的LL-37山羊抗小鼠和SLPI猪抗兔(DAKO, Glostrup,丹麦)。采用增强型化学发光Western blotting检测系统检测免疫反应性。
统计分析
数据最初被评估为正常。AMP水平上的数据没有一个是正态分布的,因此采用非参数检验进行分析。非参数数据以中位数(范围)表示;正态分布数据用均数±表示sd。采用非配对t检验和Kruskal-Wallis检验评估各组间的差异。当Kruskal-Wallis检验组间存在显著差异时,再用Mann-Whitney u检验进行进一步比较。采用Bonferroni-Holm校正法对组间的多次比较进行校正,因此显著p值的阈值有时<0.05。使用Spearman等级相关性进行相关性评估。
结果
本研究共评估62例肺移植受者(34例女性,28例男性)。62例患者中,有14例符合ISHLT标准:BOS 0-p, n = 2;BOS 1, n = 2;BOS 2, n = 6;BOS 3 n = 4。在其余48例患者中,18例经支气管活检发现急性排斥反应为ISHLT二级以上,30例肺功能稳定,无急性排斥反应或BOS。根据预先确定的排除标准,排除18例急性排斥反应患者。患者统计资料和移植前诊断见表1·。两组之间没有性别或年龄的差异。BAL取样时的处理如表2所示·。BOS组的移植时间明显长于稳定组。
中性粒细胞,IL-8和中性粒细胞弹性酶
比较稳定受者与BOS受者气道中性粒细胞、BAL、IL-8和人中性粒细胞弹性酶(HNE)浓度及AMP水平(表3)·)。有BOS的受者有明显更高的中性粒细胞百分比和HNE水平的增加。IL-8水平在BOS和稳定接受者之间没有显著差异。中性粒细胞来源的AMPs hCAP-18/LL-37和HNP 1-3的水平在BOS中显著升高,即使没有显著升高的中性粒细胞总数。BOS和稳定受体的上皮来源AMPs elafin和hBD-2水平无显著差异。SLPI是一种上皮来源的AMP,具有很强的蛋白酶抑制活性,与稳定受体相比,BOS受体的BAL液中SLPI的水平明显较低。
由于病原体的存在可能会对气道中性粒细胞内流和AMP表达产生重大的混杂影响,因此,我们对接受了稳定型和BOS型巴尔液培养的患者(无论是否培养阳性)的数据进行了重新检查(表4)·)。在稳定受体中,病原体的存在与巴尔中性粒细胞增多和IL-8和HNE升高有关。然而,在BOS受者中,病原体的存在与较高的总中性粒细胞计数或中性粒细胞百分比无关,也与IL-8或HNE水平的任何差异无关。
中性粒细胞来源的AMPs和上皮细胞来源的AMP hBD-2
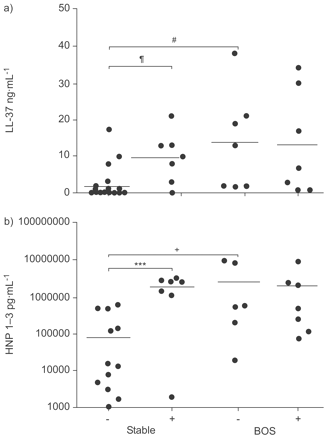
amp主要来源于中性粒细胞、LL-37和HNP 1-3,在有BAL培养病原体的稳定移植受者中显著高于培养阴性的稳定移植受者。然而,有趣的是,在BOS受者中,对于病原体的存在没有额外的AMP反应。数据显示,即使在没有病原体的情况下,与稳定受体相比,BOS受体的LL-37和HNP 1 -3水平也显著升高(图1)·)。
支气管肺泡灌洗液中中性粒细胞来源的抗菌肽LL-37和人中性粒细胞肽(HNP) 1-3的水平。之间的比较是由四个独立组移植受者,那些稳定的肺功能和没有病原体(n = 23),那些稳定的肺功能和病原体培养从BAL流体(n = 7)、接受者与闭塞性细支气管炎综合征(BOS)和没有病原体培养BAL (n = 8)和接受者文化上的BOS和病原体,BAL流体(n = 6)。−:没有病原体;+:病原体。#: p = 0.001;¶: p = 0.002;+: p = 0.007。***:P <0.001。
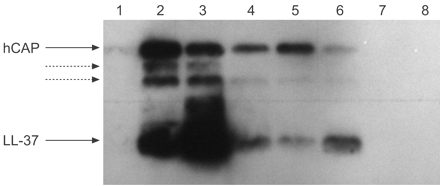
中性粒细胞将前体抗菌肽hCAP-18储存在它们的特定颗粒中。中性粒细胞刺激后,蛋白水解形成活性肽LL-3728。的HCAP-18 / LL-37 ELISA中使用是基于对LL-37的抗体,因此,检测到的两个所述前体HCAP-18和HCAP-18的加工形式含有LL-37序列。蛋白质印迹分析用于从含LL-37的BAL样品中处理HCAP-18分化完好HCAP-18。结果表明,移植受者HCAP-18和LL-37的不同之比。Some recipients have a much higher ratio of active peptide to hCAP-18 than others (fig. 2·)。
使用单克隆抗ll -37抗体对支气管肺泡灌洗(BAL)标本进行Western blot分析。采用SDS-PAGE法分离BAL样品,采用单克隆抗ll -37进行Western blot分析。然后用增强化学发光法观察免疫反应条带。泳道1-4:闭塞性细支气管炎患者;泳道5-8:稳定的领奖人。虚线箭头表示中间加工产品。hCAP:人类抗菌肽。
hBD-2主要来源于上皮细胞,不由中性粒细胞产生。各组间hBD-2水平无显著性差异(图3)·)。
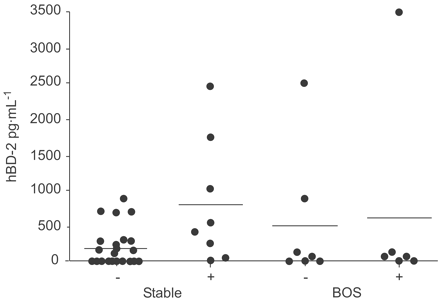
水平的人类β-defensin四个收件人组(hBD) 2。BOS:闭塞性细支气管炎综合征。−:没有病原体;+:病原体。
蛋白酶抑制剂
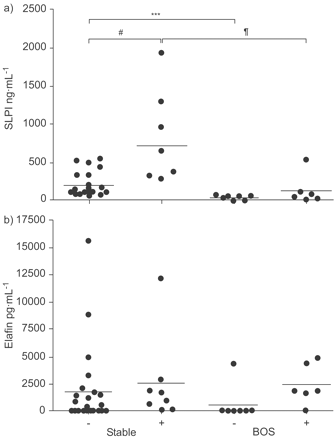
两个放大器,具有抗蛋白酶活性,抑弹性酶蛋白和SLPI,由上皮细胞主要产生。有在本研究中任何组之间蛋白酶蛋白中发现的水平没有显著差异。与此相反,有在稳定和BOS收件人SLPI表达显着不同的响应。稳定收件人已经在病原体存在,这是不在受者观察到的BOS升高SLPI。In recipients without detectable pathogens, SLPI levels were significantly lower in recipients with BOS compared with those with stable lung function (fig. 4·)。
4个受体组的蛋白酶抑制剂分泌性白蛋白蛋白酶抑制剂(SLPI)和elafin的水平。BOS:闭塞性细支气管炎综合征。−:没有病原体;+:病原体。#: p = 0.001;¶:p = 0.006. ***: p<0.001.
讨论
目前作者已经证明,肺移植受体与稳定受体相比,具有不同的抗菌肽表达模式。BOS的特点是人类中,ll - 37越显著升高和α-defensins版1 - 3,并显著降低SLPI水平(图5所示·)。
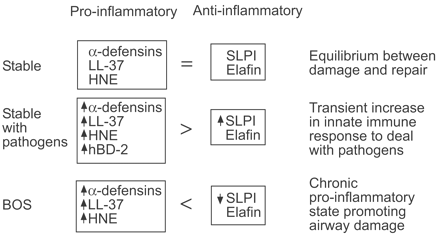
不同研究组抗菌肽水平的综述。HNE:人中性粒细胞弹性酶;人类β-defensin-2 hBD-2:;SLPI:分泌性白蛋白酶抑制剂。
这些结果对应与Nelsestuen以前的研究结果等。29落下帷幕蛋白质含量,蛋白质组学调查,高浓度的BOSα-defensins与后续发展。LL-37和HNP 1-3主要来源于中性粒细胞,尽管上皮细胞也可能对气道的LL-37水平有贡献15。hCAP18/LL-37储存在特定的中性粒细胞颗粒中28并被蛋白酶3加工成活性的LL-37,尽管其他蛋白酶也可能参与加工27,30.。Western blot分析显示,不论是否存在BOS,移植受者的前体细胞hCAP-18和LL-37的比例是不同的,因此,这为ELISA检测提供了额外的信息。然而,由于BAL不是在蛋白酶抑制剂的混合物中收集的,因此不能排除收集后处理影响结果的可能性。在脱粒过程中,HNP1-3和hCAP-18/LL-37均由中性粒细胞释放。目前的结果表明,中性粒细胞的脱颗粒存在于移植受者的气道与BOS的持续气道损伤。
这使得人们推测,肺先天反应的因素在BOS的发展中扮演了一个病因学的角色。事实上,罗斯等。31与肺功能稳定的受者相比,BOS移植受者hBD-2升高。然而,在BOS患者中没有发现hBD-2水平的升高。在Ross的研究中等。31六出8个样品从BOS收件人是病原体培养阳性。这可以解释的结果之间的差异,因为的hBD-2的表达上皮显着通过暴露于微生物产物诱导的32,33。事实上,与没有感染的稳定受体相比,有感染的稳定受体hBD-2水平出现了生物学上可能的升高;然而,这并没有达到统计学意义。相反,在存在病原体的BOS受体中,hBD-2水平没有升高。事实上,目前的结果表明,BOS受体中病原体的存在与所测的任何AMPs水平的显著升高无关。这与稳定受体对病原体的反应形成了鲜明对比。目前的作者推测,在BOS中,由于中性粒细胞脱颗粒,中性粒细胞衍生的amp已经大量存在,并且在病原体的存在下不可能有额外的反应。上皮来源的AMPs、SLPI、elafin和hBD-2缺乏应答,提示BOS受体对病原体的上皮抗菌应答减弱。
在SLPI的显著减少BOS患者看到有趣的是,尤其是在没有在其他上皮细胞衍生的介质类似的减少,相关的蛋白酶抑制剂抑弹性酶蛋白和β防御素2。有这一发现几种可能的解释作为结果可能生产,增加小区关联或SLPI的保留导致BAL减少恢复,或增加的降解反映降低。通过在BOS发炎和改造气道AMP的非特异性的电荷相关的保持不能解释目前的发现,因为所有研究的抗菌肽为阳离子和仅SLPI减少,而其他(有时多阳离子型)的蛋白质是稳定的,甚至增加。
焦曼等。34以前所示体外转化生长因子(TGF) -β1是SLPI产生的有效抑制剂。有证据表明,移植受者的气道环境TGF-β丰富135,这表明TGF-β增加1BOS中的水平可能会降低本地SLPI的产量。中性粒细胞弹力酶水平的升高也可以解释BOS中SLPI水平的降低,因为在细胞培养研究中,中性粒细胞弹力酶通过增加细胞相关SLPI的数量来阻止上皮细胞中SLPI的释放36。
赫希等。37研究表明,患有BOS的肺移植受者的SLPI水平降低,而这与BAL液中氧化蛋氨酸的存在呈负相关。他们推测,BOS中的氧化应激通过蛋白水解和氧化失活导致SLPI的消耗增加。在本研究中,我们检验了在BOS患者中较低的SLPI水平可能是由SLPI的降解所导致的,正如之前在囊性纤维化中所显示的那样38。因此,产品的样品的Western blot分析SLPI降解进行了研究。尽管用于检测上SLPI多个表位的多克隆抗体的事实,没有SLPI降解的证据在任何测定的样本被发现。因此,在BOS患者较低水平SLPI没有被增加SLPI降解解释。
目前作者认为,AMP水平的差异可能反映了稳定患者和BOS患者不同的免疫抑制机制。绝大多数受者在移植时开始服用环孢素、硫唑嘌呤和泼尼松龙。随着时间的推移,最常见的改变是由于中性粒细胞减少而停用硫唑嘌呤,以及由于副作用或反复出现的急性排斥反应而从环孢素转向他克莫司。当获得BAL液时,大多数BOS受体使用含有钙调神经磷酸酶抑制剂和泼尼松龙的方案,而最稳定的受体使用含有钙调神经磷酸酶抑制剂、硫唑嘌呤和泼尼松龙的方案。关于免疫抑制剂药物对AMP水平的影响,我们所知甚少,但阿唑嘌呤在稳定组中的高发生率不太可能解释AMP在稳定组和BOS组之间的差异表达模式。本研究的一个局限性是它是横断面的,因此没有检查AMP水平随时间的变化。两组研究对象在收集BAL前移植后时间长短上差异有统计学意义。后续纵向研究的数据将进一步阐明这一问题。
目前的研究结果支持了这样的假设:不管有没有病原体,在BOS系统中,中性粒细胞产生的amp水平都会升高。人类中,ll - 37越高的存在和α-defensins会导致释放强大的趋化因子和树突状细胞的成熟和功能的变化17,21。此外,这些抗微生物肽发挥两者的树突状细胞和T细胞的趋化活性。因此,增加的地方水平LL-37和嗜中性白细胞α防御素可以提高适应性免疫应答,这可能有助于免疫性介导的损伤的起始和传播。嗜中性粒细胞两者α防御素和LL-37已被证明影响上皮创伤修复。具体而言,嗜中性粒细胞防卫素是促有丝分裂成纤维细胞39增加真皮和角膜成纤维细胞中I型和III型胶原的表达40,41,这表明α-defensins水平的增加可能导致组织纤维化。因此,更高水平的α-defensins在移植受者BOS可能与夸张气道损伤修复反应。目前的研究结果还表明,BOS存在蛋白酶/抗蛋白酶失衡,且游离中性粒细胞弹性蛋白酶过多,而SLPI不能抵消这一失衡。这种情况将导致进一步的气道损伤和炎症。如果气道中SLPI的水平确实降低了,那么其后果将是抗菌药物的防御能力降低,并有进一步感染的风险,从而使气道炎症永久化,同时还会降低对中性粒细胞来源的蛋白酶抑制剂的保护,从而导致上皮修复能力下降。
综上所述,在闭塞性细支气管炎综合征中表现出的抗菌肽反应将有助于形成促炎微环境,并可能促进同种免疫损伤和夸张的修复反应,从而驱动闭塞性细支气管炎综合征气道重构特征。处理肺移植受者先天免疫反应异常的治疗方法可能对保护移植物很重要,需要更多的评估。
支持声明
R.L. Anderson、D. Murphy和P.A. Corris得到了欧洲呼吸学会(European Respiratory Society)长期研究奖学金的支持。188bet官网地址R.L. Anderson也是国际心肺移植学会奖学金的获得者。I.A. Forrest获得了医学研究委员会的奖学金,C. Ward获得了医学研究委员会的项目资助。洛丹得到了麦克菲尔信托基金的支持。普劳德是加拿大炎症性气道疾病研究的主席。
感兴趣的语句
A. j . Fisher的兴趣声明可在www.www.qdcxjkg.com/misc/statements.shtml
致谢
本文作者要感谢G.约翰逊,L.射手,K.古尔德(所有心肺移植单位,弗里曼医院,纽卡斯尔,英国),D Ninaber,B.林登和R. Verhoosel(学系呼吸科,莱顿大学Meical中心,莱顿,荷兰)的宝贵的技术援助。
- 收到了2007年8月23日。
- 接受2008年4月27日。
- ©ERS期刊有限公司