摘要
阻塞性睡眠呼吸暂停患者的上气道受到反复的负压波动,促使其塌陷并重新开放。本研究的目的是确定这种机械压力是否会诱发大鼠模型的上呼吸道炎症。
的上呼吸道of Sprague–Dawley rats was subjected to a periodic pattern of recurrent negative (-40 cmH2O, 1 s)和阳性(4 cmH)2O, 2s)压力导致的崩溃和重新开放5小时。使用仪器但不受负压波动影响的大鼠作为对照组。促炎症生物标记巨噬细胞炎性蛋白的基因表达(MIP) 2、肿瘤坏死因子(TNF) -α,白介素(IL) 1β和P-selectin软腭和喉组织被实时PCR进行评估。
MIP-2的过度表达标记的,TNF-α,IL-1β和P-选择(~40-,24-,47-和比对照组7倍时,分别地)在喉组织中观察到;类似的结果在软腭组织中发现(~14-,7-,35-和比对照组,分别为11倍以上)。
反复上气道塌陷并重新打开模仿那些阻塞性睡眠呼吸暂停患者经历触发的早期局部炎症过程。这些结果可以解释阻塞性睡眠呼吸暂停患者的上呼吸道中观察到的炎症。
阻塞性睡眠呼吸暂停综合征(OSA)是一种常见的疾病,其特征是反复出现上呼吸道阻塞,并伴有氧饱和度降低和睡眠结构紊乱。这些复发性阻塞和相关的呼吸障碍是由阻塞性睡眠呼吸暂停患者上呼吸道的可折叠性增加引起的。具体来说,负压,通常与吸气开始有关,促进异常顺应的上气道管腔的减少,从而增加气流阻力。通过增加阻力的气道维持吸气需要更负的吸气压力,这反过来又会导致上气道进行性阻塞,最后导致阻塞性呼吸暂停1,2。气道闭合与引起病人的清醒气道肌肉拖拉的激活解决。
由于反复出现腔内负压、塌陷和重开等事件,上呼吸道小舌粘膜固有层、软腭和上呼吸道肌肉出现炎症和水肿等结构和功能改变3.- - - - - -5。这一机械挑战也会引起上气道感觉功能障碍,如温度、压力和振动等刺激6- - - - - -8。鉴于上呼吸道起着OSA的病理生理至关重要的作用,其潜在的炎症机制有详细的了解是重大利益的。事实上,在咽部软组织结构的炎症可以发展咽壁增厚,导致上气道狭窄3.,9,并且还可以促进神经肌肉功能障碍,与上气道扩张肌音随之减少5。灵敏度在咽壁的损失可能会削弱上气道反射到管腔内的吸气负压,增加其溃散,因此,加剧了呼吸暂停事件。
虽然有假设认为负压、虚脱、重开等事件会诱发炎症,导致上呼吸道功能障碍3.,5,没有证据表明这种机械应力实际上导致局部炎症。事实上,从病人的研究中获得的有据可查的数据3.- - - - - -5因为不同的促炎症刺激物(缺氧,代谢综合征,肥胖,等。)可能有助于在OSA患者中描述的上气道的变化。因此,本研究的目的是为了建立一个现实和良好控制的大鼠模型中,以确定类似于由OSA患者经历了塌陷重启刺激是否是能够触发在上呼吸道组织的炎症反应。
方法
动物准备
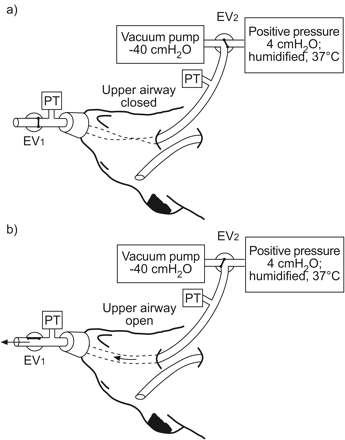
的present investigation was carried out in 28 male Sprague–Dawley rats (body mass 250–300 g) and approved by the Ethics Committee for Animal Experimentation of the University of Barcelona (Barcelona, Spain). The animals were anesthaetised with 10% urethane (1 g·kg−1),并在气管层面接受双管插管。一个小管被插入下面的气管,并指向肺部,使动物能够自然呼吸。另一根小管插入上气管,指向上气道施加反复的负压刺激。一种定制的掩模,通过电磁阀(L178B1;Sirai, Bussero,意大利),被紧紧地调整到老鼠的鼻子(图1⇓)。
在麻醉大鼠中应用间断模式的上呼吸道塌陷(持续1秒)和重新开放(持续2秒)的实验装置示意图。a)阻塞鼻罩,将上气道导管连接至-40 cmH,实现上气道塌陷2O负压源。b)打开鼻面罩阀,将上气道插管连接至4cmh,重新开放上气道2阿正压源。EV1和电动汽车2:分别电阀1和2,;PT:压力传感器。
实验装置
对上呼吸道反复施加负压摆动的实验设置如图1所示⇑。三通电磁阀(L377B03G;连接:上呼吸道小管;-40年而言不啻2O真空源;还有4厘米高2阿正压源。通过电子控制阀门,上气道受到周期性的坍塌(1秒)和重新打开(2秒)。同时封闭鼻面罩阀,将上气道导管与负压源连接,导致上气道塌陷(图1a)⇑)。通过同时向大气打开鼻罩并将上气道插管与正压源连接,实现上气道的重新开放(图1b)⇑)。正压源内的空气温度和湿度保持在生理条件下,避免了上呼吸道粘膜的干燥。连续测量鼻罩和上气道插管处的压力(Microswitch 176PC28HD2;霍尼韦尔,斯卡伯勒,ON,加拿大)。气管内的气流用肺速计测量(Fleisch-000;位于上气道导管和压力源之间(未显示)。
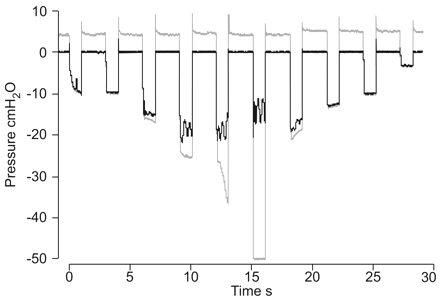
Figure 2⇓说明了实验设置(图1)⇑)允许上气道塌陷和重启的诱导。施加的负气管压力波动的大小逐渐减(六个周期),然后升高(4个循环)。当气管压力比腔内压力引起崩溃(临界压力高;P暴击),鼻压与气管压力相同,说明上气道仍然开放,因为施加在气管上的压力是传递到鼻子上的。然而,当气管压力低于P暴击,鼻压不再降低,因为上气道塌陷,因此施加在气管上的负压不能传递到鼻子上。
应用于鼻内的负压(灰色线)和记录在鼻罩上的压力(黑色线)的例子。当气管压力高于临界压力(P暴击上气道(∼15 cmH)2在这个例子中是O)。而气管负压小于P暴击,鼻压不再降低,因为上气道塌陷,因此施加在气管上的负压不能传递到鼻子上。
试验协议
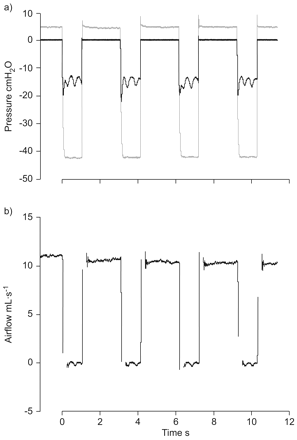
A total of 14 rats were subjected to a recurrent pattern of collapse and reopening for 5 h (fig. 3⇓)。其中有8个是P暴击在反复使用负压摆动开始和结束时测量上呼吸道。实验结束时,处死大鼠。在这些大鼠中,软腭和喉组织被切除10-80℃冷冻保存,进一步进行炎症基因表达分析。另外6只大鼠的上呼吸道被完全切除10并嵌入最佳切割温度的化合物中,冷冻并储存在-80°C进行组织病理学分析。作为对照组,一组14只大鼠接受了相同的仪器和方案,除了重复的负压波动没有应用(通过不连接压力源;图1⇑)。
应用间歇性上呼吸道塌陷和重新开放5小时所记录的信号的例子(数据来自图2中使用的同一只大鼠)⇑)。a)气管内(灰色线)和鼻面罩处(黑色线)分别记录负压变化;b)气管处记录气流。在应用负气管压力时,流量为零,表明上呼吸道塌陷。气管正压时,血流信号提示上气道开放。为了避免开阀和关阀引起的高频噪声,未绘制出正、负压过渡附近的气流信号。
基因表达分析
将组织样品解冻并随后通过一个均化器的装置器(Polytron 2100; KINEMATICA,卢塞恩,瑞士)破坏。各样品的总RNA含量使用6100核酸PrepStation在系统(Applied Biosystems公司,福斯特城,CA,USA),并从总RNA通过高容量cDNA试剂盒的试剂进行cDNA的合成仪(Applied Biosystems)中分离。的cDNA的扩增进行,一式三份,通过实时PCR(7300 RT-PCR; Applied Biosystems)中。对于巨噬细胞炎性蛋白特异性基因表达测定法(MIP)-2,肿瘤坏死因子(TNF)-α,白细胞介素(IL)-1β和P-选择(Rn00586403_m1,Rn00562055_m1,Rn00580432_m1和Rn00565416_m1,分别地)用于点播(测定TM值;Applied Biosystems公司)。GAPD(Rn99999916_s1)的基因表达被认为是每只大鼠内源参考。最后,相对基因表达,用比较的方法来定量2-ΔΔCt11。为此,我们以上气道负压大鼠的基因表达作为对照。
上呼吸道组织病理学
以4%的甲醛和石蜡包埋剂固定下咽部水平的横断面48小时。石蜡块被削减的部分5µm和苏木精和伊红染色。每个样本的水肿程度和炎症细胞的存在由两名观察人员确定,他们不知道该制剂是与受到机械刺激的大鼠一致,还是与对照组大鼠一致。
统计分析
数据以均数±表示扫描电镜。各组间比较采用不配对t检验或Mann-Whitney秩和检验。的变化P暴击通过上气道塌陷诱导每只大鼠的/重新开放用配对t检验评估。p值<0.05被认为是统计学显著。
结果
反复塌陷和上气道重开的5小时模式诱导了炎症过程。明显的过度炎性标志物MIP-2, TNF-α,IL-1βP-selectin(∼40 - 24、47和7倍大于控制,分别)在喉癌组织(图4所示⇓);在软腭组织中也发现了类似的结果(分别比对照组大14、7、35和11倍;图5⇓)。与此相反,上气道的组织的组织病理学分析比较经受塌陷大鼠的上气道时/重启和对照显示在水肿或在白细胞浸润无显著变化(数据未显示)。一般,P暴击实验开始时为-19.4±1.6 cmH2O.上气道机械刺激5小时后(-15.7±2.3 cmH),未见明显变化(p = 0.11)2O)。
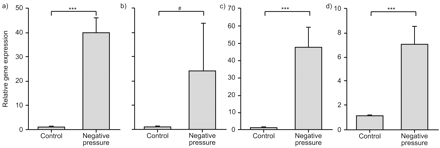
促炎性生物标志物的相对基因表达)巨噬细胞炎性蛋白-2,b)中肿瘤坏死因子α,c)中白介素1β和d)P-选择在经受反复负压控制大鼠和大鼠的喉组织波动在上呼吸道。数据以均数±表示扫描电镜。#: p = 0.002;***:P <0.001。
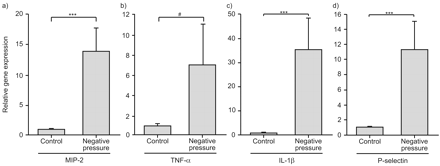
相对基因表达的促炎症生物标记)巨噬细胞炎症protein-2, b)肿瘤坏死factor-α,c) interleukin-1β和d) P-selectin软腭组织控制的老鼠和老鼠受到反复上呼吸道的负压波动。数据以均数±表示扫描电镜。#:p = 0.011; ***: p<0.001.
讨论
一个专门设计用于大鼠上呼吸道负压波动的实验设置,使作者能够诱发与阻塞性睡眠呼吸暂停患者上呼吸道所经历的类似的反复塌陷/再开放模式。上气道负压的大小(-40 cmH)2O)中阻塞性事件相似OSA患者的食管压力的值2。这种机械应力为轻度和足够短的,以避免在上呼吸道组织的结构或功能的效果,如通过没有受到刺激大鼠和对照之间差异的组织学示出,并且由一个事实,即P暴击整个机械挑战后没有变化。然而,这种现实的机械刺激能够触发早期局部炎症级联。事实上,由气管负压波动引起的5小时反复发作的上呼吸道塌陷和再开放导致了喉部和软腭组织中促炎基因的明显过度表达。
的在活的有机体内分离的上气道大鼠模型已经在早期的研究中被用来表征所述马达响应于管腔内的压力变化12- - - - - -14。然而,这些研究并没有模拟阻塞性睡眠呼吸暂停患者反复上呼吸道关闭和重新开放的动态过程。的确,上呼吸道保持开放,并使用气管内逐渐增加的负压来促进吸气流量的减少(流量限制),但不会达到完全气道塌陷12,13。一个类似的方法最近被用来研究腔内体积变化在负和正的压力下,通过磁共振成像的手段15。由于该技术需要在较长时间内持续施加正压或负压进行图像采集,因此无法模拟OSA患者上呼吸道事件的快速循环动力学。在另一项研究中,在上呼吸道的入口和出口同时施加准静态负压,导致无法记录气道闭合14。与此相反,在本工作中使用的模型能够模拟在OSA经历的机械应力,由于施加到上气道力学的事件序列诱导动态图案模仿呼吸。这个实验设置的另一个优点是,它允许直接测量P暴击(腔内压力引起闭合)的上气道的外插,而不是从使用斯塔林电阻模型部分塌陷条件的数据,或通过引入导管到上气道12,13,15。
最近已经报道,间接地与OSA相关联的其他机械刺激可以诱导在上气道的早期炎症反应。振动的类似于打鼾触发器在人类气道上皮细胞中的促炎症级联中的应用16而在大鼠软腭10。此外,有研究表明,与持续气道正压相关的机械压迫可促进大鼠鼻粘膜炎症反应17。然而,没有直接证据表明,反复出现的机械应力,包括负压、塌陷和上气道重开,会诱发局部炎症。关于类似机械应力的唯一可用数据是支气管和肺组织。特别是,据报道,在动物模型中,机械通气引起下气道的塌陷和重新打开18在培养的胎鼠肺上皮细胞中19诱导的炎症和细胞损伤,分别。此外,一些较早的数据所支持的概念,即负压可能在支气管壁中的炎症刺激。实际上,最近的一项研究中OSA患者中进行显示IL-8的痰水平和呼吸暂停/低通气指数之间的相关20。在这些患者中观察到的支气管炎症可能是由于反复吸气时支气管树上的负压增加而引起的,上呼吸道阻力增加。
本研究提供的证据表明,反复的腔内负压、塌陷和再开放所产生的机械应力会在上呼吸道引起早期的促炎级联反应。具体地说,一个戏剧性的基因超表达的炎症生物标记MIP-2, TNF-α,IL-1βP-selectin观察喉和软腭组织(无花果4⇑和5⇑分别)。细胞因子TNF-α导致内皮功能障碍21并调节活性氧和粘附分子的表达22,而细胞因子IL-1β可以诱发其他炎症分子的表达,比如MIP-2导致白细胞招募23。粘附分子P-选择,其在内皮中表达,通过内皮屏障起着白细胞外渗中起重要作用24。考虑到这些炎症介质信号通路的复杂性和冗余性,对每个个体标记的基因表达变化的解释应该谨慎对待25。然而,在所有分析的生物标志物中都发现了大量的过表达(图4)⇑和5⇑)清楚地表明,急性刺激触发了炎症级联的早期局部上调。
机械应力引起的上呼吸道炎症反应可能导致结构和功能上的后果;咽壁增厚,局部肌病和/或神经病。事实上,早期的研究表明,细胞因子如TNF-α的存在26和IL-1β27可引起肌纤维无力和收缩功能障碍。此外,TNF-α可能导致损失上呼吸道诱导神经病变的敏感性28和神经毒性29。
总之,该机械应力反复腔内压力波动,虚脱和重新打开触发器在上呼吸道的炎症过程相关联的本研究中的节目。因此,可以预期,这种机械挑战的慢性应用可以产生炎症性细胞浸润和组织变化引起的患者中观察到的结构和功能性上呼吸道损伤,从而有助于表征阻塞性睡眠呼吸暂停的进展的“恶性循环”三十。
支持声明
这项工作得到了Ciencia y Tecnologia部长(SAF2005-00110和SAF2004-00684)和Sanidad y Consumo部长(fiss - pi040929)的部分支持。
感兴趣的语句
无声明。
致谢
作者希望感谢M.A.罗德里格斯(西班牙巴塞罗那大学医学院教授)提供的技术援助。
脚注
编辑意见见255页。
- 收到了2007年11月30日。
- 接受2008年4月16日。
- ©ERS期刊有限公司