摘要
转化生长因子(TGF)-β信号在调节肺发育中起重要作用。然而,TGF-β信号在肺上皮发育中的特定调节功能与间充质细胞仍然是未知的。
通过免疫染色法,首次测定了TGF-β II型受体(TβRII)在发育小鼠肺中的表达规律。然后,通过有条件地敲除TβRII/表面活性剂蛋白c -逆转录四环素转激活剂/TetO-Cre小鼠肺上皮中的TβRII,检测TβRII在肺发育中的功能与floxed- t - β rii /Dermo1-Cre小鼠间质。
TβRII仅在妊娠早期(胚胎日(E)11.5)的远端气道上皮中表达,但在妊娠中期(E14.5)至出生后14天的气道上皮和间质中均表达。小鼠肺上皮中TβRII缺失导致出生后肺泡发育迟缓,I型肺泡上皮细胞明显减少,而产前肺发育未见异常。相反,阻断TβRII在中胚层来源的组织,包括肺间质,导致妊娠中期轻度肺分支异常和细胞增殖减少,并伴有其他器官的多种缺陷,包括膈疝。在胚胎肺外植体培养中证实了原发性肺分支缺陷。
本研究的新发现表明,转化生长因子-β II型受体介导的转化生长因子-β信号在肺上皮中发挥着独特的作用与间质对肺发育的特定阶段有不同的控制。
肺的发育是由一对初生上皮芽的形成开始的,它们从原始前肠内胚层腹侧表面的喉-气管沟外翻到周围的内脏间质1,2.呼吸树随后通过分支形态发生发育,上皮芽反复生长、伸长和细分,随后肺泡形成一个大的气体交换表面3.,4.如果肺形成受到严重影响,正常肺发育过程的中断可导致新生儿呼吸衰竭或窘迫,如果发育中的肺发生较轻微的变化,则在以后的生活中易患肺部疾病5.
由于肺发育过程保守性较好,因此小鼠肺发育是研究人类肺器官发生和先天性呼吸系统疾病机制的理想模型。小鼠肺发育开始于胚胎日(E)9.5,组织学上分为假腺期(E9.5-E16.5)、小管期(E16.6-E17.4)、囊状期(e17.5 -出生日(P)5)和肺泡期(P5-P30)。1.在肺发育过程中,上皮-间充质相互作用在指导早期肺分支形态形成和后来的肺泡形成中起着至关重要的作用,这一过程受多种生长因子的调控,包括转化生长因子(TGF)-β超家族成员6.
TGF-β1、-β2和-β3配体是TGF-β超家族中密切相关的成员,具有差异的表达模式在活的有机体内生物活动在体外.TGF-β配体结合TGF-β丝氨酸/苏氨酸激酶I型和II型受体(分别为TβRI和TβRII)的异质复合物。7,8.在配体诱导的受体聚集后,组成性激活的TβRII激酶磷酸化并激活TβRI,随后识别并磷酸化羧基端SSXS基序上与受体结合的TGF-β特异性Smad蛋白(Smad2和Smad3)。这些磷酸化的smad与受体分离,与一个共同的伙伴Smad4形成复合物,转运到细胞核中,直接或间接结合到TGF-β响应元件上,并作为转录共调节剂诱导或抑制TGF-β靶基因的表达9.此外,与smad无关的信号通路也通过相同的受体被激活10.t -β rii是唯一的TGF-β特异性II型受体。
TGF-β信号在正常肺发育中起关键作用。TGF-βs零突变可导致胎儿肺部发育异常或出生后肺部过度炎症11- - - - - -14表明TGF-β信号对于正常肺的形成和功能至关重要。此外,在完整的胚胎肺外植体培养体系中加入外源TGF-β1,可观察到肺分支形态发生异常15.此外,过度表达转化生长因子-β1由3.7 kb的人表面活性剂蛋白(SP) C转基因小鼠肺上皮启动子呈现肺发育不全表型16提示适当的TGF-β信号在适当的时间和地点对正常肺器官发生至关重要。此外,据推测内源性TGF-β信号的变化介导了雄激素升高引起的男性胎儿肺成熟延迟17,18.然而,肺是一个复杂的器官,因此TGF-β配体水平的整体改变可能会通过改变自分泌和/或旁分泌信号活动,对肺上皮或间质中TGF-β信号活动产生不同的影响,甚至两者都有影响,这可能很难区分。常规淘汰赛的关键TβRII由于在肺形成之前的造血和血管发生缺陷,导致早期胚胎死亡19.在本研究中,使用Cre/选择性地阻断了内源性t β rii介导的TGF-β信号通路在发育中的小鼠肺上皮细胞和间充质细胞中的作用loxP条件敲除方法,发现TGF-β信号在肺上皮中起着重要而独特的作用与间充质细胞在不同发育阶段对正常小鼠肺发育的控制差异。
材料与方法
小鼠品系与育种
液氧TβRII(TβRIIfx /外汇)小鼠是在H.L. Moses的实验室中产生的,如前所述20..在TβRIIfx /外汇的外显子2TβRII吉恩被两个人夹击loxPDNA元素。外显子2的缺失导致移码并消除功能性TβRII蛋白的表达。诱导的肺上皮特异性Cre转基因小鼠(spc -逆四环素活化剂(rtTA)/TetO-Cre)由J.A. Whitsett生成并提供21.Mesoderm-specificDermo1-Cre杂合敲入小鼠(Dermo1-Cre+ /−)由D.M. Ornitz制作并提供22.
定时交配TβRIIfx /外汇和TβRIIfx / +/SPC-rtTA/TetO-Cre小鼠产生肺上皮特异性TβRII条件敲除(Ep-CKO)小鼠(TβRIIfx /外汇/SPC-rtTA/TetO-Cre),杂合的TβRII基因敲除小鼠(TβRIIfx / +/SPC-rtTA/TetO-Cre)和对照小鼠(TβRIIfx /外汇,TβRIIfx / +,TβRIIfx /外汇/SPC-rtTA,TβRIIfx /外汇/TetO-Cre,TβRIIfx / +/SPC-rtTA或TβRIIfx / +/TetO-Cre),诱导剂多西环素(Dox)存在。对照组小鼠的正常肺发育与野生型小鼠相同(TβRII+/+)。从妊娠早期E6.5或P30开始至实验结束,给药剂量为625 mg·kg−1食物中的Dox (TestDiet, Richmond, in, USA)和0.5 mg·mL−1(Sigma-Aldrich Co., St . Louis, MO, USA)
定时交配TβRIIfx /外汇和TβRIIfx / +/Dermo1-Cre+小鼠产生中胚层特异性TβRII条件敲除(Me-CKO)小鼠(TβRIIfx /外汇/Dermo1-Cre+),杂合的TβRII基因敲除小鼠(TβRIIfx / +/Dermo1-Cre+)和对照小鼠(TβRIIfx / +或TβRIIfx /外汇)。所有小鼠均在C57BL/6菌株背景下饲养,采用基因组DNA PCR分型。根据Saban儿童医院研究所(Los Angeles, CA, USA)机构动物护理和使用委员会批准的方案,将研究中使用的小鼠置于无病原体环境中。
组织学和形态计量学分析
肺用4%多聚甲醛缓冲液在4℃下固定过夜,脱水后包埋石蜡。如前所述,用血红素和伊红(HE)染色5 μm厚的切片23.弹性蛋白染色采用Hart’s间苯甲素-品红溶液,反染0.5%酒黄石。为了进行形态计量学分析,每隔250 μm随机从每个样品的相同叶上选择5个切片,并用HE染色。然后根据建立的方法测量平均线性截距(MLI)23- - - - - -25.简单地说,每个切片的图像都以40倍的放大倍数被数字捕获。然后使用ImagePro软件,在矩形网格内间隔约0.9 mm的水平线和垂直线上计数肺泡表面交叉点。然后计算MLI为所有计数线的长度之和除以被计数的肺泡间隔截距总数。结果采用非配对t检验进行分析,以比较平均值之间的差异,如果p<0.05则认为显著。以避免胎儿肺成熟的性别差异26,在每个时间点对同性胎儿进行定量比较。
免疫组织化学
本研究使用的抗体为:山羊TβRII和AQP 5多克隆抗体,来自Santa Cruz Biotechnology, Inc. (Santa Cruz, CA, USA);Sigma-Aldrich公司α-平滑肌肌动蛋白(SMA)和层粘连蛋白抗体;和来自Seven Hills Bioreagents (Cincinnati, OH, USA)的SPC抗体。
免疫组织化学染色使用Zymed Laboratories, Inc. (South San Francisco, CA, USA)的HistoStain试剂盒,按照制造商的说明进行。用3-氨基-9-乙基咔唑或3,3 ' -二氨基联苯胺作为显色底物。
细胞增殖与凋亡
使用Zymed Laboratories, Inc.的PCNA染色试剂盒,通过增殖细胞核抗原(PCNA)染色分析细胞增殖,使用ApopTag试剂盒(Millipore, Billerica, MA, USA),通过末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍端标记(TUNEL)染色评估细胞凋亡,如前面所述27.
免疫印迹
肺组织蛋白的检测以前已经有过描述28.简单地说,新鲜肺组织在冰中溶解在含有1mm苯基甲基磺酰氟、蛋白酶抑制剂鸡尾酒(罗氏诊断公司,巴塞尔,瑞士)和1mm正钒酸钠的放射免疫沉淀测定缓冲液中。蛋白质浓度采用Bradford法测定,所用试剂购自Bio-Rad Laboratories (Hercules, CA, USA)。使用MOPS缓冲系统(Invitrogen, Carlsbad, CA, USA),用NuPAGE®4-12%梯度SDS-PAGE凝胶分离等量(40 μg)的总组织裂解液蛋白。将蛋白转移到聚偏二氟乙烯膜上后,用特异性抗体检测感兴趣的蛋白。细胞周期蛋白依赖性激酶(CDK)2、β-actin和t - β rii抗体购自Santa Cruz Biotechnology, Inc.,抗甘油醛-3-磷酸脱氢酶抗体购自Research Diagnostics, Inc. (Flanders, NJ, USA)。
数据展示和统计分析
每个实验亚组分析至少3对来自不同坝的TβRII条件敲除(CKO)和正常对照的同窝小鼠。所有定量数据均以均数±表示sd.统计学差异比较采用方差分析和未配对t检验,p <0.05为差异有统计学意义。
结果
小鼠肺上皮细胞在肺发育过程中条件性去除TβRII
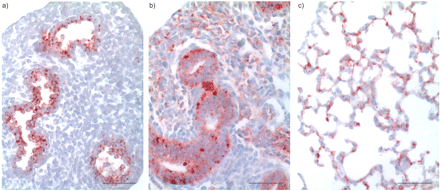
小鼠胚胎与常规TβRII零突变在E10.5之前死亡,在肺发育之前存在造血和血管发生缺陷19.因此,传统的TβRII敲除小鼠模型不适用于研究TβRII在肺形成中的功能,并且是肺特异性条件TβRII基因敲除小鼠模型-loxP这需要系统在活的有机体内研究。为了选择细胞系特异性的Cre驱动系来消除肺发育过程中TβRII的功能,首先使用免疫组织化学方法检测了TβRII蛋白在不同肺发育阶段的表达(图1)⇓)。有趣的是,在胚胎早期E11.5时,TβRII在远端肺气道上皮细胞中特异性表达,而在间充质细胞中未检测到表达,尽管上皮细胞和间充质细胞在妊娠期E14.5时均表达TβRII蛋白。出生后肺泡形成过程中,TβRII也在上皮细胞和间充质细胞中强烈表达,大多数阳性染色细胞位于肺泡间隔内。
免疫组织化学检测发育中小鼠肺中转化生长因子-β II型受体(TβRII)蛋白的表达。a)在妊娠早期,胚胎日(E)11.5,仅在气道上皮细胞中检测到TβRII蛋白,而b)在妊娠中期(E14.5),在上皮和间充质细胞中均检测到TβRII蛋白的表达。c)出生后第14天肺泡形成时,检测出生后间隔结构中TβRII蛋白的表达。标尺= 50 μm。
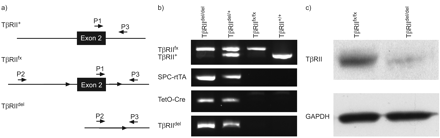
因此,肺上皮特异性TβRII通过杂交产生CKO小鼠TβRIIfx /外汇老鼠SPC-rtTA/TetO-Cre在全肺和远端支气管的气道上皮细胞中,通过肺上皮特异性诱导Cre表达程控promoter-drivenrtTA转基因,与诱导剂Dox联合在肺形成前给予(E6.5)21.作为cre介导的结果loxPDNA重组,floxed-TβRII从肺组织中分离的基因组DNA外显子2缺失通过PCR基因分型证实(图2)⇓)。全肺组织裂解物中TβRII蛋白显著降低TβRIIWestern blot也证实了p- cko小鼠P28的表达(图2)⇓)。
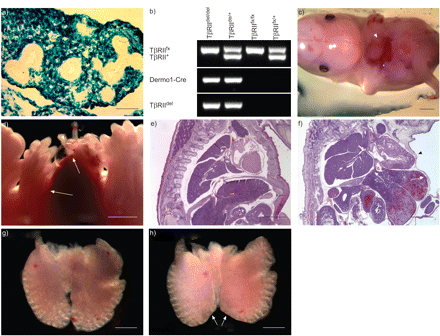
肺上皮特异性转化生长因子-β II型受体(TβRII)小鼠条件敲除(Ep-CKO)。a)基因处理小鼠TβRII基因组结构示意图。图中显示了基因分型PCR引物的位置(P1-P3)。b)肺组织基因组DNA的PCR基因型。c)全肺组织裂解液中完整TβRII蛋白水平显著降低TβRII以甘油醛-3-磷酸脱氢酶(GAPDH)为加载对照,对出生后28天的Ep-CKO小鼠进行Western blot验证。TβRII+:野生型等位基因;TβRII外汇:絮凝等位基因;TβRII▽:外显子2缺失的等位基因;SPC:表面活性剂蛋白C;rtTA:逆转录四环素激活剂。
早期小鼠肺器官发生时肺上皮中TβRII基因表达缺失导致出生后肺泡发育迟缓,但在产前肺发育中没有检测到表型
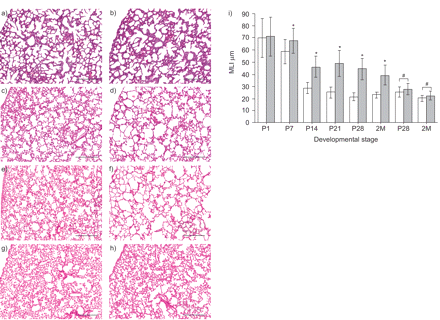
新生儿肺上皮特异性TβRIIEp-CKO小鼠(TβRIIfx /外汇/SPC-rtTA/TetO-Cre)呼吸正常,没有任何呼吸窘迫的迹象。组织学检查证实P1肺囊状结构形成正常TβRIIEp-CKO肺与同窝对照比较。肺泡化明显迟缓TβRIIEp-CKO小鼠出生后肺泡形成(图3)⇓),发生于小鼠的P5-P30。在小鼠出生后肺泡形成过程中,继发嵴发育并延伸形成新的继发间隔,进一步细分末端气囊结构,同时平均肺泡大小减小。因此,肺泡越大,肺泡越少;因此,肺泡生成可以通过计算MLI来量化。在P7,早期肺泡形成期间,MLI在TβRIIEp-CKO肺略高于正常(图3)⇓)。随着肺泡增生的继续,MLI与TβRIIEp-CKO和正常对照组在P14时显著升高,并保持升高至肺泡化结束(P28),以及进入成年早期(2个月;图3⇓),提示肺泡发育的主要成熟停止。为了排除肺泡化减少的可能性TβRIIepo - cko是由复合转基因基因型的非特异性作用引起的,并比较了不同基因型小鼠的肺泡化TβRIIEp-CKO和正常对照,但没有Dox诱导。在没有Dox诱导的情况下,形态学和形态计量学MLI测量未检测到肺泡化的变化(图3)⇓)。此外,小鼠与dox诱导TβRII杂合基因型(TβRIIfx / +/SPC-rtTA/TetO-Cre)肺肺泡化正常,与对照组相同。这些数据表明,肺泡发育迟缓TβRIIEp-CKO小鼠特异性是由于肺上皮缺乏TβRII功能。
肺上皮特异性转化生长因子-β II型受体(TβRII)条件敲除(Ep-CKO)小鼠肺的形态学变化及形态学测量正常对照出生后不同发育阶段的肺组织切片(a、c、e)TβRIIEp-CKO小鼠(b, d和f)。新生儿(出生后(P)1)肺未发现可检测到的变化TβRII与对照组相比,Ep-CKO小鼠(a和b)。然而,由于次级间隔结构生长迟缓,末端气囊仍然更大TβRIIp- cko在P14 (c和d)和P28 (e和f)的肺泡化TβRII2月龄(2M)时,与正常对照(h)相比,Ep-CKO未受多西环素(Dox)诱导(g)的影响。i)通过平均线性截距(MLI)对出生后不同肺泡形成阶段肺泡大小的形态计量量化。大约85%的肺泡形成在P14时完成,而肺泡形成明显迟缓,在P14时肺泡大小增大58%TβRIIEp-CKO小鼠(烧烧),并一直保持到成年。在胚胎第6.5天给予Dox诱导条件敲除。#基因型小鼠无Dox诱导作用TβRIIfx /外汇或TβRIIfx /外汇/SPC-rtTA/TetO-Cre.*: p < 0.05。标尺= 250 μm。
条件敲除肺上皮细胞中TβRII功能导致出生后肺泡形成过程中细胞增殖和分化异常
肺泡形成过程中继发性间隔形成是一个复杂的过程,需要上皮细胞生长的精细协调、毛细血管网络的延伸和简化、肺泡肌成纤维细胞的参与和弹性间质基质的正确沉积。这是由包括TGF-β信号在内的许多因素调节的。肺上皮细胞中TβRII的缺失导致肺泡化阶段细胞增殖减少,PCNA蛋白水平降低,PCNA阳性细胞减少TβRIIEp-CKO小鼠肺在P7(图4a-c)⇓)。此外,P14和P28中CDK2表达的降低也证实了细胞增殖的降低TβRIIEp-CKO肺(图4a)⇓)。然而,TUNEL染色显示,肺肺泡形成过程中,尤其是P28肺泡形成后期,细胞凋亡并未增加(图4d)⇓因此,在受影响的细胞系中,细胞增殖的减少,而不是细胞死亡的增加,可能导致肺泡间隔形成的减少TβRIIEp-CKO肺。
肺上皮细胞中转化生长因子-β II型受体(TβRII)的缺失导致细胞增殖能力下降。a)与对照组相比,肺上皮特异性TβRII条件敲除(Ep-CKO)小鼠的肺部增殖细胞核抗原(PCNA)和细胞周期蛋白依赖性激酶(CDK)2蛋白水平在出生后第7天(P),第14天和第28天降低。在这些印迹中,β-肌动蛋白被用作负载对照。b)对照组和c)对照组P7的PCNA(深棕色)组织学染色TβRIIEp-CKO小鼠的pna阳性细胞比CKO小鼠少。d)对照组和e) P28细胞凋亡水平TβRII然而,通过末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍端标记(深棕色)显示,Ep-CKO小鼠是相似的。标尺= 50 μm。
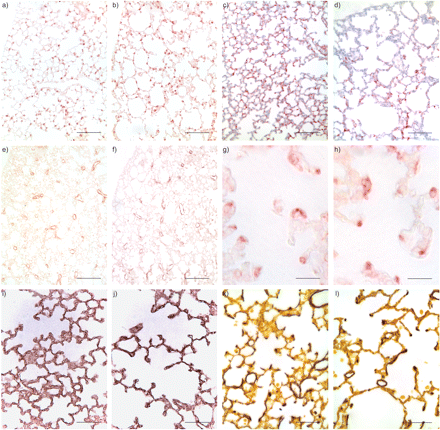
细胞分化也通过免疫染色来评估P14时肺中不同细胞系的分子标记,此时可见肺泡化明显迟缓TβRIIEp-CKO肺。SPC和AQP5分别是II型和I型肺泡上皮细胞(AEC)的细胞特异性标志物。spc阳性细胞无明显变化TβRIIEp-CKO肺(图5a)⇓然而,在肺上皮中去除TβRII后,AQP5阳性细胞和阳性染色细胞中AQP5的强度明显降低(图5c)⇓和d),提示AECI谱系分化和/或扩增减少可能是肺泡发育迟缓的重要细胞机制TβRIIEp-CKO小鼠肺。此外,通过检测隔膜结构中的SMA、层粘连蛋白和弹性蛋白纤维沉积,对肌成纤维细胞和相关重要的细胞外蛋白进行了评估(图5e - 1)⇓)。层粘连蛋白是毛细血管基底膜的主要蛋白质成分,在两者的鼻中隔尖端分布相似TβRIIEp-CKO和对照小鼠肺,表明毛细血管生长正常。在细支气管和大血管周围的平滑肌细胞以及两者的间隔结构内的肌成纤维细胞中检测到类似的SMA阳性信号模式TβRIIEp-CKO和正常对照肺。此外,弹性蛋白纤维沉积在肺泡间隔结构的尖端TβRIIEp-CKO患者的肺与正常对照相似,这表明间充质细胞增殖或分化或细胞外基质沉积的改变并不是肺泡异常的直接原因TβRIIEp-CKO老鼠。
在出生后第14天,对对照组(a、c、e、g、i和k)和肺上皮特异性转化生长因子-β II型受体(TβRII)条件敲除(Ep-CKO)小鼠(b、d、f、h、j和l)进行细胞分化评估。表面活性剂蛋白c (a和b)的免疫染色无明显变化,但水通道蛋白5 (c和d)的免疫染色降低TβRIIEp-CKO老鼠。肌成纤维细胞和相关的细胞外基质蛋白在对照组和实验组中相似TβRIIEp-CKO小鼠α-平滑肌肌动蛋白(e-h)、层粘连蛋白(i和j)和弹性蛋白(k和l)免疫染色。e、f)比例尺= 200 μm。g、h)比例尺= 20 μm。i - 1)比例尺= 50 μm。
胎儿肺发育过程中小鼠肺间充质细胞中TβRII的条件消除
由于TβRII也被发现在小鼠胚胎和成年肺的间质中表达(图1)⇑),间充质细胞中t β rii介导的TGF-β信号传导可能在调节胚胎肺形成,特别是分支形态发生中发挥独特作用。利用中胚层来源的组织特异性表达CreDermo1-Cre敲入驱动鼠标线22间质特异性cre介导loxPDNA重组在包括肺在内的多个小鼠胚胎器官中实现(图6a)⇓)。TβRIIfx /外汇然后与老鼠杂交Dermo1-Cre生成小鼠TβRIIMe-CKO小鼠,如图6b所示⇓)。这些TβRIIMe-CKO小鼠在其他重要发育过程中存在严重缺陷,包括继发性腹壁形成缺陷、先天性膈疝和心脏发育异常(图6c-f)⇓)。这些非肺异常都是由于TGF-β信号在其他关键的中胚层来源组织中被破坏。肺芽形成TβRIIMe-CKO小鼠在早期没有明显的影响(E12.5),但在E14.5时观察到明显的肺畸形,特别是在左右下叶(图6g)⇓和h),这可能是由于胸壁形成和膈关闭缺陷导致心脏和肝脏定位异常。这Dermo1-Cre简况TβRII条件敲除在E16.5时是致命的,可能是由于包括心脏在内的其他器官存在严重缺陷。
中胚层特异性转化生长因子-β II型受体(TβRII)条件敲除(Me-CKO)小鼠。a) Cre在肺间质特异性表达Dermo1-Cre小鼠通过交叉验证Dermo1-Cre和Rosa26R小鼠,其中只有cre介导的细胞loxPDNA重组表达LacZ。lacz染色(蓝色)胚胎日(E)12.5肺组织切片。除气道上皮细胞外,全肺LacZ染色呈阳性。b)肺组织基因组DNA的PCR基因型。a的顶视图(c)和侧面视图(d)TβRIIMe-CKO胎儿E14.5。胸腹和上腹部明显有腹壁形成缺陷,如图所示为一层膜而不是皮肤、肌肉和肋骨(箭头)。此外,还观察到肝脏通过膈疝向胸部突出(d;箭头)。血红素和伊红染色的E16对照矢状面切片(e)和TβRIIMe-CKO (f)胎儿。f)显示体壁缺陷(箭头)和肝脏突出(箭头)。对照组E14.5肺大体视图(g)和TβRIIMe-CKO (h)小鼠。h)肺明显畸形,尤其是左右下叶(箭头)。TβRII外汇:絮凝等位基因;TβRII+:野生型等位基因;TβRII▽:外显子2缺失的等位基因。a)比例尺= 100 μm。c-f)比例尺= 1mm。g、h)比例尺= 0.5 mm。
产前肺间充质TβRII信号的缺失破坏了正常的分支形态发生
的粗略比较TβRIIMe-CKO和对照小鼠肺分支形态发生早期(E12.5),早期肺分支未见明显变化(图7a)⇓b).然而,组织学研究发现外周气道轻度扩张伴间充质细胞密度降低TβRIIMe-CKO肺E14.5(图8a)⇓b).这些表型变化在2 d后的E16.5时更为明显。PCNA免疫染色显示TβRII与正常窝鼠对照组相比,Me-CKO肺的气道上皮和周围间质均减少(图8e)⇓然而,SPC和SMA免疫染色显示,周围气道上皮细胞和间充质肌成纤维细胞/平滑肌细胞的分化没有改变(图8g-j)⇓)。
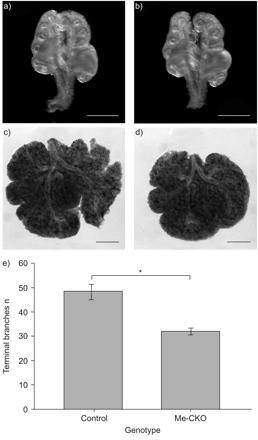
肺外植体培养中中表皮特异性转化生长因子-β II型受体(TβRII)条件敲除(Me-CKO)小鼠肺分支缺陷对照(a)与正常胚胎日(E)分离的12.5只肺进行比较TβRII然而,与对照组(c)相比,Me-CKO小鼠的肺分支减少TβRII培养3天后检测Me-CKO肺(d)在体外.e)器官培养结束时,对周围气道分支数量进行量化。外周分支明显减少TβRII与正常对照比较,观察Me-CKO肺外植体。*: p < 0.05。比例尺= 0.5 mm。
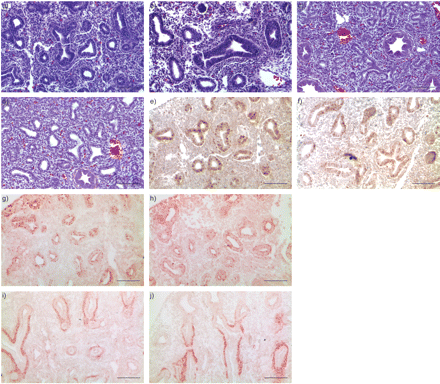
中表皮特异性转化生长因子-β II型受体(TβRII)条件敲除(Me-CKO)肺的异常分支形态发生。肺形态与对照组(a和c)的苏木精和伊红染色的比较TβRIIMe-CKO (b和d)小鼠胚胎日(E)14.5 (a和b)和E16.5 (c和d)TβRIIE14.5后的Me-CKO肺。通过增殖细胞核抗原(PCNA)免疫染色(e和f)评估细胞增殖情况。E14.5气道上皮细胞和周围间充质细胞中PCNA阳性细胞(棕色)减少TβRII用表面活性剂蛋白C (g和h)和α-平滑肌肌动蛋白(i和j)免疫染色(红色)检测外周气道上皮细胞和肌成纤维细胞/平滑肌细胞的细胞分化情况。对照组(g和i)与对照组(g和i)之间无显著变化TβRIIE14.5时肺Me-CKO (h和j)。标尺= 100 μm。
以排除异常肺分支进入的可能性TβRIIMe-CKO是由于发育中肺的物理变形引起的,采用全胚肺外植体培养。胚胎肺外植体在E12.5分离,两组间无分支差异TβRIIMe-CKO和正常对照(图7a)⇑b).培养3 d后,对生长中的肺组织的终末分支数进行计数和比较TβRIIMe-CKO和对照组(图7c-e)⇑)。的末端分支数量显著减少TβRIIMe-CKO肺移植体,占正常对照组的66%(32±2)与分别为48±3;p < 0.05)。相比之下,在3天培养的肺分支TβRII与正常对照相比,Ep-CKO肺外植体没有显著变化(数据未显示),这表明胚胎和胎儿肺间质中t β rii介导的信号传导在肺分支形态发生过程中起重要作用,而气道上皮细胞中t β rii介导的信号传导可能对早期胚胎肺分支不是必需的,但对出生后肺泡形成至关重要。
讨论
肺发育包括早期气道分支形态形成和晚期周围肺泡形成。任何一个过程的破坏都会导致肺结构和功能异常,如果早期肺形成受到严重影响,则会导致呼吸衰竭,如果发育中的肺发生轻微变化,则会导致晚年易患肺部疾病5.上皮-间充质相互作用在调节正常肺形成中起重要作用,可能通过细胞间直接接触,也可能通过改变生长因子分泌和细胞外基质蛋白沉积间接作用。TGF-βs是一组参与调节肺发育的重要生长因子。
TGF-β1、-β2、-β3均在小鼠胚胎肺中检测到29- - - - - -32.TGF-βs零突变可导致胎儿肺发育异常和/或出生后肺部过度炎症,表明TGF-β信号传导对正常肺形成和功能至关重要11- - - - - -14.相比之下,TGF-β1的过表达,由3.7 kb的人驱动程控转基因小鼠肺上皮启动子引起肺发育不全表型16提示在适当的时间和地点,适当水平的TGF-β信号对于正常的肺器官发生至关重要。然而,全器官TGF-β配体水平的改变可能通过改变自分泌和/或旁分泌信号通路来影响肺上皮细胞和间充质细胞TGF-β信号通路的活性,这两种通路难以区分。因此,为了研究内源性TGF-β信号在肺上皮中的调节功能与目前作者使用Cre/选择性地取消TGF-β细胞内信号传导活性loxP方法,通过在肺上皮或间质中特异性地删除TβRII功能蛋白的产生SPC-rtTA/TetO-Cre和Dermo1-Cre分别是驱动线。
有趣的是,仅在气道上皮细胞(Ep-CKO)中阻断内源性TβRII功能未能引起任何可检测到的产前小鼠肺形成的改变,特别是分支形态发生在活的有机体内.新生儿TβRIIEp-CKO小鼠在P1时呼吸正常,并显示出与对照小鼠相似的囊状组织。然而,继发性肺泡间隔形成严重滞后TβRIIEp-CKO小鼠对出生后小鼠肺泡形成的影响。肺泡形成是一个复杂的过程,肺泡上皮细胞(AECI和AECII)、毛细血管内皮细胞和肌成纤维细胞协同生长,细胞外基质沉积,特别是弹性蛋白沉积。这些细胞系的细胞增殖和分化有助于次级隔膜的形成,从而促进相关肺泡表面的形成,在终末空气空间和肺循环之间产生足够的气体交换膜。通过检测细胞周期特异性蛋白标记物PCNA和CDK2,发现细胞整体增殖TβRII肺上皮细胞中t β rii介导的TGF-β信号对于直接调节上皮细胞生长和/或间接影响内皮细胞或肌成纤维细胞至关重要。进一步缩小受影响的细胞系范围TβRII在不同类型的细胞中检测Ep-CKO肺细胞特异性标记物的表达模式。SMA染色结果显示,心肌成纤维细胞未见明显变化TβRIIEp-CKO小鼠肺。与此一致的是,弹性蛋白纤维在间隔细胞外间隙的沉积没有改变TβRIIEp-CKO肺。这些数据表明,在该小鼠模型中,由促进肌成纤维细胞生长的血小板衍生生长因子途径控制的肺泡生成不受取消上皮TGF-β信号活性的间接影响33.同样,在间隔结构的尖端检测到层粘连蛋白的正常沉积,层粘连蛋白是毛细血管网络的主要基膜成分,表明毛细血管内皮发育正常TβRIIEp-CKO老鼠。此外,在对照组和对照组中观察到类似的SPC阳性染色上皮细胞分布TβRII表明肺上皮细胞中TGF-β信号活性的缺乏不会破坏正常的spc阳性AECII和/或相关祖细胞分化。然而,AQP5阳性染色的AECI细胞明显减少TβRII提示在肺上皮细胞中,单独由t β rii介导的TGF-β信号传导可直接调控AECI的分化和扩增在活的有机体内.因此,AECI细胞群的减少可能导致继发性间隔生长和肺泡表面膜形成的减少。与现在一致在活的有机体内因此,Bhaskaranet al。34最近报道,在原代培养的大鼠肺上皮细胞中,通过添加TGF-β1中和抗体或使用RNA干扰沉默下游Smad4功能来消除内源性TGF-β信号传导可抑制AECI细胞分化。此外,先前有研究表明,常规敲除TβRII下游Smad3的小鼠也会出现肺泡形成迟缓23.总之,这些数据强烈表明,肺上皮细胞中TGF-β- smad3依赖的信号活性在促进AECI细胞分化和谱系扩增中起着关键的调节作用,特别是在肺泡形成过程中。
有趣的是,在常规Smad3基因敲除小鼠中,P28周围的异常肺泡形成后,预先形成的肺泡结构随之被破坏,导致中央小叶肺气肿样病理23.的常规零突变潜伏TGF-β结合蛋白4成熟的TGF-β肽分泌和激活所必需的,也会导致新生儿肺泡异常和成年小鼠肺气肿的发生35.然而,没有肺气肿样肺组织破坏观察到目前的肺上皮特异性TβRII条件性敲除,尽管肺泡发育迟缓持续到成年。这些数据提示TGF-β-Smad信号在肺上皮细胞中的活性本身TGF-β-Smad信号在其他肺细胞(包括肌成纤维细胞和/或炎症细胞(巨噬细胞和中性粒细胞))中的破坏是蛋白酶介导的组织破坏所必需的23.进一步剖析相关机制在活的有机体内将需要一个TβRIICKO在其他细胞系,如白细胞、巨噬细胞和/或肌成纤维细胞,与aTβRII肺上皮细胞突变。
以前的研究使用转基因和体外器官培养方法表明TGF-β信号在胚胎肺分支形态发生中起重要调节作用15,16.令人惊讶的是,当小鼠胚胎肺气道上皮细胞内源性TβRII功能被阻断时,肺分支形态发生正常在活的有机体内.相反,在中胚层来源的肺间充质细胞中,TβRII功能的缺失导致肺分支形态发生相对轻微的减少,仅在E14.5及以后检测到,而在妊娠早期没有检测到(E12.5)。这与免疫染色数据一致,免疫染色数据显示,TβRII在胚胎肺间质中的表达仅在妊娠中期开始检测到。与…相反SPC-rtTA/TetO-Cre驱动Cre在肺上皮中的表达;Dermo1-Cre表达不局限于肺间质组织。因此,用a代替TβRII函数Dermo1-Cre驱动鼠标行生成TβRIICKO累及多脏器,包括体壁、心脏和隔膜。因此,存在多个缺陷TβRIIMe-CKO小鼠很难确定肺表型的相关和特定机制。特别是膈疝样缺陷也可能直接导致胚胎期肺分支形态发生异常36,37.例如,在Fog2或Gata4功能缺失突变导致先天性膈疝发生之前,在缺乏Gata -1之友(Fog) 2-GATA结合蛋白(Gata)4相互作用的小鼠早期胚胎阶段也发现肺发育不全38,39.这表明肺发育不全可能是一种独立的发育缺陷,而不是由于腹部器官脱位导致胸内压力增加的继发后果通过膈疝。此外,由膈疝和胸腹壁缺损引起的肺部明显的物理畸形也可能间接影响E12.5术后肺的正常生长38,39.然而,由体外本研究证实,内源性TβRII仅在肺间质中发挥作用是正常肺分支所必需的。然而,TβRII通过交叉floxed生成的Me-CKO鼠标线TβRII和Dermo1-Cre由于这些多重混杂因素,小鼠可能不是进一步解剖间质TGF-β信号调节气道上皮分支机制的理想模型。
综上所述,由转化生长因子-β II型受体介导的转化生长因子-β信号在小鼠肺上皮发育中起着重要作用与间质。转化生长因子-β II型受体在胚胎期肺分支形态发生和出生后肺泡形成中起着重要的综合作用。因此,由转化生长因子-β信号通路成分的功能缺失突变导致的肺结构和功能发育不成熟,可能导致早期产后呼吸问题,如支气管肺发育不良。它还可能增加晚年对呼吸系统疾病的易感性,包括肺气肿。
支持声明
Shi W.获得了美国国立卫生研究院(NIH)的资助,资助号HL68597。D. Warburton获得NIH资助HL60231, HL44060, HL44977和HL75773,并得到Webb基金会(Los Angeles, CA, USA)的支持。
利益声明书
没有宣布。
致谢
作者要感谢D.M. Ornitz(华盛顿大学,圣路易斯,密苏里州,美国)提供的Dermo1-CreJ.A. Whitsett (Cincinnati Children Hospital Medical Center, Cincinnati, OH, USASPC-rtTA/TetO-Cre老鼠。他们还感谢X. Xu(南加州大学颅面分子生物学中心,洛杉矶,CA, USA)初步讨论TβRII条件剔除,和P. Minoo(凯克医学院,南加州大学)对手稿的批判性阅读。
- 收到了2007年12月6日。
- 接受2008年2月21日。
- ©ERS期刊有限公司