文摘
人工气道上皮,防御保护呼吸道的最前沿,抢救吸入粒子永久上皮细胞纤毛的跳动。不足时,这种细胞器导致原发性纤毛运动障碍,而且,尽管许多研究,但关于纤毛细胞基因表达数据仍不完整。本研究的目的是确定在人类的纤毛呼吸道细胞特异表达基因通过转录分析。
肉瘤上皮细胞的转录组是减去从完全redifferentiated细胞使用互补DNA代表性差异分析。为了验证结果,证实了基因超表达在纤毛细胞实时聚合酶链反应,并通过比较目前的纤毛细胞的基因过表达列表列出获得的先前的研究。
共有53个已知和12个未知基因过表达在纤毛细胞识别。绝大多数(66%)的已知基因以前从未被报道参与ciliogenesis,和未知的基因表示假设的小说文本亚型或新基因没有报告数据库。最后,多个基因识别是位于基因组区域参与通过连锁分析原发性纤毛运动障碍。
总之,目前的研究显示新cilia-related基因序列,新的成绩单亚型和小说基因应该进一步特征帮助了解他们的功能(s)和可能disorder-related参与。
气道上皮pseudo-stratified层,组成专门的细胞类型,包括基底细胞、杯状/分泌细胞和纤毛柱状细胞。也发挥着关键作用在气道防御保护呼吸道的感染和损伤引起吸入毒素、病原体和粒子。它对环境侵略构成物理障碍,通过分泌因素调节宿主的免疫系统,通过黏膜纤毛的清除。对呼吸道细胞,纤毛击败缺陷引起的疾病称为原发性纤毛运动障碍(PCD)。纤毛毛发状细胞器可以存在呼吸道细胞和许多其他的人类细胞。纤毛所有类型的展览许多相似之处,但他们不同取决于他们的能动性或感官功能。对呼吸道上皮细胞导致日益增加的兴趣研究人员阐明基因ciliogenesis行事。
蛋白质组学分析被用来识别组件位于我或中心粒人类纤毛或鞭毛在其他知名的生物1- - - - - -5。比较基因组搜索导致基因组的基因检测守恒的纤毛的生物与nonciliated生物6,7。为了揭示在鞭毛再生或ciliogenesis特异表达基因,几项研究已经进行了使用各种转录的策略8- - - - - -12。
基因突变在几个揭示了这些研究结果导致不同的人类纤毛疾病,如多囊肾疾病、视网膜营养不良,感觉神经的损伤,Bardet-Biedl综合症,oral-facial-digital综合征1型和纤毛运动,证明这些基因应该考虑在破译ciliopathies的病因学13。
使用不同的方法,发现在人类的纤毛呼吸道细胞特异表达基因,可以负责人类疾病,一个方法称为代表性差异分析(RDA)使用。这种方法,首先由Lisitsyn描述et al。14代表一个减法的过程耦合放大,最初应用于检测两个基因组之间的区别。随后,Hubank和进步15适应RDA使用互补DNA(互补)为了隔离在两个细胞群基因表达差异。
在目前的研究中,连续的文化系统所描述的Jorissen说道et al。16,上皮细胞覆盖在鼻腔的鼻甲骨dediffentiated在平坦nonciliated细胞然后redifferentiated纤毛细胞,利用。平nonciliated细胞的转录组的减去re-ciliated细胞为了描述记录特定于纤毛细胞。差异表达基因克隆和测序,从而识别善意的并预测基因。此外,基因组片段,躺在被克隆基因间的间隔,建议新假定的基因的存在。增加一些已知和预测基因的表达在ciliogenesis证实了实时PCR验证研究。
材料和方法
细胞培养
人类呼吸道细胞从正常受试者从鼻鼻甲骨,删除和丢弃,从而提供筛骨的窦(耳朵鼻子和喉咙服务,Croix-Rousse医院,里昂,法国)。患者的肿瘤位于筛骨的地区并没有显示出呼吸道疾病。使用非细胞培养细胞生长的方法描述Jorissen说道et al。16。短暂,纤毛细胞被孤立链霉蛋白酶消化和扩大collagen-coated 25厘米2烧瓶在nonciliated细胞去分化37°C下5%的股份有限公司2。融合时达到80 - 90%,胶原蛋白是消化和细胞悬浮在烧瓶与旋转(80转·分钟−1)37°C到redifferentiate纤毛囊泡的形式。Nonciliated收集细胞融合在80 - 90%,当他们停止增殖,囊泡时收集完全由纤毛。
隔离mRNA和互补DNA合成
从nonciliated和纤毛细胞RNA提取使用提取所有®(Eurobio、Courtaboeuf、法国),遵循制造商的指示。保利(A)+总RNA信使RNA是分开使用Dynabeads益生元(dT)25净化设备(Dynal生物技术,奥斯陆,挪威)及其质量评估在琼脂糖凝胶。互补脱氧核糖核酸合成从2.85μg保利(A) mRNA oligo-deoxythymidine (dT)启动使用上标二世逆转录酶作为推荐的制造商(美国纽约表达载体,大岛)。双链cDNA准备在一个80 -μL总量,包含20μL cDNA模板,400μM脱氧核苷三磷酸腺苷,5 U DNA连接酶(美国新英格兰生物学实验室,伊普斯维奇,MA), 24 U DNA聚合酶(表达载体)和1 U(表达载体)的前体。2 h反应进行的16°C,然后辅以6 U T4 DNA聚合酶(表达载体)额外的30分钟孵化。
没有基因组DNA污染使用α-tubulin引物PCR证实了,可以放大320 - bp cDNA片段或468 - bp基因组DNA片段(协议可以在请求)。
一代的不同产品
互补脱氧核糖核酸RDA的基础上执行Hubank和宝贝描述的协议15用细微的修改。双链cDNA(2μg)从两个细胞群被消化Dpn二世(新英格兰生物学实验室)生成检测器(纤毛细胞)和驱动程序(nonciliated细胞)cDNA表示。为了促进消化表示的净化,一对引物组是使用链霉亲和素生物素化的和删除m - 280工具包(Dynal生物技术),遵循制造商的建议。第一个减法杂交测试仪:司机cDNA比例为1:50。在第二和第三轮减法杂交,比增加到1:50 0和1:250,000,绿豆核酸酶消化PCR产品(详细协议可用请求)中被省略了。
克隆和DNA测序
第三轮PCR的产品消化Dpn二,为了方便识别,乐队200年、300年、400年和600年英国石油公司分别使用QIAquick gel-purified凝胶萃取设备(试剂盒,日耳曼敦,医学博士,美国)。净化产品是猎枪克隆到一个BamHI-digested脱去磷酸pBlueScript®II KS +矢量(美国Stratagene,圣地亚哥,CA)和用于将DH5α主管细胞(表达载体),根据制造商的协议。细菌在Luria-Bertani镀介质/氨苄青霉素盘子和殖民地为插入的筛选囊二世和Xho我双消化,传统的质粒提取。
克隆产品使用M13-20引物测序。使用质粒测序反应成立asa模板和大染料®终结者v1.1循环测序工具包(美国应用生物系统公司,培育城市,CA)后,制造商的指示。序列分析进行自动化ABI 3100测序仪(应用生物系统公司),并使用Staden序列对齐1.7.0 Staden Windows的包17在提取底漆和向量序列。
实时聚合酶链反应
Nonciliated收集和纤毛细胞,离心去除细胞培养基和洗PBS (pH值7.4)。细胞颗粒存储在-80°C到处理。纯化使用Chemagic信使rna信使rna制备直接工具包(Chemagen Baesweiler,德国)遵循制造商的建议。DNA污染被DNase我治疗(表达载体),和mRNA量化使用nd - 1000 spectrophometer(美国NanoDrop威尔明顿·德·)。信使rna(10μg)是反向转录产生cDNA使用Transcriptor第一链cDNA合成装备(罗氏应用科学,Rotkreuz,瑞士)和锚定低聚糖(dT)18根据制造商的建议。
LightCycler系统中进行实时PCR®使用由于“快速上手”项目DNA主人SYBR绿色我工具包(罗氏应用科学)。参考和目标基因引物获得QuantiTect底漆化验(试剂盒),它包含验证引物组减少glyceraldehyde-3-phosphate脱氢酶(GAPDH),axonemal动力蛋白中间链1 (DNAI1)、糖蛋白nmb (GPNMB)、色素性视网膜炎GTPase调节器(RPGR49),染色体7开放阅读框(C7orf4914号染色体)和166年开放阅读框(C14orf166)基因。PCR反应是建立在一个总量的20μL,包含2μL SYBR绿色由于“快速上手”项目反应混合,2.4毫米MgCl2、2μL 10×2μL cDNA引物组合。温度循环概要如下:95°C 10分钟,40周期在95°C的变性10年代,退火在55°C 10 s,和扩展20年代在72°C。融化曲线进行分析的范围65 - 95°C到确认的特异性PCR产品。
基因表达水平与比较阈值确定方法,使用管家基因的水平GAPDH作为一个参考价值21。的阈值的PCR循环放大产品首次检测到实时PCR (Ct)决定。为每个决心纠正Ct(ΔCt)被用来计算相对n次微分纤毛细胞中的一个特定基因的表达而nonciliated细胞样本,并表示2的比率-ΔCt值。
统计分析
一式三份实验数据均值±sd。为每个目标基因,2-ΔCt值的纤毛和nonciliated细胞分析使用一个未配对t检验的意义的假定值< 0.05为单侧检验。
结果
本研究的目的是确定在人类的纤毛呼吸道细胞特异表达基因。为此,肉瘤上皮细胞的转录组是减去从完全redifferentiated细胞。本研究中使用的RDA的互补过程密切基于Hubank和宝贝描述的协议15的浓缩,它允许记录具体表达细胞类型通过迭代周期放大/减法。
确定差异表达基因
的细菌克隆,25%含有插入。所有克隆与插入排序(n = 78),包括四个嵌合克隆,每个包含两个cDNA片段。总之,82个人cDNA片段被确定。四个cDNA片段多次被找到,并对应于以下基因:GPNMB(九个克隆),锌指蛋白236 (ZNF236;六个克隆)、大型P0核糖体蛋白(RPLP0;四个克隆)和核糖体蛋白L14 (RPL14;两个克隆)。最后,65独特的cDNA片段被识别并映射到由BLASTN人类基因组序列。其中,53例(82%)cDNA片段映射到其实已知的基因,7例(11%)intronic区域或边界intron-exon结和五个(7%)的基因间区域。
的53 cDNA片段列表对应的其实地区是表1中给出⇓。基因是集群的描述函数。值得注意的是,九个核糖体蛋白质和一个启动因子参与翻译被确定。基因与免疫有关,炎症和国防也被检测到。线粒体集群包括七个基因编码线粒体组件。其中,六核基因和线粒体(线粒体编码细胞色素b基因(MT-CYB))。组件的频道,转运蛋白相关蛋白在一组上市,其中包括两种溶质载体家族基因。细胞信号和信号转导的基因,如编码精子发生相关13 (SPATA13)和睾丸增强基因转录(TEGT;伯灵顿抑制剂1)。几种细胞骨架基因,如肌动蛋白γ1 (ACTG1)、角蛋白和原肌球蛋白基因被证明。尽管纤毛细胞不复制,几个细胞增殖基因被发现,包括2 non-metastatic细胞、蛋白质(NM23B)基因表达(NME2)。表1中剩余的基因⇓,只有一个,beta-tubulin基因(TUBB),已证明与纤毛。最后,两个基因对应预测开放阅读框,C7orf49和C14orf166。
的cDNA片段与内含子序列校准报告在表2⇓。这些互补脱氧核糖核酸片段可能代表新的mRNA亚型。只有cDNA片段映射间6基因(XPO6)包括intronic和的其实。其他6个片段来自intronic地区。一个片段映射到基因组区域的两个基因在相反的方向上重叠(家庭序列相似性82 (FAM82B)和copine III (CPNE3))。因为目前克隆策略不是面向,尚不清楚这是否片段是来自一个或另一个基因。
五个cDNA片段映射到基因间区域展示在表3⇓。前两个cDNA片段(A和B)可以代表一个新的5’或3 '外显子因为距离最近的基因是最多16 kb。相比之下,最后两个cDNA片段(D和E)是如此孤立(75 kb的最小距离最近的基因),他们只能是新基因的片段。
实时PCR验证研究
首先,为了验证目前的文化系统,表达DNAI1和RPGR,两个基因的过表达在纤毛细胞,进行了分析。DNAI1编码一个组件的外部动力蛋白臂纤毛我和纤毛功能是至关重要的,而RPGR特别表现在组织包含细胞纤毛或cilia-like细胞器,如视网膜、肺癌、耳蜗上皮细胞衬支气管和鼻窦呢22。进行数据分析,相对量化目标基因的转录本进行对每个样本,与正常化GAPDH表达式,因为它是一个内生的不受监管的基因转录。通过实时PCR,发现这两个基因表现出3696 - 83倍相对增加,分别为(表4所示⇓)。
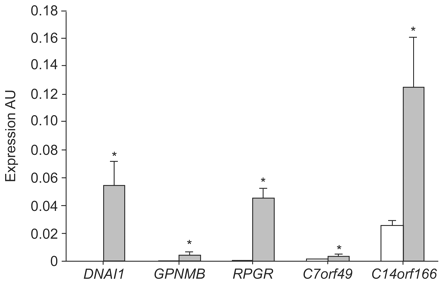
其次,为了验证基因的列表,一个基因的表达(GPNMB)和两个开放阅读框架,即C7orf49和C14orf166进行评估,实时PCR nonciliated和纤毛细胞。所选择的三个基因表现出纤毛细胞的表达明显高于nonciliated细胞(图。1⇓)。GPNMB显示一个相对增长了7.89倍,符合3.01 - -12.17倍改变报告的罗斯et al。12。C7orf49和C14orf166显示增加表达在人类呼吸道纤毛细胞,分别为2.94和4.92倍的相对变化,(表4所示⇑)。
验证表达式的数据的识别人类的纤毛细胞的基因:表达nonciliated(□),和纤毛细胞(▓)。数据意味着±扫描电镜。盟:任意单位;DNAI1中间链:axonemal动力蛋白1基因;GPNMB:糖蛋白nmb基因;RPGR:色素性视网膜炎GTPase调节基因;C7orf49:7号染色体基因开放阅读框49;C14orf166166:14号染色体开放阅读框。*:p < 0.05与nonciliated细胞。
与其他研究相比纤毛
为了确认目前的数据,获得的基因列表是相对于其他列表通过纤毛细胞的各种方法各种生物(表5所示⇓)。十的53基因显示增加合成记录在本研究报告曾经在其他的研究中:膜联蛋白A1 (ANXA1);真核翻译起始因子1 (EIF1);GPNMB;nebulette (NEBL);NME2;RPL14;secretoglobin家庭成员1 (uteroglobin) (SCGB1A1);SPATA13;胸腺素β4 x连锁(TMSB4X);和泛素52残渣核糖体蛋白融合产品1 (UBA52)1,3,11,12。两个额外的基因的研究中提到奥斯托夫斯基et al。1和Pazouret al。3:核糖体蛋白SA (RPSA);和ACTG1。TUBB也发现两次4,8。最后,computer-predicted基因,称为C14orf166提到的三倍6- - - - - -8。
同意Pazour的研究et al。31,发现吸收FK506结合蛋白,12 kda基因(FKBP1A在ciliogenesis)的表达就会增加3。相比之下,罗斯et al。12指出这种基因的表达(-2.33倍)下降。三个基因显示增加表达式在目前的研究显示ciliogenesis逆转模式研究的罗斯et al。12:serpin肽酶抑制剂,支系B(卵白蛋白),成员2 (SERPINB2;-2.82倍),原肌球蛋白1 (TPM1;-3.31/-3.73倍)和TPM3(-3.49/-3.21倍)12。
因果基因的识别在PCD和内脏逆位的定位克隆是困难的,因为潜在的许多基因参与了这些疾病。因此,重要的是要注意,22个基因从目前系列地图染色体区域可能包含一个因果基因的定位克隆方法23- - - - - -26。这些22基因展示在表6所示⇓。一半的以前从未报道研究旨在描述组件特定的纤毛/鞭毛。其中22个基因,四个位于染色体区域表现出明确的链接在家族纤毛:趋化因子(科学家)配体17 (CXCL17),硫化醌reductase-like(酵母)(SQRDL),溶质载体家庭6(氨基酸转运蛋白),14个基因和成员TMSB4X24- - - - - -26。
讨论
在目前的研究中,RDA是用来识别差异表达基因在人类纤毛细胞呼吸。减法nonciliated细胞表现的纤毛细胞导致53基因的检测和12个新编码序列已知的基因(n = 7)或公认的新基因(n = 5)。这65 cDNA片段是真正在纤毛细胞的一个子集三互补测试使用实时PCR分析,所有三个表示在更高水平上比nonciliated纤毛细胞。此外,18岁的53个互补已经在其他研究报告旨在破译成绩单或蛋白质特定于纤毛细胞。剩下的35的互补新发现基因过表达在纤毛细胞。在序列中,22个是位于位点与已知的纤毛结构缺陷和疾病有关。
RDA是一个漫长而又艰难的设置方法,但被认为是提供没有假阳性。符合这一观点,所有的互补dna测试的实时PCR过度证实,15的互补的研究以前在其他的研究报道是在纤毛细胞。这种方法的一个局限是选择短cDNA片段,这意味着没有希望获得所有的完整列表中记录。虽然微阵列提供了一个系统化的观点表达和记录只能检测预选的序列,RDA有能力探测到额外的表达序列为小说记录已知基因或即使新基因的变异。
表1中⇑,一组基因可能与细胞纤毛/鞭毛报道。事实上,七个基因编码蛋白质的线粒体呼吸链和氧化磷酸化系统被确定。纤毛细胞,增加细胞内ATP生产可能是必要的,intraflagellar运输和纤毛跳动。突变ACTG1,耳蜗的感觉纤毛细胞的重要组成部分,已被描述为引起主导耳聋27。最后,NME2被证明参与精子形成和鞭毛运动吗28,TMSB4X被发现高度代表组织类型无关的肺实质和相对于支气管上皮在先前的研究11。
实时PCR分析,两个积极的控制,曾被描述为显示纤毛组织中表达增加,DNAI1和RPGR使用。其他两个基因,GPNMB和C14orf166已报告,在其他的研究中,显示纤毛细胞中表达增加,但它们的功能在ciliogenesis还有待阐明。GPNMB,一个跨膜糖蛋白,参与增长提出推迟和减少转移的潜力29日在ciliogenesis仍然是难以捉摸的,但它的作用。的C14orf166和C7orf49基因的人类基因组生物信息学预测的搜索。C14orf166经常被发现在ciliogenesis因为它已经被其他三个研究报道。这个基因编码的蛋白质参与的功能调节人类ninein中心体结构6- - - - - -8,30.。这将是有趣的获取完整的数据C14orf166并阐明的生物功能C7orf49。
最后,五个全新的基因(∼成套的10%)被检测到。进一步工作的详细描述这些公认的新基因,特别是序列B,位于染色体区域涉及内脏逆位,lateralisation的扰动可以二次纤毛功能障碍的早期胚胎。
支持声明
b . Chhin支持法国协会的奖学金对肌肉疾病(埃夫里市、法国)在2004年和2007年之间。Cardiogenetics实验室(济贫院土木里昂,里昂,法国)支持由科学利益集团——2003年罕见疾病临床研究区域2003年和医院项目(法国巴黎)的实验室Cardiogenetics(里昂大学1,法国里昂)由ProKartagener基金会2005年(瑞士日内瓦)和Renaud Febvre基金会(Les埃塔、法国)。
感兴趣的语句
没有宣布。
确认
作者热情地感谢美国皮科的贡献寄生虫学实验室(里昂大学1,法国里昂)的实时PCR实验。
- 收到了2007年12月19日。
- 接受2008年2月8日。
- ©人期刊有限公司