文摘
嗜肺性军团菌引起社区获得性肺炎死亡率高,但对其与肺泡上皮的交互。本研究的目的是调查是否退伍军人感染的肺上皮细胞(A549)导致促炎症激活。
退伍军人感染诱导解放白介素(IL) 2, 4, 6, 8, -17,单核细胞化学引诱物蛋白1,肿瘤坏死factor-α,IL-1β,interferon-γ和粒细胞集落刺激因子,但不是IL-5、7、-10、-12 (p70)或-13或集落刺激因子。目前的研究集中在引发,发现感应退伍军人菌株130 b,费城1,寇比,在较小程度上,JR32。基因敲除的队伍,一个中央基因参与类型IVB分泌司长委任,不改变引发的感应,而缺乏鞭毛蛋白显著减少引发军团菌释放。此外,p38增殖蛋白激酶(MAPK)活性和激酶抑制诱导细胞因子的分泌减少,除了2和粒细胞集落刺激因子。相比之下,抑制MAPK激酶1 /细胞外signal-regulated激酶途径只有减少一些细胞因子的表达。退伍军人也诱导核factor-κB绑定单元RelA / p65和RNA聚合酶IIil8启动子和一个特定抑制剂核factor-κB复杂的抑制剂剂量依赖性降低引发表达式。
综上所述,嗜肺性军团菌p38增殖激活蛋白激酶和核factor-κB / RelA pathway-dependent表达式的复杂模式人类肺泡上皮细胞的细胞因子,可能导致军团病的免疫反应。
重症社区获得性肺炎的重要病原体,嗜肺性军团菌是第二个最常见的病原体检测肺炎承认在工业化国家重症监护病房吗1。大约有15%的军团病出现在社区暴发。虽然> 40军团菌属物种是已知的,大多数的人类感染所致退伍军人血清组12。退伍军人是一种革兰氏阴性兼性胞内病原体变形虫的自然和人为水生环境。人类感染后发生气溶胶飞沫吸入被污染的水。退伍军人包含时间最初不与溶酶体融合和细菌引起的膜结合室改造成内质reticulum-like细胞器3。这改造取决于细胞器贩卖的缺陷(点)/胞内增殖(Icm)类型IVB分泌司长委任装置退伍军人4。除了交付的蛋白质类型IVB分泌系统,司长委任退伍军人电池包含一个额外的毒性因子,包括II型分泌器官3。测序的退伍军人血清组1基因组显示∼3000个基因,其中许多基因有可能操纵宿主细胞信号的功能5。
根据Legionella-host交互,但最近的研究证明退伍军人脂多糖是认可toll样受体(TLR) 2, TLR5鞭毛蛋白6,7。一个终止密码子在人类TLR5基因导致对军团病的易感性增加7。有趣的是,尽管一些研究表明TLR4在军团病的次要角色6中,霍恩et al。8最近表明TLR4多态性与抗军团病有关。
基本显示结果退伍军人发病机制是通过分析获得的原生动物感染或免疫细胞如巨噬细胞。然而,肺上皮细胞构成第一机械和免疫屏障对机载病原体和肺细胞因子的重要来源9,10。促炎症信号通路的激活肺上皮细胞,包括p38增殖蛋白激酶(MAPK)和核factor-κB (NF-κB)端依赖基因转录,细菌感染,对细胞因子释放作出了重大贡献10,11。尽管有效军团菌感染和刺激肺上皮细胞7,12的机制退伍军人全身的活化和细胞因子释放的肺上皮细胞被广泛知晓。因此,肺上皮细胞的促炎症激活军团菌感染详细分析。
在目前的研究中,结果表明,退伍军人诱导释放几个重要的细胞因子在人类肺泡上皮细胞A549细胞,如。白介素(IL) 2, 4, 6, 8, -17,单核细胞化学引诱物蛋白(MCP) 1、肿瘤坏死因子(TNF) -αIL-1β,干扰素(IFN) -γ和粒细胞集落刺激因子(g - csf),以及激活p38 MAPK、细胞外signal-regulated激酶(ERK)和NF-κB通路。阻塞p38 MAPK Legionella-infected细胞分泌的细胞因子减少,除了和g - csf - 2,而阻断ERK通路减少只释放IFN-γIL-1β、il - 6和TNF-α。通过处理引发的表达详细模型细胞因子,p38 MAPK的重要作用——和NF-κB / RelA-dependent基因转录的激活退伍军人来华的上皮细胞被证实。此外,激活引发表达降低了鞭毛蛋白缺失突变,暗示TLR5的作用或可能的军团菌胞内受体感应A549细胞。然而,引发表达式在A549细胞没有影响队伍敲除突变体,这表明IVB点/ Icm司长委任型分泌系统和细胞内复制不需要引发在A549细胞表达。
材料和方法
细胞系
肺泡上皮细胞系A549从美国购买类型文化收集(写明ATCC;美国马里兰州罗克维尔市)和火腿的F-12培养基培养l谷氨酰胺和10%胎牛血清(生活技术,卡尔斯鲁厄,德国)没有抗生素。NF-κB-dependent记者细胞系A549 6 btkluc,是一种礼物的r·牛顿(生物科学部门,华威大学、考文垂、英国)。这些细胞包含一个稳定整合质粒和三个串联重复序列的5‘-AGCTTACAAGGGACTTTCCGCTGGGGACTTTCCAGGGA-3’,它包含的两个副本decameric NF-κB结合位点上游的最小胸苷激酶发起人(105 - 51)驾驶荧光素酶基因。
感染菌株和同基因的突变体
退伍军人干系人菌株130 b(写明ATCC baa - 74,请提供N.P. Cianciotto,西北大学医学院、芝加哥,美国13),费城1(写明ATCC 33152,请提供b . Neumeister图宾根大学、图宾根,德国14),JR32野生型15和JR32队伍突变(莱拉·3118,请提供h . Shuman,哥伦比亚大学,纽约,纽约,美国16),寇比野生型和寇比flaA,鞭毛蛋白缺陷突变体(请提供的k .修维尔茨堡大学维尔茨堡,德国)经常生长在缓冲charcoal-yeast提取(BCYE)琼脂2 - 3天在37°C17,随后接种到平原RPMI介质的光学密度在0.2 - -0.4的660海里。A549细胞(1×105细胞·毫升1)感染1×1051×108菌落(cfu)·毫升1退伍军人,即。在感染复数1:1-1:1,000,1毫升上皮细胞生长介质的表示。细胞外并不经常使用抗生素杀死细菌。退伍军人上皮细胞培养基上菌株没有显著增长,作为控制的串行BCYE琼脂稀释镀。
为了验证细胞内感染,A549细胞添加细菌孵育2 h有或没有激酶抑制剂,庆大霉素(100μg·毫升1)为进一步增加了2 h,然后细胞与普通介质洗了三次,除去游离细菌,治疗10%(重量/体积)皂苷(σ化学公司,德国慕尼黑)溶解的宿主细胞。连续稀释镀在BCYE琼脂。
Interleukin-8 ELISA
汇合的A549细胞被感染为15 h表示在湿润的气氛中。孵化后,上层的收集和加工为IL-8-quantification夹心ELISA,如前所述11,18。在一些实验中,改变了媒介在某些时间段(1、2或4小时)有或没有庆大霉素(100μg·毫升1),然后剩下的细胞被孵化时间在同一介质之前引发上层清液进行了分析。
Bioplex蛋白质阵列系统
汇合的A549细胞被感染为15 h表示在湿润的气氛中。孵化后,收集上清液和细胞因子释放分析使用Bioplex蛋白质阵列系统(BioRad、大力神、钙、美国)和珠子具体为- 2,4,5,6,7,8,-10年,-12年(p70), -13年和-17年,MCP-1, TNF-α,IL-1β,IFN-γ,集落刺激因子(gm - csf)和g - csf,根据制造商的指示19,20.。
西方墨点法
测定p38 MAPK和ERK的磷酸化,A549细胞被感染表示,洗两次,收获。细胞细胞溶解在缓冲Triton x - 100(σ化学公司),受到dodecylsulphate-polyacrylamide钠凝胶电泳和涂抹Hybond ECL膜(Amersham生物科学,弗莱堡,德国)。Immunodetection磷酸化MAPK的使用phospho-specific p38 MAPK和ERK抗体(细胞信号,法兰克福,德国)11。退化的抑制剂NF-κB (IκBα)分析了使用兔多克隆抗体(美国圣克鲁斯生物技术,圣克鲁斯,CA)如前所述11。在所有的实验中,磷酸化ERK2和p38 MAPK(圣克鲁斯生物技术)检测同时为了证实蛋白质负载相等。蛋白质被孵化的视觉与二级IRDye 800 -或Cy5.5-labelled抗体,分别(奥德赛红外成像系统;LI-COR Inc .,糟糕的小礼帽,德国)11,21。所有主要使用了抗体的稀释1:200和所有二级抗体的稀释下。
rt - pcr
分析引发和减少glyceraldehye-3-phosphate脱氢酶(GAPDH)基因表达在A549细胞总RNA分离通过RNEasy迷你包(试剂盒、希尔登,德国)和反向转录使用禽成髓细胞瘤病毒逆转录酶(Promega,海德堡,德国)。生成的互补DNA PCR扩大了使用特定intron-spanning引发和GAPDH引物11。引物都是购自TIB MOLBIOL(德国柏林)。35岁后放大周期,PCR产品1.5%琼脂糖凝胶上进行分析,用溴化乙锭染色的,随后形象化。为了确认使用等量的RNA在每个实验中,所有样本检查GAPDH mRNA的表达。
报告基因分析
A549细胞稳定转染NF-κB-dependent荧光素酶报告质粒22培养在12-well板块在杜尔贝科修改鹰介质(技术)。军团菌细胞孵育15 h和细胞溶解,然后用荧光素酶报告基因检测荧光素酶活性测定(Promega,曼海姆,德国)。
染色质免疫沉淀反应
A549细胞75厘米2培养瓶被感染退伍军人130 b表示受到一个染色质免疫沉淀反应试验,如前所述,使用anti-p65或anti-RNA聚合酶II抗体(圣克鲁斯生物技术)11,20.。的il8子被PCR放大使用HotstarTaq聚合酶(试剂盒)和特定的引物如下:5“-AAGAAAACTTTCGTCATACTCCG-3”(意义);和5“-TGGCTTTTTATATCATCACCCTAC-3”(反义)。总输入的PCR扩增DNA在每个样本进行控制18,19。
统计方法
数据意味着±扫描电镜至少有三个独立的实验。单向方差分析用于数字数据的数据所示。主要影响是使用Newman-Keuls测试后进行比较。的假定值< 0.01被认为是显著的。
结果
细胞因子释放
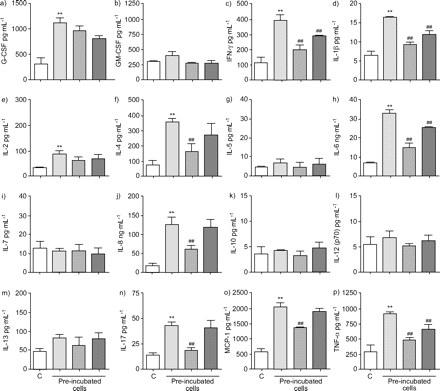
为了描述人类肺泡上皮细胞的炎症激活退伍军人1×105A549细胞被感染退伍军人菌株130 b 1×10的感染剂量7cfu·毫升1,即。1:10 0的感染复数。细胞因子释放使用Bioplex试验进行了分析。孵化15 h后,重要的感应- 2,4,6,8,-17,MCP-1, TNF-α,IL-1β,IFN-γ和g - csf,但不是IL-5、7、-10、-12 (p70)或-13或观察gm - csf(无花果。1⇓)。Pre-incubation A549细胞的特定p38 MAPK抑制剂SB202190 (Calbiochem-Merck,达姆施塔特,德国)减少水平的il - 4, 6, 8, -17, MCP-1, TNF-α,IL-1βIFN-γ,但不是2或g - csf (TNF-α来自于研发系统、威斯巴登、德国)。抑制MAPK激酶1 (MEK1) U0126减少释放只有IFN-γIL-1β、il - 6和TNF-α(图1所示⇓)。孵化与抑制剂单独显示没有细胞毒性,不改变细胞因子表达或感染上皮细胞(数据没有显示)。
嗜肺性军团菌全身的细胞因子的释放模式主要依赖p38增殖蛋白激酶(MAPK)活动:a)粒细胞集落刺激因子(g - csf);b)集落刺激因子(gm - csf);c)干扰素(IFN) -γ;d)白介素(IL) 1β;e) - 2;f) il - 4;g) IL-5;h) il - 6;我)IL-7;j)引发; k) IL-10; l) IL-12 (p70); m) IL-13; n) IL-17; o) monocyte chemoattractant protein (MCP)-1; and p) tumour necrosis factor (TNF)-α. A549 cells (1×105细胞·毫升1独自)pre-incubated(30分钟),中等(░),5μM SB202190 (p38 MAPK抑制剂;▓)或U0126 (MAPK激酶1抑制剂;▒)和感染退伍军人130 b (1×107菌落·毫升1;未受感染的控制(C;□))。上层清液中细胞因子释放被Bioplex试验测量。数据意味着±扫描电镜。* *:p < 0.01与C;# #:p < 0.01与感染细胞没有pre-incubation与抑制剂(至少在三个独立的实验)。
鞭毛蛋白,队伍依赖interleukin-8表达
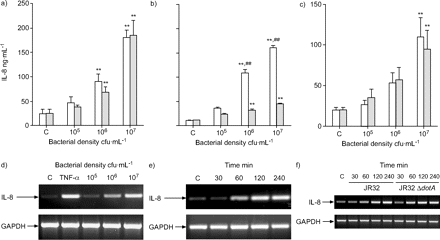
肺泡上皮细胞激活详细分析了解决引发重要的趋化细胞因子的表达。不同浓度的A549细胞被感染退伍军人菌株130 b,费城1、JR32和寇比15 h(图。2⇓)。退伍军人130 b、费城1和寇比同样诱导引发释放存在剂量依赖的相关性(图2⇓和b),而JR32-provoked细胞因子分泌较低(图2摄氏度⇓)。退伍军人130 b也诱导剂量——(图2 d⇓)和时间(图2 e⇓)引发mRNA的表达。基因表达开始早在60分钟后感染。一个flaA敲除突变体,鞭毛蛋白生产的缺陷,导致强烈引发释放减少了退伍军人Corby-infected A549细胞超过15 h(图2 b⇓)。相比之下,一个队伍敲除突变体,有缺陷的基因建立功能所必需的退伍军人IVB分泌司长委任型装置3,不改变引发释放退伍军人JR32-infected A549细胞超过15 h(图2摄氏度⇓)或时间引发的信使rna诱导4 h(图2 f⇓)。
诱导flagellin-dependent队伍独立白介素8 (IL)肺泡上皮细胞的表达不同嗜肺性军团菌菌株。A549细胞(1×105细胞·毫升1)感染退伍军人:1)130 b(□)和费城1 (░);寇比野生型(□)和Δb)flaA敲除突变体(░);c) JR32野生型(□)和Δ队伍敲除突变体(░);130 b d, e);和f) JR32野生型和Δ队伍敲除突变体。两者引发释放到上清液治疗后显示细菌密度后,ELISA测定15 h。数据意味着±扫描电镜。d-f)引发和减少glyceraldehye-3-phosphate脱氢酶(GAPDH) mRNA表达rt - pcr测定:d) 4 h后感染浓度表示退伍军人或孵化后4 h和100 ng·毫升1肿瘤坏死factor-α(TNF-α);和e, f)在指定时间点后感染1×107菌落(cfu)·毫升1退伍军人(代表凝胶3所示)。* *:p < 0.01与未受感染的控制(C);# #:p < 0.01与费城1或突变。
Interleukin-8 p38增殖释放依赖蛋白激酶激活
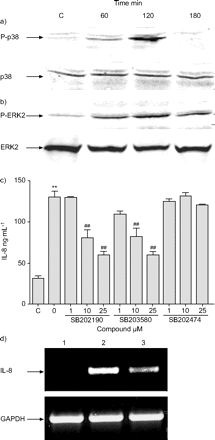
接下来,退伍军人全身的激活增殖激酶途径进行了分析。A549细胞被感染退伍军人130 b和p38 MAPK的磷酸化(图3⇓)和ERK2(图3 b⇓)是通过免疫印迹分析评估。退伍军人感染诱导磷酸化的激酶在60 - 120分钟。阻塞p38 MAPK和SB202190减少引发mRNA积累(图3 d⇓)。此外,p38 MAPK抑制剂SB202190和SB203580 (Calbiochem-Merck)存在剂量依赖的相关性降低退伍军人全身引发释放(图3 c⇓)。控制复合SB202474 (Calbiochem-Merck)没有对细胞因子释放的影响(图3 c⇓)。抑制剂和控制复合细胞数量减少或诱导形态细胞毒性的迹象。
嗜肺性军团菌,诱导白介素8 (IL)释放依赖p38增殖蛋白激酶(MAPK)激活肺泡上皮细胞。A549细胞(1×105细胞·毫升1)感染退伍军人130 b (1×107克隆形成单位·毫升1)。磷酸化(P)) p38 MAPK和b)的细胞外signal-regulated激酶(ERK) 2在指定的时间点测定免疫印迹分析(代表墨迹图3所示)。c, d) A549细胞pre-incubated(30分钟)和10μM SB202190 (c和d), SB203580 (c)和SB202474 (c)和感染退伍军人130 b。c)引发释放后上层清液用ELISA 15 h。数据意味着±扫描电镜。d)引发信使rna被rt - pcr检测4 h(后巷1:未感染的控制(C);巷2:单独细胞pre-incubated介质;巷3:pre-incubated细胞)。GAPDH:减少glyceraldehye-3-phosphate脱氢酶。* *:p < 0.01与C;# #:p < 0.01与感染细胞不pre-incubated抑制剂(至少在三个独立的实验)。
Interleukin-8释放依赖核factor-κB激活
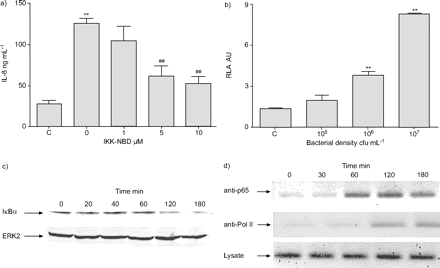
引发启动子的激活被认为是需要激活的转录因子NF-κB。IκBα激酶复杂被使用特定的肽抑制剂,IκB激酶NF-κB基本modulator-binding域(IKK-NBD;Biomol,普利茅斯会议上,PA,美国),剂量依赖性降低引发分泌退伍军人130年b-infected A549细胞观察(图4⇓)。在A549细胞,转染NF-κB-dependent报告基因构造,感应的报告基因表达存在剂量依赖的相关性被发现(图4 b⇓)。IKK-NBD显示没有细胞毒性,不改变A549的感染军团菌菌株130 b或基底细胞因子表达式(数据没有显示)。免疫印迹分析显示胞质退化NF-κB抑制剂IκBα开始后60分钟A549细胞的刺激退伍军人130 b(图4 c⇓),染色质免疫沉淀反应显示招聘NF-κB / p65和RNA聚合酶IIil8启动子(图4 d⇓)。IKK-NBD没有减少细胞或诱导形态细胞毒性的迹象。这些数据表明,退伍军人诱发引发表达规范化NF-κB通路的激活。
嗜肺性军团菌,诱导白介素8 (IL)释放依赖核factor-κB (NF-κB)激活肺泡上皮细胞。)A549细胞(1×105细胞·毫升1)与抑制剂的浓度表示pre-incubated NF-κB (IκB)激酶NF-κB modulator-binding域和感染的关键退伍军人130 b (1×107菌落(cfu)·毫升1)。引发释放在上层清液由ELISA测定。b)相对荧光素酶活性(RLA奇遇记》)立志在A549细胞稳定转染NF-κB-dependent报告基因构建感染后6 h退伍军人130 b。数据意味着±扫描电镜。c)退化IκBα决心在指定的时间点后感染1×107cfu·毫升1退伍军人通过免疫印迹分析130 b(代表墨迹图3所示)。d)招聘NF-κB / p65和RNA聚合酶II (Pol II)il8确定启动子在指定的时间点后感染1×107cfu·毫升1退伍军人130 b由染色质免疫沉淀反应(沉淀抗体表示;最初的细胞溶解产物没有免疫沉淀反应也比较显示;代表墨迹图/凝胶三所示)。盟:任意单位;兵:细胞外signal-regulated激酶。* *:p < 0.01与未受感染的控制(C);# #:p < 0.01与感染细胞没有pre-incubation与抑制剂(至少在三个独立的实验)。
庆大霉素对interleukin-8释放的影响
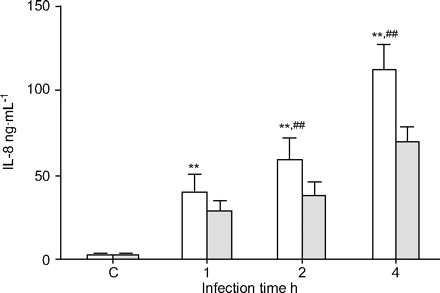
为了解决细胞激活的重要性退伍军人剩下的细胞外,改变了媒介在感染后的1、2和4 h的存在和缺乏庆大霉素和引发释放分析总感染时间后15 h(图5所示⇓)。清除胞外细菌在感染早期导致显著降低引发释放相比,后期感染4 h后删除。此外,杀死细菌细胞外与庆大霉素进一步减少引发释放。
嗜肺性军团菌全身的白介素8 (IL)发布是降低庆大霉素。A549细胞(1×105细胞·毫升1)感染退伍军人130 b (1×107菌落·毫升1)。媒介改变了指定的时间后,有(░)或没有添加庆大霉素(□)。引发释放后上层清液是用ELISA总孵化时间15 h。* *:p < 0.01与未受感染的控制(C);# #:p < 0.01与感染细胞与庆大霉素的(至少在三个独立的实验)。
讨论
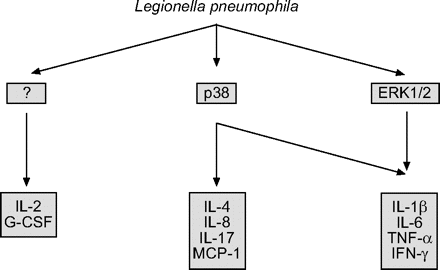
在目前的研究中,人们发现退伍军人130 b诱导释放一个复杂的由人类肺泡上皮细胞系A549细胞因子模式。详细的分析引发释放显示类似的言论引发细胞感染退伍军人菌株130 b,费城1和寇比。引发分泌取决于p38 MAPK的激活和规范NF-κB / RelA-pathway,以及在较小程度上,MEK1-ERK1/2通路(图6所示⇓)。
嗜肺性军团菌诱导细胞因子的释放模式不同依赖p38增殖蛋白激酶(MAPK)和细胞外signal-regulated激酶(ERK) 1/2的活动。退伍军人人类感染肺泡A549细胞株导致激活p38 MAPK和ERK1/2和细胞因子释放。的分泌白介素2 (IL)和粒细胞集落刺激因子(g - csf)不影响激酶抑制;il - 4、8和-17和单核细胞化学引诱物蛋白(MCP) 1被p38 MAPK抑制;和IL-1β白介素、肿瘤坏死因子(TNF) -α和干扰素(IFN) -γ也取决于ERK1/2活动。
肺上皮细胞在先天免疫有重要作用,如。他们识别病原体,包括细菌、通过通常和释放抗菌肽,以及趋化因子和促炎细胞因子9,10。尽管肺泡上皮细胞被军团菌感染有效在体外12,23,在活的有机体内在几内亚猪12,了解宿主免疫反应退伍军人主要来自与人类单核细胞/巨噬细胞和动物实验研究Legionella-permissivenaip5locus-defect / J小鼠品系24。
由于趋化因子合成重要的编排的先天和适应性免疫反应,趋化因子模式发布的退伍军人来华的肺泡上皮细胞进行了分析。为此,完善人类肺泡上皮细胞系A549,军团菌感染有效,见一些研究12,23使用。
退伍军人来华的A549细胞释放化学引诱物引发(多形核中性粒细胞(中性粒细胞))和MCP-1(单核细胞),辅助细胞(Th) 1型细胞因子- 2,TNF-αIFN-γ,Th2细胞因子il - 4和il - 6在15 h。此外,促炎细胞因子IL-1βIL-17和骨髓生长因子g - csf分泌(图6所示⇑)。依照目前的结果,常et al。23描述了il - 6和引发,以及TNF-α表达Legionella-infected A549细胞。
在人类中,军团菌感染血清水平的增加,例如,IFN-γ和il - 6, -12年和-10年25,26。在实验研究中使用小鼠模型或孤立的巨噬细胞,主要细胞因子吸引和激活中性粒细胞和moncytes /巨噬细胞进行了分析。在实验中军团菌肺炎/ J小鼠,Tatedaet al。27发现诱导趋化细胞因子的趋化因子(科学家主题)配体1 (KC)、巨噬细胞炎性蛋白质(MIP) 2和趋化因子(科学家主题)配体5 (LIX)招募中性粒细胞在肺。因此,附件退伍军人培养小鼠腹腔巨噬细胞的稳态水平增加细胞信使rna编码细胞因子IL-1β,il - 6和gm - csf和趋化因子MIP-1βMIP-2和KC28。由于中性粒细胞招募被认为在人类军团菌肺炎29日和老鼠30.,其堵塞增加死亡率/ J小鼠模型27,肺泡上皮细胞可能起着重要的作用在策划对军团菌的免疫反应。
招募了单核细胞被激活的Th1细胞因子IFN-γTNF-α;军团菌IFN-γ促进巨噬细胞的间隙31日,转基因超表达的IFN-γ/ J小鼠减少了细菌的负担32。自从IFN-γ也发现免疫防御的关键单核细胞增多性李斯特氏菌在老鼠身上33和人类34,一个重要的角色IFN-γ在宿主防御细菌细胞内,包括军团菌,必须考虑。同样,TNF-α提升退伍军人间隙在人类单核细胞和小鼠的保护35。两种细胞因子的释放减少了p38 MAPK的抑制,这种途径可能是一个有效的免疫反应的关键退伍军人感染。
退伍军人然而,来华的A549细胞没有释放Th1细胞因子il - 12 (p70), Th2细胞因子IL-5, -10或-13,或淋巴和骨髓生长因子IL-7和gm - csf。有趣的是,高白介素(p70)水平陪同/ J小鼠死亡率下降退伍军人感染27。表达式也发现在人类退伍军人肺炎25,它可以由Legionella-exposed树突细胞36,但肺泡上皮似乎没有这个细胞因子的来源。相比之下,il - 10 IFN-γLegionella-protective效应的逆转37。综上所述,退伍军人人类肺泡上皮细胞分泌趋化现象的CC和科学家来华的趋化因子,以及Th1、Th2趋化因子(图6所示⇑)。其中,TNF-αIL-1β6和8和g - csf视为统一的炎症反应的因素,如。引起TLR2而IFN-γ、2、4和-17和MCP-1似乎pathogen-specific反应的一部分38。因此,Legionella-infected肺泡上皮细胞有说服力地特别是可能导致军团病的宿主免疫反应的调节。
为了获得更多的洞察肺泡上皮细胞的激活退伍军人细胞因子,表达的重要chemotatic引发更详细地进行了分析。退伍军人血清组1菌株130 b,费城1、JR32和寇比诱导引发感染A549细胞分泌。费城1-derived应变JR32诱导引发表达程度低于其他菌株在肺上皮细胞,强调现有的这些菌株之间的差异。按照霍恩的最新发现et al。7,任et al。39和Molofskyet al。40寇比,实验使用flaA敲除突变株表明识别TLR5或其他可能的鞭毛蛋白胞内受体似乎是必要的早期诱导引发释放在肺泡上皮细胞在体外。此外,去除或杀死(庆大霉素)的胞外细菌引发释放A549细胞明显减少。
此外,使用JR32获得的数据队伍敲除突变表明类型IVB-secreted效应器似乎并没有必要的早期诱导引发释放在肺泡上皮细胞在体外。此外,这意味着细菌复制没有必要引发释放的感应。然而,张et al。23有发现,淘汰赛的吗dotG / icmE在退伍军人菌株80 - 045在之后的时间点细胞因子表达减少23。退伍军人基因组显示显著的可塑性和多样性,最近证明,例如,菌株的巴黎和镜头5,显示不同的表达模式的因素之一。生理而且强调这种差异的重要性,例如,观察到费城1-derived应变JR32诱导引发肺上皮细胞表达一定程度上。因此,它不能排除特定的毒力因子的重要性可能不同感染之间的不同退伍军人菌株。此外,不同的基因中icm /点位点被诱变处理。按照常et al。23的时间进程引发mRNA JR32应变或感应队伍4 h基因敲除突变体没有差别。总体而言,它似乎是合理的军团菌细胞外的识别通常最初导致肺泡上皮激活6,7。
激活p38 MAPK已被证明有助于bacteria-related引发感染的肺上皮细胞的表达11,威尔士et al。41早期发现p38 MAPK和Janus激酶被激活在吸收退伍军人巨噬细胞。p38 MAPK在肺上皮细胞,激活后60分钟感染的关键所有诱导细胞因子的释放,除了2和g - csf,但似乎没有必要入侵细胞(数据未显示)。因此,应该考虑关于复制的特异性影响退伍军人。有趣的是,尽管在感染上皮ERK2激酶被激活,ERK激酶活性的贡献程度较轻的上皮细胞激活细胞因子和趋化因子的释放。除了p38 MAPK活性,刺激引发的表达依赖于激活的转录因子NF-κB退伍军人来华的上皮,如上所示链球菌引起的肺炎肺上皮细胞11。进一步的实验解决不同的军团菌致病因素的作用,如脂多糖、鞭毛或水解酶,这些重要的促炎症通路的激活需要为了获得更多的洞察的分子机制。
总之,它显示在这里嗜肺性军团菌感染诱导强烈趋化因子和细胞因子释放人类肺泡上皮细胞A549细胞。这些分子的表达主要取决于p38增殖作用的激活蛋白激酶通路和核factor-κB-dependent A549细胞的基因转录。总体而言,活化的肺泡上皮似乎做出显著贡献的编排军团病的免疫反应。
确认
j . Hellwig优秀的技术援助和美国Schapke(内科医学部门/传染病和呼吸医学、柏林夏洛——夏洛蒂,柏林,德国)和k Rydzewski(德国柏林罗伯特•科赫研究所)是极大的赞赏。
- 收到了2005年11月30日。
- 接受2006年8月7日。
- ©人期刊有限公司