文摘
Epithelial-mesenchymal转型是现在被认为是组织改造的一个重要特征。目前的报告关注腺病毒感染诱导的作用这个变换在慢性阻塞性肺疾病的动物模型。
豚鼠主要外围肺上皮细胞(我们)与腺病毒转染E1A (E1A-PLECs)比较豚鼠正常的肺成纤维细胞(独立)转染E1A (E1A-NLFs)。这些细胞的特点是PCR,免疫细胞化学,电子显微镜,西部和北部污点分析。电泳迁移率改变分析进行,以检查核转录因子(NF) -κB和激活蛋白1(美联社)绑定活动。
E1A-PLECs E1A-NLFs E1A DNA阳性,信使rna和蛋白质表达细胞角蛋白和波形蛋白但不是平滑肌α-actin。都表现出立方形的形态和交叉的复合体,但不包含片状体或表达蛋白质表面活性剂,B或C mrna。这两种细胞类型不同,然而,在他们NF-κB和AP-1绑定脂多糖刺激后,可能由于表达的差异这些转录复合体亚基组成。
E1A转染结果转换的外围肺上皮细胞和正常的肺成纤维细胞表型之间的中间两个主要的细胞。假定这中间表型可能发挥重要作用改造的航空公司在慢性阻塞性肺疾病与腺病毒E1A基因的持久性。
慢性阻塞性肺疾病(COPD)是全球发病率和死亡率的主要原因1。肺弹性反冲的丧失引起的肺气肿和改造的过程,阻碍小航空公司导致在一秒钟用力呼气量逐渐下降,正是这种情况2。最近的研究基于国家卫生研究院国家肺气肿治疗试验表明,慢性阻塞性肺病的进展与增厚的墙壁进行小航空公司的维修和改造的过程2。虽然吸入的有毒气体和粒子是慢性阻塞性肺病的主要危险因素3病毒感染,尤其是儿童感染,增加发展中这种情况的风险1。Adenoviral DNA是由外围保留肺上皮细胞(我们)在人类的病毒E1A基因表达4没有一个完整的病毒的复制5。病例对照研究表明,C组的E1A基因腺病毒存在于更大的数量在COPD患者的肺比在控制与正常肺功能与年龄、性别和吸烟史5,吸烟者的肺部过度炎症严重肺气肿与增加肺泡上皮细胞表达E1A的数字6。
支持这些人类观测实验豚鼠,在那里,在缺乏积极复制病毒但E1A基因的存在,腺病毒感染导致过度单一暴露于香烟烟雾后肺部炎症7,增加了实质和气道壁炎症与慢性接触后更大的气性破坏8。此外,E1A基因和蛋白质坚持在这些动物的肺上皮细胞9。
来自几个实验室的报告表明,这种现象称为epithelial-mesenchymal变换,在上皮细胞转化为生产能力结缔组织基质成纤维细胞,是组织改造的一个重要特性10,11。在目前的研究中,假设adenoviral感染随后持续表达的E1A基因能产生epithelial-mesenchymal转换被调查研究豚鼠表达adenoviral E1A的我们。的变化发生在adenoviral E1A的变换主要豚鼠我们也与那些经常发生在转变成纤维细胞污染主要上皮文化,和证据提出了单元类型都转换为一个中间表型。
材料和方法
动物
女性无菌豚鼠(Cavia porcellus;凸轮哈特利应变;200 - 250 g)获得来自查尔斯河加拿大(St-Constant、QC、加拿大)。这些研究被批准的英属哥伦比亚大学的动物保健委员会(加拿大温哥华BC)。
隔离和我们的文化
我们将从豚鼠肺孤立如前所述12,其中一个修改来提高纯度。而不是免疫球蛋白(Ig) G平移,平移原油细胞悬浊液裸75厘米2提供的30分钟和收集不依从细胞培养瓶3.0±0.5×107我们将每豚鼠(n = 14),与93±5%的细胞不含台盼蓝染料。
净化我们镀在3×1055×105细胞·厘米2在裸six-well盘子或24毫米TranswellTM盘子(合演,剑桥,妈,美国)包含组织culture-treated聚碳酸酯(nucleopore)插入涂1毫升2:1(卷(v) / v)基底膜基质(协同生物医学产品,贝德福德,妈,美国)/杜尔贝科修改鹰介质(DMEM;Gibco BRL公司,马里兰州,美国)和培养在含10%胎牛血清的DMEM(的边后卫,美国UT HyClone实验室,洛根),1%青霉素和链霉素(σ化工有限公司,圣路易斯,密苏里州,美国),10μg·毫升1庆大霉素(Gibco BRL, Inc .)和2.5μg·毫升1二性霉素b (Gibco BRL, Inc .)。第二天,贴壁细胞再辅以DMEM包含5 ng·毫升1角质细胞生长因子(西格玛化工有限公司)来刺激ⅱ型细胞增殖13;青霉素、链霉素、庆大霉素和二性霉素b以上;2%的边后卫;1×insulin-transferrin-selenium(西格玛化工有限公司);10 ng·毫升1表皮生长因子(西格玛化工有限公司)和100 nM氢化可的松(西格玛化工有限公司)。
细胞纯度主要文化的评估
我们将从两个豚鼠分别纯化,镀在培养皿中包含三个玻璃盖玻片。细胞从一个豚鼠进行分析后3天,那些从其他经过4天的文化。冷甲醇固定后,细胞使用光学显微镜检查。400细胞识别每个盖玻片(1200·动物1)分为我们(鹅卵石形态),正常的肺成纤维细胞(nlf;纺锤状形态)或非保密。
基本我们将不灭
质粒pE1Aneo(从f·格雷厄姆,麦克马斯特大学,汉密尔顿,加拿大)携带整个E1A基因及其启动子(腺病毒5的核苷酸25 - 1770)和新霉素抗性基因,由猴病毒40大t抗原启动子驱动的。
主要我们从八豚鼠培养3×1055×105细胞·厘米2在裸six-well盘子或Matrigel-coated Transwell板1 - 4天之前接触pE1Aneo多元Lipofectamine试剂(Gibco BRL, Inc .) 6 h根据制造商的指示。3天后,细胞被选中(耐新霉素)μg·250毫升1G418 (Gibco BRL, Inc .),氨基糖苷类。细胞生长在耐药2周后裸six-well盘子都山肩新six-well板块,而那些生长在基底膜基质首次收获如前所述14然后re-plated裸six-well盘子。选择G418-resistant单细胞克隆后,所有后续的分析选择数量的这些克隆(见结果部分)进行了细胞上三到四个段落。相同的限制通过应用于以下E1A-NLFs数量。
文化和豚鼠nlf不朽
独立,孤立如前所述15从两个豚鼠,镀在分离裸six-well盘子2×10的密度4细胞·厘米2在DMEM含有青霉素、链霉素的边后卫10%和1%。转染前细胞培养2 - 3天pE1Aneo-liposome复杂。G418-resistant细胞re-plated 12-well板块。
检测E1A基因的信使rna和蛋白质
E1A DNA提取的DNA转染和untransfected细胞是由PCR如前所述7。从这些细胞是反向转录RNA,然后放大使用正向和反向引物5 -AGTGACGACGAGGATGAAGAGG-3和5 -TCTCAGGAGGTGTGTTAGAAGG-3,相当于核苷酸953 - 974和1381 - 1402年,分别为5型腺病毒序列(基因库gi: 58484)。的预测大小PCR产品194和334个碱基对的12和13 s E1A mrna,分别。E1A蛋白免疫荧光染色检测4和免疫印迹。
小学和转染细胞的描述
电子显微镜
新孤立我们(∼3.0×107)加工成五个透射电子显微镜的Epon块16。一个超薄部分从每一块沾醋酸双氧铀及柠檬酸铅检查使用飞利浦400透射电子显微镜(飞利浦、埃因霍温、荷兰)。每个细胞类型的数量表示为一个百分比总数的细胞检查。这些细胞的形态与净化我们和我们转染子培养在聚碳酸酯插入涂以2:1 (v / v)基底膜基质/ DMEM 24毫米Transwell板块4天。Untransfected和转染nlf支流文化4天后在裸露的聚碳酸酯插入内24毫米Transwell盘子,在类似的方式进行。
免疫组织化学
免疫组织化学17使用鼠标进行单克隆抗体反人类的(Dako、斯特鲁普、丹麦)针对细胞角蛋白(酸性和碱性)和波形蛋白4.6μg·毫升1和平滑肌α-actinμg·5.0毫升1。各自的浓度isotype-matched老鼠免疫球蛋白(西格玛化工有限公司)担任控制。30个细胞的染色强度随机领域的得分是——(与消极的控制),+(温和的染色)或+ +(强烈的染色)视觉评估。
北部的污点分析表面活性剂蛋白mrna
RNA提取从新鲜洁净我们或主我们培养在100毫米的塑料盘子或聚碳酸酯插入涂层与基底膜基质内24毫米Transwell板块和E1A转染子使用试剂盒(Gibco BRL, Inc .),而RNeasy马克西工具包(试剂盒,Inc .,米西索加、加拿大)被用于豚鼠肺。北部污点分析后,使用下面列出的互补的dna。
人类表面活性剂蛋白A、B、C和18 s核糖体互补DNA探针cross-hybridise各自的豚鼠rna。探针与[α-标签32P]脱氧胞苷三磷酸(美国新泽西州Amersham,皮斯卡塔韦)随机启动。
电泳迁移率改变分析
细胞种植在75厘米2水瓶是刺激μg·10毫升1脂多糖(LPS) 2 h。从这些和未经处理的细胞,核提取准备和电泳迁移率改变分析(emsa)核因子(NF) -κB和激活蛋白(美联社)1,以及各自的寒冷的竞争和supershift化验,进行如前所述18。
结果
评估主要我们纯洁
光显微镜检查1200年主要我们培养3天显示50.3±6.7%表现出鹅卵石形态典型的我们,4.6±0.7%是纺锤状纤维母细胞和45待定的±7.3%的细胞来源。文化的另一个1200个细胞检查4天后我们将分别为45.8±6.9%,15.8±1.7%成纤维细胞和38.4±5.3%的待定。
不灭的主要我们和独立
主要我们生长在裸板和转染pE1Aneo产生G418-resistant三12井的殖民地。9个抗单细胞克隆(E1A-PLEC克隆1 - 9)从其中一个扩大殖民地和九都保持在不断选择μg·100毫升1G418。同样,主要我们生长在基底膜基质产生G418-resistant殖民地的两个12井,从这六个耐单细胞克隆(E1A-PLEC克隆10 - 15)。从所有15我们克隆细胞表现出鹅卵石形态,达到融合后继续分裂。克隆1、2、10和11被用于本研究。
主要独立转染与pE1Aneo G418-resistant殖民地四12井的生产。一个从单一耐药细胞克隆获得了从每个(E1A-NLF克隆1 - 4)。所有四个显示鹅卵石形态,达到融合后继续分裂,并保持与G418下选择。E1A-NLF克隆1和2被用于本研究。
E1A基因,信使rna和蛋白质在转染细胞系
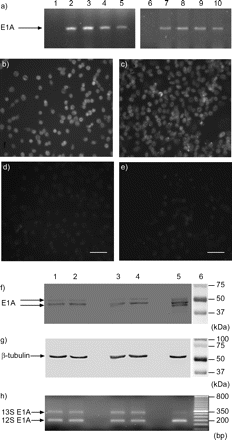
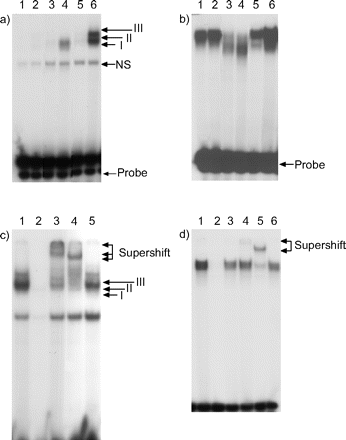
E1A基因中检测出E1A-PLEC克隆1,2、10和11和E1A-NLF克隆1 - 4(图1⇓)。逆转录酶聚合酶链反应(RT) RNA从E1A-PLEC E1A-NLF克隆导致两个乐队的放大的预期大小12和13年代E1A mrna,分别,这也出现在RNA A549细胞感染腺病毒5(图1 h⇓)。没有见过这样的乐队在RNA主要国家,与18 s核糖体核糖核酸rt - pcr证实平等RNA加载(数据未显示)。免疫组织化学显示强大的核染色E1A E1A-PLEC和NLF转染克隆(图1 b⇓分别和c),而没有染色观察isotype-matched控制免疫球蛋白(图1 d⇓和e)。在西方的屁股,同样的两个E1A单克隆抗体结合蛋白被发现在E1A-PLECs E1A-NLFs,和大小相似的两个最大E1A蛋白质中发现G293细胞(美式文化收藏、马纳萨斯,弗吉尼亚州,美国;图1 f⇓和g)19。大小标记表明,这些蛋白质相对分子质量的40 - 50 kDa,这比预测的氨基酸序列。磷酸化可以解释这种差异的一部分,但是,由于这种差异,很难分配2 - 12和13年代亚型。尽管mRNA富足并不一定预测蛋白质丰富,代表两种亚型的mRNA表达的这两个细胞(正如前面所讨论的那样)。
检测腺病毒E1A基因的PCR,信使rna逆转录酶聚合酶链反应(RT)和蛋白质的免疫荧光染色和免疫印迹。a) Ethidium-bromide-stained琼脂糖凝胶E1A PCR产品(486碱基对(bp)) E1A外围肺上皮细胞(我们)克隆1、2、10和11(分别为道2 - 5)和E1A正常的肺成纤维细胞(NLF)克隆1 - 4(分别为车道7 - 10)。Untransfected我们(巷1)和Untransfected nlf(巷6)被用作消极的控制。单克隆抗体针对E1A (b, c)和同型的控制抗体(d, e)应用于E1A-PLEC克隆1 (b, d)和E1A-NLF克隆1 (c, e) = 10μm规模酒吧。应用程序相同的E1A抗体免疫印迹(f)显示两个E1A亚型在E1A-PLEC克隆1和2(通道1和2)和E1A-NLF克隆1和2(车道3和4),相当于两个最大的E1A多肽在G293发现细胞(巷5)。抗体针对β-tubulin蛋白质被用来控制加载相应的车道(g)。相应的尺寸标记巷6所示。h) Ethidium bromide-stained rt - pcr产物的琼脂糖凝胶E1A mRNA在f(车道),除了腺病毒5-infected A549细胞取代G293巷5)是一个积极的控制。
电子显微镜
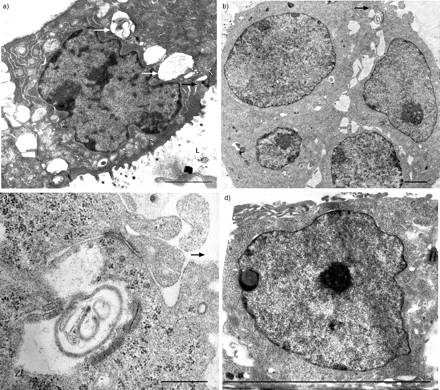
共有324个细胞从一个新孤立我们准备,28%是肺泡巨噬细胞,25%表现出的特征克拉拉细胞,包括叠层水泡夹杂物和异构电子致密颗粒(图2一个人口⇓),25%是ⅱ型细胞与层状的身体特征(图2 b⇓),12%是肺泡i型细胞,6%是纤毛细支气管上皮细胞,4%为嗜酸性粒细胞。没有发现这些电子显微镜研究成纤维细胞。
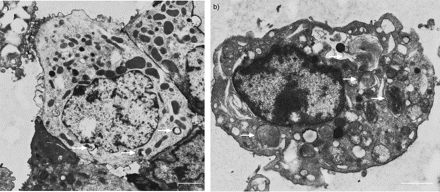
电子显微图新鲜洁净的外围肺上皮细胞。与层压)克拉拉细胞内含物(箭头)和异构的电子致密颗粒。b)ⅱ型细胞层状的身体特征(箭头)。酒吧= 2μm规模。
主要我们生长在Matrigel-coated聚碳酸酯插入形成两极分化的三维(3 d)总量由立方形的细胞面临中央腔,与大量的微绒毛细胞顶端,片状夹杂物在细胞质,细胞间交叉的复合物(图3⇓)。相比之下,E1A-PLEC克隆生长在同样的方式形成3 d聚合组成的三个或四个立方细胞联接的复合体,但缺乏片状体或微绒毛(图3 b⇓)。生长在裸聚碳酸酯过滤器时,这些细胞形成单层膜,细胞分化立方形,联接的复合物(图3 c⇓)。
电子显微图的纯化外围肺上皮细胞(我们)的主要文化和E1A-PLEC克隆。)主要培养我们生长在Matrigel-coated聚碳酸酯过滤器形成三维聚合物的立方形的细胞,与层状组织(白色箭头),交叉的复合物(黑色箭头),顶端微绒毛(*)衬里中央腔(L)。b) E1A-PLEC克隆1生长在Matrigel-coated聚碳酸酯过滤器连接复合体(黑色箭头)细胞之间。c)更高的连接复合体b所示)放大。d) E1A-PLEC克隆1生长在一个裸聚碳酸酯过滤器形成单层细胞的分化立方形的形态和交叉的复合物(箭头所指)。酒吧= 2μm规模。
独立生长在裸聚碳酸酯过滤器形成两种类型的集群在同一道菜。一些集群组成的层的纺锤状细胞胞质较长的扩展(图4⇓),和其他细胞的多层不规则形态(图4 b⇓)。没有观察到在任何类型联接的复合物。E1A-NLF克隆,相反,形成单层膜,细胞分化立方形,联接的复合物(图4 c⇓和d)。
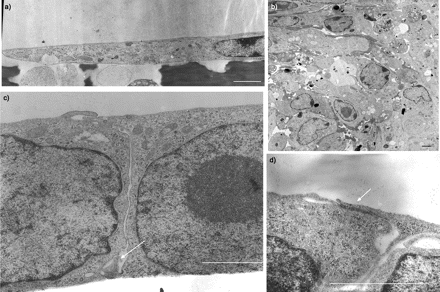
电子显微图正常的肺成纤维细胞(独立)和E1A-NLF克隆1种植在裸露的聚碳酸酯过滤器。独立形成的区域)单层和b)多层增长。1 c) E1A-NLF克隆生长与立方形的单层细胞形态和交叉的复合物(箭头所指)。d)更高的放大倍数的顶端连接复合体(箭头所指)之间的两个相邻E1A-NLF细胞。酒吧= 2μm规模。
免疫组织化学
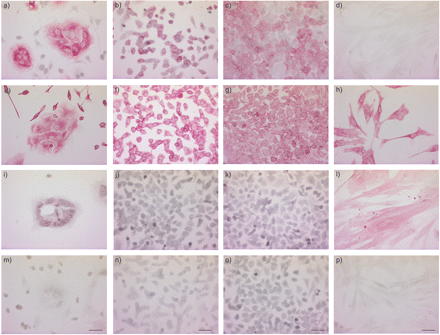
表1⇓总结了免疫组织化学结果如图5所示⇓。主要我们(图5⇓),E1A-PLEC克隆(图5 b⇓)和E1A-NLF克隆(图5度⇓)所有显示细胞质染色细胞角蛋白,而主要国家没有(图5 d⇓)。染色强度相似E1A-PLEC E1A-NLF克隆,但明显低于主我们(表1⇓)。
疣状模拟)细胞角蛋白、超高频)波形蛋白,我)平滑肌α-actin和mp)控制。主要外围肺上皮细胞(我们)文化(A, e,我和m), E1A-PLEC克隆1 (b, f, j和n), E1A-normal肺成纤维细胞(NLF)克隆1 (c、g、k和o)和独立(d、h、l和p)是生长在盖玻片和沾有特定的单克隆抗体或isotype-matched免疫球蛋白g(控制)。污染周围成纤维细胞是上皮殖民地(a和e)。酒吧= 10μm规模。
所有四个细胞类型显示波形蛋白阳性胞质染色(图5的情况⇑),细胞之间的染色强度无显著差异(表1所示⇑)。
主要我们显示弱染色细胞核周围的平滑肌α-actin(图5⇑),而独立显示强大的胞质染色(图5 l⇑)。相比之下,没有染色观察E1A-PLEC(图5 j⇑)或E1A-NLF克隆(图5 k⇑)。
污染我们周围发现肺成纤维细胞在初代培养为阴性细胞角蛋白(图5⇑),但波形蛋白染色强烈(图5 e⇑)和平滑肌α-actin(数据没有显示)。
没有染色观察细胞染色时isotype-matched控制抗体(图5 mp⇑)。
表面活性剂蛋白mRNA表达
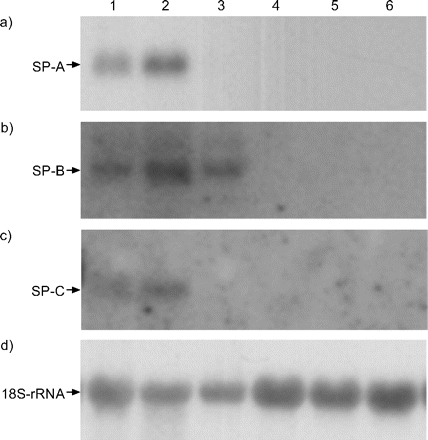
北方杂交(图6所示⇓)表明,豚鼠肺和新鲜洁净我们(分别为通道1和2)表达表面活性剂蛋白A, B和C mrna。我们生长在Matrigel-coated聚碳酸酯过滤器的主要文化表示只有表面活性剂B蛋白mRNA(巷3),和那些生长在塑料碗没有表面活性剂蛋白mRNA表达(巷4)。E1A-PLEC克隆生长在Matrigel-coated聚碳酸酯过滤器(车道5和6)或塑料餐具(数据未显示)没有表面活性剂蛋白mRNA表达。在这些细胞,18 s核糖体RNA,用作内部控制,相似(图6 d⇓)。
北部污点分析来确定表达式的)表面活性剂蛋白(SP) - a, b) SP-B和c) SP-C信使RNA在细胞总RNA提取豚鼠肺(巷1),新鲜净化周围肺上皮细胞(我们;巷2),一个主要的文化净化我们生长在一个Matrigel-coated聚碳酸酯过滤器(巷3),相同的细胞生长在塑料(巷4),和E1A-PLEC克隆1和10 Matrigel-coated聚碳酸酯过滤器(车道5和6)。d) 18 s核糖体RNA (rRNA)作为内部控制。
EMSA
LPS刺激诱导核提取物E1A-NLFs和E1A-PLECs NF-κB绑定活动但不独立(图7⇓)。E1A-PLECs,特定的绑定复合物检测编号我三世为了通过凝胶迁移的,从最快到最慢,复杂II(巷6)表现出最大的强度。E1A-NLFs绑定活动是由迁移速度通常比那些E1A-PLECs复合物,有可能重叠与复杂的我(巷4)但绑定强度低于E1A-PLECs中找到。
a、b)电泳迁移率改变分析(EMSA)检测核转录因子(NF) -κB和激活蛋白1(美联社)绑定活动正常的肺成纤维细胞(nlf;通道1和2),E1A-NLF克隆1(车道3和4)和E1A-peripheral肺上皮细胞(我们)克隆1(车道5和6)。试验进行核提取物治疗细胞(通道1、3和5)和细胞刺激μg·10毫升1脂多糖(LPS) 2 h(通道2、4和6)使用)免疫球蛋白(Ig)κNF-κB探测器,5“-AGTTGAGGGGACTTTCCCAGGC-3”(NF-κB绑定序列GGGACTTTCC)和b) AP-1探针,5 -CGCTTGATGAGTCAGCCGGAA-3 (AP-1绑定序列TGAGTCA)。具体的位置protein-DNA复合物(》),非特异性的复杂(NS)和游离探针。c) NF-κB绑定在核提取物E1A-PLECs刺激μg·10毫升1有限合伙人为2 h的多余的未标记的AP-1(巷1)或NF-κB(巷2),寡核苷酸和抗体针对p65(巷3)或p50(巷4),或控制免疫球蛋白(巷5)。复合物》和乐队supershifted p65和p50抗体表示。d) AP-1绑定在核提取物E1A-PLECs刺激μg·10毫升1有限合伙人为2 h的多余的未标记的NF-κB(巷1)或AP-1(巷2),寡核苷酸和抗体针对JunB(巷3),c-Jun(巷4),c-Fos(巷5),或控制免疫球蛋白(巷6)。乐队supershifted c-Jun和c-Fos抗体所示。类似结果NF-κB和AP-1绑定活动当一对不同的细胞,即E1A-NLF克隆2和E1A-PLEC克隆2、比较。
EMSA AP-1证明本构绑定在核提取物的国家不改变LPS刺激,然而,在E1A-NLFs和E1A-PLECs,有限合伙人增加AP-1绑定(图7 b⇑)。乐队代表AP-1绑定在E1A-NLFs迁移速度比单一NLF或双E1A-PLEC乐队。
在E1A-PLEC supershift化验,使用抗体针对p50和p65 NF-κB和JunB c-jun和c-fos AP-1和竞争分析使用多余的未标记的特定或不相关的特异性寡核苷酸证实蛋白质绑定到相应的寡核苷酸(图7 c⇑和d),对NF-κB抗体主要针对p65 supershifted复合物三世和二世,而抗体针对p50转移复合物I和II(图7 c⇑)。这表明p50和二p65是复杂的一部分。关于AP-1 c-Jun和c-Fos抗体产生supershifted乐队,而JunB抗体没有(图7 d⇑)。的E1A-NLF supershifted乐队平行E1A-PLECs (NF-κB和AP-1(数据未显示),除了supershifted乐队来自较小的复合物形成的这些转录因子在E1A-NLFs。
讨论
目前的结果表明,腺病毒E1A基因可用于豚鼠流芳百世的我们和成纤维细胞。无性繁殖系地派生E1A-expressing我们将展示一个有限数量的ⅱ型细胞表型,但未能显示更具体的这种区分的标志,如叠层水泡包裹体和微绒毛或表面活性剂蛋白mrna的表达。生长在裸塑料餐具时,他们显示一些上皮特征,如弱细胞角蛋白表达和鹅卵石形态、生长在裸聚碳酸酯过滤器时,他们显示立方形的形态和交叉的复合物。这些特性都与先前的报道一致描述E1A-immortalised细胞系建立的大鼠ⅱ型的主要文化pneumocytes种植在裸露的塑料20.- - - - - -22。这些老鼠细胞表现出上皮细胞角蛋白表达的表型,联接的复合物和立方形的形态也缺乏ⅱ型细胞的分化标记。尽管目前试图改善主要分化培养的保留主要我们将矩阵,前和转化细胞转染过程期间,未能维持ⅱ型细胞的特定特性。
对成纤维细胞,目前的研究结果表明,E1A引起mesenchymal-to-epithelial转换。尽管独立生长层的细胞纺锤状形态穿插多层疫源地的细胞形状不规则给文化peak-and-valley外观,E1A-expressing nlf开关这父表型,想起我们转染子。这样epithelialisation,包括立方形的形态、交叉的复合体,细胞角蛋白生产、平滑肌的差别进一步支持对这些α-actin,间充质标记强烈积极的父母独立。这些结果是由弗里希的报告23腺病毒E1A-induced mesenchymal-to-epithelial转换在人类间充质来源的肿瘤细胞。E1A-expressing肿瘤细胞,如目前转染nlf,表达了联接的复合体,细胞角蛋白。弗里希23建议转换到一个上皮表型要求间充质反式激活因子,抑制上皮基因转录,由E1A不表达或灭活,尤其是12 s E1A的形式,这可能是E1A-NLFs在当下所表达的研究。基于这一假设,E1A引入间充质细胞,在目前的情况下,可以这些阻遏蛋白活性,导致上皮基因的诱导。间接证据的缺乏这样一个潜在的抑制因子在当下转染nlf来自AP-1 EMSA分析的结果,与国家相比,转染nlf显示AP-1复杂的更大的流动性,即。小复杂,暗示可能缺席的抑制因子的一部分AP-1 untransfected复杂的国家。
Alcornet al。24表明成纤维细胞污染的主要来源在ⅱ型细胞的主要文化。在目前的情况下,纺锤状细胞角蛋白纤维母细胞为阴性,但波形蛋白阳性和平滑肌α-actin,占5 - 15%的主要文化的3和4天后我们将准备,分别。在成纤维细胞与我们相比,这三倍增加的数量仍然几乎不变,表明高污染成纤维细胞的有丝分裂活动。因此,E1A-transfected细胞最初认为是我们可以从污染成纤维细胞出现,与后续mesenchymal-to-epithelial转换,建议由弗里希23。
与前面的解释,相反证据提出了强烈表明,E1A-transfected细胞的两种类型是不同的。最初,差异dna结合转录因子的活动NF-κB AP-1 nlf, E1A-NLFs E1A-PLECs和这个活动在LPS刺激的变化。核提取物nlf NF-κB绑定活动非常微弱,这个基底活动并不是增加与LPS刺激后。E1A-transfected nlf也显示基底结合活性低,但与独立,E1A-transfected细胞应对有限合伙人增加绑定。转染我们,同样的,表现出低基底活动,像转染nlf,应对有限合伙人,但是,在这种情况下,更强烈。除了这种差异的反应强度,额外的复合物,大,在转染nlf,。对AP-1,独立显示本构绑定活动不受有限合伙人。转染nlf不仅显示出较低的基底AP-1绑定活动也形成一个小复杂,目前对有限合伙人。转染我们也应对有限合伙人,但更像是发现形成的复合物在untransfected独立。尽管E1A NF-κB和AP-1绑定活动增强,反应有限合伙人在这两个国家,我们将每个单元中的转录复合物形成的差异表明,这些细胞在本质上是不同的,尽管其他E1A引起的表型相似性。
活跃的dna结合蛋白NF-κB和AP-1都是二聚体的形式,由五NF-κB NF-κB / Rel家庭的成员25,为AP-1的安全系数和小君的家庭的成员,分别为5和三个成员组成的26。为了确定组成的子单元形成的复合物的两个转录因子,从而确定其来源的区别在转染复合物形成我们和独立,supershift化验使用。有趣的是,目前的结果表明,一些单元贡献各自的复合物在E1A-PLECs和E1A-NLFs是相同的。总体规模以来的一些绑定复合物在两个细胞类型不同,这表明其他亚基形成各自的二聚体可能有所不同。除此之外,或者,蛋白质与这些转录因子构建multiprotein转录过程中复杂的可能出现细胞特定类型的表达式27从而导致的大小差异sequence-specific dna结合蛋白复合物中确定两种细胞类型。这些可能性的细胞特定类型的表达转录因子子单元和/或相关因素进一步支持目前作者的论点E1A-transfected我们并非来源于污染成纤维细胞的转染。因此,我们得出结论,转染和nlf结果与中间epithelial-mesenchymal E1A-expressing细胞系特征可能与由E1A去分化诱导。这个结论与·拉蒙-卡哈尔在协议et al。28,他改变了上皮细胞和成纤维细胞的肿瘤细胞和腺病毒E1A发现聚合类似的表型,无论细胞起源。
E1A诱导豚鼠我们更多的间质表型,即。表面活性剂损失减少蛋白质和cyokeratin表达式,上皮细胞的标记,但保留波形蛋白的表达。Epithelial-mesenchymal转换已经被记载在成纤维细胞来源于上皮细胞在进步的肾脏疾病10、特发性肺纤维化11和肝硬化,肝星状细胞转化为myofibroblasts29日。由于腺病毒E1A抑制许多启动子的转录活动30.- - - - - -32,E1A镇压分化标记在我们将可能诱发过程我们将第一次失去分化标记移动到一个中间表型,然后可能通过transactivation间叶细胞基因的13 s同种型33,间质表型。
epithelial-mesenchymal转换引起的腺病毒E1A在豚鼠肺上皮细胞是特别有趣,因为外围改造周边航空公司增加增厚的墙最近被证明是与慢性阻塞性肺疾病严重程度有关2。目前作者怀疑上皮细胞间质转化可能导致改造过程观察到在慢性阻塞性肺疾病肺外围通过解除对矩阵气道壁的沉积。E1A-induced转换的外围肺上皮细胞,因此,支持一个角色腺病毒感染的发病机理气道重塑过程。这些豚鼠细胞还提供一个模型为研究底层机制导致更多的间质表型的表达以及相关的变化,可能会影响气道重塑。此外,持久E1A的当前模型表达式后adenoviral感染豚鼠可以提供一个有用的手段,研究这方面的慢性阻塞性肺疾病的发病机理在活的有机体内因为它可以放大的影响慢性吸烟暴露和增加多形核白细胞,巨噬细胞和CD4和CD8淋巴细胞数量在外围的航空公司8在老鼠身上,显然没有观察到。这个豚鼠模型,只有少数的肺上皮细胞保留E1A9,可能会更好地反映人类肺部的情况4相比之下,lung-specific E1A的转基因小鼠模型表达式33,所有的肺泡和细支气管细胞[34]有可能这些病毒蛋白表达。
确认
作者要感谢f·格雷厄姆(加拿大麦克马斯特大学,汉密尔顿)pE1Aneo质粒,和d .英语和已故的美国格林(从詹姆斯·霍格iCapture心血管和肺研究中心圣保罗医院,温哥华BC,加拿大)与数字图像技术援助。
- 收到了2005年5月20日。
- 接受2006年7月31日。
- ©人期刊有限公司