文摘
甘露醇吸入增加尿排泄9α11β-prostaglandin F2(前列腺素D的代谢物2和肥大细胞激活的标志)和白三烯E4。本研究检测β的假设2肾上腺素能受体受体激动剂和色甘酸二钠(SCG)防止mannitol-induced支气管收缩的抑制肥大细胞释放中介。
十四哮喘受试者吸入甘露醇(平均剂量252±213毫克),以导致一秒钟用力呼气量下降(FEV1)≥25%。相同剂量被吸入后15分钟formoterol延胡索酸酯(24µg) SCG(40毫克)或安慰剂。预处理和post-challenge尿样进行分析通过对9α酶免疫分析法,11β-prostaglandin F2和白三烯E4。
FEV最大的下降132±10%安慰剂是继SCG formoterol后减少了95%和63%。安慰剂后,增加尿中值9α,11β-prostaglandin F2从61年到92年ng·更易与肌酐浓度−1,但没有显著增加9α,11β-prostaglandin F2浓度的formoterol (69与67 ng·更易与肌酐−1)或SCG (66与60 ng·更易与肌酐−1)。的增加尿白三烯E4在安慰剂(从19岁到31 ng·更易与肌酐−1)是受药物的影响。
这些结果支持假设药物影响气道反应甘露醇是由于肥大细胞抑制前列腺素D2释放。
吸入甘露醇引起的哮喘患者的气道,但不健康受试者,缩小1。假设机制甘露醇引起支气管收缩是中介发布针对渗透性增加呼吸道表面的液体2,3。相同的机制提出了运动性支气管收缩4,5。
药物用于预防运动诱发支气管狭窄也防止气道反应甘露醇6,7。响应运动和甘露醇被认为是依赖于炎症细胞,肥大细胞和嗜酸性粒细胞等,在航空公司。气道反应都刺激可以抑制长期吸入糖皮质激素治疗8,9。
Nedocromil钠,抑制中介从肥大细胞释放10,还能抑制气道反应甘露醇6。这一发现与气道反应的概念是一致的甘露醇涉及从呼吸道肥大细胞释放bronchoconstricting介质。肥大细胞参与的进一步证据的发现是减少气道敏感性甘露醇组胺受体的存在(H1)拮抗剂盐酸非索非那定7。白细胞三烯(LTs)也涉及对甘露醇气道反应,尤其是在维持支气管收缩。这已经被证明了的快速复苏基线后肺功能的挑战与甘露醇在肝移植受体拮抗剂montelukast的存在7。LTs回应甘露醇的来源是未知的挑战,,与组胺不同,许多不同的细胞类型,除了肥大细胞,可能导致LT的形成。
它最近被报道,甘露醇吸入后,有一个尿排泄增加9α,11β-prostaglandin (PG) F2,mast-cell-derived PGD的代谢物23。这一发现肥大细胞激活是一致的,表明有潜力bronchoconstricting后卫参与气道对甘露醇的回应。在相同的研究中,持续增加(90分钟)LTE的尿排泄4的肺end-metabolite cysteinyl-LTs,报道3。
目前尚不清楚药物抑制中介从肥大细胞释放在体外11- - - - - -13也抑制中介发布针对甘露醇的挑战在活的有机体内。在目前的研究中,一个长效β的影响2受体激动剂和色甘酸二钠(SCG)甘露醇和尿排泄的气道反应介质是双盲安慰剂对照交叉试验研究。
方法
研究设计
受试者参加实验室4次,每个大约在同一时间和间隔≥2天。第一次担任控制天,甘露醇的挑战进行评估的响应性和皮试评估特异反应性。逐步增加剂量甘露醇的挑战是执行,如前所述1,在一秒用力呼气量(FEV1)被用作索引呼吸道口径的变化(麦蓝3300肺活量计;Micromedical英国查塔姆)。完成了挑战FEV减少≥25%1时记录或甘露醇的最大累积剂量(635毫克)管理。
第二、第三和第四列在图1⇓。这两种药物被选中,是因为他们可以交付作为干粉。为了保持致盲,实现类似的沉积,在甘露醇,formoterol SCG和安慰剂都使用吸入器管理TM(勃林格殷格翰集团、殷格翰集团、德国)。这个设备显示良好的色散特性,发现微粒的百分比保持或改进使用吸入器TM。细粒分数SCG formoterol为29%和37%,并与25和11%相比获得的分数与吸入器通常用于交付formoterol (AerolizerTM;诺华澳大利亚,澳大利亚北方莱德)和SCG (SpinhalerTM;赛诺菲-安万特,澳大利亚麦格理公园)。
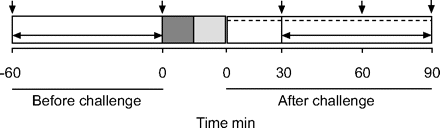
尿液收集的时间点(垂直箭头),点时间(在基线水平箭头)之前和之后(−60分钟)和甘露醇的挑战(░)formoterol,色甘酸二钠或安慰剂。使用累积剂量的甘露醇的挑战,导致在一秒钟用力呼气量下降25% (FEV1)控制,治疗开始后15分钟管理(▒)。的时间完成甘露醇的挑战是12±3分钟(平均±sd;n = 14)。FEV的复苏1是自发和测量每隔10分钟为90分钟(- - - - - -)。
每个药物管理有两个地吸入包含formoterol(12µg·吸入−1;瑞士诺华制药,巴塞尔),SCG (20 mg·吸入−1;Rhone-Poulenc ror, Baulkham Hills,澳大利亚)或安慰剂。甘露醇的挑战进行15分钟治疗后使用剂量的增加导致了FEV下降25%1在控制。FEV的复苏1甘露醇后基线水平的挑战是自发和测量5和10分钟,然后每隔10分钟直到90分钟完成后的挑战。受试者被要求喝100毫升水1 h每个访问之前。他们给100毫升每小时访问期间。收集的尿液样本要求主体空虚到干净的容器。两个基线样本,第一个到达实验室,第二个一小时后,立即在药物管理和甘露醇挑战(图。1⇑)。进一步收集尿液样本30、60和90分钟后的挑战。尿样都装上干冰在斯德哥尔摩卡罗林斯卡医学院(瑞典),进一步存储没有防腐剂−20°C到分析。
主题
不吸烟的过敏性哮喘受试者基线FEV1≥70%的预测价值14和没有胸部感染前四周内初始访问(n = 35)进行了控制甘露醇挑战评估是否FEV下降≥25%1可以实现。14个学科进入研究;剩下的受试者显示气道反应过于温和的(n = 16),没有换取后续访问(n = 2)或退出研究由于胸部感染,病毒感染或恶化哮喘(n = 3)。
短效β26 h和长效β受体激动剂被扣留2受体激动剂,nedocromil和SCG保留48 h在每一天的学习。抗组胺药被扣留在整个研究期间,吸入型皮质类固醇激素在这项研究。所有的受试者被要求放弃咖啡因和酒精从20:00 h晚前研究和没有咖啡因或niacin-containing食物或饮料和剧烈运动被允许研究的一天。悉尼中央区域卫生服务伦理委员会(Camperdown、澳大利亚)批准了研究(协议号x02 - 0171)和所有受试者签署了同意书。研究进行的临床试验方案通知下澳大利亚治疗性商品管理(澳大利亚堪培拉;卡通# 2002/383)。
中介分析
酶免疫分析法的9α,11β-pgf2进行连续稀释尿液样本,使用兔多克隆抗血清和acetylcholinesterase-linked示踪(开曼化学公司,安阿伯市,美国)如前所述5。9α的抗体交叉作用,11β-pgf2(100%),2、3-dinor-9α11β-pgf2(10%)和PGD2,PGF2α和8-epi-PGF2α(< 0.01%)。尿分析LTE4执行以下类似的协议吗15采用兔多克隆抗血清针对cysteinyl-LTs acetylcholinesterase-linked LTE(开曼化学公司)4作为示踪剂。LTC的特异性的抗血清4为100%,有限公司吗4100%,LTE467%。化验的检出限为7.8 pg·毫升−1。使用比色测定肌酐分析(Sigma-Aldrich瑞典,斯德哥尔摩,瑞典)。肌酐的所有尿液样本进行分析,结果表示为毫微克每毫摩尔的肌酐的排泄中介。
统计分析
气道反应数据表示为±sd。差异评估使用t检验和方差分析重复测量和关系评估使用皮尔逊相关性(rp)。样本容量需求计算使用数据从先前的研究3。结果给出了高峰与基线,基线值表示为值的均值以−60 0分钟和峰值作为最高价值观察到30,甘露醇吸入后60或90分钟。尿中介排泄水平不是正态分布,提出了中位数(四分位范围)。以上两组之间的差异是决定使用弗里德曼的重复测量方差分析排名。两组之间的差异决定使用Wilcoxon符号秩检验。差异显著p < 0.05。提供保护的程度(百分比)formoterol和SCG计算表达之间的差异最大FEV比例下降1药物治疗的安慰剂日天FEV占最大比例的下降1在安慰剂的一天。
结果
气道反应甘露醇
累积剂量的甘露醇交付控制天是252±213毫克,这FEV下降引起的129±4%(表1⇓)。相同剂量的甘露醇激起了FEV下降32±10%1在双盲安慰剂的会话的研究(表2⇓)。
SCG和formoterol显著地抑制响应吸入甘露醇(p < 0.001),提供63±19和95±7%保护FEV下降最大1分别为(表2所示⇑)。在基线FEV没有区别1在所有测试的日子里发现了(p = 0.99);然而,formoterol管理后,FEV增加7.6±6.4%1与基线相比(图2所示⇓)。这种改善在回答支气管扩张剂很小,可能是因为大多数科目FEV显示正常1在基线(表1⇑)。所提供的保护,formoterol气道反应甘露醇几乎是完整的。FEV的增加1由于formoterol与它的保护作用在气道敏感性甘露醇(挑衅剂量的甘露醇引起FEV下降15%1;rp= 0.07,p = 0.83)。
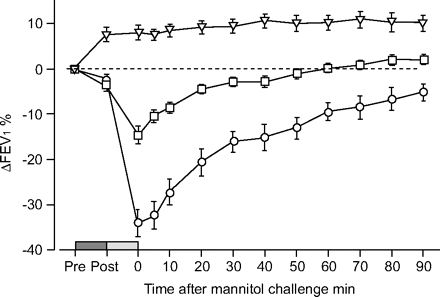
减少一秒用力呼气容积(FEV1)前(前)和15分钟后(Post)吸入(▒)安慰剂(○)色甘酸二钠(□)和formoterol延胡索酸酯(▿)和甘露醇后90分钟挑战(░)意味着±14哮喘受试者sd累积剂量的甘露醇252±213毫克。数据意味着±sd。········:基线值。
尿排泄的介质
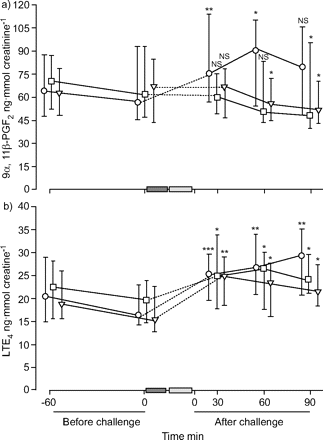
在协会mannitol-induced支气管狭窄安慰剂的一天,有一个增长的尿排泄9α,11β-pgf2和LTE4。中位数(四分位范围)尿排泄的9α,11β-pgf2和LTE4给出在每个时间点为安慰剂和图3中两种药物吗⇓。在安慰剂,11β-pgf 9α水平2从61年(45 - 84)增加到92 (63 - 130)ng·更易与肌酐−1(p = 0.001)和LTE4(15 - 24)19日至31日(巢族)ng·更易与肌酐−1(p < 0.001)。数据表示为基准与甘露醇后峰值水平的挑战。
尿浓度:a) 9α11β-prostaglandin (PG) F2;和b)白三烯(LT) E4超过60分钟前和后90分钟甘露醇挑战的安慰剂(○)色甘酸二钠(□)和formoterol (▿)。数据中位数(四分位范围)。·······:在两个1小时尿液收集,其中包括15分钟的治疗(▒)和时间(平均±sd12±3分钟)管理甘露醇的挑战(░;n = 14)。ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001与的意思是两个基线样本。
相比之下,没有明显的尿排泄增加9α,11β-pgf2在formoterol或SCG的存在。formoterol,甘露醇后的峰值水平的挑战是67(48 - 80)与69年相比(46 - 77)ng·更易与肌酐−1在基线(p = 1.0),在SCG的存在,post-challenge 9α水平最高,11β-pgf260岁(51 - 96)与66年相比(56 - 85)ng·更易与肌酐−1在基线(p = 0.952)。事实上,9α的水平,11β-pgf2甘露醇挑战后显著降低在90分钟与基线相比SCG的存在(p = 0.035)和低60和90分钟formoterol (p = 0.042, p = 0.049;图3⇑)。
相比之下,峰值与LTE的基线水平的尿排泄4在formoterol或SCG维持与安慰剂相比(图3 b⇑)。formoterol,水平从16(15 - 23)增加到26日(22日)ng·更易与肌酐−1(p < 0.001),在SCG的存在,从20 (17-28)28 (21-33)ng·更易与肌酐−1(p = 0.002)。
没有不同的基线水平的尿9α,11β-pgf2或LTE4三服药治疗之间的会话(分别为p = 0.931, p = 0.395)。
随着时间的推移尿排泄时表示为排泄下的面积的变化与时间曲线(AUC)之前和之后甘露醇挑战,下面的结果。比较9α的排泄,11β-pgf2甘露醇组之间的挑战后,显著降低水平被发现后和SCG formoterol治疗与安慰剂相比(分别为p = 0.013, p = 0.003)。没有区别这两种药物被发现(图4⇓)。在SCG 9α11β-pgf2排泄也减少甘露醇后挑战相比基线(p = 0.02)。没有明显减少9α,11β-pgf2排泄的formoterol与基线相比(p = 0.091;图4⇓)。相比之下,LTE的排泄4甘露醇后挑战仍然是增加的SCG和formoterol AUC每小时的增加并没有不同于安慰剂组(p = 0.6;图4 b⇓)。
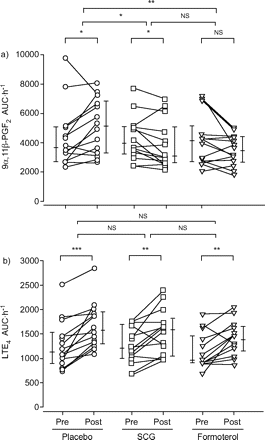
尿浓度:a) 9、11β-prostaglandin (PG) F2;和b)白三烯(LT) E4前(前)和后(post)甘露醇挑战的安慰剂,色甘酸二钠(SCG)或formoterol (n = 14)。个人数据显示;竖线表示中位数(四分位距)。AUC:面积排泄与时间曲线;ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
五个受试者服用经常吸入类固醇;这些课程通常容忍更高的剂量甘露醇。然而,没有尿排泄的差异组之间的介质,并不是采取吸入类固醇。
讨论
这是第一个报告演示在活的有机体内抑制肥大细胞释放的中介SCG和β2受体激动剂formoterol在回应一个渗透刺激。
它证实了以前的发现吸入的甘露醇与9α的尿排泄,增加11β-pgf2和LTE43。它扩展了以前的研究通过展示SCG的抑制作用和排泄的formoterol 9α,11β-pgf2。作为尿methylhistamine水平没有显著改变在协会mannitol-induced支气管狭窄的先前的研究3,注意力都集中在尿代谢物的排泄PGD2。
PGD2生产几乎只在肥大细胞是主要的环氧酶产品在这个细胞类型16,17。尽管嗜酸性粒细胞不具备形成PGD的能力2他们可以代谢PGD29α,11β-pgf2在体外18。尚不清楚这在多大程度上代谢途径导致的尿水平9α,11β-pgf2在目前的研究中找到。尽管嗜酸性粒细胞的数量增加哮喘患者的气道和嗜酸性粒细胞cysteinyl-LTs的来源19这些药物的活性,嗜酸性粒细胞的渗透刺激是未知的。
PGD对其他潜在的因素2有关巨噬细胞释放,有矛盾的结果及其形式PGD的能力2。Balter等。20.发现PGD2在肺泡巨噬细胞来源于支气管肺泡灌洗液从哮喘和对照组。然而,没有数据提出了关于大使用的抗体在免疫测定或细胞用于实验数据。Vicenzi等。21还发现PGD2在上层清液从支气管肺泡巨噬细胞刺激后14花生四烯酸。然而,缺乏信息使用的细胞数量很难解释他们的数据。
根据最近的数据,肺泡巨噬细胞的支气管肺泡灌洗液的健康受试者与甘露醇不产生免疫反应性的PGD刺激2高于控制水平(未发表的数据)。这与mannitol-stimulated肥大细胞,能产生45-fold增加PGD的水平2如果细胞相比22。因此,PGD的可能贡献2释放hyperosmolar刺激巨噬细胞的研究似乎可以忽略不计。
这一发现PGD的浓度的增加2代谢物9α,11β-pgf2在尿液的挑战与甘露醇与前面的建议是一致的甘露醇激活肥大细胞3。两个PGD2和9α,11β-pgf2是强有力的支气管收缩的在活的有机体内主要代理在支气管平滑肌的TP受体23。受试者患有哮喘显示肥大细胞的数量增加气管平滑肌层与正常对照组相比24痰和肥大细胞的数量增加25。同时,致命的哮喘患者表现出更高的脱粒肥大细胞在气道平滑肌与nonasthmatic控制26。
SCG可以防止组胺和PGD2人类分散肺肥大细胞释放免疫激活10- - - - - -12,从其他组织肥大细胞的准备12或来源13在体外。在目前的研究中,肥大细胞的重要性osmotically支气管收缩进一步支持由PGD SCG的效果2代谢物9α,11β-pgf2。9α的尿水平下降,11β-pgf2也与保护支气管狭窄即使SCG没有bronchodilatory效果。
预处理与formoterol更有效和更强有力的预处理和SCG至于甘露醇后的气道反应的挑战。formoterol提供的优越的保护很可能是由于的功能对立bronchoconstricting其他介质对气管平滑肌的影响。行动的两个不同的网站(即。肥大细胞和平滑肌)β2受体激动剂被用来解释提供的优越的保护一个β气溶胶的准备2受体激动剂与口服配方上气道狭窄,以应对运动27,28。β的屏蔽效应2受体激动剂对肥大细胞释放介质被认为是更重要的是预防运动诱发的支气管收缩比对平滑肌的影响29日。有一些气道狭窄的SCG可能是由于LTs无功能性formoterol提供的对抗。众所周知,SCG不是有效地抑制有限公司4全身的支气管收缩30.。
免疫刺激引起cysteinyl-LTs和PGD的释放2从肥大细胞在体外,而hyperosmolar甘露醇刺激会导致释放组胺和PGD2但是只有少量的LTs22,31日。β的影响2受体激动剂在中介发布以前在肥大细胞被调查在体外,显著抑制cysteinyl-LTs PGD2和组胺被发现后免疫刺激11,13。
目前发现借给小支持这一概念,肥大细胞的来源是LTs发布针对甘露醇刺激,还有其他细胞,嗜酸性粒细胞等可能的来源LTs生产的航空公司。LTC的重要版本4在甘露醇刺激后嗜酸性粒细胞报道32。在目前的研究中,LTE的尿排泄4保持不变,这一发现表明LT除了肥大细胞的来源。然而,LTs可能参与气道反应甘露醇作为肺功能的恢复的时间进程更快LT拮抗剂montelukast的存在7。发现LTE的释放4甘露醇后进入尿液持续挑战也支持LTs在维持气道的作用缩小甘露醇3。LTs维持气道的反应也是非常重要的运动33。cysteinyl-LT拮抗剂扎鲁司和组胺拮抗剂氯雷他定,鉴于在锻炼之前,明显抑制,但没有完全阻止气道反应运动34。这其中牵扯到的其他活性代谢物的重要性,如cyclooxygenase-derived产品。有证据表明,环氧酶抑制剂吲哚美辛,由吸入时,提供了一些预防运动性支气管收缩35。然而,在一项研究使用凝血恶烷受体拮抗剂,对运动性哮喘没有提供保护,尽管对手并抑制吸入PGD的影响2在相同的主题36。
尽管formoterol气道反应的保护作用甘露醇可以占到支气管平滑肌功能对立,这不是SCG的情况。结果,尽管没有明确的因果关系,表明SCG防止甘露醇引起的气道狭窄通过抑制PGD的释放2。formoterol也抑制了PGD的尿排泄增加2代谢物9α,11β-pgf2挑战与甘露醇后,这种模式的行动也可能导致其保护作用。的长效β2受体激动剂formoterol被选中,因为它可以作为粉和展品迅速开始行动。本研究的局限性是只有一个特定的测量柱状细胞中介PGD2与气道反应及其相关。未来的研究可能需要包括其他测量。
总之,甘露醇是已知的人类肺肥大细胞释放介质在体外31日,和特定的受体拮抗剂显示肥大细胞介质导致甘露醇引起的支气管收缩7。目前作者考虑呼吸道肥大细胞位于或接近表面前列腺素D的最可能的来源2因为甘露醇和交付的药物气溶胶。目前的发现与β的假设相一致2肾上腺素能受体受体激动剂和色甘酸二钠防止mannitol-induced支气管收缩,抑制肥大细胞中介发布。作者推测,这是,至少在某种程度上,通过释放的抑制前列腺素D2的重要性,进一步暗示在呼吸道肥大细胞激活对甘露醇的回应。
确认
作者要感谢c·佩里在准备手稿和技术援助即利林优秀实验室技术援助。使用甘露醇申请中描述这项研究是由美国专利号5817028年,国际PCT / AU95000086。专利属于中央悉尼地区卫生服务(现在称为南西悉尼地区卫生服务)和许可Pharmaxis有限公司(澳大利亚悉尼两个)。
- 收到了2005年7月4日。
- 接受2005年12月16日。
- ©人期刊有限公司