摘要gydF4y2Ba
颗粒物空气污染与呼吸道疾病有关,并具有细胞毒性和促炎症作用。研究了柴油机废气颗粒(DEP)对A549肺上皮细胞增殖和凋亡的影响。gydF4y2Ba
当剥夺血清(血清饥饿)时,上皮细胞数量下降,但DEP(5-200µg·mLgydF4y2Ba−1gydF4y2Ba)阻止了这一切。采用流式细胞术分析碘化丙啶(PI)染色,DEP(10µg·mLgydF4y2Ba−1gydF4y2Ba48 h后,细胞周期S期细胞数量由12.85增加到18.75%,逆转血清饥饿诱导的GgydF4y2Ba0/1gydF4y2Ba逮捕。DEP还降低了血清饥饿后观察到的annexin V/PI双表达的凋亡细胞的增加(从28.35%到15.46%)。抗氧化剂,gydF4y2BaNgydF4y2Ba乙酰半胱氨酸(NAC);n端c-jun激酶抑制剂SP600125(33µM)和核因子-κB抑制剂SN50(33µM)抑制depp诱导的细胞数量增加。NAC抑制dep诱导的GgydF4y2Ba0/1gydF4y2Ba以及S和G细胞的增加gydF4y2Ba2gydF4y2Ba/ M阶段。p21表达gydF4y2BaCIP1 / WAF1gydF4y2Ba血清饥饿时的mRNA和蛋白含量因DEP而降低。gydF4y2Ba
总之,柴油废气颗粒通过诱导细胞周期进程和防止凋亡,包括氧化应激和抑制p21的过程来阻止血清饥饿导致的A549上皮细胞的减少gydF4y2BaCIP1 / WAF1gydF4y2Ban端c-jun激酶和核因子-κB的表达及刺激。因此,低剂量柴油机废气颗粒暴露可导致肺上皮细胞增生。gydF4y2Ba
随着柴油发动机的使用越来越多,颗粒物空气污染越来越被认为是一种主要的公共健康危害,并是肺部和心血管疾病负担的一个因素。因此,颗粒物空气污染与肺功能受损、肺功能生长缺陷、哮喘症状恶化以及哮喘和慢性阻塞性肺疾病急诊次数增加之间存在密切联系gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba.此外,据报道,生活在大都市地区的成年人的全因死亡率、心肺死亡和肺癌死亡率与颗粒物空气污染水平之间存在关系gydF4y2Ba3.gydF4y2Ba- - - - - -gydF4y2Ba5gydF4y2Ba.gydF4y2Ba
微粒对肺部有害影响的机制尚不清楚。气道上皮细胞构成了对抗颗粒的第一道先天免疫防线,一旦暴露于颗粒物,就会产生炎症介质,如白细胞介素(IL)-8、粒细胞-巨噬细胞集束刺激因子(GM-CSF)、RANTES和可溶性细胞间粘附分子(sICAM)-1gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba活性氧,过氧化氢(HgydF4y2Ba2gydF4y2BaOgydF4y2Ba2gydF4y2Ba)和超氧化物(OgydF4y2Ba2gydF4y2Ba−gydF4y2Ba)gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,可激活转录因子、核因子(NF)-κB和激活蛋白(AP)-1通路gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba.此外,诸如直径为10微米的颗粒(PMgydF4y2Ba10gydF4y2Ba)也会导致细胞坏死和细胞凋亡gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba.小鼠气道上皮细胞增殖的剂量依赖性增加gydF4y2Ba在活的有机体内gydF4y2Ba也有报道称gydF4y2Ba14gydF4y2Ba.增殖和凋亡的过程可能同时发生gydF4y2Ba15gydF4y2Ba.微粒对细胞数量调节的影响可能与特定的细胞类型、不同浓度的微粒和物种之间的差异有关。它们也可能是由于颗粒对调节细胞凋亡和增殖的信号转导途径的影响的平衡。gydF4y2Ba
颗粒物诱导气道上皮细胞存活或增殖或死亡的分子机制也不清楚。NF-κB活化是颗粒暴露的细胞效应,与细胞存活和诱导凋亡有关gydF4y2Ba16gydF4y2Ba.在一些氧化应激模型中,丝裂原活化蛋白激酶(MAPK)通路的激活gydF4y2Ba通过gydF4y2Bac-jun n -末端激酶(JNK)与程序性细胞死亡或凋亡有关gydF4y2Ba17gydF4y2Ba,gydF4y2Ba18gydF4y2Ba.在一定情况下,JNK还可能增加细胞存活,并在细胞增殖中发挥作用gydF4y2Ba19gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba.细胞周期、生长阻滞和分化的最终关键决定因素是周期蛋白依赖性激酶抑制剂p21gydF4y2BaCIP1 / WAF1gydF4y2Ba21gydF4y2Ba后者对氧化应激反应强烈gydF4y2Ba22gydF4y2Ba,gydF4y2Ba23gydF4y2Ba;然而,颗粒物对p21的影响gydF4y2BaCIP1 / WAF1gydF4y2Ba肺上皮细胞的表达尚不清楚。gydF4y2Ba
目前调查的目的是提高对细胞分子机制的理解,通过颗粒物造成气道上皮损伤。为了解决这一问题,研究了柴油废气颗粒(DEP)对人上皮A549细胞系的活力、增殖和死亡的影响。在现在gydF4y2Ba在体外gydF4y2Ba模型中,这些细胞的存活和增殖状态取决于血清的存在,血清的存在使细胞处于增殖状态,而血清的去除导致细胞死亡gydF4y2Ba24gydF4y2Ba.该模型可能反映了气道炎症过程中渗出血浆的影响;正常情况下,气道上皮细胞不与血清因子接触。假设DEP的作用取决于血清是否存在,因为血清的存在决定了基底细胞周期的状态。也有假设认为,细胞周期的结果取决于JNK和NF-κB的激活和p21的表达gydF4y2BaCIP1 / WAF1gydF4y2Ba在这些过程中。gydF4y2Ba
研究发现,低浓度DEP可抑制去血清时的细胞凋亡,并引起气道上皮细胞增殖,其作用是通过激活JNK和NF-κB诱导氧化应激介导的。这些机制表明,在正常的、未发炎的上皮细胞中,低剂量暴露于DEP可通过防止细胞凋亡来增加上皮细胞的存活率。gydF4y2Ba
方法gydF4y2Ba
柴油机排气颗粒悬浮液的制备gydF4y2Ba
DEP是H. Takano(日本筑波国立环境研究所)赠送的礼物。它们是从一台4jb1型轻型四缸2.74 l五十铃柴油发动机(五十铃汽车公司,日本东京)中收集的,使用标准柴油,转速为1500转/分,负载为10公斤·米gydF4y2Ba−1gydF4y2Ba扭矩。如前所述收集DEPgydF4y2Ba8gydF4y2Ba,颗粒平均直径为0.4 μ mgydF4y2Ba25gydF4y2Ba.纯化后的DEP悬浮在无色的Dulbecco改性Eagle培养基(DMEM;Gibco, Invitrogen,佩斯利,英国)含2毫米gydF4y2BalgydF4y2Ba-谷氨酰胺和1mm丙酮酸钠(无血清培养基(SF);Sigma Chemical Company, Poole, UK),浓度为1-200µg·mLgydF4y2Ba−1gydF4y2Ba,如前所述gydF4y2Ba7gydF4y2Ba.gydF4y2Ba
A549细胞培养及细胞活力测定gydF4y2Ba
A549细胞(ATCC, LGC Promochem, Teddington, UK)使用含10%胎牛血清(FCS)和2 mM的苯酚红(-)DMEM (Gibco, Invitrogen)培养gydF4y2BalgydF4y2Ba-谷氨酰胺(Sigma Chemical Company) 12孔板(Falcon;BD Biosciences, Oxford, UK)培养72小时,直到达到70-80%的汇合度,此时培养基被SF取代。24小时后,DEP悬浮液(0、5、10、50、100和200µg·mLgydF4y2Ba−1gydF4y2Ba)在研究药物(包括抗氧化剂NAC、催化抗氧化剂和超氧化物模拟物AEOL10113)不存在或不存在的情况下,分别添加24、48和72小时gydF4y2Ba26gydF4y2Ba, JNK抑制剂,SP600125gydF4y2Ba27gydF4y2Ba,以及转录因子NF-κB p50亚基易位的抑制剂SN50gydF4y2Ba28gydF4y2Ba.作为阳性对照,A549细胞在含10% FCS的培养基中培养。活细胞数量的测量是基于四唑盐3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑溴化(MTT)被与代谢活性相关的线粒体酶还原为不溶性甲醛染料,表明活细胞。因此,该试验可用于检测细胞毒性和细胞增殖gydF4y2Ba29gydF4y2Ba.用含1mg·mL的SF代替培养基gydF4y2Ba−1gydF4y2BaMTT (Sigma Chemical Company),在37°C下孵育15分钟。除去MTT溶液,代之以二甲基亚砜(DMSO),并在550nm处使用比色板阅读器读取颜色变化。gydF4y2Ba
细胞周期进展和凋亡的测量gydF4y2Ba
如前所述,使用碘化丙啶(PI)染色细胞,通过荧光激活细胞分选分析测量细胞周期进展gydF4y2Ba30.gydF4y2Ba.根据制造商说明书(Becton Dickinson Pharmingen, Oxford, UK),使用细胞凋亡检测试剂盒测定膜联蛋白V和PI结合。为了区分细胞凋亡和坏死,用膜联蛋白V(绿色荧光)和PI(红色荧光)对细胞进行双染色。简单地说,细胞(10万个细胞·样本gydF4y2Ba−1gydF4y2Ba)在冷PBS中洗涤2次,悬浮在含有异硫氰酸荧光素偶联膜蛋白V (10 μg·mL)的结合缓冲液中gydF4y2Ba−1gydF4y2Ba)和PI (10 μg·mLgydF4y2Ba−1gydF4y2Ba).细胞悬液在黑暗中培养15分钟,然后使用Becton Dickinson FACScan流式细胞仪采集信号。使用Cell Quest软件(BD Biosciences, San Jose, CA, USA)对每个样本共10,000个事件进行分析。gydF4y2Ba
西方墨点法gydF4y2Ba
用含有蛋白酶抑制剂(200 μ M Na)的冰冷PBS冲洗细胞gydF4y2Ba3.gydF4y2Ba签证官gydF4y2Ba4gydF4y2Ba, 2 mM苯甲基磺酰氟),并在放射免疫沉淀试验缓冲液(含有0.5%脱氧胆酸钠、0.1%十二烷基硫酸钠(SDS)、1% Igepal®(Sigma化学公司)和完全蛋白酶抑制剂鸡尾酒片(罗氏诊断公司,英国路易斯)的PBS中溶解)。从烧瓶中刮取细胞,超声溶解,然后离心(10,000×gydF4y2BaggydF4y2Ba, 4°C, 4分钟)。使用Bradford蛋白测定法(Bio-Rad Laboratories, Hemel Hempstead, UK)测定蛋白质浓度。裂解物煮沸5分钟,总蛋白提取物(20µg·lanegydF4y2Ba−1gydF4y2Ba)通过sds -聚丙烯酰胺凝胶电泳(PAGE)在16% Tris-SDS聚丙烯酰胺预制凝胶(Novex;Invitrogen,佩斯利,英国)。分离的蛋白质被电转移到硝化纤维膜(Amersham Biosciences, Amersham, UK),如前所述gydF4y2Ba31gydF4y2Ba,和兔抗人p21gydF4y2BaCIP1 / WAF1gydF4y2Ba抗体(Santa Cruz Biotechnology, Calne, UK)在1:200的稀释中使用。通过制造商推荐的增强化学发光来观察条带(Hybond ECL;Amersham Pharmacia Biotech, Little Chalfont,英国),并使用密度计与Grab-It和GelWorks软件(UVP,剑桥,英国)进行量化。p21的每个通道的单个波段光密度值gydF4y2BaCIP1 / WAF1gydF4y2Ba表示为与内控β-肌动蛋白光密度值的比值。gydF4y2Ba
p21的定量逆转录聚合酶链反应gydF4y2BaCIP1 / WAF1gydF4y2Ba
收集细胞进行总RNA分离。使用市售试剂盒提取细胞总RNA (RNeasy;Qiagen, Crawley, UK)和进行反向转录(Omniscript RT;试剂盒)。p21基因转录水平gydF4y2BaCIP1 / WAF1gydF4y2Ba和管家基因GAPDH在tor- gene 3000 PCR仪(Corbett Research, Sydney, Australia)上使用Taqman系统(Applied Bioscience, Arlington, VA, USA)进行实时PCR定量。GAPDH引物对购自Applied Bioscience, p21引物对购自Applied BiosciencegydF4y2BaCIP1 / WAF1gydF4y2Ba设计如下所述。(向前;F) 5 ' -CAGACCAGCATGACAGATTTC,(反向;R) 3 ' -GGCTTCCTCTTGGAGAAGAT, (Taqman探针)5 ' -FAM-TACCACTCCAAACGCCGGCT-TAMRA。通过将感兴趣基因的计算值除以管家基因值,对每个cDNA样本中GAPDH表达的cDNA浓度变化进行校正。gydF4y2Ba
研究药物gydF4y2Ba
NAC (Sigma Chemical Company)和SN50 (NF-κB抑制剂;Calbiochem,诺丁汉,英国)溶解在DMEM中,并在相同的介质中进一步稀释到所需的工作浓度。一种催化抗氧化剂,AEOL10113,化学名称为锰(III)gydF4y2Ba内消旋gydF4y2Ba-tetrakis - (gydF4y2BaN -gydF4y2Ba甲基吡啶-2-基)卟啉(来自J.D. Crapo,美国科罗拉多州丹佛市国家犹太医学和研究中心的礼物)溶解在DMEM中。JNK抑制剂SP600125(来自B. Bennett, Celgene, San Diego, CA, USA的礼物)溶解在50 mM DMSO的原液中,然后在SF中稀释到所需的浓度。DMSO最终浓度不大于0.33%体积/体积。gydF4y2Ba
统计分析gydF4y2Ba
数据分析采用非配对t检验或单因素方差分析/Bonferroni's多重比较检验。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba.p值<0.05被认为是显著的。gydF4y2Ba
结果gydF4y2Ba
DEP对A549细胞数量、细胞周期及凋亡的影响gydF4y2Ba
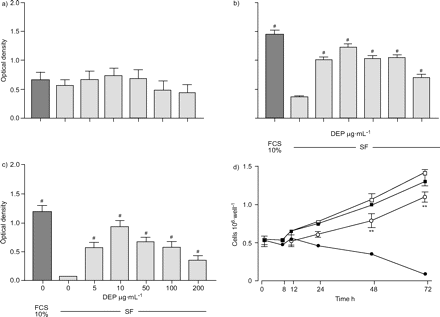
A549细胞在10% FCS的作用下呈时间依赖性生长,融合时间为48h。在FCS(1,3.3和10%)存在时,DEP为10µg·mLgydF4y2Ba−1gydF4y2Ba对48小时内的细胞数量没有影响。在没有血清的情况下,48和72 h后细胞数量减少(表1gydF4y2Ba⇓gydF4y2Ba图1gydF4y2Ba⇓gydF4y2Ba).MTT染色显示,A549细胞用5 ~ 200µg·mL孵育gydF4y2Ba−1gydF4y2BaDEP在24 h内不影响其生存能力;在48 h时,DEP可防止血清去除引起的细胞数量减少,在10µg·mL时效果最大gydF4y2Ba−1gydF4y2Ba(p < 0.0001;表1gydF4y2Ba⇓gydF4y2Ba图1gydF4y2Ba⇓gydF4y2Ba).72 h也得到了类似的结果。为了确认DEP(10µg·mLgydF4y2Ba−1gydF4y2Ba)诱导A549细胞增殖,重复实验,用血球仪直接计数孔中的A549细胞。如图1d所示gydF4y2Ba⇓gydF4y2Ba,在没有FCS的情况下,细胞数量减少,但DEP在培养48和72 h时诱导细胞数量增加。在单独存在FCS时,A549细胞数量增加,但在DEP存在时没有进一步增加。这些结果证实了MTT法获得的数据。gydF4y2Ba
柴油机废气微粒(DEP;0 - 200µg·毫升gydF4y2Ba−1gydF4y2Ba)在无血清培养基(SF)中a) 24、b) 48和c) 72 h后,通过3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四氮唑法评估A549细胞的活力。在10%胎牛血清(FCS)的存在下生长的细胞数量进行比较。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少五个实验。gydF4y2Ba#gydF4y2Ba: p < 0.0001gydF4y2Ba与gydF4y2Ba0µg·毫升gydF4y2Ba−1gydF4y2BaDEP(10µg·mL)的影响为DEP. dgydF4y2Ba−1gydF4y2Ba)在72小时内,细胞数量上是否存在FCS,直接通过血细胞测定法测量。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少有三个实验。**p与FCS(-)比较<0.01。□:FCS (+) + DEP;▪:FCS (+);○:FCS (-) + DEP;•:FCS(-)。gydF4y2Ba
柴油废气颗粒(DEP)对A549上皮细胞数48 h的影响将3-(4,5-二甲基噻唑-2-基)-2,5-二苯四唑溴化至不溶性甲醛染料,在550nm光密度下测定48小时后细胞数量gydF4y2Ba
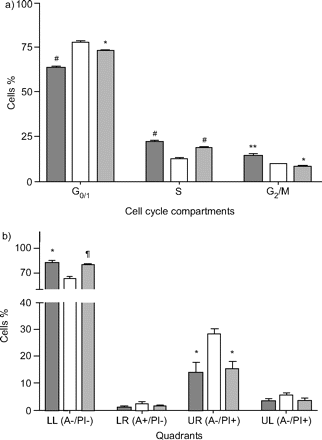
其次,DEP(10µg·mLgydF4y2Ba−1gydF4y2Ba)对细胞周期和凋亡的影响。当细胞处于血清饥饿状态时,GgydF4y2Ba0/1gydF4y2Ba相数量增加,S和G相数量增加gydF4y2Ba2gydF4y2Ba/M期较10% FCS残留细胞减少。DEP(10µg·mLgydF4y2Ba−1gydF4y2Ba)增加S期血清饥饿A549细胞百分比(18.8±0.46%;p<0.0001),与48 h后未处理的血清饥饿细胞(12.9±0.66%)相比,GgydF4y2Ba0/1gydF4y2Ba(73.2±0.16%;p<0.0001)和GgydF4y2Ba2gydF4y2Ba/ M(8.1±0.42%;p<0.02)相比较血清饥饿细胞(GgydF4y2Ba0/1gydF4y2Ba77.4±0.66%gydF4y2Ba2gydF4y2Ba/M 9.75±0.37%)gydF4y2Ba⇓gydF4y2Ba).血清细胞饥饿48小时增加膜联蛋白V-和PIgydF4y2Ba-gydF4y2Ba与10% FCS中剩下的细胞相比,凋亡细胞呈阳性(SF 28.35±2.03)gydF4y2Ba与gydF4y2BaFCS 13.94±3.95;p<0.05),但未引起pi阳性、膜联蛋白v阴性细胞(代表坏死细胞)的变化。因此,经膜联蛋白V和PI阳性染色显示,DEP可阻止血清饥饿时凋亡细胞的增加(15.46±2.79%)gydF4y2Ba与gydF4y2Ba28.35±2.03%;p < 0.03;图2 bgydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
a) 10µg·mL效应gydF4y2Ba−1gydF4y2Ba柴油废气颗粒(DEP)对A549细胞培养48 h后细胞周期的影响。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少有三个实验。*: p < 0.05;* *: p < 0.01;gydF4y2Ba#gydF4y2Ba: p < 0.0001gydF4y2Ba与gydF4y2Ba无血清治疗。b) DEP的作用(10µg·mL .gydF4y2Ba−1gydF4y2Ba通过流式细胞术分析膜联蛋白V (A)和碘化丙啶(PI)对A549细胞在无血清培养基(SF)培养48小时后凋亡或坏死的影响。左下=活细胞;LR:右下=凋亡细胞;UR:右上=晚期凋亡/早期坏死细胞;UL:左上=坏死细胞。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少有三个实验。*: p < 0.05;gydF4y2Ba¶gydF4y2Ba: p < 0.005gydF4y2Ba与gydF4y2BaSF-treated细胞。gydF4y2Ba
的影响gydF4y2BaNgydF4y2Ba乙酰半胱氨酸gydF4y2Ba
3.3和10 mM的NAC对SF的细胞数量没有影响,但在33 mM时,细胞数量显著增加,这表明氧化机制在血清饥饿诱导的细胞死亡中很重要。相反,对DEP(10µg·mL)诱导的细胞增加有抑制作用gydF4y2Ba−1gydF4y2Ba), NAC分别为10和33 mM,分别增加27%和35%,发生在48小时(图3agydF4y2Ba⇓gydF4y2Ba).这表明氧化剂可能在DEP诱导的细胞数量增加中起介导作用。gydF4y2Ba
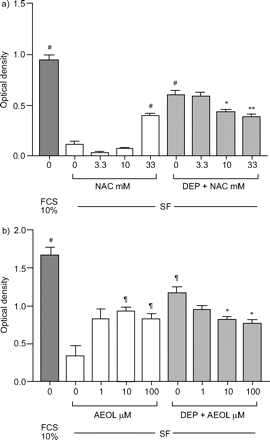
a)的影响gydF4y2BaNgydF4y2Ba-乙酰半胱氨酸(NAC)和b) AEOL10113 (AEOL)在48 h对柴油机废气颗粒(DEP;10µg·毫升gydF4y2Ba−1gydF4y2Ba)添加到无血清培养基(SF)中生长的细胞中。在10%胎牛血清(FCS)的存在下生长的细胞数量进行比较。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少有三个实验。gydF4y2Ba#gydF4y2Ba: p < 0.0001gydF4y2Ba与gydF4y2Ba科幻小说;gydF4y2Ba¶gydF4y2Ba: p < 0.05gydF4y2Ba与gydF4y2Ba科幻小说;*: p<0.05, **: p<0.01gydF4y2Ba与gydF4y2Ba管理。gydF4y2Ba
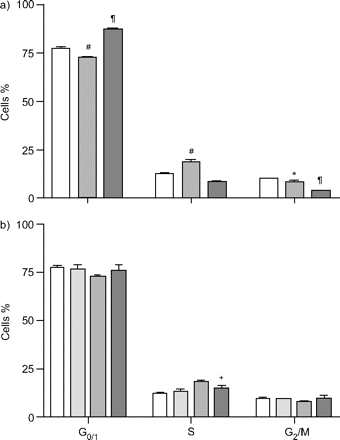
NAC (10 mM)抑制dep诱导的A549 S期细胞数量的增加(p<0.0001),而导致G期细胞数量的增加gydF4y2Ba0/1gydF4y2Ba阶段(p < 0.001)。G中细胞的百分比gydF4y2Ba2gydF4y2Ba与单独使用DEP相比,/M相进一步减少了10 mM NAC (p<0.0001;见图4agydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
a)的影响gydF4y2BaNgydF4y2Ba-乙酰半胱氨酸(NAC) (*: p<0.05和gydF4y2Ba#gydF4y2Ba: p < 0.0001gydF4y2Ba与gydF4y2Ba无血清培养基(SF);gydF4y2Ba¶gydF4y2Ba: p < 0.0001gydF4y2Ba与gydF4y2BaSF+柴油排气患者(DEP))和b) AEOL10113(10µM) (gydF4y2Ba+gydF4y2Ba: p < 0.05gydF4y2Ba与gydF4y2BaSF+DEP)对A549细胞培养48 h后细胞周期进展的影响(10µg·mL)gydF4y2Ba−1gydF4y2BaDEP结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少两个实验(NAC:三个实验;对于AEOL:两个实验)。a)□:SF;烧嘴句子:SF+DEP (10 μg·mLgydF4y2Ba−1gydF4y2Ba);▒:SF+DEP+NAC(10米gydF4y2Ba米gydF4y2Ba).b)□:SF;░:SF+10米gydF4y2Ba米gydF4y2BaAEOL10113;烧嘴句子:SF+DEP (10 μg·mLgydF4y2Ba−1gydF4y2Ba);▒:sf + dep + aeol10113(10µgydF4y2Ba米gydF4y2Ba).gydF4y2Ba
AEOL10113的效果gydF4y2Ba
在DEP存在时,AEOL10113引起细胞数量的剂量依赖性下降(10µg·mLgydF4y2Ba−1gydF4y2Ba),在10 μ M和100 μ M时影响显著。在这些浓度下,当A549细胞单独缺乏血清时,细胞数量也显著增加(图3b)gydF4y2Ba⇑gydF4y2Ba).A549细胞与AEOL10113(10µM)孵育也导致10µg·mL诱导的s期细胞百分比显著降低gydF4y2Ba−1gydF4y2Ba大(p < 0.05;图4 bgydF4y2Ba⇑gydF4y2Ba).gydF4y2Ba
JNK抑制剂的作用gydF4y2Ba
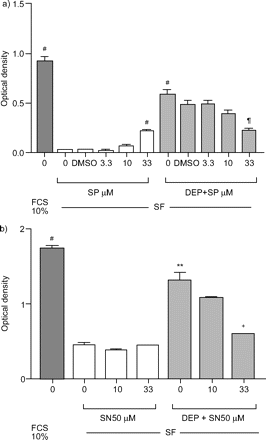
当JNK抑制剂(SP600125)在3.3 μ M或10 μ M时都没有作用,在33 μ M时,它增加了SF单独的细胞数量(平均光密度(OD)从0.033±0.003增加到0.219±0.015;P <0.0002)gydF4y2Ba⇓gydF4y2Ba).相反,SP600125(33µM)引起10µg·mL诱导的细胞数量减少gydF4y2Ba−1gydF4y2BaDEP(图5a .gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
c-jun n端激酶抑制剂a) SP 600125 (SP)和核因子-κB抑制剂SN50在48 h对柴油机废气颗粒(DEP;10µg·毫升gydF4y2Ba−1gydF4y2Ba)添加到无血清培养基(SF)中生长的细胞中。在10%胎牛血清(FCS)的存在下生长的细胞数量进行比较。对于a),显示了控制二甲基亚砜(DMSO)实验,因为SP600125溶解在0.33% DMSO中。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少三个实验;gydF4y2Ba#gydF4y2Ba: p<0.0001, **: p<0.01gydF4y2Ba与gydF4y2Ba科幻小说;gydF4y2Ba+gydF4y2Ba: p < 0.01gydF4y2Ba与gydF4y2Ba部;gydF4y2Ba¶gydF4y2Ba: p < 0.0001gydF4y2Ba与gydF4y2Ba0.33% DMSO +管理。gydF4y2Ba
NF-κB抑制剂的作用gydF4y2Ba
SN50对SF细胞数量无影响,但剂量依赖性地抑制了DEP对A549细胞数量的增强(10µg·mL)gydF4y2Ba−1gydF4y2Ba),在33µM时影响显著(平均OD从1.319±0.102下降到0.595±0.004;p < 0.01;图5 bgydF4y2Ba⇑gydF4y2Ba).gydF4y2Ba
DEP对p21的影响gydF4y2BaCIP1 / WAF1gydF4y2Ba表达式gydF4y2Ba
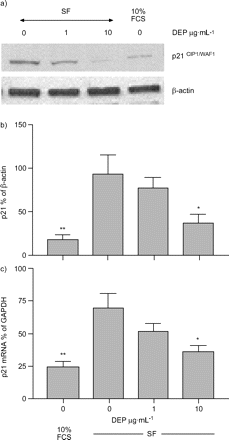
p21gydF4y2BaCIP1 / WAF1gydF4y2Ba血清饥饿48小时后蛋白表达增加,与持续用10% FCS培养的细胞相比(p<0.01)。添加DEP到sf处理的细胞中,剂量依赖性地降低了p21gydF4y2BaCIP1 / WAF1gydF4y2Ba蛋白表达(p<0.05;图6gydF4y2Ba⇓gydF4y2Bab). p21的mRNA表达gydF4y2BaCIP1 / WAF1gydF4y2BaDEP在10µg·mL时降低mRNAgydF4y2Ba−1gydF4y2Ba(p < 0.05;图6 cgydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
柴油机废气微粒(DEP;0,1和10µg·mLgydF4y2Ba−1gydF4y2Ba)第21页gydF4y2BaCIP1 / WAF1gydF4y2BaWestern blot检测蛋白表达(a和b)和定量PCR检测A549细胞在无血清培养基(SF)培养48小时后的mRNA表达(c)。a)显示有代表性的Western印迹,并显示仅在10%胎牛血清(FCS)中培养的效果。结果以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba至少有三个实验。*: p<0.05, **: p<0.01gydF4y2Ba与gydF4y2Ba细胞在无血清条件下,未暴露于DEP。gydF4y2Ba
讨论gydF4y2Ba
下gydF4y2Ba在体外gydF4y2Ba在细胞培养的条件下,在血清因子的退出下,A549细胞在48小时内发生程序性细胞死亡,活细胞数量减少。在这些条件下,发现DEP提高了细胞活力,但不以剂量依赖的方式,在浓度为10µg·mL时效果最大gydF4y2Ba−1gydF4y2Ba.低剂量DEP至少抑制了50%血清戒断时细胞死亡的增加。DEP还能预防GgydF4y2Ba0/1gydF4y2Ba细胞阻滞,同时在无血清条件下提高细胞周期S期的细胞百分比。DEP可减少A549细胞凋亡,可见孵育48 h后膜联蛋白V和PI双染色细胞数量减少;活细胞百分比(膜联蛋白V/PI阴性)也增加。因此,DEP可以防止血清停药引起的细胞数量减少;换句话说,它诱导了一种增殖反应,并抑制了血清饥饿条件下发生的细胞凋亡。尽管所获得的数据有局限性gydF4y2Ba在体外gydF4y2Ba在肺泡上皮细胞系上gydF4y2Ba在活的有机体内gydF4y2Ba在这种情况下,这些数据将表明,在相对低浓度的DEP暴露会导致正常表面上皮细胞的增殖,而不是处于炎症状态。这可能反过来导致上皮层的增加,并可能导致化生变化。gydF4y2Ba
抗氧化剂NAC和AEOL10113对血清饥饿A549细胞的作用是增加它们的存活率,这对超氧化物歧化酶模拟AEOL10113尤其有效。另一方面,抗氧化剂在一定程度上抑制了dep对A549细胞活力和细胞周期的影响。NAC抑制JNK、p38-MAPK和氧化还原敏感AP-1的激活,以及NF-κB转录因子的活性,这些转录因子调节着许多基因的表达gydF4y2Ba32gydF4y2Ba.此外,NAC通过激活细胞外信号调节激酶途径防止细胞凋亡并促进生存。这些抗氧化剂的作用是减少S期细胞,从而阻止DNA复制。因此,氧化应激产物是DEP抑制细胞凋亡和刺激血清饥饿细胞生长的原因。相反,在未暴露于DEP的血清饥饿细胞上,氧化应激产物参与细胞凋亡并降低细胞生长。这些数据表明,抗氧化剂可能有助于抵消DEP暴露对气道上皮细胞的增殖效应;然而,抗氧化剂的抑制作用只是部分的。gydF4y2Ba
为了进一步阐明DEP影响细胞存活的潜在信号通路,研究了JNK选择性抑制剂SP600125的作用。SP600125还抑制了dep诱导的细胞活力的增加,与抗氧化剂的作用类似,增加了血清饥饿细胞的细胞活力。因此,DEP对JNK和氧化应激的激活与细胞活力的增加有关,而血清饥饿不仅与JNK和氧化应激的激活有关,而且通过诱导凋亡与细胞活力的降低有关。SP600125已被证明抑制腺癌细胞系KB-3的增殖,具有类似的剂量依赖性。反义寡核苷酸对JNK2的抑制作用与JNK类似,说明SP600125的作用是通过选择性抑制JNK的激活来实现的gydF4y2Ba19gydF4y2Ba.JNK在血清饥饿的A549细胞中被激活,与凋亡的启动同时发生gydF4y2Ba24gydF4y2Ba.因此,JNK通路可能与细胞凋亡和生存信号传递有关gydF4y2Ba20.gydF4y2Ba.gydF4y2Ba
SN50抑制了NF-κB的核转位,可抑制dep诱导的细胞活力,但不能单独抑制血清饥饿的影响,这表明NF-κB激活在dep诱导的细胞凋亡抑制中的重要性。NF-κB通过转录激活参与肺部炎症反应的细胞因子、趋化因子和粘附分子基因。dep诱导人支气管上皮细胞释放IL-8、GM-CSF和RANTES等细胞因子,以及粘附分子sICAM-1可能是NF-κB活化的继发作用gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba.上皮细胞暴露于DEP也会导致双调节蛋白的表达和分泌增加,双调节蛋白是表皮生长因子受体的配体,进而诱导GM-CSF的分泌gydF4y2Ba33gydF4y2Ba.然而,也有可能双调节蛋白直接调节细胞凋亡gydF4y2Ba34gydF4y2Ba.gydF4y2Ba
已有研究表明,DEP可抑制血清抽提诱导的p21表达增加gydF4y2BaCIP1 / WAF1gydF4y2BamRNA和蛋白质。DEP可能通过抑制p21对A549细胞的凋亡起至少部分的预防作用gydF4y2BaCIP1 / WAF1gydF4y2Ba因为它是调节细胞周期、生长阻滞和分化的关键蛋白之一gydF4y2Ba35gydF4y2Ba,对氧化应激有反应gydF4y2Ba23gydF4y2Ba.因此,DEP抑制p21gydF4y2BaCIP1 / WAF1gydF4y2Ba表达可能会阻止GgydF4y2Ba0/1gydF4y2Ba细胞停滞,由血清去除引起。A549细胞在血清饥饿状态下表达高水平p21gydF4y2BaCIP1 / WAF1gydF4y2Ba,而在10% FCS中培养的细胞p21水平较低,在这些条件下,p21被调节gydF4y2BaCIP1 / WAF1gydF4y2Ba可能控制细胞周期,因为它结合并灭活周期蛋白D/周期蛋白依赖性激酶复合物。gydF4y2Ba
已知DEP对不同类型肺细胞的不良影响涉及氧化应激途径gydF4y2Ba10gydF4y2Ba,gydF4y2Ba36gydF4y2Ba,gydF4y2Ba37gydF4y2Ba.因此,DEP及其有机提取物诱导活性氧的生成,如HgydF4y2Ba2gydF4y2BaOgydF4y2Ba2gydF4y2Ba和OgydF4y2Ba2gydF4y2Ba−gydF4y2Ba在巨噬细胞和人支气管上皮细胞gydF4y2Ba13gydF4y2Ba,gydF4y2Ba38gydF4y2Ba,gydF4y2Ba39gydF4y2Ba,进而激活NF-κB和AP-1等转录因子gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba.氧化应激可在巨噬细胞和支气管上皮细胞中启动促炎作用gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba13gydF4y2Ba,gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba由磷酸化依赖的细胞信号通路介导,包括MAPK通路的激活。数据表明,DEP具有直接作用,部分通过氧化应激直接抑制血清饥饿条件下发生的细胞凋亡,从而增加细胞数量,并在此条件下激活JNK和NF-κB。gydF4y2Ba
总之,目前的观察结果可能具有一些临床意义。正常情况下,上皮细胞完整,无血清,无炎症反应,上皮细胞处于增殖细胞和凋亡细胞的平衡翻转状态。本研究的数据表明,在低水平的暴露下,柴油废气颗粒可能通过防止细胞凋亡诱导正常上皮细胞的增生,可能形成化生上皮的基础。然而,在炎症和血清外渗的情况下,柴油废气颗粒对细胞数量的影响被血清的影响所掩盖,血清本身会诱导细胞增殖。氧化应激因子可能是柴油机排气颗粒诱导的上皮细胞凋亡的基础,抗氧化剂可以防止柴油机排气颗粒诱导的上皮细胞凋亡的增加。核因子-κB和c-jun n -末端激酶通路抑制剂也可能有用。gydF4y2Ba
致谢gydF4y2Ba
作者感谢J. Crapo提供的AEOL10113和H. Takano提供的柴油排气颗粒。gydF4y2Ba
- 收到了gydF4y2Ba2005年2月5日gydF4y2Ba
- 接受gydF4y2Ba二六年一月四日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba