文摘
Eosinophil-associated条件,如哮喘和嗜酸性支气管炎,慢性持续性咳嗽有关,通常对皮质类固醇治疗。
这个案例研究报告的持续咳嗽与gastro-oesophageal返流(气油比)和hypereosinophilia有关。治疗气油比与质子泵抑制剂和fundoplication没有控制的咳嗽。然而,高剂量强的松,但不吸入糖皮质激素。
的存在FIP1L1-PDGFRA在证实了髓细胞荧光融合基因原位杂交分析使用CHIC2作为一个代理标记删除。咳嗽和其他疾病的特征是随后抑制酪氨酸激酶抑制剂,伊马替尼。
这是第一例hypereosinophilic综合症引起的持续性咳嗽为特征FIP1L1-PDGFRA融合基因和异常的酪氨酸激酶活性。
慢性咳嗽是一种常见的临床问题1,2。在后滴鼻哮喘,或rhino-sinusitis gastro-oesophageal回流是最常见的慢性咳嗽的原因3,但在许多患者,无法确定原因尽管彻底调查和治疗经验4,5。条件与嗜酸性粒细胞的航空公司,如哮喘和嗜酸性支气管炎,一直与慢性咳嗽和皮质类固醇治疗,抑制嗜酸性粒细胞,通常是有效的咳嗽等控制。本研究描述了一个病人持续咳嗽有关FIP1L1-PDGFRA积极hypereosinophilia,最近被描述6。这个咳嗽是由高剂量口服皮质类固醇疗法和获得一个特定抑制剂,持续活跃的酪氨酸激酶,伊马替尼。
病例报告
以前好54-yr-old男科学家,拆弹专家在2001年发明了一种慢性咳嗽。他是调查使用肺量测定法,计算x线断层照片的肺和支气管活检;都是正常的。然而,他的嗜酸性粒细胞计数为1.7×109·L−1。他与吸入糖皮质激素治疗3个月,一个星期的课程组没有好处。他抱怨的正则集gastro-oesophageal回流和一个24小时的录音食管pH值显示重要的胃酸倒流。质子泵抑制剂治疗6周,尼森fundoplication并没有解决他的咳嗽,尽管他手术后反流的症状消失了。
2003年,他被称为皇家主管布朗普顿医院,因为地铁站棘手的咳嗽,这阻止了他的工作。他是生产少量的痰。他还抱怨腹泻和盗汗,失去了15公斤体重前2年。他停止吸烟15岁以前15 pack-yr历史。临床检查是正常的。血嗜酸性粒细胞计数是5.0×109·L−1和免疫球蛋白E 61 IU·毫升−1(正常范围3 - 150 IU·毫升−1);未发现anti-neutrophil胞质抗体。肺的计算机断层扫描显示增厚与远端气道堵塞肺内的航空公司。一秒钟用力呼气量中,肺容积和一氧化碳气体传输是正常的,但他吸入辣椒素敏感的咳嗽反应。支气管活检显示,杯状细胞增生和嗜酸性基质炎症。支气管肺泡灌洗液中含有25%的嗜酸性粒细胞。因为他的广泛传播在热带国家,粪便检查和血清学调查进行和寄生虫排除在外。伊维菌素的过程没有影响他的咳嗽或嗜酸性粒细胞。腹部电脑断层显示肝脾肿大身高16厘米长脾脏和肝脏的19厘米。
口服强的松(40毫克·−1)开始,在2周内,咳嗽和腹泻被控制,但是在类固醇逐渐减少(至少20毫克的剂量所需症状控制)。血嗜酸性粒细胞持续∼1×109·L−1。
因为他的持久hypereosinophilia,他被称为进一步血液学的调查。骨髓吸入环钻活检显示,嗜酸性粒细胞增多和松散聚集肥大细胞没有增加爆炸异常细胞或淋巴浸润。没有的重排TCRB或TCRG基因显示淋巴细胞单克隆。细胞遗传学分析是正常的。单步执行rt - pcr的FIP1L1-PDGFRA融合基因是负数,但嵌套PCR间歇性是积极的。荧光原位杂交(鱼)分析显示CHIC2删除,暗示这种融合基因的存在,在23%的间期细胞(正常:≤10%)(图。1⇓)。弱阳性结果与rt - pcr和鱼的低比例的异常细胞进一步分析导致分子调查,显示一个断点涉及外显子16的FIP1L1基因外显子12的PDGFRA下游基因比先前报道(图2所示⇓)。之前从未描述断点的位置可能解释的困难检测融合基因的mRNA使用标准的PCR引物。
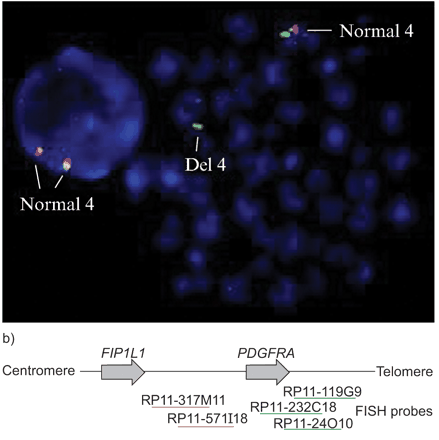
荧光原位杂交(鱼)分析。与两个重叠的红/绿)间期正常信号对应于两个正常染色体4的副本。右边的中期传播显示一个正常染色体4和一个CHIC2删除4号染色体(绿色)的信号。b)计划指示和鱼的基因探针的位置。

分子的调查FIP1L1-PDGFRA融合在这个案例研究中,显示在坐标系mRNA结和预测的氨基酸序列。的FIP1L1序列所示平原类型、四个碱基对插入在小写和来历不明的PDGFRA以粗体显示。
在演示FIP1L1-PDGFRA融合基因10个月后开始强的松治疗,酪氨酸激酶抑制剂伊马替尼(100 mg·−1)开始,迅速消失,血液嗜酸性粒细胞。强的松的剂量伊马替尼治疗的2个月后逐渐停止。病人的咳嗽没有复发和他腹泻开始伊马替尼以来有所改善。没有注意到副作用和融合基因不再是由特定的rt - pcr检测为断点出现在这个病人。
讨论
这个病人有严重gastro-oesophageal回流的证据,但他的咳嗽与质子泵抑制剂治疗后未见起色。一个Nissen fundoplication废除回流也未能改善病人的咳嗽,相反之前已经报道过的病人咳嗽显然回流的结果7。这因此排除gastro-oesophageal回流的可能性作为潜在他的咳嗽。
协会的持久hypereosinophilia咳嗽是下一个调查。有证据显示气道嗜酸性粒细胞炎症的粘膜,但病人没有症状的哮喘和他的组胺支气管反应并非不正常。hypereosinophilia使他的水平属于特发性hypereosinophilic综合症,但这现在可以诊断只是hypereosinophilia后严格排除所有其他的原因。寄生虫,针对他的广泛前往热带地区,被排除在外。它也不太可能,他代表了急性嗜酸性肺炎,如被描述在美国军人在伊拉克服役,由于暴露在沙漠沙子或爆炸物8。
Hypereosinophilic综合症包括一系列的条件,但是最近的发展导致了两种截然不同的实体识别,除了残余特发性病例。首先,淋巴细胞变异与hypereosinophilia辅助t细胞淋巴增殖性疾病的存在一个循环克隆t细胞被描述9,10。这是排除在这个病人的缺乏重排TCRB或TCRG基因。其次,骨髓增殖性疾病造成的间隙删除4号染色体的长臂,导致形成的FIP1L1-PDGFRA融合基因和蛋白质的合成异常的酪氨酸激酶活性,已被描述6。因为脾肿大和胃肠道和肺部症状是承认这种综合症的特点,这个病人在这方面研究,并演示了融合基因的存在。其他FIP1L1-PDGFRA综合症患者也显示骨髓细胞学上异常肥大细胞的浸润11。伊马替尼选择性地抑制ABL酪氨酸激酶PDGFR和工具包。FIP1L1-PDGFRA对伊马替尼特别敏感,因此较低的初始剂量是合适的。FIP1L1-PDGFRA综合症会导致死亡,要么从终末器官损害(特别是心脏)或者从转换到急性白血病。引人注目的对伊马替尼治疗意味着其正确识别和治疗病人是至关重要的。当临床怀疑强,非典型分子的结果,在这个病人,为进一步的调查表明,直到明确诊断。
这个病人支持概念,嗜酸性粒细胞可能会造成咳嗽。嗜酸性粒细胞哮喘的发病机制的作用受到质疑后,最近的观察,一个anti-interleukin-5单克隆抗体对晚期反应没有影响哮喘的过敏原和支气管高反应性12。然而,anti-interleukin-5疗法没有完全耗尽嗜酸性粒细胞的呼吸道粘膜,同时,其它也可能参与嗜酸性介质激活。嗜酸性粒细胞如何诱发咳嗽需要进一步的研究。
- 收到了8月2日,2005年。
- 接受2005年10月13日。
- ©人期刊有限公司















