抽象
诱导化疗手术治疗后的争议的结果,尤其是在相对于切除的程度,先前已报道。死亡率和发病率在欧洲组织的研究和治疗癌症(EORTC)08941试验的手术手臂进行了研究。
EORTC 08941是一项多中心,前瞻性,随机,相-III手术切除的试验与放射治疗已证实为iii - n期患者2到基于铂的化疗诱导的客观响应后非小细胞肺癌。在手术手臂随机的167例手术结果本研究中提出的。在这些患者中,一个切换到放胳膊和17名患者没有得到任何协议处理或信息尚未公布。
在74名患者(49.7%),得到根治术负手术切缘。在61名患者(40.9%),病理性向下分级为N0或N1是礼物。手术30天死亡率为4.0%。术后并发症主要为肺炎、呼吸功能不全、心律失常、漏气、心脏失代偿、脓胸、支气管胸膜瘘等。共有12例(8.1%)患者因边缘阳性、血胸、脓胸和支气管胸膜瘘再次手术。
总之,在欧洲多中心研究组织和癌症治疗试验的治疗化疗后手术切除取得了可以接受的发病率和死亡率率。
IIIA期非小细胞肺癌(NSCLC)与同侧纵隔或隆突节点的参与(N2)表示的患者一组异质性,范围从最小的结内参与到囊外笨重疾病1。迄今为止,病理证实的IIIA-N2期疾病的管理是有争议的手术,以获得本地控制的确切作用尚未确定。许多二期,和两个较小三期,研究已证实与诱导化疗效果良好其次是手术切除2。然而,手术切除的作用与放射治疗以获得最佳的局部控制并没有在这些研究中得到了解决。出于这个原因,大,多中心III期临床试验在美国和欧洲都开始提供了更明确的答案2,3。在欧洲组织的研究和治疗癌症(EORTC)08941试验中,患者与成熟阶段IIIA-N2疾病患者,以诱导化疗的响应后,随机分为手术或放疗。
诱导化疗或放化疗后手术治疗的变量结果已经报告,和高死亡率右全肺切除后的特别关注4,五。在本研究中,对手术效果的死亡率手术的患者在EORTC 08941试验中,特别强调,相对于切除范围的报道。
患者和方法
The general treatment scheme of the EORTC 08941 trial is depicted in figure 1⇓and eligibility criteria at registration are given in table 1⇓。在这项研究中,患者的成熟阶段IIIA-N2非小细胞肺癌接受顺铂为主的诱导化疗。在胸部的CT扫描的响应的情况下,患者手术和放疗之间随机的。患有进行性疾病列入了研究,但没有考虑随机化(关闭研究)。
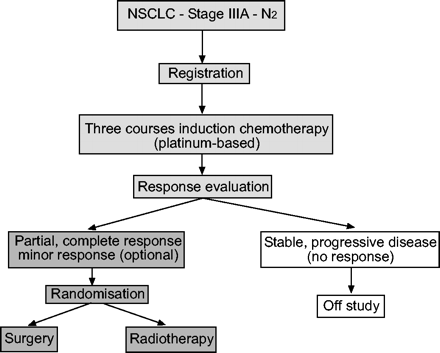
研究和治疗癌症(EORTC)08941试验欧洲组织的一般治疗方案。非小细胞肺癌:非小细胞肺癌。
手术治疗本实验的最终目的是彻底切除,即自由基除去原发性肿瘤,肺门和纵隔淋巴结。区分在下述之间进行:R t0切除,即完全切除,无肉眼可见肿瘤的留下,切缘阴性和病理检查最高纵隔淋巴结阴性;[R1,微观残留病;和R2切除宏观残余肿瘤。手术后的额外放射治疗仅在不完全切除的情况下施用的(R1或R2)。分期是根据最近的肿瘤,淋巴结,转移(TNM)分类进行6。死亡率,急性手术后的事件和发病率的数据进行前瞻性收集每个病人。这项研究是在中心在胸外科特定兴趣进行。出于这个原因,并发症一般大纲规定,但管理是留给机构的地方政策。
在EORTC 08941试验注册于2002年12月结束总共有333例患者随机,166到放射治疗手臂和167到手术切除组。后者的患者在本研究中进行了描述。
At registration, the median age of the patients randomised to surgery was 60 yrs (range 29–78), of which 119 were males and 48 females.
N的证明2127例患者行颈椎纵隔镜检查,14例患者行前纵隔镜检查,4例患者行电视胸腔镜手术,8例患者行开胸手术通过穿刺活检14个例。
除一人外所有患者铂类诱导化疗三个周期。该方案最常用是顺铂,吉西他滨,卡铂,紫杉醇,顺铂,足叶乙甙,顺铂,长春地辛。联合化疗用丝裂霉素,其可以与呼吸系统并发症的发生率较高有关,7例只用了7。
的组织学类型在随机分别为:在65例(38.9%)鳞状细胞癌;在57(34.1%)腺癌;在41(24.6%)大细胞癌;和混合细胞或在四名患者其他恶性类型(2.4%)。
在手术手臂接受治疗:手术治疗127例(76.0%);手术,随后在22(13.2%)辅助放疗;一个患者(0.6%)切换到放疗臂;名患者(5.4%)根据方案没有处理;并在治疗实际收到的信息是不可用的8例(4.8%)。The group of 149 patients who had surgery (n = 127) or surgery followed by radiotherapy (n = 22) was considered for further analysis.
关于手术的类型,69例(46.3%),58(38.9%),21例(14.1%),肺叶切除或bilobectomy,剖胸探查和1例(0.7%),其他干预谁remediastinoscopy行,进行全肺切除其是违反协议。作为remediastinoscopy仍为阳性,该患者没有手术切除。
有35(50.7%)的左侧右侧pneumonectomies,33(47.8%),并且对于一个患者(1.4%),肺的一侧是未知的。
使用单因素和多因素(落后选择)逻辑回归模型的几个基础因素对术后发病率和死亡率的风险的影响进行了研究。这些分析需要考虑的探索。
结果
基团R0在74名患者(49.7%),R进行切除1在53(35.5%),R2在21例(14.1%)。此外,1例(0.7%)没有开胸手术,但经历remediastinoscopy如前所述。
临床(c)中,肿瘤(T)和节点(N)分期诱导化疗之前与术后病理(p)、T、N分期见表2⇓。后者更明确的叫法展翅和YPN所有这些患者诱导化疗。降期到N0或N140.9%的患者获得了疾病。
手术30天死亡率为4.0%(六名患者)。在这些患者中,5例肺切除(三级在右侧左侧两个),以及一个右路的剖胸探查。因此,探索性开胸术后30天的死亡率发生在一出21例(4.8%),后叶切除0%和肺五明的69例患者(7.2%)后。右全肺切除后的三十天死亡率为5.7%,左全肺切除后的9.1%。一位患者在手术后一天(POD)4死于成人呼吸窘迫综合征(ARDS),一个在POD 5由于肺动脉高压和心功能失代偿,一个在因术后出血的POD 7,两个在POD 11由于心脏代偿和呼吸功能不全,以及一个在POD 26推测是由于心律失常,虽然死亡的确切原因无法确定。
第九天的死亡率为8.7%(13例),七名病人31天和90天在术后之间死亡。这些患者中有三个肺切除,俩人肺叶切除术,一个是bilobectomy和一个一剖胸探查。死亡原因是疾病进展的两个病人,两种感染,一种有毒死亡,两名患者其他原因。
总共12名患者(8.1%)进行再次手术由于血胸(4例),支气管瘘(5名患者),脓胸(1例)和正边缘(2例)。
关于对血胸重新操作,在两种情况下的特定原因可能是确定的,没有确切的原因是在一名患者中发现,和第四患者无血胸,但血小板紊乱被发现。四明五口支气管胸膜瘘是由Clagett程序(打开的窗口胸腔)和一个由瘘口直接关闭处理。
具体的发病率数据是可用的136例患者。这些被细分为肺,心脏,胸腔空间等并发症。The different categories are listed in table 3⇓。肺部并发症是最常见的,尤其是肺炎和呼吸功能不全。观察到的支气管胸膜瘘切除术后均发生。肺切除术后该并发症的发生率为8.7%。其他呼吸系统并发症主要包括咳嗽和呼吸困难,由于痰液潴留,支气管炎,慢性阻塞性肺疾病的恶化。
并发症组的其他活动包括尿路感染,血小板紊乱和控制的糖尿病。
调查年龄,性别,病理类型,CT阶段,手术侧,手术和根治性切除的存在对发病率或30天的手术死亡率,单因素和多因素分析的风险类型的影响表明,只有手术的类型是与这样的事件的发生相关联的显著。Although patients with bilobectomy did not appear to have a significantly different risk of morbidity or mortality (p = 0.9341) than patients with pneumonectomy, patients with exploratory thoracotomy and other surgery did have a significantly lower risk of such an event (p = 0.0048) than patients with a pneumonectomy.
讨论
1994年,EORTC发起了一项前瞻性多中心试验中,患者与久经考验的ñ2疾病最初是由诱导化疗处理,接着,在响应的情况下,手术和放疗之间随机2。在2002年12月为权责发生制封闭该研究的主要终点是生存。在这些报告的结果(2004年11月)的时间,最终结果尚未公布,由于未能达成事件使统计分析的数量。
在本研究中,随机分配到手术组患者的手术效果都集中在。化疗后手术切除,尤其是放化疗后,在技术上要求更高,由于纤维化不同程度,往往是新辅助治疗后遇到8。这使纤维化手术解剖比较繁琐,因为它是在不同的站淋巴结的初始参与的网站往往明显。因此,肺门及纵隔区经常参与。这些淋巴结的冷冻切片分析可用于确定切除范围有用的,但可以是不可靠的,特别是当只有微坚持。当广泛粘连存在,在肺门释放肺动脉或其主要分支裂缝可能是相当困难的,即使是有经验的胸外科医生,因此有必要心包内,逆行或后清扫。
出于这个原因,它是不奇怪的争议结果已经报告的诱导化疗或放化疗后手术发病率和死亡率。在未来的国际多中心EORTC 08941试验的手术组,死亡率分别为4.0%和8.7操作30-%和90天。发病率包括呼吸道(27.9%)和胸腔空间问题(18.4%)为主。
较早的报告中已经强调在此设置与肺中遇到的风险较高。在一个较小的一系列13个例,福勒等。4报道的23%的整体手术死亡率,其肺切除术后增加至43%。随后的社论中警告此过高风险9。
在距离Memorial Sloan-Kettering癌症中心(美国纽约)大系列,470例患者接受诱导化疗或放化疗后肺叶切除或全肺进行回顾性分析五。总死亡率为3.8%,肺叶切除后2.4%和肺切除术后11.3%。在这一系列的右全肺切除携带的死亡率为23.9%,具体的原因,其中无法确定。总体患病率为38.1%,上升到58.7%,右全肺切除后。心脏并发症的患者和25.7%,呼吸系统并发症12.3%;主要由肺炎,呼吸功能不全,脓胸及支气管胸膜瘘。Multivariate analysis demonstrated right pneumonectomy, blood loss >500 mL and forced expiratory volume in one second <80% to be independent risk factors for morbidity; whereas the type of induction therapy had no specific effect10。在EORTC 08941试验中,未观察到右肺切除术后较高的死亡率。
在休斯敦,美国的一系列11,76例患者接受化疗后手术切除,用一系列的259例患者仅接受手术切除相比。虽然这不是一项随机研究,在手术后的发病率和死亡率数据进行了前瞻性收集。死亡率手术仅组中为5.0%,并将合并的诱导化疗手术组只有1.3%。然而,pneumonectomies的数量在这个系列较低,仅为10.5%。主要肺部并发症,包括肺炎,再插管,气管切开和急性呼吸窘迫综合征,发生在具有诱导化疗后手术切除患者的13.2%,但没有脓胸或支气管胸膜瘘的情况。目前的研究结论是,诱导化疗不显著影响整体的发病率和手术切除的死亡率。但是,应该强调的是,大多数患者有一个肺叶切除术或bilobectomy。
另一大系列350名后患者放化疗诱导报道了斯塔马蒂斯谁了手术切除等。12。在此回顾性研究中,35%的患者接受了肺和45%肺叶切除术。医院死亡率为4.9%,全肺切除后7.2%,而肺叶切除或bilobectomy后3.8%。早期或晚期并发症的患者,这是主要的心律失常(13%,肺切除后27%),延长的空气泄漏(16%),肺炎(5.1%),肺不张(4.3%),和化脓性并发症,包括44%的支气管瘘(4.1%)和未经脓胸支气管瘘(1.7%)。风险因素是肺炎高发年龄和低卡氏指数,而且,对于心律失常,手术前异常超声心动图检查。支气管残端覆盖的缺席是对围手术期并发症的另一个风险因素。Rethoracotomy对术后出血是9例(2.6%),五个肺叶切除术后和四个肺切除术后必要的,具有特定的原因,4例被发现。
北美间试验0139的初步结果调查手术的相对作用与iii - n期放射治疗2非小细胞肺癌近日报道3。与此相反的EORTC研究中,患者放化疗前期和诱导化疗的全过程,随后手术切除之间随机的。总共429例患者随机,有392的存在评估。在诱导治疗手术臂,201名患者参与,14中或合并在治疗后(6.9%),手术后和10 4死亡。死亡的最常见原因是急性呼吸窘迫综合征。有在双臂之间的3年总生存率无差异,但无进展生存期是显著更好的诱导治疗手术组3。
匹兹堡大学(University of Pittsburgh)最近的一项研究报告了115名在1990年至2002年间接受全肺切除术的患者13。共有50名患者接受了右侧肺切除术,65名患者接受了左侧肺切除术。52名患者(45%)接受了新辅助治疗,其中25人接受了右肺切除术,27人接受了左肺切除术。平均停留时间为5天。比较左右肺切除术。30天死亡率右侧为6%左侧为3%室上性心律失常多见于左侧,支气管胸膜瘘多见于右侧。中位生存期无差异,右位生存期为18.5个月,左位生存期为19.1个月。新辅助治疗增加了术后心律失常的风险,但没有增加支气管胸膜瘘的发生率13。
总之,诱导化疗对成熟的阶段IIIA-N后手术切除2非小细胞癌灵被认为是可行的EORTC 08941试验,前瞻性随机对照的国际多中心研究。总体而言,六名患者在术后第一月期间死亡,给人的4.0%,30天死亡率。的谁死了肺,三左边,两个在右侧的病人五。发病率也不是很不同与其他大型系列报道相比,warranting的综合治疗,包括手术治疗早期或局部晚期非小细胞肺癌的进一步研究。
致谢
作者想要感谢所有参与EORTC肺癌组的医生和机构,他们如下。来自荷兰的参与医生是:B-H。Liem (Lievensberg Ziekenhuis, Bergen Op Zoom);B. Biesma (Bosch medical entrum- groot Ziekengasthuis, Hertogenbosch);P. van Valenberg (Elkerliek Ziekenhuis, Helmond);A. Termeer (Canisius-Wilhelmina Ziekenhuis, Nijmegen);T. van Boxem (Ziekenhuis Franciscus, Roosendaal);H. Goey (Maria Ziekenhuis, Tilburg);F. Schramel (Nieuwegein-Utrecht, St. Antonius Ziekenhuis/Diakonessenhuis);A. van Bochove (Ziekenhuis de Heel, Zaandam); P.I. van Spiegel (Slotervaart Ziekenhuis, Amsterdam); N. van Zandwijk (Antoni van Leeuwenhoekhuis, Amsterdam); J. van Meerbeeck /T.A.W. Splinter (Erasmus M.C., Rotterdam); F. van Breukelen (Spaarne Ziekenhuis, Haarlem); V. Tjan-Heijnen (St. Radboud University Hospital, Nijmegen); N.J.J. Schlosser (Universitair Medisch Centrum, Utrecht); G. Giaccone (Academisch Ziekenhuis der Vrije Universiteit, Amsterdam); H.B. Kwa (Onze Lieve Vrouw Gasthuis, Amsterdam); L. Willems (Academisch Ziekenhuis Leiden, Leiden); B.M. Drenth (Atrium Medisch Centrum, Heerlen); J. Stigt (Sophia Ziekenhuis, Zwolle); E. Lammers (Leyenburg Ziekenhuis, Den Haag); G.W.P. Kramer/S. Gans (Arnhem's Radiotherapeutisch Instituut/Ziekenhuis St Jansdal, Arnhem).
来自比利时的参与医生为:P. Pinson (Ziekenhuis大学,Gent);D. van Renterghem (A.Z. St. Jan, Brugge);D. Galdermans (Algemeen Ziekenhuis Middelheim, Antwerpen);P. van Schil(安特卫普Ziekenhuis大学);L. Delaunois(伊沃伊尔蒙特戈迪尼纳大学);J. Vansteenkiste(加索伊斯堡大学,鲁汶);博杜安先生(荷利蒙医院,海涅·圣保罗);A. Baudoux (Clinique Sainte Elisabeth, Namur);W. Moorkens (AZ Hoge Beuken, Antwerpen);J. Verschuere (AZ Zusters van Barmhasrtigheid, Ronse); J-P. D'Odemont (Clinique Saint Joseph, Mons); W. Verbeke (Stedeljik Ziekenhuis, Aalst).
从意大利参加医师分别为:S。达尔维什(Policlinicl Monteluce,佩鲁贾);A. Ardizzoni(Istittuto国立每拉Ricerca Sul的巨蟹座,热那亚);G. Scagliotti(奥斯佩达莱(Ospedale)S.路易冈萨加-UNIVERSITA都灵,都灵);和C. Gridelli(Istittuto国立每LO工作室ËLA库拉棣Tumori,那不勒斯)。
来自波兰的与会医生是:T.莱温斯基(肿瘤中心研究所,华沙)。
来自斯洛文尼亚的参加医生是:A. Debeljak(卢布尔雅那克里尼奇尼中心格尔尼克,格尔尼克)。
来自英国参加的医生们:M.哈顿(韦斯顿公园医院,谢菲尔德);M.奥布莱恩(皇家马斯登医院,萨顿);A.价格(西部综合医院,爱丁堡);和K.奥伯恩(莱斯特皇家医院,莱斯特)。
- 收到2004年11月7日。
- 公认2005年4月30日。
- ©ERS期刊有限公司











