摘要
t辅助细胞1型(Th1)细胞被认为在对过敏性疾病的保护性免疫中具有重要作用。然而,最近使用极化Th1细胞的研究显示,在小鼠哮喘模型中,对气道反应性和嗜酸性粒细胞炎症的影响相互矛盾。目前的研究探讨了已建立的Th1克隆对小鼠特应性哮喘模型的过继性转移的影响。
用卵清蛋白(OVA)致敏小鼠(BALB/c),并用雾化的卵清蛋白(5%,20分钟)攻毒5天。就在开始第一个挑战之前,Th1克隆(5×10)6·身体−1)或单独注射PBS通过尾静脉。评估气道对甲胆碱的反应性后,取支气管肺泡灌洗液(BALF)。还进行了组织学检查,包括形态计量学分析、BALF中细胞因子的测量和肺趋化因子的Northern印迹。
与单独注射载体或脾单核细胞的小鼠相比,过继移植的Th1克隆细胞的细胞总数明显增加,而BALF中的嗜酸性粒细胞明显减少。注射Th1克隆显著降低嗜酸性粒细胞的浸润,但增加支气管周围区域的单核细胞。Th1克隆也能抑制杯状细胞增生和支气管周围纤维化。Th1细胞的转移显著降低气道反应性。注射Th1显著增加了BALF中的干扰素γ,但显著降低了白细胞介素(IL)-5和IL-13。Eotaxin mRNA主要在哮喘模型小鼠的肺中表达,而RANTES(受激活、正常t细胞表达和分泌的调控)在Th1转移小鼠中占主导地位。
综上所述,在哮喘小鼠模型中,t辅助细胞1型克隆的过过性转移可以抑制肺嗜酸性粒细胞和气道反应性,但会增加非嗜酸性粒细胞炎症。
哮喘气道炎症被认为是由辅助性t (Th) 2型细胞驱动的1,2。哮喘患者支气管肺泡灌洗液(BALF)或支气管活检标本中的t细胞主要表达白细胞介素(IL)-4或IL-5 mRNA,提示这些t细胞为Th2细胞。在小鼠哮喘模型中,小鼠对鸡卵清蛋白(OVA)敏感,然后用雾化OVA攻毒,由于BALF中细胞因子的Th2模式和肺淋巴结和脾脏细胞的t细胞产生的细胞因子,表型也被认为是Th2显性的。此外,将Th2克隆或极化Th2群体过继转移到幼稚小鼠中,然后经支气管抗原激发,在肺部诱导哮喘样表型3.,4。
因此,Th1细胞的诱导或过继性转移可能是哮喘的一种可能的治疗策略,因为Th1细胞可以对抗th2驱动的机制。先前的报道表明,由Th1细胞产生的干扰素(IFN)-γ可以抑制Th2细胞的增殖,减少嗜酸性粒细胞炎症和气道反应性。用IL-12、IFN-γ或BCG、分枝杆菌、李斯特菌和CpG DNA序列等th1诱导物质治疗哮喘模型小鼠可抑制小鼠哮喘表型5- - - - - -8。然而,尚不清楚Th1细胞是否能单独诱导哮喘表型的平衡。这些物质诱导的作用可能涉及Th1细胞以外的细胞类型,如IL-10或产生转化生长因子-β的调节性T细胞9- - - - - -11。
通过将倾斜的Th1细胞过继转移到小鼠或大鼠哮喘模型中,研究了Th1反应的直接影响12- - - - - -14。在先前的研究中,嗜酸性粒细胞向肺部的募集增加12,虽然在其他方面受到抑制13,14。这些Th1人群对气道反应性的影响也显示出相互矛盾的结果13,14。在这些实验中,分别将来自大鼠或T细胞受体(TCR)转基因(Tg)小鼠的细胞因子极化细胞注射一次到致敏的同基因大鼠或小鼠中,然后反复暴露于雾化的相应抗原。
利用这种稳定性,目前的研究使用了长期培养的已建立的Th1克隆,而不是极化细胞。通过过继转移实验来阐明Th1细胞对小鼠哮喘模型表型的调节作用。
材料与方法
辅助t细胞1型克隆的过继性转移
小鼠(BALB/c, 6-8周龄雌性;Charles River Laboratories,神奈川,日本)用OVA致敏(V级;Sigma Chemical Co., St. Louis, MO, USA)加明矾(哮喘模型和哮喘- th1组)或PBS(单独th1组和PBS组),每周间隔三次(第0,7和14天),如前所述15- - - - - -17。然后连续5天(第15-19天)给这些小鼠注射雾化的OVA(5%)。就在开始挑战之前(第15天),Th1克隆(5×10)6/500µL PBS/只;哮喘-Th1和单独Th1组),脾单个核细胞(SMNC;5×106/500µL PBS/只;哮喘- smnc组)或单独注射PBS(哮喘模型组和PBS组)通过尾静脉。ova -反应性Th1克隆(D2、S1和S4)的特征已在前面描述过17。克隆在添加10%热灭活胎牛血清(Gibco, Grand Island, NY, USA), 100 U·mL的RPMI 1640培养基中培养−1青霉素G, 100 μg·mL−1链霉素,50 μM 2-巯基乙醇(Sigma)和10 mM HEPES(2-[4-(2-羟乙基)-1-哌嗪基]乙磺酸)(Sigma)。
挑战在一个50毫升的塑料管中进行,OVA气溶胶由喷雾器输送(DeVilbiss Corp., Somerset, PA, USA)。最终暴露于OVA 24 h后,小鼠在麻醉下颈椎脱位死亡。通过对手术暴露的气管插管获得全肺BALF (0.5 mL,三次)。使用血细胞计计数BALF中的细胞。采用细胞自旋制剂(May-Giemsa染色法)测定细胞差异计数。
组织学和形态计量学分析
支气管肺泡灌洗后,穿刺右心室灌注10ml PBS。取左肺,保存于- 80℃,用于RNA提取。取右肺,4%多聚甲醛固定,石蜡包埋,切成5µm切片。切片在pH 2.5/周期性酸-席夫(AB-PAS)条件下用血红素和伊红、弹性马松三色或阿利新蓝染色。
嗜酸性粒细胞、杯状细胞(ab - pas阳性细胞)和总上皮细胞(上皮细胞核总数)的数量使用前面描述的图像分析系统进行计数16。数据以每毫米上皮基底膜下的细胞数表示。气道纤维化的形态计量学分析采用前面描述的方法进行,并进行了一些修改16。简而言之,通过记录的肺内气道图像,通过弹性马松三色染色,测量基底膜周长(Pi)和蓝色染色区域的外周长(Pe)。假设Pi和Pe均为圆形,则基底膜下胶原沉积面积为: 均值±sd分别为4.64±0.40、4.71±0.42、4.60±0.34和4.66±0.39 (×10)−1mm;n = 7-8),分别为哮喘模型组、哮喘- th1组、单独th1组和PBS组。各组间差异无统计学意义(p值= 0.98)。
均值±sd分别为4.64±0.40、4.71±0.42、4.60±0.34和4.66±0.39 (×10)−1mm;n = 7-8),分别为哮喘模型组、哮喘- th1组、单独th1组和PBS组。各组间差异无统计学意义(p值= 0.98)。
测量气道反应性
如前所述,在有意识和不受约束的情况下,通过身体体积脉搏图(Buxco, Troy, NY, USA)测量气道反应性15,16,18。在暴露于雾化生理盐水或逐渐增加剂量的甲基胆碱(MCh)之前和之后进行测量。数据取3分钟平均值,表示为增强暂停(Penh): 式中,Te为呼气时间(s), Tr为松弛时间(呼气时压力衰减到总箱压36%的时间),PEP为呼气压力峰值(m·s−1), PIP为吸气峰值压力(m·s−1).结果表示为在每种浓度的MCh攻毒后Penh的增加百分比,其中在攻毒后盐水获得的Penh值为100%。
式中,Te为呼气时间(s), Tr为松弛时间(呼气时压力衰减到总箱压36%的时间),PEP为呼气压力峰值(m·s−1), PIP为吸气峰值压力(m·s−1).结果表示为在每种浓度的MCh攻毒后Penh的增加百分比,其中在攻毒后盐水获得的Penh值为100%。
BALF分析及细胞因子测定
用上述方法获得BALF (0.5 mL×3,共1.5 mL)15- - - - - -18。IFN-γ (Endogen, Boston, MA, USA)、IL-5 (Endogen)和IL- 13 (R&D Systems, Minneapolis, MN, USA)的浓度根据制造商推荐的程序进行测定。检出限为1.5 pg·mL−1IL-13为5 pg·mL−1IL-5和15 pg·mL−1干扰素-γ。
互补脱氧核糖核酸探针
采用ISOGEN (Nippon Gene, Tokyo, Japan)的方法提取各组冷冻肺组织的总RNA。从BALB/c小鼠肺中提取趋化因子cDNA探针的总RNA。使用cDNA合成试剂盒(Life Sciences, St. Petersburg, FL, USA)在42°C下进行反转录(RT) 60分钟,聚合酶链反应(PCR)在94°C下进行初始5分钟,然后在94°C下进行变性30秒,在58°C下进行退火45秒,在72°C下进行延伸60秒的30个循环。eotaxin引物为:5′-CGCGGATCCACCATGCAGAGCTCCACA-3′;反义,5 ' - ccgctcgaggttgttgtttatggttttgga -3 ',对于RANTES是义,5 ' -CGCGGGATCCATGAAGATCTCTGCA-3 ';反义5“-GAATCTAGAAACCCTCTATCCTAGC-3”。内控RT-PCR使用还原甘油醛磷酸脱氢酶(GAPDH)特异性PCR引物(R&D Systems, Minneapolis, MN, USA)。cDNA探针用(α-)标记32P)脱氧胞嘧啶三磷酸通过随机寡核苷酸引物技术使用Prime It II试剂盒(Stratagene, La Jolla, CA, USA)。
肺趋化因子的northern印迹
变性rna(10µg)在1%琼脂糖/5%甲醛凝胶上通过凝胶电泳进行分级,并转移到尼龙膜(Hybond-N)上+;英国白金汉郡Amersham)。用20µg·mL的QuickHyb Hybridisation Solution (Stratagene)在68℃下预杂交15 min−1在含有50 ng·mL的缓冲液中进行杂交−1heat-denaturedα-32p标记探针在68°C下放置1小时。杂交后,在2×saline柠檬酸钠(SSC) (1×SSC = 150 mM氯化钠和15 mM柠檬酸钠)和0.1%十二烷基硫酸钠(SDS)中分别在室温和0.1×SSC中洗涤两次,分别在60°C和0.1% SDS中洗涤30分钟。将斑点暴露于x射线胶片中,温度为- 80℃,时间为48 h。
统计分析
数据以平均值±表示sd,除非另有说明。Dunnett分析气道反应性事后方差分析后检验。变量分析使用Mann-Whitney u检验对两个变量进行比较。
结果
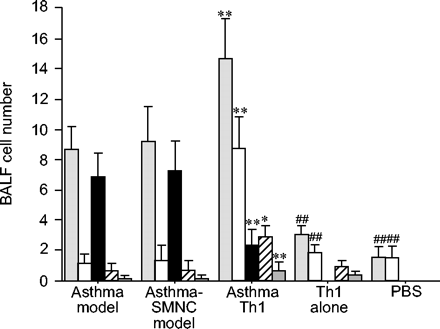
如图1所示⇓哮喘模型组小鼠BALF细胞总数和嗜酸性粒细胞明显增加。给予这些小鼠(哮喘-Th1组)Th1可减少嗜酸性粒细胞的数量。但总细胞、巨噬细胞、中性粒细胞和淋巴细胞数量明显增加。在哮喘- smnc组小鼠中未观察到这些影响,表明这些不是转移细胞的非特异性影响。与PBS组相比,单独注射th1组小鼠的BALF中细胞总数、巨噬细胞、中性粒细胞和淋巴细胞明显增加。PBS组小鼠BALF中炎症细胞较少,无嗜酸性粒细胞。虽然显示了克隆D2的数据,但基本上在其他Th1克隆(S1和S4;数据未显示)。
哮喘模型小鼠支气管肺泡灌洗液(BALF)、哮喘脾单核细胞(SMNC)、哮喘辅助t细胞1型(Th1)、Th1单用及PBS组小鼠细胞的分析哮喘模型小鼠在BALF中显示明显的嗜酸性粒细胞增多。将Th1细胞而不是SMNC转移到这些模型小鼠中,可减少嗜酸性粒细胞的数量。而Th1细胞使BALF细胞总数增加,巨噬细胞、淋巴细胞和中性粒细胞数量增加。结果以平均值±表示sd6-7只老鼠。 :总细胞数;□:巨噬细胞;▪嗜酸性粒细胞;└:淋巴细胞;▓:中性粒细胞。*: p < 0.05;* *: p < 0.01与哮喘模型组;# #: p < 0.01与asthma-Th1组。
:总细胞数;□:巨噬细胞;▪嗜酸性粒细胞;└:淋巴细胞;▓:中性粒细胞。*: p < 0.05;* *: p < 0.01与哮喘模型组;# #: p < 0.01与asthma-Th1组。
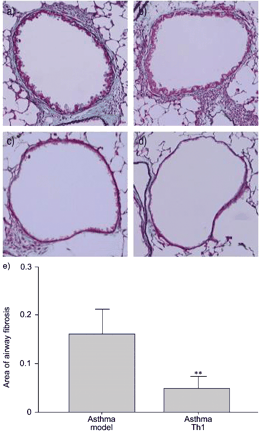
哮喘模型组小鼠在支气管周围区域表现出明显的嗜酸性炎症反应,气道上皮中ab - pas阳性杯状细胞显著增加(图2a)⇓, g,图3a⇓这些结果在哮喘- smnc组肺中基本相同(数据未显示)。哮喘- th1 -组小鼠表现出进一步的炎症,但炎症主要由单个核细胞组成,观察到少量嗜酸性粒细胞(图2c)⇓,图3a⇓哮喘- th1组小鼠杯状细胞数量明显少于哮喘模型组(图2h)⇓,图3c⇓).单独注射th1的小鼠在气道内没有明显的炎症(图2e)⇓).这些结果表明,Th1细胞转移到哮喘模型小鼠可在气道产生非嗜酸性炎症。在哮喘模型小鼠和哮喘- th1组小鼠中观察到气道周围的胶原沉积,而在其他组小鼠中则没有(图4a, b)⇓).然而,哮喘- th1组小鼠的胶原沉积面积明显小于哮喘模型组(图4b)⇓).
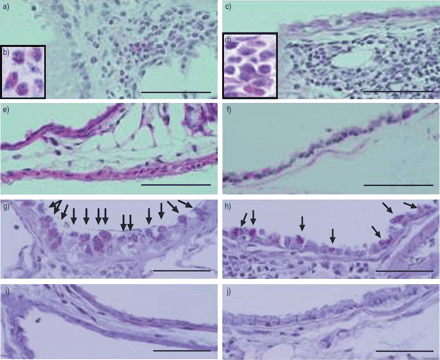
对肺组织改变的影响。哮喘模型组(a, g)、哮喘- t辅助细胞1型(Th1)组(c, h)、单独Th1组(e, i)和PBS组小鼠(f, j)肺的代表性照片。肺切片用血红素和伊红染色(a - f),或阿利新蓝/周期性酸-希夫(AB-PAS);g-j)。箭头显示ab - pas阳性的气道上皮细胞。标尺= 100 μm。
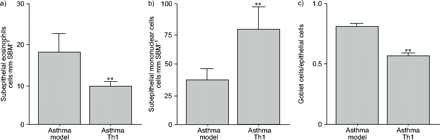
哮喘模型组和哮喘辅助t细胞1型(Th1)组小鼠气道炎症形态计量学分析。图示上皮下嗜酸性粒细胞(a)、上皮下单核细胞(b)和杯状细胞增生(c)。数据以每毫米上皮基底膜(SBM)的细胞数或杯状细胞/上皮细胞比率(n = 7-8,平均值±)表示sd).* *: p < 0.01与asthma-model组。
对支气管周围纤维化的影响。哮喘模型组(a)、哮喘辅助性t细胞1型(Th1)组(b)、单独Th1组(c)和PBS组小鼠(d)肺的代表性照片。标本用elastic - masson三色染色。e)哮喘模型组和哮喘- th1组小鼠支气管周围纤维化形态计量学分析。* *: p < 0.01与哮喘模型组。标尺= 100 μm。
根据以前的报告15,18哮喘模型小鼠对MCh有明显的气道反应(图5)⇓).Th1给药哮喘模型小鼠(哮喘-Th1组)引起的气道反应性明显低于哮喘模型小鼠。哮喘模型小鼠的气道反应性不受SMNC的影响(数据未显示)。单独Th1转移小鼠的气道反应性与阴性对照组相同。哮喘模型组和Th1转移哮喘模型组暴露于雾化MCh前的Penh(基线Penh)无显著差异(0.41±0.02)与分别为0.46±0.02)。虽然显示了克隆D2的数据,但在其他Th1克隆(S1和S4;数据未显示)。
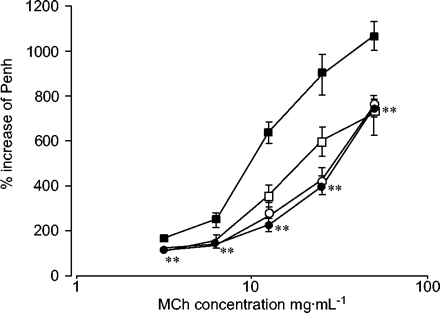
对气道反应的影响。数据表示为平均%增强暂停(Penh)±扫描电镜每组6-8只。每只小鼠生理盐水刺激后的基线Penh被认为是100%。妇幼保健:醋甲胆碱。▪:哮喘模型;•:哮喘t辅助细胞1型(Th1);〇:Th1单独;□:PBS。* *: p < 0.01与哮喘模型组。
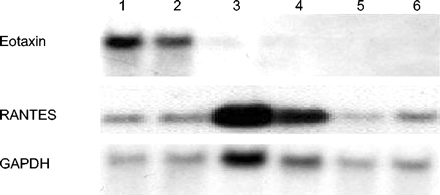
BALF细胞因子水平如图6所示⇓。哮喘- th1组小鼠BALF中IFN-γ水平明显升高,而哮喘模型组小鼠仅少量检测到。哮喘- th1组小鼠Th2细胞因子、IL-5、IL-13水平明显低于哮喘模型组。肺eotaxin mRNA在哮喘模型小鼠中主要表达,而在其他组小鼠中不表达(图7)⇓).Th1的转染降低了eotaxin mRNA的表达,但显著增加了RANTES mRNA的表达。
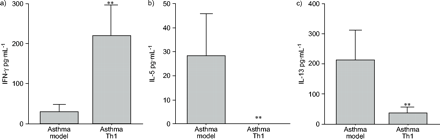
哮喘模型组和哮喘辅助t细胞1型(Th1)组支气管肺泡灌洗液中细胞因子水平的变化与哮喘模型小鼠相比,哮喘- th1组模型小鼠的干扰素(IFN)-γ水平显著升高(a),而白细胞介素(IL)-5 (b)和IL-13 (c)水平显著降低。数据以平均值±表示sd。* *: p < 0.01与哮喘模型组。
Northern blot分析哮喘模型组和哮喘- t辅助细胞1型(Th1)组肺中eotaxin和RANTES(正常t细胞表达和分泌的激活调控)mRNA的表达。小鼠甘油醛磷酸脱氢酶(GAPDH)探针作为同样印迹的对照。三个独立的实验结果相同,给出了具有代表性的结果。1、2组:哮喘模型小鼠;第3、4组:哮喘- th1组小鼠;第五、六道:PBS组小鼠。
讨论
将Th1克隆转移至哮喘模型小鼠可诱导嗜酸性气道炎症、气道反应性减弱、杯状细胞增生和支气管周围纤维化。这些作用伴随着Th2细胞因子的抑制和BALF中IFN-γ的增加。然而,这种治疗增加了非嗜酸性气道炎症。这可能至少部分是由肺中趋化因子的不同表达引起的。Th1降低了eotaxin mRNA的表达,增加了RANTES。这些结果表明,Th1克隆在哮喘模型小鼠中的过养性转移减少了哮喘的病理生理,但增加了非嗜酸性气道炎症。
嗜酸性气道炎症、杯状细胞增生和支气管周围纤维化的抑制可能是由于Th2细胞因子的抑制和BALF中IFN-γ的增加。Th2细胞因子IL-4和IL-13参与杯状细胞增生和支气管周围纤维化19,20.IL-5对嗜酸性粒细胞炎症的影响21。因此,抑制这些细胞因子有助于减轻嗜酸性气道炎症、杯状细胞增生和纤维化。IFN-γ抑制Th2细胞增殖,抑制嗜酸性粒细胞增多22。此外,由于IFN-γ是胶原合成的有效抑制剂,IFN-γ增加的主动抑制也有助于减少纤维化23。气道反应性的抑制也可以通过IL-4和IL-13的抑制以及IFN-γ的增加来解释。IL-13被认为是气道反应性的诱导剂,IFN-γ被认为具有抑制气道反应性的能力24。
虽然Th1细胞的转移抑制了th2介导的病理,但这种治疗增强了非嗜酸性气道炎症。本研究结果清楚地表明,Th1细胞的转移对趋化因子的表达有一定的影响在活的有机体内。Th1细胞抑制eotaxin的表达,而eotaxin在哮喘模型中强烈表达。RANTES的mRNA是由Th1细胞的转移诱导的,而在哮喘模型中没有诱导(图7)⇑).已知IL-4和IL-13都是强诱导剂,IFN-γ是eotaxin的强抑制剂24,25。然而,IFN-γ是RANTES的强诱导剂。Eotaxin被认为是一种有效的嗜酸性粒细胞特异性化学引诱剂。RANTES不仅是嗜酸性粒细胞的趋化因子,也是单核细胞的趋化因子。RANTES在支气管上皮的短暂过表达诱导单核细胞数量的急剧增加,而非嗜酸性粒细胞的增加26。这种趋化因子的差异表达可能解释了肺和BALF中炎症细胞的变化。
如前所述,显示Th1细胞对哮喘模型直接影响的报告显示了相互矛盾的结果12- - - - - -14。在以往的研究中观察到的差异的原因目前尚不清楚。实验动物的不同之处,即。小鼠或大鼠和Th1群体的克隆性,即。来自TCR-Tg小鼠的单克隆或来自野生型动物的多克隆可能是造成差异的因素。另一种可能的解释是,这种差异可能是由于极化Th1种群的纯度或成熟度所致。以往的研究均采用偏斜培养条件下3周的极化群体。虽然这些细胞的稳定性已被证实,但群体中仍含有Th0细胞,在诱导细胞因子的影响下,Th0细胞会进一步分化为Th1或Th2细胞27,28。此外,仔细治疗3周对于极化细胞的承诺是必不可少的,因为众所周知,在相反的条件下培养时,过早细胞将具有表型可逆29。因此,至少部分分化的Th1人群的特征可能会发生变化在活的有机体内在一个特别极化的Th2环境下,比如哮喘气道。然而,即使在IL-4的刺激下,已建立的t细胞克隆的表型也被证明是不可逆和稳定的。因此,在本研究中使用了长期建立的T细胞克隆。
综上所述,哮喘模型小鼠中辅助性t细胞1型反应的同时存在降低了气道的反应性和气道中的嗜酸性粒细胞,但增加了非嗜酸性粒细胞炎症通过抑制t辅助细胞2型细胞因子并导致肺趋化因子表达的变化。这些结果表明,t辅助细胞1型细胞的管理可能是治疗有用的。然而,需要进行进一步的研究,以确定治疗是否有不良的功能后果。他们还表明,成功治疗t辅助细胞1型诱导剂,如Bacille Calmette-Guellan和CpG,不伴有炎症增加,可能不是单独诱导t辅助细胞1型反应引起的。
脚注
编辑意见见第591页。
- 收到了2004年2月17日。
- 接受2004年12月9日。
- ©ERS期刊有限公司