摘要
本研究评估了引导鞘(GS)引导支气管内超声(EBUS)作为经支气管活检(TBB)诊断周围性肺病变(PPL)和提高诊断准确性的作用。
对24例直径≤30 mm(平均直径=18.4 mm)的ppl患者进行ebus - gs引导TBB。插入一个20 mhz放射状超声探头,覆盖GS通过一个工作支气管镜通道,并推进到PPL,以产生EBUS图像。经EBUS显像和x线透视证实带GS的探针到达病灶。当EBUS图像未发现病变时,取下探头,用刮匙引导GS到病变处。病灶定位后,取下探针,进行TBB和支气管刷检通过GS。
外周病变19个(79.2%)。所有在EBUS图像上可见ppl的患者随后接受EBUS- gs引导的诊断程序。共诊断14个病灶(58.3%)。即使局限于直径<20 mm的ppl,诊断敏感性为53%。
综上所述,超声引导下经支气管活检对周围型肺病变的诊断是可行且有效的。
周围性肺病变(PPL)的调查是一个具有挑战性的诊断问题。自20世纪70年代以来,x线透视引导下使用纤维支气管镜(FB)经支气管入路已成为最普遍接受的诊断pls的方法1- - - - - -3..然而,据报道,在X射线荧光透视引导下使用FB诊断PPLS的准确性为14-71%1- - - - - -8.一个潜在限制标准支气管镜诊断准确性的因素是病变的大小,小于2cm的病变的诊断率很低,仅为11-42%6- - - - - -10..一些呼吸内科医生更喜欢从经皮穿刺细胞学或活检获得的组织样本中诊断小的ppl11.- - - - - -15..虽然这些技术的成功率可能非常高,有76-97%的诊断准确性6,15.在美国,这些技术有几个问题。首先,它们有将恶性细胞从肿瘤扩散到胸腔的潜力11.,12..对于肺功能差的患者,这些技术会增加气胸的风险。此外,全身动脉空气栓塞是一种罕见但严重的并发症13.,14..
因此,在许多机构中,有小的周围性肺病变的患者会进行手术活检,如视频辅助胸外科手术,尽管这种侵入性的操作对于老年患者和呼吸功能较差的患者是不可取的。为了使病人免于这些手术过程,新的成像和引导技术是必要的。
最近开发的小口径超声探头使超声检查(US)更广泛的临床应用来气管和支气管病变。由FB引导,可以成功地将小口径US探针引入气管和支气管,以评估和诊断内部病变或肿瘤转移到纵隔或肺门淋巴结16- - - - - -18.在内核超声检查(EBUS)指导下的跨界针吹血有改善了肺癌的N-分期产量,而没有明确的内窥镜地标17- - - - - -20..EBUS也已被应用于pls的评估16,21.Kurimotoet al。22分析EBUS图像,以区分良恶性疾病,鉴别肺癌类型,确定分化程度。此外,Herthet al。23应用ebus作为PPLS的跨界活检(TBB)的成像指导。在本研究中,EBUS与引导鞘(GS)技术进一步结合。覆盖GS的活检钳可以移动到EBUS指导下的病变,之后可以通过保持损伤中的GS依次获得活检和刷涂样品。进行本研究,以检验新技术的有用性,以GS(EBUS-GS)为GS(EBUS-GS),作为TBB和支气管刷涂细胞学的指导,用于诊断PPLS。
方法
病人
2002年12月1日至2003年7月31日,在日本北海道大学医院(Sapparo, Japan)和岩见泽市综合医院(Iwamizawa, Japan), 24名平均直径≤30 mm的PPLs患者被纳入诊断性支气管镜检查。ppl的定义是那些被肺实质包围且在支气管镜下看不到的病变(没有支气管内病变、外部压迫、粘膜下肿瘤或支气管狭窄、炎症或出血的证据)。复查所有胸部CT,记录PPLs的平均直径。在书面知情同意后,患者接受支气管镜检查。
ebus - gs引导TBB和支气管刷牙
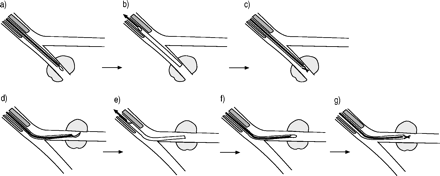
在上述两家医院,作为TBB的常规治疗程序,每位患者预先使用15 mg盐酸戊唑辛和0.5 mg硫酸阿托品。上呼吸道局部麻醉采用4%利多卡因。使用内镜超声系统(EU-M30S;配备20mhz机械放射状探头(XUM-S20-17R;其外径为1.4毫米(图1)⇓).使用具有2.0mm的工作通道的FBS(BF-P-260F,BF-P-240,BF-P-200; Olympus)。将探针插入GS中,通过FB的工作通道插入GS覆盖的探针,并向外周肺病变前进以获得EBUS图像。确认探针和GS通过EBUS成像和X射线荧光检查达到病变。在使用EBUS成像定位病变后,除去探针,并且GS保持在外周病变中。引入了活组织检查钳和支气管刷通过行病理和细胞学检查(图2)⇓a - c)。当EBUS图像未发现病变时,将双铰链刮匙插入GS,通过操作刮匙选择合适的支气管。刮匙近端手柄可使刮匙弯曲旋转。当EBUS图像或EBUS图像旁未发现病变时,按标准程序拉动GS,用载刮匙的GS选择近端位置下一个支气管,操作刮匙。一旦确定了支气管,就取出刮匙。然后通过GS插入探针,再次检查采集的EBUS图像。通过试错法重复这些步骤,直到发现探头和GS已经到达正确的位置(图2)⇓ d–g).

超声探头和导管鞘在引导鞘(GS)支气管超声检查(US)中的应用。GS a)与超声探头连接b)。带GS的超声探头通过纤维支气管镜的工作通道插入c)。活检钳也插入GS d)。
内胚层超声(ebus) - 导甲鞘(GS) - ~geD跨越横近脉冲活检(TBB)。a)GS的EBUS探针是前周肺病变通过fibreoptic支气管镜。经EBUS显像确认后,b)拔出US探头,c)进行TBB和支气管刷扫通过GS。当EBUS显像未发现病变时,d)将刮匙插入GS并选择合适的支气管。e)然后拔出刮匙,f)再次将EBUS探针插入GS进行EBUS成像。经EBUS显像确认后,g)行TBB及支气管刷片。
结果
患者数据
共24例患者(10名男性,14名女性),平均年龄为67.5±14.8毫升(24-83 YRS)。PPLS的平均直径为18.4±6.3mm(8.0-27.5mm)。PPLS的定位是右上叶,5名患者(20.8%),右中瓣三名患者(12.5%),右下叶10名患者(41.7%)和左上叶六名患者(25.0%)。在左下叶中没有检查PPLS。
EBUS-GS引导的跨晶活组织检查和支气管刷牙
19例(79.2%)患者EBUS检测到PPL。在10例患者中,EBUS探针在刮帚导航下到达周围病灶。所有在EBUS显像中可见ppl的患者随后接受EBUS- gs引导的TBB和支气管刷牙。ebus - gs引导的TBB平均标本数为3.5±1.3。诊断14例(58.3%);原发性肺癌10例,甲状腺转移性肺癌1例,子宫转移性肺癌1例,良性疾病2例(肺炎1例;尘肺病,1例)。病理诊断11例(45.8%),细胞学诊断11例(45.8%)(表1)⇓).共有5个病变可以通过EBUS看到,但无法获得诊断,活检和刷检样本不足。在对比EBUS可见的19个病变时,14例(12例恶性病变,2例良性病变)超声探头位于病变内部的支气管。其中13例获得细胞病理诊断。5例(2例恶性,3例良性),超声探头位于病灶旁的支气管内,其中1例恶性病变得到细胞病理诊断。
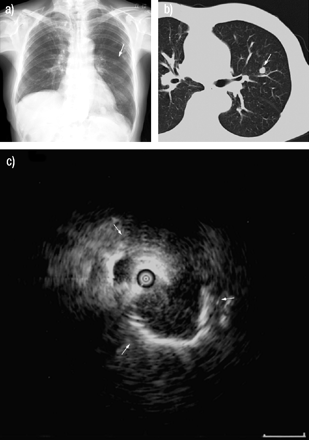
一个典型的案例如图3所示⇓.一位82岁男性,因肺腺癌接受右上肺叶切除术,12年前患有甲状腺癌,曾因异常胸影入院。胸片和CT显示左侧S3a有一个直径8mm的肺结节。EBUS显示一个低回声结节,被充气肺和病变之间产生的强反射界面所包围。ebus - gs引导TBB诊断为甲状腺转移腺癌。
一位82岁男性,因肺腺癌接受右上肺叶切除术,12年前患有甲状腺癌,因异常胸影入院。a)胸片和b)计算机断层扫描显示左侧S3a(箭头)有一个直径8mm的肺结节。c)支气管内超声显示一个低回声结节,被充气肺和病变之间产生的强反射界面包围(箭头;比例尺= 0.5厘米)。甲状腺转移腺癌经ebus引导鞘引导支气管活检诊断。
在10例有10个病灶的患者中,ebus - gs引导的支气管镜检查没有诊断价值。这10个病变中有7个被诊断为恶性疾病,通过使用更厚的钳或更厚的支气管刷,使用超薄支气管镜和虚拟支气管镜导航的ct引导TBB,或通过手术切除。在其他三个病变中,病变的大小减小,这些病变被指定为良性。
当根据大小进行评估时(表1⇑), 15个病灶平均直径<20 mm。10个病变(66.7%)在EBUS图像上可见,8个病变(53.3%)通过该程序诊断(6个病变通过病理诊断,5个病变通过细胞学诊断)。9个平均直径为20 ~ 30 mm的病变均在EBUS图像上可见,其中6个病变(66.7%)被诊断(5个病变经病理诊断,6个病变经细胞学诊断)。ebus - gs引导下的支气管镜检查对恶性和良性病变的诊断准确率分别为66.7%和33.3%。
当局限于恶性病变时,平均直径<20 mm病变的诊断敏感性为60%。EBUS-GS对支气管段的诊断敏感性无显著差异。
并发症
一名患者开发了通过管胸腔造口术治疗的气胸(4.2%)。诊断程序期间没有发生重大出血。
讨论
US在支气管内的应用于1990年首次被描述24.到目前为止,已有几份报告显示了EBUS在识别PPLs方面的有用性16,17,21- - - - - -23.肺实质空气含量完全反映了美国信号。与周围组织相比,肺团块具有低回声结构,由于充气肺与病变之间产生了强烈的反射界面,边界清晰25.缓冲物和Hanrath16报告26例中19例成功显示周围性肺病变et al。17据报道,EBUS在25例(包括六个外周病灶和19个肺门肿瘤)中提供了独特的信息。Kurimotoet al。22对PPLs内部结构的EBUS模式进行了分类,并根据EBUS模式对病变的组织学进行推测。
本研究表明,ebus - gs引导下的TBB和支气管刷拭对评价多侧前额叶皮质是有用的。EBUS显像显示肺部病变的精确位置,EBUS- gs使诊断标本从最合适的位置获得。EBUS和载刮器的GS技术的结合,使探针无法获取的ppl得以可视化,并允许从常规技术无法获取的ppl中获取活检标本。在目前的研究中,使用刮匙可获得10个病灶。此外,本报告有3个病变x线透视无法发现,其中1个病变经EBUS-GS诊断为腺癌。本研究中ebus - gs引导TBB和支气管刷扫对平均直径≤30 mm ppl的诊断敏感性为58.3%。当局限于平均直径<20 mm的病变时,该方法的诊断敏感性高达53.3%,其中40.0%的病变是通过病理诊断的。据报道,在x线透视下使用FB诊断直径< 20mm的ppl的准确性非常低,范围为11-42%6- - - - - -10..在本研究参与机构,过去一年x线透视指导下,FB对直径<20 mm的小ppl的诊断敏感性为35%,获得诊断活检样本的比率低至13%(数据未显示)。2例良性疾病(1例尘肺病和1例肺炎)和2例转移性肺癌被诊断。在这四个病例中,由于EBUS-GS的诊断结果,不必要的外科手术可以避免。
可能需要几种改进,以提高EBUS-GS引导的TBB和支气管刷涂的产量。在本研究中,通过EBUS成像检测到79.2%的PPLS。然而,通过EBUS-GS引导的支气管镜手术,无法诊断EBUS可见的五个病变(20.8%)。这主要是因为活组织检查钳和支气管刷小(直径1.2mm),不能获得足够的样品。此外,ebus的位置可能会影响结果。在本研究中,US探针位于病变内的支气管中的14例中,细胞病理学上的13例诊断。相反,在与病变邻近病变的支气管中的五种情况下,仅诊断了一种细胞病理学诊断出一种情况。
本研究的作者通常经历了<1ml出血和凝固血液,偶尔被困在GS中,但即使除去Gs时,也几乎没有看到GS之外的出血。假设支气管中的楔形GS导致活组学病变可用于止血。
偶尔会遇到GS位错。当美国探针或活检钳从GS中强力拔出或患者深呼吸时,GS偶尔会脱位。当支气管镜插入支气管亚段时,可以最大限度地减少GS脱位。即使在这些未被诊断的病变中,EBUS图像在随后使用更厚的钳和支气管刷的常规支气管镜检查过程中对识别合适的支气管非常有用。
对于TBB和支气管刷涂的EBUS-GS的益处如下:1)即使在X射线荧光透视上不可见的情况下,通过EBUS成像确认PPLS的精确位置;2)通过将GS留在PPLS中,促进屡获多次获得活组织检查和刷涂样品;3)从使用刮匙只能获得的PPL中获得活组织检查标本通过GS;4)减少捕获支气管中的GS引起的出血;5)评估PPLS的内部结构。要点2),3)和4)是GS技术的额外值单独高于EBUS。
综上所述,经引导鞘引导支气管穿刺活检和支气管刷检的支气管超声检查是安全的,并被发现是诊断周围性肺病变的有效方法。支气管内超声和导管鞘技术是一种很有前景的诊断小周围性肺病变的新方法。目前正在计划一项随机、前瞻性的研究,以诊断周围性肺病变并检查支气管镜的成本效益,包括或不包括带引导鞘的支气管内超声检查。
- 已收到2003年12月15日。
- 接受2004年6月23日。
- ©ERS期刊有限公司