摘要
气道炎症和气道重塑在哮喘的病理生理过程中起着重要作用。重塑可能影响儿童肺功能,而这一过程可能被抗炎治疗逆转。目前的研究纵向评估了哮喘是否会影响相对于气道的气道功能的增长,如果是,是否可以通过吸入皮质激素(ICS)来纠正。
在长达3年的时间里,每4个月对54名哮喘儿童(初始年龄7-16岁)进行肺功能评估,这些儿童吸入0.2 mg沙丁胺醇t.i.d。0.2毫克布地奈德t.i.d。(β.2‐激动剂(BA)+ICS)或安慰剂(PL)t.i.d.(BA + PL)在随机化的,双盲设计。测量前,最大支气管扩张后进行。气道生长从用力呼气量的变化在一个第二和最大呼气的评估流(在60%和总肺活量(TLC)残留在肺的40%)相对于TLC,如措施多个中央,中间和更外围的气道。增长模式与376名健康儿童的纵向研究结果进行了比较。
与健康受试者相比,BA + PL患者最大支气管后的气道通畅仍然减少,而在BA + ICS患者中,观察到亚型患者。可以对中央和中间气道功能的生长模式证明患者和对照之间没有差异。符合BA + IC的符合额为75%的规定剂量,导致2个月内对中央和中间气道的症状和中间气道的症状和中间气道的显着改善,但与BA患者相比,近期气道通畅仍然减少了减少+ pl。
哮喘儿童的抗炎治疗与中央路气道的正常功能发育有关。支气管扩张剂后周围气道开放持续降低可能反映了气道重塑或抗炎治疗不足。
这项研究得到了荷兰健康研究促进计划(SGO)的支持。
轻症患儿的中央气道有明显的组织病理学改变1严重2,3.哮喘,但是这样的结构改变和功能恶化之间的直接关系目前还不清楚。虽然哮喘儿童的30-70%之间提高或青春期后期或成年早期“成长性哮喘去”4- - - - - -7,已无症状的年轻哮喘患者可能仍有残留的组织学异常8,9,气道阻塞6,10,11,肺容量增加6,12- - - - - -14.此外,在成年哮喘学龄衰老的肺功能下降似乎与非高血压受试者的速度较大5,7,15长期哮喘可能难以与慢性支气管炎和慢性阻塞性肺病(COPD)区分开来。16,17.这些研究结果,以及哮喘气道重塑的概念1- - - - - -3.,9,18- - - - - -20.提示哮喘与开始于儿童、持续至成年的进行性功能改变有关,并可能以具有实质性不可逆成分的COPD结束。事实上,一些研究表明,早期干预可能有利于肺功能的长期结果21.- - - - - -23.,尽管这不是基于最大支气管扩张后获得的肺功能数据。
整个儿童哮喘的气道阻塞可能是由于肺生长减弱等因素造成的24.,25.由于气道炎症,增强支气管音调音调和/或气道壁增厚和重塑。考虑到抗炎药对肺生长的任何影响,需要具有最大支气管扩张剂数据的纵向研究。几项前瞻性纵向研究,评估儿童哮喘对肺功能发展的影响5,6,11,14描述降低呼气流相比校正高度和/或年龄后正常受试者5,6,11,14,即不能总是由(测量用力呼气量在一秒钟内检测到的FEV1)6,11,14.人们应该谨慎地从这些研究中推断,哮喘患者的肺生长减弱。首先,结论是基于支气管扩张剂前的数据,因此不排除增强的支气管运动张力和/或炎症。其次,使用参考方程而不是健康对照可能会引入人为因素:青春期身高和肺功能之间的关系是复杂的26.,27.以及哮喘病患者延迟的青春期发育高峰28.可能会带来其他问题。第三,应使用总肺活量(total lung capacity, TLC)而不是强迫肺活量(forced vital capacity, FVC)来衡量肺的大小,因为残余体积(RV)/TLC取决于性别,并在青春期随着年龄的增长而增加29.- - - - - -31.,并且由于哮喘儿童的气道闭合可能比控制在控制中更加明显29.,30..
本研究的目的是探讨呼吸道和空域的患儿谁,随机吸入安慰剂或皮质类固醇在固定剂量治疗中度哮喘的成长,不论症状。准肺功能测量期间22个月的中位周期之前和最大支气管扩张后获得。这项研究是1988 - 1992年之间进行的大规模多中心干预研究,这表明在儿童哮喘结果抗炎治疗症状,恶化率,住院的改进的一部分,支气管高反应性32..目前的研究使用了气道功能的测量,以TLC的百分比来校正肺的大小,以避免由于性别差异而产生的虚假结果。由于在青春期生长突增期间出现的人为因素,未使用性别特异性参考方程26.,27..目前的作者认为,强制呼气时气流限制反映了呼气时气道远端进行性的波速流动,FEV1, 60%TLC时最大呼气流量(MEF60%TLC), MEF40%TLC反映了咽喉点位于更中央(气管和主支气管)气道、中间(第二代和第三代)气道和更远端(第4 - 6代)气道时的气道通畅。在患有严重哮喘的成年人和健康对照组中进行了支气管内测量33..根据肺大小(TLC)校正气道功能,并与一项大型纵向研究中不吸烟、无呼吸道症状的荷兰儿童获得的气道功能进行比较26.,29..
材料和方法
主题
研究对象包括参加临床试验的哮喘患者32.,并于1988年和1992年之间招募从门诊的朱莉安娜儿童医院,海牙和鹿特丹大学医院/索菲亚儿童医院呼吸内科。入选标准是:1)中度至中重度哮喘34.,定义为有慢性或间歇性呼吸短促、气喘和/或咳嗽病史;2) FEV1的预测55-90%35.和/或FEV1/ FVC 50 - 75%;引起FEV降低的组胺刺激剂量120%(PD20.)<150 µg; 4) ages 7–16 yrs. The reference population comprised 287 male and 89 female children who participated in a longitudinal study and who had had no respiratory symptoms prior to and during that study26.,31..在长达7年的时间里,每6个月采集一次人体测量和肺功能数据。获得了参与者及其家长的知情同意,当地医学伦理委员会批准了该研究。
设计
在研究之前,皮质类固醇或克隆激素逐渐减少。在4周的磨合期间,药物包括吸入β2agenist(ba)按需。接下来,评估基线肺功能,随机分配给两个治疗臂中的一个,具有性,年龄,医院和吸入的皮质类固醇(ICS)和/或romogycate的分层分配给两个治疗臂之一32..Double-blind inhalation medication consisted of salbutamol 0.2 mg plus budesonide 0.2 mgt.i.d.(BA + ICS)或安慰剂(PL)t.i.d.(BA + PL)通过垫片(Volumatic®)。出于本研究的目的,所有罐头都具有相同的设计,以适应相同的间隔物。每天允许额外吸入的Fenoterol允许4次。当12个月需要超过四种泼尼松龙疗程时,患者从研究中撤出。从罐体重减轻估计遵守疗法。
最大支气管扩张和肺功能测量
In patients, maximum expiratory flow volume (MEFV) curves and measurements of total lung capacity (TLC) were obtained once every 4 months for up to 3 yrs, before and 20 min after bronchodilation achieved with 2 sequential inhalations of (800+200) µg salbutamol at 20 min intervals, using a spacer (Volumatic ®)36..来自先前的一项研究,78名哮喘儿童(年龄范围:9-18岁)的基线FEV1范围从41到预解码值109%,可以得出结论,该剂量是足以获得最大的支气管扩张。After 1,000 µg salbutamol, a plateau was reached in the dose/response curve for all parameters from the MEFV curve, with values that did not differ from those obtained after 1,200 µg salbutamol, and this occurred irrespective of severity of airways obstruction (personal communication: P.J.F.M. Merkus, Sophia Children's Hospital, Erasmus University Medical Center, Rotterdam, The Netherlands). In healthy controls composite MEFV‐curves were constructed using the same protocol as in patients26..RV和TLC分别通过已在受试者验证了氮强制重新呼吸技术确定37.没有38.气道阻塞。
哮喘呼吸道功能的发展
在健康对照和哮喘患者中,通过叠加在TLC上的MEFV数据的插值来计算肺部剩余的MEF60%TLC和MEF40%TLC。从FEV评估年龄的肺功能的发展1%TLC,MEF60%TLC和MEF40%TLC分别作为中央,中间和外围气道口径的衡量标准。RV和FEV.1以TLC的百分比表示,MEF60%TLC和MEF40%TLC以TLC / s表示,以校正肺大小。
结果
六十五名患者(45名男性)参加了该研究。基线数据总结在表1中⇓.表2总结了研究开始和结束时的肺功能指标⇓和3⇓.在随机化的一年内,6名接受BA+PL的男性退出了研究,因此不能纳入分析;一名男性因非医学原因退出研究,另外五名男性因临床恶化而经常需要紧急药物治疗。由于选择性和显著的BA+PL患者退出,一个独立的监测委员会决定在中位随访22个月后停止BA+PL治疗32..因此,BA+ICS组的中位随访时间比BA+PL组长。服用BA+ICS的患者临床改善,特别是在前2个月32..在剩下的59例患者中,有5例(4例采用BA+PL)被排除在分析之外,因为没有观察到TLC的生长(由于早期辍学或在青春期结束时生长缓慢)。34例患者接受了BA+ICS治疗,20例患者接受了BA+PL治疗,并保持了相同的治疗。BA+ICS患者的中位(范围)随访时间较长:2.9(2.0-3.2)年,而BA+PL患者的中位(范围)随访时间为1.7(0.8-2.2)年。
在健康受试者RV / TLC在雄性和雌性明显不同:11岁的年平均数±标准差RV / TLC为18.0±5.3%和20.0±4.7%,(p < 0.001),分别用平均数±标准差随年龄的增加而在两性0.7±1.3%年。两组患者RV / TLC bronchodilation后显著降低(表2所示⇓);前和支气管扩张后的值分别为两性类似,比健康受试者更大的:在11岁时患者与健康对照之间的平均(95%CI)的支气管扩张剂后RV差/ TLC为3.6(1.7-5.4)%为男性和在女性2.9(0.6-5.2)%。The mean±sd longitudinal increase of prebronchodilator RV/TLC in patients (fig. 1⇓)的差异取决于治疗(p=0.007),但治疗对支气管扩张剂后RV/TLC的演变没有显著影响(p=0.52)。支气管扩张剂后RV/TLC在患者中的平均±sd纵向增加与健康受试者没有差异(功率为88%)。
呼吸功能随年龄的发展
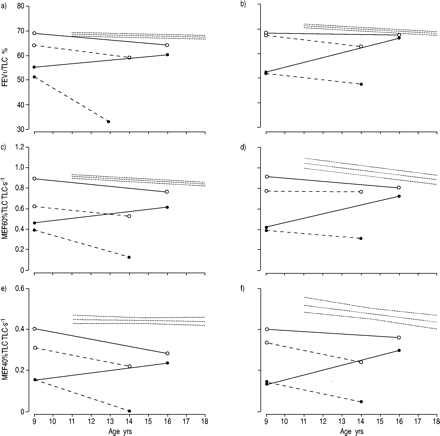
在健康受试者中,气道直径指标以FEV表示1% TLC, MEF60%TLC (TLC·s-1)和MEF40%TLC (TLC·s-1)均显著下降,且女性降幅大于男性(表4)⇓,图2⇓).在整个研究中,接受BA+PL后支气管扩张剂的患者血流仍然低于正常范围,MEF40%TLC的缺陷最为明显。吸入BA+ICS后支气管扩张剂的患者平均FEV1%TLC和MEF60%TLC一般下降在正常范围内(图2a-d)⇓),与MEF40%TLC不同(图2E,F⇓).Postbronchodilator FEV1%TLC对于两种治疗组相似,但MEF60%TLC和MEF40%TLC在BA + ICS治疗患者中较高。患者和健康儿童之间没有差异,可以对濒临困境的近摄加速器FEV的纵向开发来证明1% TLC和MEF60%TLC。MEF40%TLC表达为TLC·s-1在哮喘的男性中越来越快,而不是健康的男性(P = 0.01,表4⇓).The changes of postbronchodilator measures of airway function were unrelated to treatment except for MEF40%TLC which declined faster in patients taking BA+PL than in those taking BA+ICS (table 5⇓,ANOVA,P = 0.01)。The development of pre- and postbronchodilator indices of airway calibre was significantly different in patients taking BA+ICS from those on BA+PL (fig. 2⇓).在前者中,前和支气管舒张气道口径之间的差异减少,而在患者BA + PL它增加或保持在研究过程中类似的。随机分组前,平均值±SEM FEV1最大支气管扩张后,BA+PL组pred增加17.7±1.6%,BA+ICS组pred增加20.4±1.4%。在研究结束时,BA+PL组的支气管扩张剂反应增加到22.7±2.4% pred (p=0.02),而BA+ICS组的支气管扩张剂反应下降到11.6±1.5% pred (p<0.001)。BA+PL组患者的平均±sd治疗依从性为430±180 μ g沙丁胺醇和470±240 μ g安慰剂,而BA+ICS组患者的依从性分别为450±160 μ g沙丁胺醇和453±203 μ g布地奈德,而不是600 μ g每日,在试验期间没有变化(p=0.15)。
讨论
儿科呼吸道的哮喘炎症导致组织学变化1- - - - - -3.,8这可能考虑持续功能异常5,6,11,14,16,17成人哮喘患者支气管扩张剂前气道直径的进行性下降5,7,15.这表明哮喘与儿童时期开始的渐进性功能恶化有关21.,40,进化到慢性阻塞性肺病5,9,19.所涉及的机制可能与变化,如气道减少生长,气道实质相互依存的变化,改变的气道力学由于重塑,或现象如增强bronchomotor音调和炎性支气管粘膜的肿胀。如果炎症和/或重塑的影响相对于肺实质气道功能的增长,但有一个重要的可逆组分,气道功能可通过用吸入糖皮质激素治疗正常化。
目前的研究发现,在哮喘患儿无抗炎治疗(BA + PL),中部,中间和小气道的最大支气管扩张后气道通畅仍然降低,相对于气道功能的追赶生长的肺体积没有迹象.Randomised treatment with inhaled corticosteroids during nearly 2 yrs resulted in a significant and sustained improvement of pre- and postbronchodilator expiratory flows, while growth of central and intermediate airway function was not affected and remained similar to that found in healthy subjects. At the same time, symptom scores, bronchial hyperresponsiveness and exacerbation rates improved dramatically32..因此,看起来,在生长期间,在高水平肺充气气道力学,气道口径和上呼气流量肺弹性回缩力的联合作用是相同的患者上BA + ICS如在健康受试者。然而,由于相对较少的哮喘患儿,这可能是学习动力缺乏实际证明FEV的是水平和发展1%TLC和MEF60%TLC在患者和对照组中非常相似。此外,患者和对照组之间的气道功能差异可能被低估,因为对照组没有吸入支气管扩张剂。此外,也不能排除哮喘气道的僵硬33.,41.,42.可能会弥补因重塑而缩小的不可逆气道。然而,这些数据表明,在哮喘的儿童和青少年可以实现主要和中间气道的正常功能发展,哮喘对ICS维护治疗,这些儿童可以用正常的濒临困境进入成年人1相对于肺的大小。
本研究进一步证明,根据维护治疗的类型,哮喘儿童中的近伯类加速器肺功能的开发可能会显着不同。它还强调的是,患有哮喘肺部大小的肺部估计的预下调,因为患者的RV / TLC受支气管调节和维护治疗类型的影响。在BA + IC患者中预伯克加速器RV / TLC的降低说明了该组中的气道闭合的改善。这些发现与根据治疗不同的气道口径的其他指数的演变一致。在BA + PL支气管扩张剂的患者中,不受影响或增加,而在BA + ICS患者中,预伯克朗加速器气道口径逐渐改善,并且与近伯替尼加速器气道口径的差异减少。因此,吸入的皮质类固醇也充当了间接支气管扩张剂。这里应该提到的是,由于BA + PL患者的选择性辍学,这些治疗效果可能被低估,具有更严重的呼吸症状(导致在22个月的中间后续延续后停止BA + PL处理),具有患者留在BA + PL处理组中,哮喘较小,比BA + ICS组的哮喘较小32..
然而,在所有患者中,包括接受BA+ICS的患者,最大支气管扩张后,MEF40%TLC评估的外周气道功能降低,仍然低于对照组。此外,与健康受试者相比,经支气管扩张剂后RV/TLC评估的气道闭合程度增加,尽管坚持良好的抗炎治疗,但仍存在异常。这些持续的异常不太可能是由于支气管运动张力升高所致,因为该方案涉及最大限度的支气管扩张。此外,它们甚至可能被低估,因为在健康受试者中,肺功能的评估没有支气管扩张。它们可能反映了不可逆的变化,或可能表明布地奈德的剂量和/或沉积不足以完全消除周围气道壁炎症;MEF40%TLC和RV/TLC随局部剂量增加可能有进一步改善。在目前的研究中观察到的布地奈德的影响是由于平均每天摄入0.45毫克而不是处方的0.6毫克,并且与显著的全身副作用无关43..如果支气管高反应性反映了气道炎症,则确实有一些指示患者仍有活跃的气道炎症:PD20.仍在改善,但患者对BA + ICS中位随访22个月后还没有正常化32..尽管如此,绝大多数患者对BA + ICS在审讯过程中成为无症状32.,提示这些残存功能异常可能具有统计学意义,但在儿童和青少年时期与临床无关。
据作者所知,这是第一个同时采用最大剂量支气管扩张和固定剂量吸入糖皮质激素随机治疗的研究,而不考虑呼吸道症状。仅有的两个涉及安慰剂对照抗炎治疗和支气管扩张剂后肺功能测试的纵向研究是儿童哮喘管理计划(CAMP)研究22.以及吸入类固醇治疗作为早期哮喘的常规治疗(START)研究40.目前的研究结论与营地研究相反,其中对患有轻微哮喘的儿童的抗炎治疗给予抗炎治疗导致了改善的支气管高反应性和症状评分,降低了加剧率和救援药物的使用,以及预灌注剂的改善FEV.1但不是支气管扩张剂后FEV1.与本研究相反,在CAMP研究中,支气管扩张不是最大的,儿童哮喘较轻,每日处方皮质类固醇剂量为200µg,并允许皮质类固醇治疗逐渐停止或在症状改善时停止,符合国际指南34..这可以解释为什么在濒临困境的营地研究中观察到吸入的皮质类固醇的有益效果在营地的突行妇女研究员FEV1与安慰剂治疗相比。在START研究中40,children also had less severe asthma, prescribed daily corticosteroid dose was 200 or 400 µg, and the improvement of pre- and postbronchodilator FEV1是显著,但不是临床相关,(<的预解码值3%)。此外,在营和START研究,治疗依从性没有监测,而在目前的工作,病人和他们的父母意识到,符合监测。因此,该研究的设计,哮喘的严重程度,并在端点的差异使得这些研究很难进行比较。
综上所述,尽管本研究样本量小,且存在方法上的局限性,但结论仍然是无症状哮喘儿童仍存在残余的功能异常,即使每日处方600µg布地奈德,支气管张力完全消除。这表明,仅根据症状对哮喘儿童进行抗炎治疗不足以使支气管扩张剂后气道功能恢复正常。在成年人44.,需要基于炎症标记的吸入皮质类固醇治疗,以进一步降低气道炎症,改善外周枢流函数,并在青春期结束时实现最佳的近伯丙酮肺功能。是否在没有呼吸系统症状的情况下这种治疗哮喘的儿童是现实的,并且可以是道德合理的是辩论,以及是否需要最佳的长期预后需要显示。
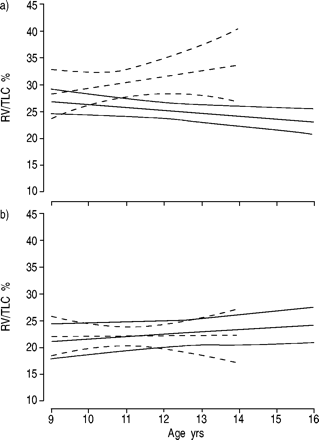
治疗对支气管扩张前后残气量(RV)/总肺活量(TLC)纵向发育的影响。实线表示β治疗2‐激动剂(BA)+吸入皮质激素,虚线指的是BA+安慰剂治疗。给出了平均组趋势和95% CI。
a, b) 1秒用力呼气量(FEV)纵向发展1)/ a)雄性和b)在最大支气管扩张之前和之后的雌性的总肺容量(TLC)(%)。C,d)纵向开发最大呼气流量为TLC的60%(MEF60%TLC(TLC·S.-1))在c)哮喘雄性儿童和d)最大支气管扩张前后的哮喘女性儿童。E,F)MEF40%TLC的纵向开发(TLC·S.-1(e)有哮喘的男性儿童和f)有哮喘的女性儿童在最大支气管扩张前后。实线是指接受β治疗的患者的平均回归线2‐激动剂(BA)+吸入皮质类固醇(ICS),虚线指接受BA+安慰剂(PL)患者的平均回归线。连接闭合符号的线(下)为支气管扩张剂使用前数据,连接开放符号的线(上)为支气管扩张剂使用后数据。虚线为健康受试者的平均回归线和95% CI。服用BA+ICS的患者的中位随访时间比服用BA+PL的患者长(见正文)。
致谢
作者感谢儿童及其父母的贡献,以及Astrazeneca,Boehringer Ingelheim和Glaxosmithkline,用于提供免费学习药物。
脚注
↵编辑评论见第795页。
- 收到了2003年3月20日。
- 接受2004年1月5日。
- ©ERS期刊有限公司