摘要
据报道,肺动脉高压(pH)的动物模型升高了物质P(SP)水平,并且已经显示SP的慢性施用来诱导pH值。在本研究中,分析了活性氧物质(ROS)作为SP诱导的血管重塑和pH的介质的作用。
通过用[SAR的治疗方法在精密切割肺切片中诱导血管重塑。9.,见面11.(o.2) - sp和缺氧。用功能分析用于研究慢性[SAR9.,见面11.(o.2)] - 上ROS,其参与PH的发病机理的增殖和产生SP介导的作用。非肽NK-1受体拮抗剂CP 96345被用于块[肌氨酸9.,见面11.(o.2) - sp效果。DichlorofloureesIndetate方法测定ROS产生和增殖,分别掺入5-溴-2'-脱氧尿苷。
1%的氧(5.8倍)或[Sar9.,见面11.(o.2) - 肺泡区中常氧中的sp(8倍)。[SAR.9.,见面11.(o.2) - SP没有进一步提高缺氧中的ROS水平,表明氧中依赖性机制。高ROS水平稳定缺氧诱导因子-1α并诱导小血管的增殖(4.3倍缺氧和[SAR9.,见面11.(o.2) - sp)。在CP 96345,NitroBluetazolium,CP 96345的存在下阻止了ROS产生和增殖。N-acetylcysteine-和diphenyleneiodonium。
本研究表明的结果表明SP在肺动脉高压血管重塑相关的增殖事件中的作用。
参与初级肺动脉高压(pH)和更常见的仲pH的发育病理学途径仍然不清楚。所有形式的pH的常见特征是肺血管重塑和右心室肥大。pH在人类pH的主要原因是肺泡缺氧1由于慢性肺部疾病导致继发pH值2。缺氧诱导包括肺血管平滑肌细胞(VSMC)在内的各种细胞中活性氧(ROS)的生成,并导致VSMC和外膜成纤维细胞的增殖3.。该机制涉及普遍表达的缺氧敏感转录因子缺氧诱导因子(HIF)-1α,其被ROS稳定1。HIF-1α激活在氧气上最大化(O.2)浓度为0.5-2%4.,而在常氧条件下,泛素促使途径迅速降解5.。
几种观察结果表明,物质p(sp)涉及病理生理事件,导致pH中观察到的血管重塑。稳定SP类似物的药理应用诱导血管重塑,导致介质增厚和大鼠pH的发育,同时已经显示出与TachykinnN-1受体拮抗剂CP 96345的预处理以防止SP诱导的pH值6.。在患有PH的患者中,SP不能引起在健康受试者中观察到的明显的内皮依赖性血管扩张7.。而血管扩张剂反应已被证明是通过激活NK‐1受体和释放NO和前列环素介导的8.,SP诱导的重塑机制仍不清楚。在肺血管的一官碱诱导炎症的大鼠模型中,建议ROS增加SP水平9.,可能通过灭活SP降解酶中性内肽酶(EC 3.4.24.11)。
由于缺氧和SP诱导的血管重塑和pH的相似性,在本研究中解决了SP通过产生ROS产生其效果的假设。使用小鼠的精密切割肺切片(PCLS)作为模型,研究了SP对ROS产生和HIF-1α稳定的影响,以及肺血管中增殖的影响。PLC将细胞培养物在有机体系中的优点结合在一起。它们主要用于药理学10.那11.或毒物学研究,并允许使用人体组织(回顾见12.)。
方法
组织处理
通过宫颈脱位杀死动物后,将500 u甲普丁(Hoffmannla Roche,Grenzachwyhlen,Green)和1毫米甘油林硝酸盐(Merk,Darmstadt,德国)注射到右心室中。然后将肺血管床灌注,用10ml含有0.2%丙基蒽氯化物(重量/体积; Merck),500 U肝素和10μM甘油硝酸盐的10ml预胶水床。然后用1%的低熔胶琼脂糖(德国慕尼黑BioRad)滴注肺部via将气管和胸内脏转移到冷却的林格中。使用vibraatome(Leica,Bensheim,德国)以250μm的厚度切割pcls。这些部分在最低基本培养基(MEM; Gibco,Heidelberg,德国)中培养,在38°C下没有额外的血清,含有21和1%的o2分别。在4小时后改变培养基以除去溶解的琼脂糖。
反应性氧物种测定
在两组使用二氯荧光素二乙酸酯的11只小鼠的pcl中测定了ROS的产生(DCF‐DA;Alexsis, Grünberg,德国),如前所述13.。在1μmDCF-DA存在下孵育六只动物的组1小时,用21或1%o孵育2。在两者o.2条件,5 nM [Sar9.,见面11.(o.2)] - SP,在非肽NK-1受体拮抗剂CP 96345(1μM)的存在下和不存在下,加入。Control sections were incubated with 1 µM CP 96345 or MEM alone. In a second set of experiments, the effects of ROS scavengers, 1 µM nitroblue tetrazolium (NBT; Sigma, Deisenhofen, Germany) and 1 µMN- 在常氧的条件下,仅在常氧的条件下在五只动物中检查了抑制主要ROS发电酶的五苯基碘(DPI;10μm; Calbiochem,Bad Sodene,Germany)的乙酰胞嘧啶抑制剂二苯基碘化物(DPI;10μm;
然后将这些部分固定在4%多聚甲醛(PFA)中,在4%磷酸盐缓冲盐水中洗涤20分钟,在4℃下在0.1M磷酸盐缓冲盐水中洗涤10分钟并保持在黑暗中。共聚焦激光扫描显微镜用于评估转化的DCF-DA的相对量,从而评估ROS的量。在薄壁的五个领域中,以致盲的方式量化每场的ROS产生细胞的数量。在相同水平的各个部分随机选择这些字段,但注意到没有看到大型气道或血管。
增殖试验
在含有1×10的血清红外MEM中孵育一组新的12只动物-4 M 5‐Bromo‐2′‐Deoxyuridine (BrdU) and gassed with 21 or 1% O272 h。在两者o.2条件,5 nM [Sar9.,见面11.(o.2) - 在存在和不存在1μmCC96345的情况下SP。另外,1μmnbt,1μmnac和10μmdpi的影响[sar9.,见面11.(o.2)] - SP在含氧量正常调节增殖活性进行了研究。
切片在4% PFA中固定45分钟,并包埋在TissueTek®(OCT化合物;Sakura Finetek Europe BV, Zoeterwoude, Netherlands),随后用低温恒温器(Leica, Weiterstadt, Germany) 10µm切片进行免疫组化。检测合并的BrdU需要双链脱氧核糖核酸的变性。切片在4°C 0.1 N HCl中孵育10分钟以去除组蛋白,在室温下转移到2n HCl中30分钟,用0.1 M硼砂(pH 8.5)中和10分钟。用单克隆抗体(DAKO, Hamburg, Germany)和小鼠免疫试剂盒(DAKO)观察BrdU合并,然后用strepavidin Texas Red (Amersham, Freiburg, Germany)观察BrdU合并,然后用多克隆兔vonWillebrand Factor抗体(DAKO)进行反染色,用异硫氰酸荧光素标记的山羊抗血清(Dianova, Germany)检测。Hamburg,德国)来识别脉管系统和4 ',6 -二氨基- 2 -苯吲哚,diactate (Sigma)来识别细胞核。在每个实验条件下,每只动物用荧光显微镜(DMRA2;徕卡,Weiterstadt,德国)在200倍放大。结果给出了每条血管的BrdU阳性核。
缺氧诱导因子1α的免疫组化定位
使用单克隆抗体(1:50; DPC Bieromann,Bad Nauheim,Germany)使用单克隆抗体(DPC Biermann,Bad Nauheim,Germany)来定位HIF-1α的平行抑制液部分。
统计分析
使用kruskalwallis分析数据,曼海夫尼U-test和p≤0.05被认为是显着的。错误被给出SEM。
结果
活性氧的生成
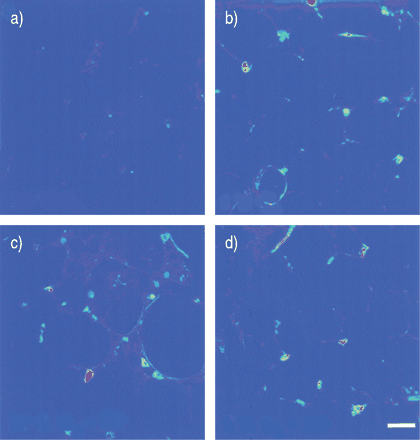
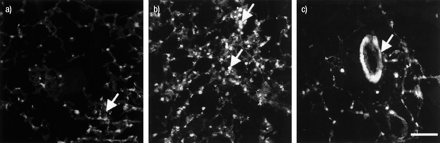
To determine the effect of SP on ROS generation, PCLS were incubated with DCF‐DA for 1 h under 21 and 1% O2后者作为ROS生成和血管重塑的后一种代替,作为缺氧下的ROS产量增加,并且慢性肺泡缺氧经常用于在动物模型中诱导pH值。五个nm [sar9.,见面11.(o.2) - 在存在和不存在1μmCCC96345的情况下,向培养基中添加1μmCCC96345。ROS生产在常见条件下非常低(图1⇓和2⇓)虽然缺氧导致肺泡区内的个体细胞中的ROS产生强大而显着增加(图1⇓和2⇓),但不是在较大的脉管系统,其使用相差显微镜鉴定。Sections incubated with SP displayed a similar ROS‐generation pattern under normoxic conditions as compared to hypoxia (figs. 1⇓和2⇓)但是,生产的细胞数量明显高于缺氧(图2⇓)。对SP和缺氧的主观细胞单独减少阳性细胞的数量(图2⇓)。in.cubating the sections with the NK‐1 receptor antagonist CP 96345 (1 µM) for 15 min prior to the administration of [Sar9.,见面11.(o.2) - SP显着减少了常氧基产生的ROS产生的细胞数量(图2⇓)但没有影响缺氧条件下的ROS生成(图2⇓)。单独对拮抗剂的应用对该系统中该系统中的ROS产生没有影响(图2⇓)。正如预测的那样,用NBT,NAC和DPI的肺切片的温育导致引起[肌氨酸DCF-DA或减少自由基的产生的完全抑制9.,见面11.(o.2)]‐SP在常氧条件下(图3a⇓)。
在21%氧(A和C),1%氧(B和D)和[SAR中的重要肺截面中的反应性氧物种的反应性氧物种(超过1小时)的图像9.,见面11.(o.2)]物质p(c和d)。秤杆=20μm。
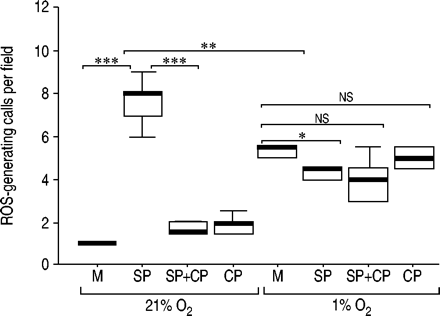
定量检测活性氧(ROS)生成细胞,平均每只动物5个电场(n=5)。M:中等;Cp: Cp 96345(1µm);SP:[SAR9.,见面11.(o.2)] - SP(5纳米)。***:P≤0.001;**:P≤0.01;*:P≤0.05;ns.:不重要的。
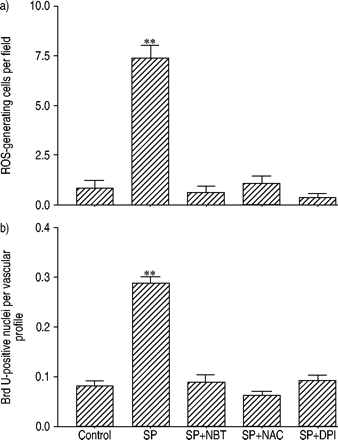
抑制物质P(SP)诱导的活性氧(ROS)产生(超过1小时)和增殖活性(以上超过72小时)通过自由基清除剂切割肺切片,降低烟酰胺腺嘌呤二核苷酸磷酸氧化酶抑制。a)每只动物的五个场的平均值定量ROS生成细胞(n = 5)。b)将增殖活性的定量为每实验条件和动物的25个田地(n = 5)。DPI:二苯基碘鎓(1μm);NBT:Nitroblue四唑(1μm);NAC:N- 缔酸盐(1μm);SP:[SAR9.,见面11.(o.2) - sp(5 nm)。**:p≤0.01。
增殖活动
切片在常氧条件下孵育导致小血管中低增殖活性(图4)⇓和5⇓),通过Brdu定量在72小时和随后的免疫组织中掺入核中。通过免疫组化检测vonfillebrand因素(数据未显示)鉴定小脉管系统。在同一段时间内使细分缺氧诱导小脉管系统(<50μm;图4)的巨大增殖增加⇓和5⇓),而较大的血管没有显示任何o下的任何增殖活动2浓度(>150μm;数据未显示)。五个nm [sar9.,见面11.(o.2)]‐SP在常氧条件下强烈诱导小血管介质内增殖(图4)⇓和5⇓),与缺氧时相同(图5)⇓)但是,[SAR9.,见面11.(o.2) - 在缺氧中施用时SP显着降低(图4⇓和5⇓)。在[萨9.,见面11.(o.2)] - 在常氧条件下的SP效果被强烈拮抗至几乎控制水平1μmCCC96345(图5⇓)。缺氧在[SAR造成的增殖降低9.,见面11.(o.2)] - 通过施用拮抗剂来逆转SP(图5⇓)。
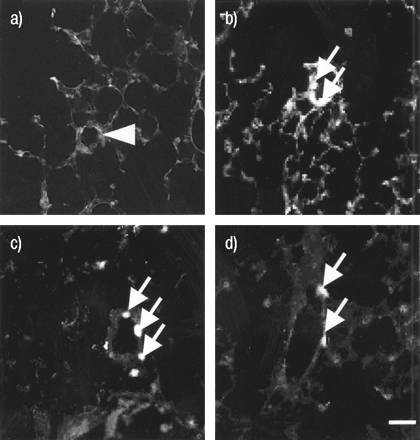
免疫组化定位5‐Bromo‐2’‐Deoxyuridine (BrdU)掺入检测肺小血管的增殖(超过72小时),在21%氧(a和c)、1%氧(b和d)和[Sar]的存在下9.,见面11.(o.2)]物质p(cand d)。箭头:Brdupositive核;箭头:船只。秤杆=20μm。
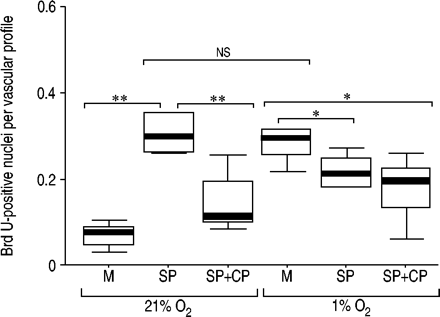
增殖的定量测定为平均每个实验条件和动物(N = 6)25个的字段。M:中等;Cp: Cp 96345(1µm);SP:[SAR9.,见面11.(o.2)] - SP(5纳米)。**:P≤0.01;*:P≤0.05;ns.:不重要的。
在[萨9.,见面11.(o.2) - 通过使用NBT或NAc清除ROS或通过DPI抑制黄曲霉素来完全阻断常氧条件下的SP诱导的增殖活性(图3B⇑)。
检测缺氧诱导因子-1α
正如预测的那样,在常氧条件下肺实质中无法检测到转录因子HIF‐1α(图6a)⇓)。Subjecting the sections to hypoxia stabilised HIF‐1α in cells of the lung parenchyma (fig. 6b⇓)。本地化仅限于核(图6B和C.⇓)。在肺部孵育[SAR9.,见面11.(o.2) - spunder normoxic conditions, HIF‐1α was detected in the parenchyma, as well as a small number of vessels (fig. 6c⇓),而较大的血管没有显示任何HIF-1α稳定(数据未显示)。
72小时后72小时后缺氧诱导因子-1α的免疫型诱导因子1α(21%氧气(o2))),b)缺氧(1%o2c)[sar9.,见面11.(o.2)]常氧中的物质p。箭头:船只。秤栏:50μm。
讨论
PH值的增殖事件是标志性病理特征。这些包括VSMC,成纤维细胞和内皮细胞的增殖,导致在pH中观察到的重塑14.。其结果是,在肺血管床异常增殖活性可以用作血管重塑的指示。
本研究已经解决了SP对扩散表明的ROS和血管重塑的产生的影响,而不试图在PCLS中表征增殖细胞,其显示在支气管中的睫状体击打纤毛,并且在72小时培养后药理学刺激(数据未显示)。这与M观察到的结果一致阿廷等等。10.。此外,已经表明,PCLS保持结构完整性长达60天,但内皮可能在7天后可能在其完整性下降15.。
SP对肺截面的应用导致ROS介导的血管重塑,其增殖活性增加表明。这与通过慢性治疗大鼠的结果获得的结果一致6.。如缺氧所观察到16.,PCLS的72小时培养中的SP治疗是研究肺动脉中血管重塑的有价值模型,这允许时间和动物数减少。
在一角质碱诱导的pH中,显示ROS促使SP的水平9.。该研究的结果表明,在PCLSTO严重缺氧或低剂量的曝光后产生的氧气基数是产生的[SAR9.,见面11.(o.2)] - 在(Peri)血管细胞中的1小时内。[sar的影响9.,见面11.(o.2) - 由于拮抗剂CP 96345显着减少了ROS发电单元的数量,因此SP被NK-1受体介导。使肺部肺截面缺氧和SP对ROS产生没有协同效应,表明SP引起的ROS生产是o2依赖。
Proliferation of vascular cells occurred only in small (<50 µm), resistancetype vessels, which is the part of the pulmonary vascular bed responsible for the pressure elevation observed in PH3.。缺氧导致增加的ROS产生在各种细胞中由任一膜结合还原的烟酰胺腺嘌呤二核苷酸磷酸(NADPH)氧化酶复合物17.那18.或增加线粒体ROS生成13.。已经显示NADPH氧化酶产生的ROS通过激活细胞外信号调节蛋白激酶(ERK)-2与C-FOS的后续表达,在人体主动脉的VSMC中诱导增殖viap21.RAS/ RAF-1 / MEK2路径19.,而线粒体强化RO通常导致细胞死亡20.那21.。事实上,缺氧NADPH氧化酶的激活已经VSMC描述22.。已显示低剂量的ROS在各种细胞中诱导增殖23.包括VSMC24.。
血管增生事件[Sar9.,见面11.(o.2)] - SP似乎也通过NK-1受体介导的,如CP 96345的给药做不仅抑制ROS的产生,而且血管的增殖。由于由[肌氨酸诱导增殖活性9.,见面11.(o.2- SP被活性氧清清剂NBT和NAC以及黄酮蛋白抑制剂DPI所阻断,似乎有可能对[Sar .]产生增殖反应9.,见面11.(o.2) - SP由ROS生成介导。
通过用NBT DPI orscavenging ROS membranerelated ROS产生的抑制已显示导致acomplete停止在缺氧诱导增殖thepulmonary脉管16.。此外,给予[SAR的大鼠的CP 96345是否抑制了大鼠pH的发育。9.,见面11.(o.2) - sp6.。相比于单独的缺氧,血管细胞的增殖是当下标[肌氨酸9.,见面11.(o.2) - 在缺氧中加入SP,表明稍微拮抗作用,这可能是Dueto激活不同信号转导途径的激活。ROS响应缺氧和[SAR的ROS引发的增殖事件9.,见面11.(o.2) - 根据常氧条件下的SP可能涉及HIF-1α的稳定性,因为通过免疫组织化学鉴定蛋白质。臭日中缺氧或[SAR中的妥善核中的血清中1α-阳性核的分布相同9.,见面11.(o.2) - SP孵育,但血管在与[SAR孵育的部分中展示了Strontoner免疫反应性。9.,见面11.(o.2) - SP,同样可能是由于不同信号转导途径的激活。
广泛表达的HIF-1α是缺氧基因表达的全局调节子虽然它被认为是与细胞typespecific调节因子相互作用,以唤起特定小区反应,如。促红细胞生成素或血管内皮生长因子的表达25.。ROS也可能导致诱导Protooncogenes CMYC和C-FOS26.,这反过来通过诱导细胞周期蛋白表达来激活细胞周期27.。其他研究表明,蛋白激酶C介导的磷脂酰肌醇3磷酸激酶/哺乳动物雷米霉素靶蛋白/p70的激活S6K.肺部VSMC中的激酶信号转导通路28.,这可以通过ROS被触发29.那30.。ROS也可能激活ERK‐5 (BMK‐1)via所述的c-Src激酶31.,它在缺氧时被激活,被认为是HIF‐1α的激活激酶32.。
总之,本研究提供了物质P对肺动脉高压病理学病理学涉及的重塑过程作用的依据。在此过程中,活性氧speciesinduced物质P水平的增加,如图中箭头C母鸡等等。9.和P物质介导的活性氧的产生,在本研究中所示,可能导致恶性循环延续肺动脉高压。将得到的血管重塑与阻力血管的受损血管扩张反应相关联。这些机制在本地进行,不涉及中央反射,在生活精密切割肺片观察疗效。
- 收到2003年3月13日。
- 接受2003年5月7日。
- ©ers Journals Ltd