抽象的
细胞衰老是不可逆转的生长停滞状态。本文作者研究博莱霉素,导致肺纤维化的药物,是否诱导肺泡上皮细胞的衰老。
II型肺泡上皮细胞(A549)或大鼠初级II型细胞暴露于博来霉素,然后评估细胞衰老的标志物。在C57BL/6小鼠气管内给予博莱霉素。
作者发现暴露于博莱霉素可诱导A549细胞和大鼠原代II型细胞衰老。衰老的特征是衰老相关的β‐半乳糖苷酶活性的剂量和时间依赖性的增加,衰老相关的细胞形态变化,细胞大小和溶酶体质量的增加,p21蛋白的过表达,和不可逆的生长阻滞。小鼠气管内注射博莱霉素诱导II型上皮细胞衰老相关β‐半乳糖苷酶活性增加,在第7天达到最大值。
这些结果表明,博莱霉素诱导的表型与肺泡上皮细胞衰老的表型难以区分。博莱霉素诱导上皮细胞衰老可能参与了受损的再上皮化导致肺纤维化的途径。
肺纤维化的特点是连续急性肺损伤和进行性纤维化和结构扭曲1.肺纤维化发病机制的原始假设是慢性炎症刺激成纤维细胞2,3..然而,一个新的假设提出,上皮损伤和受损的再生足以刺激成纤维细胞,而不需要持续的炎症4.这一假设表明,肺损伤后受损的再上皮化触发了肺纤维化的过程。肺纤维化患者的一个重要病理特征是I型细胞明显丢失,没有适当的再上皮化,而其他部位出现异常的II型细胞增生4- - - - - -7.再上皮化的缺失被认为诱导活化的成纤维细胞迁移,通过上皮细胞的缺陷从间质室到腔内室,从而导致肺纤维化7.然而,肺纤维化再上皮化受损的机制尚不清楚。
细胞衰老是一种细胞不能再分裂的状态,尽管存在适当的生长因子8.这种状态可以由端粒缩短(复制性衰老)或端粒独立信号,如脱氧核糖核酸(DNA)损伤和氧化应激(应激性衰老)诱导。细胞衰老的状态与以下几个方面有关:不可逆的生长停滞;明显的扁平和扩大的细胞形态;衰老相关的β -半乳糖苷酶(SA β - gal)活性增加;以及细胞周期抑制剂,如p16的表达墨水4a.和p21CIP1 / WAF1 / Sdi18- - - - - -10.大量证据表明,细胞衰老对衰老的表型方面很重要,如伤口愈合延迟、免疫反应减弱和皮肤变薄11.近年来的研究也表明,细胞衰老在肝硬化、动脉粥样硬化等慢性疾病的发病机制中发挥着重要作用12,13.然而,在肺纤维化细胞衰老的作用尚未研究。作者假设,当上皮细胞达到衰老的阶段,上皮再生停止和纤维化得到促进。在本研究中,作者研究博莱霉素,导致肺纤维化的药剂,是否诱导肺泡上皮细胞的衰老。
材料和方法
动物待遇
动物议定书被东京女性医科大学的动物护理和使用委员会批准。如前所述,产生了一种用于博莱霉素诱导的肺纤维化的动物模型14.用腹膜内注射戊巴比妥钠(雅培实验室,北芝加哥,IL,USA)麻醉小鼠,其次是含有50μl含有盐酸霉素的磷酸盐缓冲盐水(PBS)溶液(5 mg·kg−1体重;Nippon Kayaku,Co.,Tokyo,日本)。在玻莱霉素注射后的第1,4,7和21天,用30μg溴脱氧核素(Brdu)腹膜内处理小鼠;4小时后,使用腹膜内注射戊巴比妥过量而被处死。除去肺,通过用50%OCT化合物(组织TEK®; Sakura Finetechnical Co. Ltd,Tokyo,Japan)的手工滴注膨胀,迅速冷冻,并段(3μm)。
细胞培养物和博来霉素治疗
含有10%胎牛血清(FCS)的II型肺泡状上皮细胞系,A549(ATCC#CCL-185),保持在Dulbecco改良的Eagle氏培养基(DMEM)。将细胞(104细胞·cm.-2)在第27和35代之间被放置在8孔腔载玻片或35或60毫米组织培养板上,预先涂有I型胶原(Vitrogen)TM值,凝聚力,帕洛阿尔托,CA,USA)并生长在上面的平台。Once they reached 50% confluence, the cells were rinsed three times with PBS and incubated with DMEM containing 0.1% FCS with or without bleomycin (0.1–50 µg·mL−1)对于所指出的时间。
Primary rat type II alveolar epithelial cells were isolated from adult male Sprague-Dawley rats, weighing 250 g, and maintained in DMEM containing 20% FCS, as previously described15.原代细胞在培养的第2天进行研究,根据公认的形态学和生化标准,这段时间它们是II型细胞样15.主细胞制备物纯度> 90%的由改性柏氏染色和> 90%的存活率的评估,台盼蓝染色评估的。II型细胞暴露在含有20个%FCS的DMEM,因为血清枯竭杀死细胞博来霉素。
细胞增殖分析
博莱霉素处理120小时后,8孔腔载玻片中的A549细胞用PBS冲洗3次,并与含0.1% FCS或10% FCS的DMEM孵育。48 h后,用10µM BrdU脉冲标记细胞60 min,用免疫细胞化学检测含有BrdU的细胞,如下图所示。
细胞大小分析
8孔载玻片中的细胞用3%多聚甲醛固定,并用伊红溶液染色。使用奥林巴斯BX60显微镜(Olympus Optical Co., Ltd, Tokyo, Japan)和奥林巴斯DP50 CCD相机捕捉细胞的数字视频图像,并发送到奥林巴斯成像显微镜工作站(CUSL2G40;奥林巴斯光学有限公司(Olympus Optical Co., Ltd)配备一台运行微软视窗98的电脑和电脑化彩色图像分析软件系统(Win Roof Version 3.5, Mitani Corporation, Fukui, Japan)。然后对每张图像进行测量单元格大小的操作。取每孔300个细胞的平均大小。
溶酶体质量分析
如前所述进行溶酶体质量的形态学检查16.8孔腔载玻片中的细胞用3×10预处理-7 M of bafilomycin A1 (Sigma, St. Louis, MO, USA) or the vehicle dimethyl sulfoxide alone for 15 min at 37°C and then incubated with 5 µg·mL−1吖啶橙(Sigma)10分钟。用PBS洗涤后,将盖玻片安装在载玻片上,并使用由带通450-490nm激励器,510nm二向色镜的奥林巴斯长通滤波器组立即在Olympus BX60显微镜下观察,并且长通过520nm发射器。
Senescence-associatedβ检测牛乳糖
根据先前描述的方法进行SAβ-加染料17,稍作修改。细胞标本在8孔腔载玻片上用2%甲醛和0.2%戊二醛在PBS中室温固定5分钟。冷冻肺组织切片用0.2%戊二醛PBS在4℃下固定5 h。PBS冲洗载玻片,用SA β - gal染色液孵育,该染色液含有40 mM柠檬酸钠(pH 6.0)、150 mM氯化钠、5 mM铁氰化钾、5 mM铁氰化钾、2 mM氯化镁和1 mg·mL−1的(5-溴-4-氯-3-吲哚基β-d半乳糖苷(X-gal的))。一些幻灯片然后如下所述进行免疫染色。
利用博莱霉素治疗21天后小鼠的肺组织切片进行半定量评估SA β - gal强度与纤维化的关系。每张玻片分别选择5个纤维化区域和5个非纤维化区域。对每个电场的SA β‐gal强度进行分级:0=未染色,1=弱染色,2=中等染色,3=强烈染色。在纤维化区和非纤维化区均得到SA β - gal强度的平均级别。
免疫组织化学和免疫细胞化学
SAβ-gal染色后,将组织切片进行处理用于常规免疫。初级抗体是兔多克隆antilaminin(1:50稀释; Sigma公司),小鼠单克隆antipancytokeratin(1:100稀释; Sigma公司),兔多克隆antisurfactant蛋白A(SP-A; 1:100,Santa Cruz Biotechnology公司公司,Santa Cruz公司,CA,USA),大鼠单克隆抗小鼠CD31(1:25,研究Diagnostics公司,富兰德,NJ,USA),大鼠单克隆抗小鼠CD45(1:100,Pharmingen公司,圣地亚哥,CA),和小鼠单克隆抗BrdU(1:100,Chemicon International公司,蒂梅丘拉,CA,USA)。For immunostaining with anti-BrdU, the slides were pretreated with 3 N HCl for 30 min and neutralised with 0.1 M borax buffer, pH 8.5, for 10 min. The primary antibody was reacted with biotinylated anti-IgG conjugated with horseradish peroxidase (HRP)‐labelled polymer (EnVison+ peroxidase; DAKO Japan, Kyoto, Japan). Immunoreactants were visualised by 3,3′‐diaminobenzidine and counterstained with a nuclear fast red solution. For the immunocytochemistry, cell samples on 8‐well-chamber slides were fixed in 70% ethanol at −20°C for 10 min and incubated with 0.3% H2O2然后用3%牛血清白蛋白在PBS中孵育30分钟。载玻片用3 N HCl处理30 min,用0.1 M硼砂缓冲液(pH 8.5)中和10 min,与抗brdu抗体反应,处理如上所示。
组织切片的双染色SA的β-gal活性,无论是SP-A,pancytokeratin,或CD31抗原进行半定量评估。对于每个滑动,随机选择10个显微镜视野。对于每个字段,阳性细胞的每种抗原和阳性细胞与SA的β-gal活性的每种抗原的数量的数量进行计数。计算阳性细胞每种抗原和细胞阳性每种抗原的人口SA的β-gal活性的平均百分比。
免疫印迹分析
细胞裂解液经多环硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,转移到聚偏二氟乙烯膜上,用小鼠单克隆抗p21抗体(1:400;或兔多克隆抗肌动蛋白(1:25 00;σ)。使用辣根过氧化物酶(HRP)标记的抗体检测一阶抗体,然后通过增强化学发光(SuperSignal)显示该抗体TM值,皮尔斯,罗克福德,IL,USA)。
统计分析
所有数据均表示为平均值±sem。使用方差分析和Scheffe检验或适当的双尾非配对t检验检验差异的显著性。
结果
博莱霉素对A549细胞和大鼠II型原代细胞均可诱导细胞衰老
为了确定博莱霉素是否诱导肺上皮细胞衰老,作者用不同浓度的博莱霉素处理肺泡ii型上皮细胞(A549)。因为博莱霉素浓度为100µg·mL−1或更高导致A549细胞的20%死亡,由Trypan Blue染色确定,作者将细胞在含有≤50μg·mL的含有≤50μg·ml的含有含有玻璃霉素的细胞治疗−1.When A549 cells were treated with 50 µg·mL−1通过SA β‐gal活性的增加判断,它们表现出典型的细胞衰老表型(图1b)⇓);a distinct, flat, and enlarged morphology (fig. 1d⇓);溶酶体质量增加(图1f)⇓);和不可逆生长抑制(图1h)⇓)8,16- - - - - -18.细胞衰老的定量分析表明,用博莱霉素处理A549细胞可引起SA β‐gal活性的剂量依赖性和时间依赖性的增加(图2a和b)⇓),细胞大小增加了5倍(图2c⇓),以及剂量依赖性的细胞生长抑制(图2d⇓).如图2b所示,⇓> 50µg·mL处理后,95%的A549细胞表达SA β - gal活性−1博莱霉素处理120 h。免疫印迹分析也显示,用博莱霉素处理A549细胞可引起p21表达量的剂量依赖性增加CIP1 / WAF1 / Sdi1蛋白,一种周期蛋白依赖的激酶抑制剂,介导多种类型细胞的细胞衰老(图3)⇓)9,19.A549细胞是一种肺癌细胞系,可能不能反映正常肺泡上皮细胞的衰老特性。然而,用博莱霉素处理大鼠原代II型细胞也可引起SA β - gal活性的增加,并形成扁平和增大的形态(图4)⇓),这表明博莱霉素诱导衰老主要II型细胞的。然而,作者不能完全排除博莱霉素治疗后肺泡上皮细胞的衰老表型反映了II型的变化I型表型的可能性。两者合计,这些结果表明用博来霉素诱导的表型是由,在肺泡上皮细胞的细胞衰老的不可区分的该治疗。
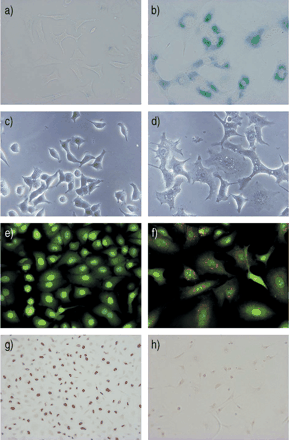
博莱霉素处理A549细胞的衰老表型。A549细胞不加(a、c、e、g)或加博莱霉素(50µg·mL)处理−1) (b, d, f,和h),并检测细胞衰老的标志物。衰老相关β‐半乳糖苷酶活性的染色(a, b)。博莱霉素处理后的细胞形态(c, d)以扁平、增大的细胞为特征(d)。吖啶橙溶酶体染色(e, e)f)显示经博莱霉素处理后,细胞中溶酶体(橙色荧光)的数量和大小显著增加(f)。在博莱霉素暴露前,用溶酶体抑制剂巴菲霉素A1预处理A549细胞时,橙色荧光消失(未显示照片),证实其选择性溶酶体定位。绿色荧光是由吖啶橙与核酸结合而发出的。用(h)或(g)博来霉素处理A549细胞,用磷酸盐缓冲盐水冲洗,然后用10%胎牛血清(FCS)刺激48小时,进行抗溴脱氧尿苷(BrdU)免疫染色。在刺激期的最后60分钟,对细胞进行BrdU脉冲标记。博莱霉素处理可消除FCS刺激的细胞对brdu的掺入(h),表明博莱霉素可引起不可逆的生长阻滞。这些显微照片代表了三次实验所得的结果。
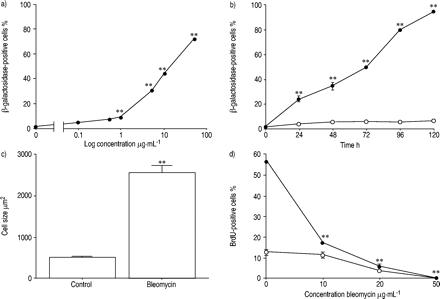
在A549细胞中的细胞衰老的定量分析用博来霉素处理。a)用于衰老相关β半乳糖苷酶活性染色。A549 cells were treated with or without various concentrations of bleomycin for 96 h or b) with (•) or without (○) 50 µg·mL−1不同时期的博莱霉素。c) 50µg·mL处理或不处理A549细胞的大小−1博莱霉素处理120 h。d)溴脱氧尿苷(BrdU的)由A549细胞的掺入。A549 cells were treated with or without various concentrations of bleomycin for 120 h, rinsed with phosphate-buffered saline and incubated with 0.1% foetal calf serum (FCS; ○) or 10% FCS (•) for 48 h. During the last 60 min of the incubation, the cells were pulse-labelled with 10 µM of BrdU; cells that had incorporated BrdU were detected using immunocytochemistry. **: p<0.01相对未经过博莱霉素处理的细胞。4个样品的所有数据均以平均值±sem表示。三次实验中有两次的结果具有代表性。
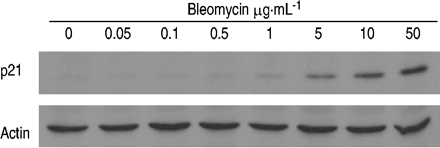
p21的免疫印迹分析CIP1 / WAF1 / Sdi1经博莱霉素治疗后的蛋白。用不同浓度的博莱霉素处理A549细胞120 h。使用抗p21或抗肌动蛋白抗体免疫印迹分析细胞裂解液(每通道50µg)。结果具有代表性的两个实验。
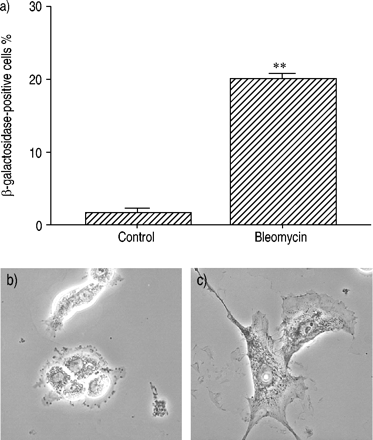
a) Senescence-associated β‐galactosidase activity and b, c) cell morphology in primary rat type II cells treated with or without bleomycin (5 µg·mL−1)对于24小时(B显示未经处理的细胞和C Bleomycin处理的细胞);**:P <0.01相对未经过博莱霉素处理的细胞。数据显示为四个样本的平均值±SEM。结果具有代表性的两个实验。
博莱霉素的气管内注射引起肺泡上皮细胞的增加衰老相关β半乳糖苷酶活体内
要确定是否博莱霉素诱导肺泡上皮细胞的细胞衰老体内,气管内注射博莱霉素的小鼠肺组织切片用SA β - gal染色检测。在博莱霉素注射前(第0天),肺细胞中SA β‐gal染色几乎为阴性(图5a和5f)⇓)other than alveolar macrophages (fig. 5n⇓),其富含溶酶体β半乳糖苷酶20..在博来霉素注射之后,在第4天或之后染色SAβ-GAL阳性的肺细胞的数量(图5C-5E,5H-5J⇓).SA β‐gal染色细胞倾向于定位于塌陷或纤维化的肺病变(图5i和5j)⇓).使用抗韧皮肽,抗SP-A,抗CD31和抗CD45的免疫组织化学分析证明了SAβ-加仑染色的细胞是肺泡上皮细胞(图5K和5L⇓),特别是II型细胞(图5m)⇓)和肺泡巨噬细胞(图5o⇓),而不是内皮细胞(图片未显示)。与预期的一样,SA β‐gal染色细胞在检测的任何时间点均未加入BrdU(图5p)⇓).单独注射PBS后,将细胞阳性SA的数量的β-gal没有增加(数据未示出)。一种半定量分析也显示,肺泡上皮细胞的发生率和类型II阳性细胞SAβ-gal染色在第7天的最大和的增加阳性细胞的发生率达到下保持至少21天(图. 6a⇓).在本分析中,SP-A阳性细胞可能还包括非纤毛细支气管细胞,它们也表达SP-A21.在第21天肺部肺部治疗后,纤维化区域的SAβ-GAL强度的得分远高于非纤维化区域(图6B⇓),这表明细胞衰老可在肺纤维化有关。
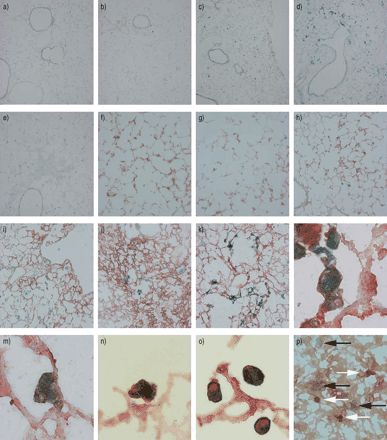
Senescence-associatedβ检测牛乳糖(SA)β加)应承担的活动从小鼠肺组织部分牺牲(a、f (n)和前1天(b, g), 4天(c、h), 7天(d,我,k, l, m, o, p),和后21天(e, j)气管内的注射博来霉素(5 U·kg−1体重)。在处死前4小时,小鼠腹腔注射30µg溴脱氧尿苷(BrdU)。a) -e) SA β‐gal染色(蓝色)。f) -j)显示SA β - gal染色,然后抗层粘连蛋白免疫染色(棕色),以识别肺泡结构。k)和l)用SA β - gal染色,然后用抗泛细胞角蛋白免疫染色(棕色)来识别上皮细胞。细胞核用核坚牢红溶液染色。m)显示SA β - gal染色,然后是抗SP - A免疫染色(棕色),以识别II型细胞,细胞核用核坚红溶液染色。n)和o)显示SA β - gal染色,然后是抗CD45免疫染色,以识别造血细胞(棕色)。细胞核用核坚牢红溶液染色。腔内肺泡巨噬细胞呈SA β - gal阳性染色。 p) SA β‐gal staining (black arrows) followed by anti-BrdU immunostaining (white arrows) shows that the SA β‐gal-stained cells do not incorporate BrdU.
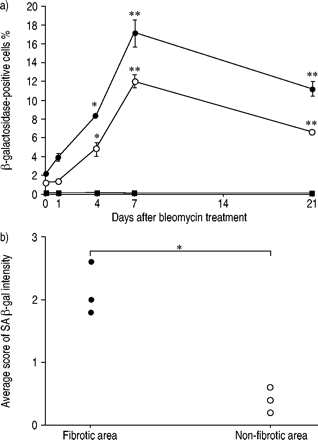
肺组织切片中衰老相关β -半乳糖苷酶(SA β - gal)活性的半定量分析a)气管内注射博莱霉素前(第0天)和第1、4、7和21天小鼠肺组织切片中SA β‐gal活性的时间历程(•:SA β‐gal活性和抗SP‐a免疫染色均阳性的细胞;〇SA β - gal活性和抗泛细胞角蛋白免疫染色均阳性;▪:SA β - gal活性和抗CD31免疫染色均阳性的细胞。所有数据均为平均±扫描电镜三只小鼠在每个时间点。*: p<0.05, **: p<0.01相对一天0。b)气管内注射博莱霉素后21天小鼠肺纤维化相关的SA β - gal强度的平均分级。本文给出了三只小鼠的个体数据。*: p < 0.05。
讨论
尽管最近的证据表明肺纤维化中上皮细胞再生受损,但其机制尚不清楚4.目前的研究表明,在肺泡上皮细胞中,博莱霉素诱导的表型与衰老的表型难以区分在体外和体内.这些结果表明,细胞衰老可能负责岩石霉素诱导的肺损伤后发生的上皮再生受损。
细胞衰老是一种不可逆的生长停滞状态,其特征是明显的形态和生化变化9,10.这种状态是由端粒缩短或端粒独立信号(如DNA损伤和氧化应激)引起的9.目前的研究使用肺泡上皮细胞支持先前的发现,DNA损伤剂,如博莱霉素、放线菌素D和依托泊苷,诱导正常成纤维细胞和一些肿瘤细胞系的衰老表型21.
受伤上皮的再生涉及肺泡II型细胞的增殖。在腹腔内注射博莱霉素后,肺泡型I细胞的早期死亡之后是II型细胞的尝试增殖22.然而,下面的博来霉素诱导损伤II型细胞的增殖能力受到严重影响,从而导致在矿井缺乏适当的上皮再形成的;缺乏上皮再形成的允许活化的成纤维细胞迁移,穿过上皮缺损,从间隙中的管腔内部隔室22.受损的上皮细胞再生导致肺纤维化的这个途径是由以前的研究结果表明上皮细胞增殖的通过与角质细胞生长因子或肝细胞生长因子的治疗改善增强博来霉素诱导的小鼠肺纤维化支持23,24.这些发现提示肺泡上皮细胞的增殖对于防止博莱霉素诱导的肺纤维化的进展是重要的。在此背景下,本研究提示,由于细胞衰老,肺泡上皮细胞的增殖可能受到限制,为肺纤维化的机制提供了新的认识。
细胞衰老的诱导并不表明细胞功能受到抑制。例如,许多研究表明,与正常细胞相比,衰老细胞产生更高水平的基质金属蛋白酶,如胶原酶和基质溶酶,以及促纤维化细胞因子,如白细胞介素- 1β和转化生长因子- β (TGF - β)25- - - - - -27.这些研究表明,衰老细胞可能不仅参与受损的组织再生,而且参与炎症反应和细胞外基质重塑。肺泡上皮细胞的衰老是否与功能异常有关,尚需进一步研究。
这项研究的局限性在于作者使用的是A549细胞,这是一种在非转化细胞中发现的缺乏增殖控制的永生化癌细胞。这个概念很重要,因为博莱霉素是一种能破坏癌细胞DNA的抗癌药物。因此,很难对目前的研究进行推断在体外发现A549细胞对正常的肺泡上皮细胞。然而,作者发现,用博来霉素的原代大鼠II细胞的治疗也诱导衰老表型,其特征在于增加的SAβ-加仑活性和扁平和扩大的细胞形态。作者还发现了一个体内在小鼠中的博来霉素引起的曝光在正常肺泡上皮细胞的增加SA的β-gal活性,这表明A549细胞对博来霉素的响应不是来自正常肺泡上皮细胞的非常不同。
本研究的第二个限制是作者使用的SA的β-gal染色法,以确定肺组织中衰老细胞17.这种方法已经被广泛使用,谁表现出SAβ半乳糖苷酶活和衰老的开始之间有很好的相关许多研究者在体外和比起现场12,13,15.然而,SA的β-gal活性可能并不特异于衰老在所有组织中,因为它也可以表示正常内源溶酶体酸性β半乳糖苷酶的表达,并可能无法区分静态衰老细胞或终末分化细胞16,28.事实上,目前的作者发现正常小鼠肺中的肺泡巨噬细胞也表现出SA β‐gal活性(图5n)⇑),提示必须谨慎使用此标记。目前的作者也不排除博莱霉素可能直接影响SA β - gal活性的可能性。SA β‐gal在啮齿动物和人类细胞中的表达也可能不同。检测衰老细胞的另一种方法体内端粒长度是由什么决定的呢原位杂交。然而,这种方法不适用于检测由DNA损伤和氧化应激引起的端粒不依赖的衰老,在博莱霉素的情况下。因此,这是一个绝对的标志,使特定的鉴定细胞衰老体内,特别是压力导致的衰老,目前还不清楚。在这种情况下,本文作者并没有完全排除SA β - gal活性也可能反映细胞衰老以外的条件的可能性。
本研究的第三个局限性是,尽管博莱霉素诱导的啮齿动物肺纤维化常被用作人类肺纤维化模型,但该模型与人类特发性肺纤维化(IPF)的组织学和生理学特征不相似。例如,最近的一项研究表明,博莱霉素诱导的大鼠模拟弥漫性肺泡损伤(DAD)的早期肺损伤,而晚期、更慢性的阶段表现为局灶性支气管周围炎症和纤维化,并伴有围气肿性改变29.在人类中,博来霉素诱导的肺损伤已被证明toresemble DAD或闭塞性细支气管炎机化性肺炎29,而不是IPF。因此,博莱霉素诱导的模型仅类似于人类一组间质性肺病,主要与支气管血管周围病变相关30..因此,人类需要在博莱霉素致肺纤维化tothe情况本研究结果外推到非常谨慎进行。
虽然本研究有几个限制,但目前的作者提出了上皮衰老可能参与岩土霉素诱导的纤维化,并且可能是其他类型的肺纤维化。在肺纤维化中,重复的脱氧核糖核酸(DNA)和氧化损伤促进上皮细胞衰老,从而限制了它们的增殖能力。再生受损上皮所需的上皮细胞的连续增殖也加速了端粒缩短并促进上皮细胞衰老。当上皮细胞达到衰老阶段时,上皮再生停止和纤维化进展。该模型为肺纤维化的慢性本质提供了合理的解释,这在多年后发出缓慢。细胞衰老在肺组织样品中的详细表征应有助于提供更好地了解肺纤维化的发病机制,并且可能是识别治疗的新靶标。
致谢
作者非常感谢M.四野和Y.杉的出色技术援助。
- 收到了2003年2月4日。
- 接受2003年4月30日。
- ©ERS期刊有限公司