摘要gydF4y2Ba
住在潮湿的建筑物里与呼吸道症状有关,怀疑是由于炎症反应。因此,研究了家庭暴露于霉菌和炎症迹象之间的关系。gydF4y2Ba
非吸烟受试者高(G-high, >4.0 ng·mgydF4y2Ba−3gydF4y2Ba, n=17)或低(G-low, <2.0 ng·mgydF4y2Ba−3gydF4y2Ba, n=18),收集了室内霉菌生物量指标β(1→3)-d-葡聚糖的空气传播量。分析血液样本的粒细胞酶,t细胞亚群和分泌的细胞因子gydF4y2Ba在体外gydF4y2Ba培养的外周血单个核细胞。gydF4y2Ba
与低g组相比,高g组细胞毒性t细胞(CD8+S6F1+)比例降低,PBMCs分泌肿瘤坏死因子-α增多。两组间PBMCs分泌干扰素γ和白细胞介素(IL)-4无明显差异。在非特应性受试者中,g -高组的干扰素- γ和IL-4的比值明显高于g -低组,这与家庭中β(1→3)-d-葡聚糖的含量有关。外周血管细胞、血清中嗜酸性粒细胞阳离子蛋白或髓过氧化物酶分泌IL-10或IL-1β,或血液中细胞计数差异均未发现显著差异。gydF4y2Ba
在家庭中发现的与β(1→3)-d-葡聚糖相关的炎症标志物的影响表明,由于霉菌暴露,炎症/免疫系统的某些部分上调。gydF4y2Ba
- 细胞毒性t细胞gydF4y2Ba
- β(1→3)-d-glucangydF4y2Ba
- 干扰素γgydF4y2Ba
- interleukin-4gydF4y2Ba
- 模具gydF4y2Ba
- 肿瘤坏死因子-αgydF4y2Ba
本研究得到了瑞典斯德哥尔摩Vårdal基金会(赠款A96 082)和瑞典斯德哥尔摩瑞典心肺基金会(赠款199941383)的支持。gydF4y2Ba
许多报告描述了生活在潮湿的建筑物与呼吸道症状以及普遍的疲劳和头痛之间的联系gydF4y2Ba1gydF4y2Ba- - - - - -gydF4y2Ba3.gydF4y2Ba.一些研究表明,儿童和成人患哮喘的风险增加gydF4y2Ba4gydF4y2Ba- - - - - -gydF4y2Ba6gydF4y2Ba.室内湿度的增加为微生物的生长创造了条件,霉菌生长的存在经常与症状有关。因此,这些症状背后的机制可能与呼吸道中对吸入的微生物或来自这些微生物的物质的反应增加有关gydF4y2Ba7gydF4y2Ba.gydF4y2Ba
以前关于在潮湿和/或发霉的建筑物中生活或工作对健康的影响的大多数研究都使用问卷调查来评估症状的流行程度。一些研究对健康影响进行了客观测量,如肺功能的变化、气道反应性或身体隔室炎症标记。在特应性哮喘儿童中,呼气流量变异性峰值与β(1→3)-d-葡聚糖相对于客厅地板面积的含量有关gydF4y2Ba8gydF4y2Ba.学校工作人员鼻灌洗液中肿瘤坏死因子-α (TNF-α)、白介素-6和一氧化氮水平的增加与呆在霉菌污染的学校有关gydF4y2Ba9gydF4y2Ba.生活在>1 ng空气中β(1→3)-d-葡聚糖·m的受试者血清髓过氧化物酶(MPO)水平升高gydF4y2Ba−3gydF4y2Ba与暴露于< 1ng空气中的β(1→3)-d-葡聚糖·m的受试者相比gydF4y2Ba−3gydF4y2Ba10gydF4y2Ba.gydF4y2Ba
暴露于室内霉菌也与免疫系统的影响有关,是对空气过敏原的特应性致敏的一个可能的风险因素。在一项针对儿童的研究中,记忆t细胞数量的增加和CD4/CD8比率的降低与家庭中的霉菌接触有关gydF4y2Ba11gydF4y2Ba.在一项来自德国的儿童研究中,报告住宅中的潮湿和霉菌与高频率的特应性致敏相关gydF4y2Ba12gydF4y2Ba.在一组澳大利亚儿童中,室内接触曲霉菌是过敏性的危险因素gydF4y2Ba13gydF4y2Ba来自芬兰的一项研究表明,接触霉菌的学生中特异反应性疾病的发病率有所上升gydF4y2Ba14gydF4y2Ba.gydF4y2Ba
为了进一步评估家中霉菌暴露对炎症和免疫系统的影响,在空气中β(1→3)-d-葡聚糖水平高(g -高)或低(g -低)的家庭中进行了一项研究。这种存在于真菌细胞壁中的葡萄糖化合物被用作空气中霉菌总生物量的指标。通过测量炎症标志物水平和血液中淋巴细胞亚群数量以及培养的外周血单个核细胞(PBMCs)分泌的细胞因子来评估临床效果。gydF4y2Ba
方法gydF4y2Ba
主题gydF4y2Ba
该研究的对象是从此前在一个梯田住宅地区的调查中招募的gydF4y2Ba10gydF4y2Ba通过在当地报纸上登广告,寻找家中有霉菌问题的人。入选标准为年龄19-65岁,不吸烟,无医生诊断的哮喘或需要药物治疗的疾病。瑞典Göteborg Göteborg大学医学院伦理委员会批准了该研究,所有参与研究的受试者都给予了知情同意。gydF4y2Ba
测量受试者家中空气中β(1→3)-d-葡聚糖含量,并在招募人群中定义两组:β(1→3)-d-葡聚糖含量<2.0 ng·m的组gydF4y2Ba−3gydF4y2Ba>为4.0 ng β(1→3)-d-葡聚糖·mgydF4y2Ba−3gydF4y2Ba(g -高),总共35个受试者。用于高暴露和低暴露的限值是基于之前的排屋研究的结果,在接受检查的75所房屋中,30%的β(1→3)-d-葡聚糖水平为>4 ng·mgydF4y2Ba−3gydF4y2Ba<2.0 ng·m的30%gydF4y2Ba−3gydF4y2Ba10gydF4y2Ba.gydF4y2Ba
除了G-low组的三个家庭和G-high组的两个家庭,每个家庭都招募了一个人。在广告招募的21个人中,43%被归为g -高组,在之前研究招募的14个人中,57%根据上述标准被归为g -高组。gydF4y2Ba
表1gydF4y2Ba⇓gydF4y2Ba显示β(1→3)-d-葡聚糖水平和受试者特征。gydF4y2Ba
Home β(1→3)-d-葡聚糖水平与受试者特征gydF4y2Ba
每位受试者抽取两份血样,用于分析血清标志物水平和PBMCs细胞因子分泌。每隔2-3周采集一次样本,取每个人两次测量结果的平均值。使用每位受试者的单一血液样本进行淋巴细胞分型。gydF4y2Ba
β(1→3)-d-葡聚糖水平的测定gydF4y2Ba
空气中的灰尘是用一种机器产生的,这种机器的设计大致相当于几个人在房间里走动所产生的灰尘gydF4y2Ba15gydF4y2Ba.粉尘发生器运行了5分钟,然后是10分钟的暂停。抽样使用了两个这样的周期。通过孔径为0.8µm的聚碳酸酯过滤器(Isopore®;Millipore, Inc., Boston, MA, USA)并排安装在距地面0.8米的高度,速率为5 L·mingydF4y2Ba−1gydF4y2Ba.每个家庭都调查了两个房间。在30个家庭中,有25个家庭的卧室和26个家庭的客厅进行了采样。其他采样的房间是工作室、餐厅和地下室。gydF4y2Ba
为了使β(1→3)-d-葡聚糖的三重螺旋结构松散,使其溶于溶于无热原水的10ml 0.3 M氢氧化钠中,使滤膜振荡10min。然后用β(1→3)-d-葡聚糖特异性分析溶液gydF4y2Ba鲎gydF4y2Ba溶菌产物gydF4y2Ba16gydF4y2Ba.50µL的过滤提取样品被放置在微孔板和50µL特异性β(1→3)-d-葡聚糖裂解物(funtic G Test®;Seikagaku Corp., Tokyo, Japan)。在分光光度计(Well reader®;sciics公司,东京,日本),随后的显色反应动力学读取光度,转化为吸光度单位,并与使用Fungitech G TE参考标准(Seikagaku公司)创建的标准曲线进行比较。结果以纳克/毫升液体表示,检出限为20 pg·mLgydF4y2Ba−1gydF4y2Ba.根据通过过滤器的气流计算β(1→3)-d-葡聚糖的空气浓度。在分析中使用了从两个采样点确定的平均暴露量。gydF4y2Ba
症状gydF4y2Ba
受试者回答了一份关于前3个月出现的症状的问卷。治疗的症状包括咳嗽(干咳或有痰)、胸闷、气短、眼睛、鼻子或喉咙发炎、鼻塞和鼻子发痒。问题还包括头痛、异常疲劳、胸部喘息和皮肤问题。对于每种症状的流行程度,采用了1 - 4级的评分:1:从不或很少;2:一个月几次;3:一周几次;4:日常。gydF4y2Ba
血细胞计数gydF4y2Ba
在含有乙二胺四乙酸的试管中收集静脉血,并在May-Grünwald Giemsa染色的涂片上进行差异细胞计数,并使用光学显微镜计数。淋巴细胞亚群用流式细胞术量化。辅助/诱导(CD3+CD4+)和细胞毒性/抑制(CD3+CD8+) t细胞群被鉴定。CD3+CD8+细胞也与单克隆抗体结合S6F1进行分析,S6F1是白细胞功能相关抗原-1复合物(CD11a) α链的表位。表达S6F1的CD8+ t细胞被归类为细胞毒性细胞,而对S6F1染色较弱的CD8+ t细胞要么是原始细胞,要么是抑制效应细胞gydF4y2Ba17gydF4y2Ba.由于技术问题,两名低g受试者和三名高g受试者的细胞毒性t细胞(CD8+S6F1+)数量无法测定。gydF4y2Ba
粒细胞激活的标记物gydF4y2Ba
血清嗜酸性阳离子蛋白(ECP)采用荧光酶免疫分析(CAP ECP FEIA;Pharmacia Diagnostics, Uppsala,瑞典)。采用放射免疫分析技术(CAP MPO RIA;法玛西亚诊断)。gydF4y2Ba
特异反应性gydF4y2Ba
采用荧光酶免疫分析技术(CAP Phadiatop®FEIA; CAP Phadiatop®FEIA;法玛西亚诊断)。使用截止值为0.35 kU·L的特异性免疫球蛋白E校准器将结果表示为阳性(特应性)或阴性(非特应性)gydF4y2Ba−1gydF4y2Ba作为参考,按照制造商的说明。gydF4y2Ba
细胞因子的生产gydF4y2Ba
静脉血收集在含有柠檬酸钠、凝胶屏障和密度梯度液体(CPT)的真空管中gydF4y2BaTMgydF4y2Ba管;Becton Dickinson,富兰克林湖,新泽西州,美国)。在1500 ×水平转子中离心后gydF4y2BaggydF4y2Ba室温20分钟,收集pbmc,在添加10%同源血清的Hank's盐溶液中洗涤两次。然后将pbmc悬浮在AIM V®培养基中(Gibco BRL, Life Technologies,佩斯利,英国),并添加4×10gydF4y2Ba−5gydF4y2BaM -巯基乙醇到最终浓度2×10gydF4y2Ba6gydF4y2Ba细胞·毫升gydF4y2Ba−1gydF4y2Ba.细胞与植物血凝素(PHA, Murex Diagnostics Ltd, Dartford, UK)一起或不一起孵育,最终浓度为250 ng·mLgydF4y2Ba−1gydF4y2Ba或脂多糖(大肠杆菌026:B6;Difco实验室,底特律,MI, USA),最终浓度为500 pg·mLgydF4y2Ba−1gydF4y2Ba.PHA作为主要的t细胞刺激用于测量干扰素γ (IFN-γ)和IL-4的分泌,脂多糖作为主要的单核细胞刺激用于测量TNF-α的分泌。在5% CO中孵育48小时后gydF4y2Ba2gydF4y2Ba在37°C时,收集上清液,在细胞因子分析前保存于−25°C。使用酶联免疫吸附试验(ELISA)试剂盒分析来自未受刺激PBMCs的TNF-α,灵敏度为0.1 pg·mLgydF4y2Ba−1gydF4y2Ba(Quantikine高敏感;研发系统,阿宾顿,英国)。使用pelikincompact分析受刺激PBMCs中的IL-1β、IL-4、IL-10、IFN-γ和TNF-αgydF4y2BaTMgydF4y2Ba人细胞因子ELISA(荷兰红十字会输血中心实验室,荷兰阿姆斯特丹)。gydF4y2Ba
我们分析了所有g值低的受试者和14个g值高的受试者的PBMCs细胞因子。在两个不同的情况下测量受刺激和非受刺激PBMCs的细胞因子分泌,方法用于分析。所有细胞因子分析的受试者内变异中值为~ 30%。gydF4y2Ba
统计分析gydF4y2Ba
对于同一个人的重复测量,计算变异系数(CV),以评估第一次和第二次测量之间的变异。结果以括号内第10和第90百分位的组中位数表示。采用Mann-Whitney u检验检测高g组和低g组血液分析的差异。症状差异用卡方检验检验。对非特应性受试者亚组也进行了分析。低数量的特应性受试者不证明单独的统计分析这一组。使用Spearman秩相关检验计算连续变量之间的相关性。gydF4y2Ba
结果gydF4y2Ba
表2gydF4y2Ba⇓gydF4y2Ba显示淋巴细胞分型结果。高g组的CD8+细胞数量和细胞毒性t细胞(CD8+S6F1+)数量呈下降趋势。高g组细胞毒性t细胞(CD8+S6F1+)的比例明显低于低g组。在对非特应性受试者的单独分析中也看到了类似的结果(数据未显示)。g -低组与g -高组间CD4+ t细胞无差异。gydF4y2Ba
家中(1→3)-d-葡聚糖水平低(G-low)和高(G-high)人群血液中不同CD8+ t淋巴细胞的数量和比例gydF4y2Ba
与低g组相比,高g组未受刺激PBMCs分泌的TNF-α明显更多(10.7 (5.9-15.3)gydF4y2Ba与gydF4y2Ba7.3 (4.1 - -15.9) pg·毫升gydF4y2Ba−1gydF4y2Ba,p < 0.05)。在对非特应性受试者的单独分析中也发现了类似的趋势,尽管差异不显著(数据未显示)。重复TNF-α分析在g高组的中位受试者内CV为31%(最高84%),在g低组的中位受试者内CV为21%(最高52%)。当重复样本间CV <20%的受试者进行比较时,组间仍发现显著差异(9.3 (7.4-14.8)pg·mLgydF4y2Ba−1gydF4y2Bag -高组(n=6)gydF4y2Ba与gydF4y2Ba4.2 (4.1 - -5.5) pg·毫升gydF4y2Ba−1gydF4y2Ba低g组(n=5), p<0.01)。gydF4y2Ba
脂多糖刺激PBMCs可使TNF-α分泌显著增加,但在低g组和高g组间无差异。gydF4y2Ba
与低g组相比,高g组pha刺激的pbmc中IFN-γ的分泌量较高,IL-4的分泌量较低,但两组间无显著差异(IFN-γ: 1305 (163 - 6520) pg·mL)gydF4y2Ba−1gydF4y2BaG-low组gydF4y2Ba与gydF4y2Ba1783年(202 - 10935)pg·毫升gydF4y2Ba−1gydF4y2BaG-high组;IL-4: 7.3 (1.1-46.2) pg·mLgydF4y2Ba−1gydF4y2BaG-low组gydF4y2Ba与gydF4y2Ba6.6 (1.2 - -26.8) pg·毫升gydF4y2Ba−1gydF4y2BaG-high组)。重复样品间IFN-γ的CV中位数在G-low组为34%(最大值为129%),在G-high组为27%(最大值为133%)。低g组IL-4 CV为33%(最大值126%),高g组为43%(最大值112%)。两组之间的一致关系促使我们分析两种细胞因子之间的比率,作为t辅助细胞(Th) 1型和2型相关激活的平衡评估。与低g组相比,高g组IFN-γ/IL-4比值升高的趋势不显著(228(86-675)。gydF4y2Ba与gydF4y2Ba129(54 - 554))。当单独分析非特应性受试者时,高g组的IFN-γ/IL-4比值明显高于低g组(247(116-734))。gydF4y2Ba与gydF4y2Ba126 (34 - 514), p < 0.05)。IFN-γ/IL-4比值与家庭测定的β(1→3)-d-葡聚糖含量之间也存在显著相关性(r=0.47, p<0.05)。图1gydF4y2Ba⇓gydF4y2Ba说明了这种关系,排除了一个非常高的β(1→3)-d-葡聚糖在家里(51.7 ng·m)的受试者gydF4y2Ba−3gydF4y2Ba干扰素-γ/ il - 4 = 172;r = 0.50, p < 0.05)。gydF4y2Ba
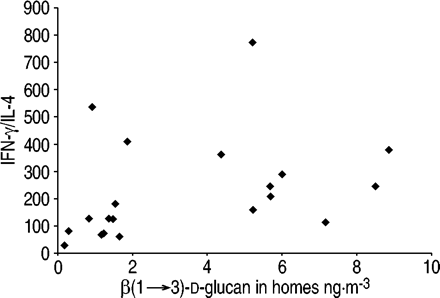
家庭β(1→3)-d-葡聚糖水平与干扰素γ (IFN-γ)和白细胞介素(IL)-4从植物血凝素刺激的外周血单个核细胞分泌的比值之间的关系,不包括一个家庭β(1→3)-d-葡聚糖非常高的受试者(51.7 ng·m)gydF4y2Ba−3gydF4y2Ba干扰素-γ/ il - 4 = 172)。gydF4y2Ba
g -高组和g -低组在PBMCs分泌IL-10或IL-1β、血清中ECP或MPO水平、血液中差异细胞计数或症状流行率方面没有发现显著差异。gydF4y2Ba
讨论gydF4y2Ba
被招募的人代表了有偏见的人群样本,因为他们意识到与家庭霉菌接触有关的问题,或回答了一则要求家庭有霉菌问题的人参与的广告。从之前的研究中招募的人群gydF4y2Ba10gydF4y2Ba在之前的研究中,与总体人群相比,报告的一些症状,如涉及鼻子和中枢神经系统相关症状的患病率略高。对于其他症状,如喉咙刺激和咳嗽,患病率相似。对于通过广告招募的人群,可以合理地假设该群体的症状患病率高于随机人群样本。然而,根据受试者家中β(1→3)-d-葡聚糖的测量结果,而不是根据家庭霉菌问题的主观报告,对暴露组进行了分配。在两个招募组中,高g组和低g组的受试者分布相似(见方法部分),高g组和低g组之间的症状流行率无差异。综上所述,根据症状或招募途径的选择偏差不太可能解释低g组和高g组之间血液中炎症标志物水平的差异。gydF4y2Ba
结果表明,g -高组细胞毒性CD8+ t细胞比例较低,对淋巴细胞有影响。先前的一项研究表明,只有表达S6F1的CD8+ t细胞可以通过内皮层迁移gydF4y2Ba18gydF4y2Ba另一项研究表明CD8+S6F1+ t细胞具有细胞毒性作用gydF4y2Ba17gydF4y2Ba.g含量高的那组血液中这些细胞的比例减少,可能是由于气道中的炎症活动增加了滞留在肺中的结果。事实上,消防员gydF4y2Baet al。gydF4y2Ba19gydF4y2Ba当他们比较特发性肺纤维化患者的血液和支气管肺泡灌洗液时,发现CD8+S6F1+ t细胞数量呈反比关系。家庭霉菌暴露与血液淋巴细胞影响之间的关系已在先前的研究中进行了探讨gydF4y2Ba11gydF4y2Ba.本研究调查了儿童,与目前的结果相反,数据显示CD4+ t细胞数量略有减少,CD8+ t细胞数量略有增加,导致霉菌暴露儿童CD4+/CD8+比值较低。造成这种差异的原因尚不清楚;成人和儿童在接触或反应上的差异是可能的解释。gydF4y2Ba
一些研究表明,住在有霉菌和/或潮湿的房子里与儿童特异反应风险增加有关系gydF4y2Ba12gydF4y2Ba- - - - - -gydF4y2Ba14gydF4y2Ba.这种关系得到了小鼠实验研究数据的支持,在小鼠实验中,β(1→3)-d-葡聚糖诱导肺组织细胞中编码IL-10 (th2驱动细胞因子)的信使核糖核酸表达增加,而促进IFN-γ产生的IL-12的表达被抑制gydF4y2Ba20.gydF4y2Ba.然而,在本研究中,非特应性g -高组比非特应性g -低组表现出更高的IFN-γ/IL-4比值,该比值与家庭β(1→3)-d-葡聚糖水平相关。这表明,在非特应性受试者中,β(1→3)-d-葡聚糖在家暴露与细胞因子分泌Th2模式无关。之所以只有在非特应性受试者中发现高g组和低g组之间的比例不同,可能是因为在特应性受试者中,高g组的IFN-γ和IL-4的分泌有增加的趋势。gydF4y2Ba
在本研究中,发现了非受刺激PBMCs分泌TNF-α的影响,以及血液t细胞亚群的变化和IFN-γ/IL-4比值与受试者家中β(1→3)-d-葡聚糖水平的关系。根据之前对一个梯田住宅地区的研究gydF4y2Ba10gydF4y2Bag -高组血清中MPO浓度高于g -低组,但差异不显著。对于研究的其他炎症标志物,未发现显著影响。这表明,在本研究的水平下,暴露于β(1→3)-d-葡聚糖的受试者不存在大规模炎症反应,这一结论的依据是,报告的症状程度与家庭中β(1→3)-d-葡聚糖水平之间缺乏关联。gydF4y2Ba
空气中的β(1→3)-d-葡聚糖与炎症细胞因子之间的关系并不一定意味着霉菌是致病因子。霉菌生长所需的条件也促进了其他微生物的生长和建筑材料中挥发性有机化合物的形成gydF4y2Ba21gydF4y2Ba.在之前的研究中,发现了地板灰尘中革兰氏阴性菌内毒素的数量与哮喘的严重程度之间的关系gydF4y2Ba22gydF4y2Ba- - - - - -gydF4y2Ba24gydF4y2Ba.本研究未对内毒素进行分析,因为根据作者从早期研究中获得的经验,使用当前技术采样的住宅空气中内毒素水平通常低于所使用的检测限(0.6 pg·m)gydF4y2Ba−3gydF4y2Ba).gydF4y2Ba
相反,霉菌细胞含有许多生物活性物质。真菌毒素的gydF4y2Ba分枝杆菌murale有售gydF4y2Ba而且gydF4y2Ba葡萄穗霉属atragydF4y2Ba与症状和疾病有关gydF4y2Ba25gydF4y2Ba.细胞壁物质β(1→3)-d-葡聚糖本身对免疫系统有重要作用gydF4y2Ba27gydF4y2Ba.需要进一步的工作来评估这些来自微生物的潜在炎症因子在与室内暴露有关的症状中的作用。gydF4y2Ba
总之,目前的结果表明,生活在β(1→3)-d-葡聚糖水平较高的家庭与炎症和免疫系统某些部分的变化之间存在关系。在非特应性患者中,发现干扰素γ /白细胞介素-4比值与在家中测定的β(1→3)-d-葡聚糖量之间存在剂量/反应关系。血液细胞肿瘤坏死因子-α分泌增加,血液中细胞毒性CD8+ t细胞比例减少,提示与霉菌接触相关的呼吸道炎症活性上调。gydF4y2Ba
致谢gydF4y2Ba
作者感谢D. Söderberg, G. Arvidsson, E. Kerekes和R.M. Olofsson娴熟的技术管理。gydF4y2Ba
- 收到了gydF4y2Ba2001年10月1日。gydF4y2Ba
- 接受gydF4y2Ba2002年8月8日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba














