摘要
T -辅助性(Th)1细胞在超敏性肺炎的发病机制中起关键作用。持续低水平接触抗原可诱导慢性超敏性肺炎伴肺纤维化。虽然这种暴露可能激活肺中的Th1细胞,但尚不清楚Th1细胞是否被激活本身可导致肺纤维化。为了确定这一点,研究了Th1克隆诱导的肺病理。
小鼠(BALB/c)腹腔注射Th1克隆1-4次。每次注射间隔4天,然后重复暴露于雾化卵清蛋白(OVA),每天一次,持续5天。
支气管肺泡灌洗液(BALF)中巨噬细胞和淋巴细胞数量随着Th1转移数量的增加而增加。中性粒细胞的数量也增加,但在第二次转移时达到峰值,然后在进一步转移后下降。肺细胞浸润增多,肺泡壁增厚,II型细胞增多。然而,组织学结果显示没有纤维化的证据,羟脯氨酸水平没有增加。组织学和BALF结果在停止暴露OVA 2周后得到改善,表明th1诱导病理的可逆性。
总之,T辅助1细胞的过养转移导致可逆性肺泡炎,但不会导致肺纤维化。
间质性肺疾病由100种已知或未知病因的个体疾病组成1.它们作为原发疾病或全身性疾病的一部分,如胶原-血管疾病,有时可导致呼吸衰竭和死亡。这组疾病有共同的特点和临床病程。最初上皮细胞损伤后被认为是肺泡炎。肺泡炎有时是自限性的,但也可能进展。在后一种情况下,发生肺纤维化。这些病理变化的机制尚不完全清楚。然而,T细胞可能在这些疾病的病理生理学中起重要作用。
在T细胞中,CD4+细胞可根据细胞因子的分泌模式分为两个亚群。T辅助(Th)1细胞特征性地分泌干扰素(IFN)‐γ和淋巴毒素。Th2细胞分泌白介素(IL)‐4、IL‐5和IL-132.慢性铍病、肺结节病、移植后闭塞性细支气管炎和韦格纳肉芽肿病等间质性肺疾病的肺中均可检出Th1细胞3.- - - - - -6.此外,越来越多的证据表明th1细胞介导的迟发性超敏反应在超敏性肺炎(HP)的发病机制中起着关键作用。7.HP是由吸入各种各样的国内环境抗原引起的,可发生三种临床形式:急性、亚急性或慢性。持续低水平接触病原抗原可诱发亚急性和慢性HP。未被发现和未经治疗的亚急性HP可能发展为慢性HP,其特征是不可逆的肺纤维化。虽然持续暴露抗原可激活肺中的Th1细胞,但尚不清楚Th1细胞是否会持续激活本身可导致肺纤维化。
在本报告中,研究了过养转移卵清蛋白(OVA)特异性Th1克隆的影响,以了解Th1诱导的肺病理,特别是确定Th1细胞的慢性激活是否可以诱导肺纤维化变化。
材料与方法
T细胞克隆的特征
OVA (V级;Sigma Chemical Co., St. Louis, MO, USA)反应性Th1克隆是通过皮下注射抗原(500µg乳化在Complete Freund’s佐剂中)到小鼠的尾巴和脚垫中产生的。注射后5-7天,从引流性腘窝淋巴结和腹股沟淋巴结中提取单细胞悬浮液。克隆通过直接放置引物淋巴结细胞(1细胞·孔)分离−1),丝裂霉素C处理的脾细胞(1×106·好−1)、抗原(100 mg·mL−1)和IL‐2 (50 U·mL−1),在96孔平底组织培养板中,含有罗斯威尔公园纪念研究所(RPMI) 1640培养基,补充10%热灭活胎牛血清(Gibco, Grand Island, NY, USA), 100 U·mL−1青霉素G, 100µG·mL−1链霉素、50 mM 2‐巯基乙醇(西格玛)和10 mM N‐2‐羟乙基哌嗪‐N‐2‐乙烷磺酸(西格玛)。扩增阳性孔中的细胞,选择细胞生长至抗原,以0.3细胞·孔重新克隆−1.用于本研究的克隆至少维持了10个月。用刀豆蛋白A(1µg·mL)刺激培养T细胞克隆培养基−1;Vector Labs, Burlingame, CA, USA)在48小时后收集,并在−80°C保存直到使用。根据制造商的说明,使用市上可用的酶联免疫吸附试验(ELISA)试剂盒(Endogen, Boston, MA, USA)测量T细胞克隆培养基中IFN - γ、IL - 4和IL - 5的浓度。为了进行增殖试验,这些克隆被接种(2×105·毫升−1)在有或无OVA的96孔平板中(1 mg·mL−1)、抗il‐2单克隆抗体(S4B6)和抗il‐4单克隆抗体(11B11)8.克隆体在37°C的二氧化碳(CO2)培养72 h。3.H‐胸腺嘧啶(0.5 μ Ci·well−1)在收获前15 h加入3.H‐胸腺嘧啶用液体闪烁计数器测定。
辅助T - 1克隆的过继转移
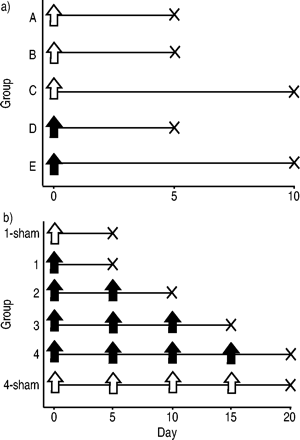
小鼠(BALB/c, 6-8周龄雌性;Charles River实验室,神奈川,日本)腹腔注射Th1克隆(5×106·500µL−1磷酸盐缓冲盐水(PBS每只小鼠)或单独PBS,然后用雾化OVA (50 mg·mL)反复挑战−1, 20分钟),持续5天或10天(图1a⇓).挑战在50 mL塑料管中进行,OVA气溶胶由5 L·mL压缩空气驱动的DeVilbiss 646喷雾器(DeVilbiss Corp., Somerset, PA, USA)输送−1,如前面所述,只是做了一些修改9,10.
实验小鼠的实验方案。a).小鼠腹腔注射T‐helper 1克隆(5×106;D、E组;填充箭头)或磷酸盐缓冲盐水(PBS)单独(A组,B组,C组;开箭头),然后反复挑战雾化卵清蛋白(OVA) 5天(B组和D组)或10天(C组和E组),或PBS 5天(A组)。B)小鼠腹腔内重复注射相同数量的Th1克隆(5×106)或单独PBS(1‐假和4‐假)最多4次,每次注射(间隔4天)后重复暴露于雾化OVA (50 mg·mL)−1, 20分钟),持续5天。最后一次暴露于OVA 24小时后对小鼠进行检测。
Th1克隆的串行传输协议如图1b所示⇑.小鼠腹腔注射相同数量的Th1克隆(5×106)最多4次,每次注射(间隔4天),随后重复暴露于雾化OVA (50 mg·mL)−1, 20分钟),持续5天。因此,四次转移涉及每天暴露于OVA,持续20天。
最后一次暴露于OVA后24小时,麻醉下颈椎脱位处死小鼠。通过手术暴露的气管插管,从全肺获得支气管肺泡灌洗液(BALF) 0.5 mL,分3次。用血细胞计计数BALF中的细胞。用细胞旋液制剂(May-Giemsa染色)获得细胞计数差异。为进行组织学检查,取肺用4%多聚甲醛固定。然后将组织包埋在石蜡中,切成5微米的切片。切片用苏木精、伊红和马尾松三色染色。
特异性抗体水平的测定
采用间接ELISA法测定ova特异性免疫球蛋白(Ig)E和IgG2a血清抗体滴度9,10.板(Costar, Cambridge, MA, USA)涂覆200µg·mL−1用0.1 M NaHCO稀释的OVA3.(pH值8.3)。在4°C孵育过夜后,用1%牛血清白蛋白(Sigma)在37°C下冲洗并堵塞2小时。将连续稀释的血清样本应用于堵塞的孔中,并在4°C下孵育过夜。将山根过氧化物酶标记的大鼠抗鼠IgE和IgG2a单抗(Pharmingen, San Diego, CA, USA)加入50%山羊血清(Gibco, Grand Island, NY, USA)稀释到培养皿中,然后在37°C下孵育2小时。清洗三次后,使用OPDA溶液(0.3%o‐二盐酸苯二胺,0.02% H2O2, 0.15 M柠檬酸缓冲液,pH 4.9),在492-620 nm处用微孔板自动读数仪测定吸光度。作为内部标准,每个实验都包括ova免疫的BALB/c小鼠的混合血清。标准血清赋值为100 U·mL−1ova特异性IgE和IgG2a
II型肺细胞计数
为了分析II型细胞,肺在4°C下固定在3%戊二醛0.1 M磷酸盐缓冲液(pH 7.3)中,然后固定在2% OsO中4在4°C的水溶液中放置2小时。标本被保存起来全体在2%的醋酸铀酰中浸泡4℃过夜,脱水后嵌入Epon 812。用金刚石刀切割0.5 μ m半薄切片,安装在玻片上,用甲苯胺蓝染色,用光学显微镜观察。然后在离子涂布器中离子蚀刻(IB‐5;Eiko, Ibaragi, Japan), 300v, 0.03 kPa (mmHg), 60分钟。铂涂层后,在20kv下用扫描电镜观察切片(S‐800;日立,东京,日本)。通过识别特征性板层体来区分肺泡II型细胞。每个标本至少10个区域的肺泡区II型细胞在×1000倍率下计数。数据以II型细胞数·mm表示−2.
测定羟脯氨酸
为了估计胶原蛋白总量作为肺纤维化的指标,根据前面描述的方法测量各组左肺羟脯氨酸含量11.测定湿重后,将均质左肺进行水解,并使用高效液相色谱法分析水解物中的羟脯氨酸含量。数据以mg·g表示−1湿润肺组织。
病理变化的可逆性
为了评估肺泡炎的可逆性,在没有进一步治疗的情况下,在最终暴露于OVA后观察了四次Th1细胞转移的小鼠2周。处死后进行BALF分析和组织学检查。
统计分析
除另有说明外,数据均以平均值±标准差表示。变量分析采用Mann-Whitney U‐检验进行两个变量的比较。
结果
T细胞克隆的特征
T细胞克隆产生的细胞因子模式见表1⇓.D2、S1和S4产生大量的IFN‐γ,少量或不产生IL‐4和IL‐5。这些克隆对OVA抗原产生增殖反应,它们的增殖被抗il‐2单抗抑制,但不被抗il‐4单抗抑制(数据未显示)。这些结果表明这些克隆属于Th1子集。
辅助T - 1克隆的单一过继转移效应
如表2所示⇓小鼠腹腔注射Th1细胞后,反复暴露于雾化OVA 5天(D组)或10天(E组),BALF细胞的增加明显高于pbs启动的pbs挑战对照组小鼠(a组)。在5天(B组)和10天(C组)挑战中,BALF细胞的增加速度分别是对照组的3倍和5倍。增加的细胞为巨噬细胞、中性粒细胞和淋巴细胞(表2)⇓).然而,在肺中只观察到有限的细胞浸润(图2a⇓).对照组小鼠在未注射Th1的情况下暴露于OVA中5天(B组)或10天(C组),与pbs启动的pbs挑战小鼠(A组)相比,没有明显变化。其他Th1克隆S1和S4获得了基本相同的结果。在目前的条件下,将Th1细胞转移后暴露于OVA,既不诱导抗原特异性IgG2a反应,也不诱导IgE反应(数据未显示)。
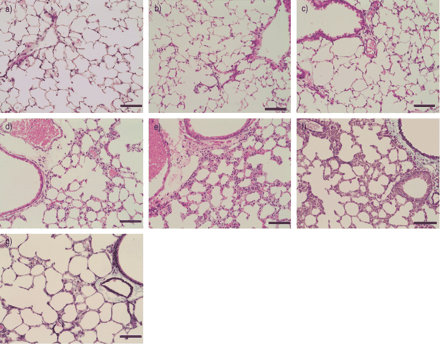
肺的代表性照片(a-e:苏木素和伊红染色,f和g:弹力马松染色)。接受T辅助细胞1克隆(D2;5×106): a)阴性对照(表1中的a组)⇑), b) 1次转移,c) 2次转移,d) 3次转移,e和f) 4次转移,g) 4次转移小鼠卵清蛋白暴露停止两周后。所有比例尺=100µm。
辅助T - 1克隆序列过继转移的影响
如上所示,单一的Th1细胞转移在肺部引起有限的炎症。因此,通过增加转移数量来探索肺中Th1细胞的慢性激活的影响。
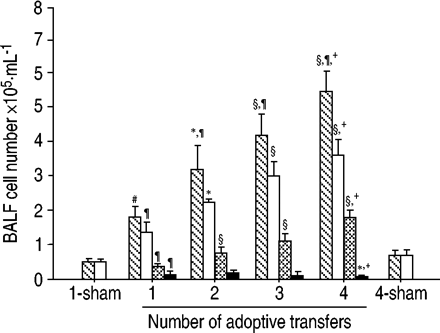
BALF中的细胞总数随着Th1细胞转移的增加而增加(图3)⇓).进行四次移植的小鼠在BALF中显示的细胞数量是仅进行一次移植的小鼠的3倍。BALF中细胞类型的增加不均匀。中性粒细胞的增加在第二次转移时达到峰值(19.7±3.1×10)3.·毫升−1),其后逐渐减少。相反,巨噬细胞和淋巴细胞随着th1细胞转移数量的增加而增加。重复的Th1细胞转移诱导了强烈的抗原特异性IgG2a,但没有IgE抗体应答(图4)⇓),表明转移的Th1细胞是活跃的在活的有机体内.Th1细胞促进IgG2a亚类的产生,而Th2细胞有利于IgG1和IgE抗体的产生12.
细胞总数(镜像)和细胞分化(□:巨噬细胞; :淋巴细胞;*中性粒细胞)支气管肺泡灌洗液(BALF)来自小鼠,经Th1克隆体(D2)过过性转移1-4次,然后反复暴露于卵清蛋白气溶胶。数据以总细胞数·mL表示−1(mean±sd)(每组n=6)。细胞差异显示为每个的平均值。*: p<0.05和§: p < 0.01与1传输。#: p<0.05和¶: p < 0.01与1列车骗局;+: p < 0.01与.4的骗局。
:淋巴细胞;*中性粒细胞)支气管肺泡灌洗液(BALF)来自小鼠,经Th1克隆体(D2)过过性转移1-4次,然后反复暴露于卵清蛋白气溶胶。数据以总细胞数·mL表示−1(mean±sd)(每组n=6)。细胞差异显示为每个的平均值。*: p<0.05和§: p < 0.01与1传输。#: p<0.05和¶: p < 0.01与1列车骗局;+: p < 0.01与.4的骗局。
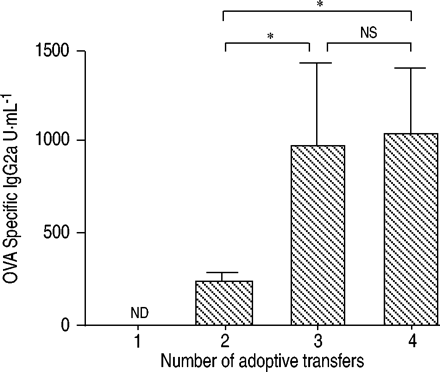
血清卵清蛋白(OVA)特异性免疫球蛋白(Ig)G2a浓度。采用间接酶联免疫吸附法测定ova特异性血清IgG2a抗体滴度。各组均未检测到ova特异性IgE。数据以均数±标准差表示。Nd:不可检测;ns:无意义的。*:组间p<0.01。
组织学上,随着Th1转移数量的增加,肺内细胞浸润更明显(图2b-e)⇑).在四次Th1转移的小鼠中观察到单个核细胞的大量浸润和肺泡壁的显著增厚(图2e⇑).显示了Th1克隆D2的数据,并且在其他Th1克隆S1和S4中获得了基本相同的结果。
T辅助因子1转移对II型肺细胞数量和肺纤维化的影响
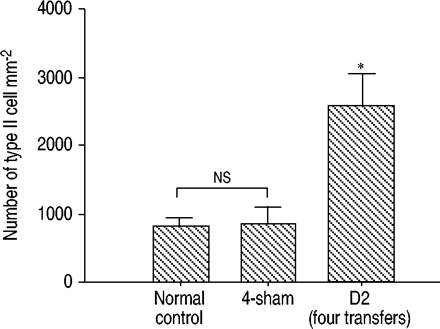
II型上皮细胞的再生是间质性肺疾病中上皮损伤的标志。在显微镜检查中,II型细胞似乎在有两次以上Th1转移的小鼠中突出。因此,采用电子显微镜对II型肺泡上皮细胞进行计数。如图5所示⇓与仅暴露于OVA的正常小鼠或对照小鼠相比,四次转移小鼠的II型细胞数量显著增加。
II型细胞数量。II型细胞在电子显微镜下1000倍放大10个场计数。数据以每毫米的平均值±标准差表示2(每个n=6)。ns:无意义的。*: p < 0.01与正常对照组或4‐sham组。
如图2e所示⇑在美国,即使有四次Th1转移的小鼠的肺部似乎也没有纤维化。为了证实这一点,肺纤维形成通过马尾松染色和羟脯氨酸含量进行评估。Elastica-Masson染色显示肺内无胶原沉积(图2f)⇑),羟脯氨酸含量没有增加(图6⇓).
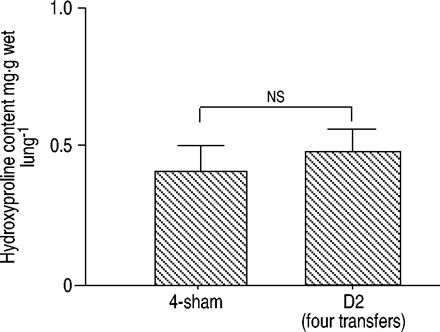
肺部羟脯氨酸含量。采用高效液相色谱法测定左肺羟脯氨酸含量。各组数据以均数±标准差表示(n=6)。
病理变化的可逆性
为了评估肺泡炎的可逆性,有4个Th1细胞转移的小鼠在最终暴露于OVA后2周被杀死。BALF细胞数量显著减少(细胞总数1.5±0.3×105,巨噬细胞87.7±5.8%,淋巴细胞12±5.7%,中性粒细胞0.4±0.5%,嗜酸性粒细胞0%,嗜碱性粒细胞0%;n = 6)。此外,肺泡炎的病理特征,如细胞浸润和肺泡壁厚度,在这些小鼠中得到改善(图2g⇑).
讨论
本研究表明,反复转移抗原反应性Th1克隆,然后暴露于雾化抗原可诱导小鼠间质性肺炎。间质性肺炎的特点是单个核细胞浸润,肺泡壁增厚,无纤维化,这些变化是可逆性的。这些病理改变类似于人类间质性肺疾病,如超敏性肺炎和结节病。然而,该病的病理特征是肉芽肿性间质性肺炎。由于在本模型中未观察到肉芽肿,因此需要注意的是,单独Th1细胞诱导的肺部病理与这些人类肺部疾病明显不同。
最近,通过将抗原特异性的Th1或Th2细胞过继转移到naive小鼠,然后重复吸入相应的抗原,评估了诱导的实验模型13- - - - - -19.从T细胞受体转基因(TCR-Tg)小鼠中过继转移Th2克隆或极化Th2群体导致气道高反应性和嗜酸性粒细胞和单个核细胞显著的血管周围和支气管周围浸润13- - - - - -16.Th2细胞诱导的这些特征类似于人类支气管哮喘。相反,据报道,TCR-Tg小鼠的Th1细胞过继转移可诱导与Th2细胞相同程度的细胞浸润,其周围有单个核细胞和中性粒细胞,但只有少量嗜酸性粒细胞15- - - - - -16,18.即使在Randolph描述的短期转移模型中et al。19在输注OVA特异性TCR-Tg Th1人群后,单次OVA挑战导致明显的气道炎症,但没有肺泡炎症。在这些报告中未观察到肺泡炎。此外,在th1转移小鼠的支气管灌洗中观察到明显的中性粒细胞(占总细胞的20-50%)15- - - - - -17,尽管这一发现并不总是被观察到18.与TCR-Tg小鼠的Th1细胞相似,经反复接种抗原诱导的HP小鼠模型脾细胞中获得的Th1显性细胞群单次输注可诱导显著的HP样病理20..
在本研究中,单次给药Th1细胞仅导致微弱变化。进一步转移是发展特征性肺泡炎的必要条件。尽管BALF中中性粒细胞有所增加,但即使在第二次转移时增加达到峰值(<3%),增加也非常小。这些观点与上面提到的报道不同。目前的模型与以往报告存在差异的原因目前尚不清楚。静脉注射Th1克隆后暴露于OVA导致BALF中淋巴细胞略多,但组织学结果基本相同(未发表的观察)。因此,给药途径可能不是造成差异的一个因素。在以前的报道中,细胞因子和抗细胞因子抗体诱导的极化种群在短时间培养后使用。因此,群体可能是Th1显性的,但群体中的许多细胞可能仍然具有Th0的特征。更重要的是,这种极化细胞的特性可能会丧失或交换这些特性在活的有机体内.先前研究中使用的Th1群体的这些特征可能导致先前和目前结果之间的差异。
th1诱导的肺泡炎无纤维化(弹力马松染色),羟脯氨酸含量无增加。因此,作者得出结论,在本模型中,单独激活的Th1细胞不能导致纤维化变化。值得注意的是,遗传背景可能会影响这一点。BALB/c菌株对博莱霉素反应较差21.然而,BALB/c也易受二氧化硅颗粒、石棉和辐射诱导的肺纤维化影响22- - - - - -24.尽管肺泡炎先于纤维化,但纤维化发生可能需要额外的细胞因子。IL‐1、肿瘤坏死因子‐α和转化生长因子(TGF)‐β是纤维化的重要介质25- - - - - -27.IL‐4可以刺激成纤维细胞合成胶原蛋白,而IFN‐γ是一种有效的合成抑制剂28.在这种情况下,Th1或Th2细胞因子的优势与间质性肺炎的可逆性之间的关系是有趣的29,30..th1显性超敏性肺炎通常是一种可逆性疾病,而特发性肺纤维化通常导致不可逆性肺纤维化,被称为Th2显性疾病31,32.从这个意义上说,单用Th2克隆或与Th1克隆一起过继转移将会揭示它们在肺纤维化中的作用。此外,应该提到的是,CD8+ T细胞的作用在人类HP中是重要的,因为在BALF和实质中CD8+细胞群通常大于CD4+ T细胞亚群。根据细胞因子的分泌模式,CD8+ T细胞群也可以在功能上分为两个亚群,Tc1和Tc233.最近的报道揭示,它们可能有助于肿瘤排斥、预防病毒感染和慢性阻塞性肺疾病的病理改变34,35.虽然目前Tc1和Tc2对肺泡炎的临床研究相当有限,但利用Tc1或Tc2克隆进行过过性转移实验也将对肺间质性疾病的病理生理学有重要的见解。
发现肺Th1细胞活化诱导的肺泡炎伴有II型上皮细胞的增加。II型细胞增殖几乎发生在所有类型的弥漫性肺损伤后。I型上皮细胞优先剥蚀是间质性肺炎实验模型的共同初始特征,如博莱霉素、辐射、百草枯和二氧化硅。在几天内,II型细胞的去分化和复制发生,因为这些细胞扩散以取代受损的I型细胞。暴露于雾化的OVA不会对对照组小鼠造成任何明显的损伤。因此,Th1细胞可能损伤同基因上皮细胞。II型细胞增加的另一种解释是它们的优先生长。即使这种生长发生了,也可能不是Th1细胞因子的直接作用。虽然II型细胞的一些生长因子是已知的,如表皮生长因子、肝细胞生长因子、TGF‐α和酸性碱性成纤维细胞生长因子36- - - - - -37Th1细胞因子尚未被证明能诱导生长。
总之,肺中活化的T -辅助性1细胞可诱发肺泡炎。这种肺泡炎不会导致纤维化,而且是可逆的。肺泡炎导致肺纤维化的因素尚不明确。
致谢
作者要感谢近藤幸和片山幸在本研究过程中的协助。
- 收到了2001年10月31日。
- 接受2002年5月22日。
- ©ERS期刊有限公司