摘要
呼出一氧化氮(eNO)是一种容易测量的气道炎症标志物。本研究旨在评估系列eNO在研究吸入倍氯米松(BDP)的剂量-反应关系方面的有效性,并将eNO与其他气道炎症标志物进行比较。
在停止吸入性皮质类固醇(ICS)治疗后,65名患者进入了一项双盲、平行组、安慰剂对照试验,共50名、100名、200名或500名患者 µg·BDP·天-1了8周。每周进行eNO和肺活量测定,在治疗开始和结束时进行痰诱导高渗盐水激发。
ICS剂量与eNO和1秒用力呼气量(FEV)变化之间的关系1)在第1周和治疗结束时呈线性。痰嗜酸性粒细胞也呈线性剂量-反应关系。eNO的变化与痰中嗜酸性粒细胞的变化显著相关。刺激剂量的变化导致FEV下降15%1在不同的治疗组中,生理盐水没有差异,也没有与其他测量的变化相关。
呼出的一氧化氮可用于评估吸入倍氯米松抗炎作用的剂量-反应关系。本研究中发现的关系在0-500剂量范围内呈线性 微克·天-1开始治疗后不久,随着时间的推移继续。
这项研究由新西兰健康研究委员会和奥塔哥大学管理的奥塔哥研究基金资助。S.L. Jones获得了葛兰素史克(GSK)研究基金的支持,GSK提供了教育经费。
吸入糖皮质激素(ICS)是治疗哮喘气道炎症最有效的方法1.它们的使用可以改善症状和肺功能,以及减少支气管活组织检查中的炎症细胞2和诱导痰3..因此,气道高反应性(AHR)也降低了4.那5..目前的指导方针建议使用ICS治疗,除了最温和的哮喘6..该指南是基于治疗气道炎症可以改善哮喘控制的假设。然而,一些研究表明症状与肺功能和气道炎症之间的关系不一致7.-9..这就提出了一个问题,即使用ICS的主要目标是否是实现症状控制、优化肺功能、最小化气道炎症或降低AHR。
过去,ICS的剂量-反应关系已被描述为使用症状和肺功能作为主要结局变量。虽然这些终点存在剂量-反应关系,但在相对较低的剂量时,它可能会趋于平稳。因此,在区分相邻剂量的影响方面可能有些困难1那10.其他研究表明,当使用其他端点时,剂量响应关系变化11. 例如,控制气道高反应性所需的ICS剂量远远高于症状11那12.澄清这些关系的数据较少,即使对气道炎症的控制是给予这些药物的主要原因。这些信息可能在临床上有助于评估不同IC剂量和优化长期治疗的指南的相对疗效。
呼出一氧化氮(eNO)是一种可重复、易于测量的气道炎症标志物13那14.在steroid-naïve哮喘中均可见高水平15在急性恶化期间16那17.此外,两种吸入治疗后水平均降低3.那18那19和口服类固醇20.. 这些结果表明eNO可能是测量ICS治疗对气道炎症影响的剂量-反应关系的有用终点。
最近,目前的作者证实了eNO测量在预测停用ICS后哮喘控制恶化方面的有用性17.在这项随访研究中,目的是评估连续eNO测量在测量不同剂量吸入倍氯米松(BDP)的抗炎作用方面的有效性,并与其他终点(包括肺功能、痰嗜酸性粒细胞和AHR)与高渗盐水的比较。
方法
主题
轻、中度哮喘患者21接受维持性ICS治疗。如果患者有需要住院治疗的急性哮喘病史、以突发性哮喘为特征的哮喘史或在过去3个月内使用过口服强的松,则将其排除在外(因为该研究涉及停用ICS治疗)。
研究设计
磨合后,ICS治疗中断。每周对患者进行检查,直到出现“失控”,或最多6周。那些没有失去控制的人随后被撤回。失去控制的定义是预先确定的标准17包括:1)(过去7天内)早晨呼气流量峰值率(PEFR)较基线平均下降10%,或连续2天上午或晚上PEFR下降至≤基线的80%;或2)平均每日>支气管扩张剂使用时间比使用时长3次;或3)≥3夜·周有哮喘症状的夜间醒来-1大于磨合期间的值;或4)令人不快或痛苦的哮喘症状。
在失去控制后,患者口服20 mg强的松2天,以缓解他们恶化的症状。尽管这在理论上可能会影响后续1周ICS效应的解释,但出于安全原因,这种策略是必要的。患者随机接受为期8周的双盲ICS治疗,从两个相同的计量吸入器(Autohaler;3M pharmaceuticals, St Paul, MN, USA)的标签为“morning”和“evening”。治疗方法为:安慰剂(每日两次安慰剂)b.i.d));50μg·日-1(早上50μgbdp,晚上安慰剂);100μg·日-1(100 早上服用µg BDP,晚上服用安慰剂);200 微克·天-1(100 µg BDPb.i.d);500µg·-1(250µg和平民主党b.i.d).
在服用随机药物的同时,哮喘显著恶化的患者从治疗组中撤出,给予20 mg强的松口服2天,并进入1000µg·天的开放标签治疗组-1(250µg BDP 2泡芙b.i.d).
随机化(第1次就诊)后,在前4周(第2次就诊至第5次就诊)和治疗结束时(第8周,第6次就诊),每周对患者进行一次检查。ICS剂量需要增加到1000的患者 微克·天-1每周审查4周,并在8周的治疗结束时再次审查。
研究过程
在每日记录卡上记录每日PEFR、支气管扩张剂使用情况和症状评分。在每次研究来访时测量eNO和肺活量,在治疗开始和结束时进行痰诱导高渗盐水激发。
呼出一氧化氮
在所有其他研究程序之前,使用校准化学发光分析仪测量eNO,并根据标准方案在线测量单次呼气13那14,流量除外(250 毫升·秒-1)(研究在共识指南发表之前开始)。在对应于二氧化碳曲线70-80%的平台上读取eNO水平。这些读数是由一个对病人的临床状况一无所知的人在以后的日子里做出的。
食盐水的挑战
采用改良标准化方案测量高渗盐水(4.5%)的AHR22那23.在每种盐雾化后1分钟进行肺活量测定。当在一秒钟内强迫呼气量20%下降时,挑战已停止(FEV1),或累计吸入时间为20分钟。PD15计算为导致FEV下降15%的盐水累积激发剂量1.
诱导痰
在高渗盐水激发过程中,鼓励患者在雾化之间产生痰液。如果FEV下降20%1发生在获得足够的痰样本之前,给予吸入沙丁胺醇,痰诱导持续最大累积时间为20分钟。一旦获得足够的痰标本,使用标准化的方法对整个标本(痰加唾液)进行分析24.用台台蓝排除试验评估细胞活力,用血球计进行细胞计数。用May-Grunwald-Giemsa染色,两次计数共400个非鳞状细胞。对于任何类型的细胞,两种计数之间的差异为>10%,然后重复计数两次,记录所有四种细胞的平均值。
道德考量和安全
在整个研究过程中,密切监测每个患者的哮喘控制情况。出于伦理原因,不管PEFR的变化如何,失去控制的标准包括“令人不快或痛苦的”症状。所有患者均提供个性化的自我管理计划、急诊卡和泼尼松片供应。患者有24小时接触研究人员的机会通过医院的传呼系统。此外,认识到ICS停药可能导致哮喘控制不良,研究人员在随机分组后的第1天和第3天给每位患者打电话。获得了Otago伦理委员会的伦理批准,并获得了所有研究参与者的知情同意。
统计分析
该研究的主要结果是评估吸入皮质类固醇剂量在0-500 μ g·d范围内是否存在剂量-反应关系-1和eno的变化。用痰嗜酸性粒细胞,FEV进行比较1和PD15生理盐水。在意向治疗的基础上,使用协方差分析对数据进行分析,并对随机化的值进行调整,以及对在积极治疗期间因安全性原因切换到1000µg·day的患者进行调整-1.在随机化基团上拟合多项式对比以建立剂量反应关系的性质。PD.15盐水值分析为基线剂量变化的两倍。计算估计的边际平均数,以及后HOC对剂量间的两两比较进行分析,并对多重比较进行Bonferroni调整。计算Pearson相关性以评估eNO、痰嗜酸性粒细胞、FEV之间的关系1和PD15随机分组和研究结束时服用生理盐水。
在设计时,设计的时间没有关于该电力计算的信息。基于轶事证据,计算每组15名患者提供> 80%的权力,以检测组之间> 0.8 SD的差异。虽然这得到了足够的力量来检测整个组的线性趋势,但这没有确定先验.
结果
随机化
87名患者参与了这项研究。3例患者在ICS撤药前撤回了同意书。65名患者(77%)失去控制,随机分为5个治疗组。人口统计数据见表1⇓.在表2中显示了在基线(撤回IC,访问0)和随机化之前(访问0)和随机化之前测量的研究终点数据⇓.
治疗提款
一名患者随机接受500μg·日-1由于他们的哮喘严重程度,在第1次访视时被撤回,并且在分析中没有进一步考虑。其余64例患者中有25例在随机分组后出现哮喘恶化,并进入开放标签1000µg·day-1研究的一个分支。安慰剂组、50µg·天、100µg·天、200µg·天、500µg·天,每个治疗组的患者数量分别为6、5、8、4和2例-1BDP组分别。从随机治疗臂退出的人与完成治疗的人之间的比较显示在表2中⇑.两组间eNO、痰嗜酸性粒细胞和PD无显著差异15随机分组时的生理盐水。那些退出的人FEV较低1预测比没有退出的人(73.9与分别为82.5%,p=0.005)。退出研究的患者在研究开始时也有较高剂量的维持性ICS(平均95%可信区间(CI)776(635–917)微克·天)-1和614(536–694)微克·天-1分别为p=0.042)。
剂量反应
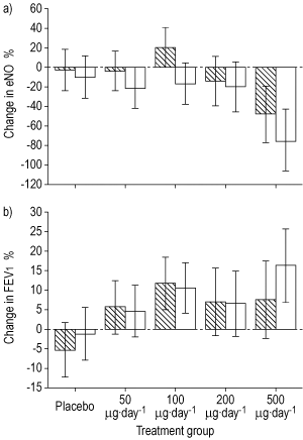
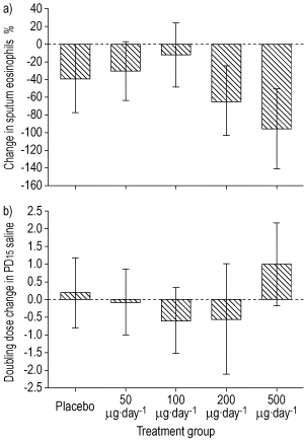
eno和fev的变化1(在1周和治疗结束时)和痰嗜酸性粒细胞和PD15盐水(在处理结束时)如图1和图2所示。 1⇓和2⇓, 分别。
a)呼出一氧化氮(eNO)和b)1秒用力呼气量(FEV)的百分比变化1),吸入皮质类固醇治疗1周后(对照),吸入皮质类固醇治疗8周后(□)。数据以均值±95%置信区间表示。数据来自所有患者,但根据基线测量的差异和每个时间点组中剩余的患者数量进行了调整。a)治疗1周时(p=0.005)和治疗结束时(p=0.015)有显著差异。这些差异呈线性关系(p=0.022, p=0.003)。b)在治疗1周时(p=0.014)和治疗结束时(p=0.036),治疗组间有显著差异。这些差异呈线性关系(p=0.043, p=0.006)。
a)治疗结束时痰中嗜酸性粒细胞的百分比变化。各治疗组之间存在显著的线性关系(p=0.037)。b)生理盐水累积刺激剂量增加一倍,导致一秒内强迫呼气量下降15% (PD)15盐水)在治疗结束时。治疗组中没有看到显着差异(P = 0.837)。数据显示为±95%的置信区间。数据来自所有患者,而是调整基线测量和每个时间点剩余患者的数量。
ICS剂量与下列各项之间存在显著的线性关系:治疗1周和结束时eNO的变化(分别为p=0.022和p=0.015);FEV的变化1治疗1周和治疗结束时(分别p=0.043和p=0.006);治疗结束时痰嗜酸性粒细胞的变化(p=0.037)。ICS剂量与PD的变化无明显关系15生理盐水。所有这些比较都针对基线测量进行了调整,并由于提取而导致的数量变化。当那些进入1,000μg·日的时候-1arm被排除在分析之外。eNO变化在各组间呈线性关系的显著性持续存在(p=0.003),然而,FEV呈线性关系1痰嗜酸性粒细胞变得不显着。
在评估ICS治疗的剂量效应中,进行对每个治疗组的成对比较。100μg·日之间的eno存在显着差异-1和200和500μg·日-11周时(p<0.05), 500µg·d时-1安慰剂和100µg·天-1在治疗结束时(P = 0.01和P = 0.023)。对于FEV.1,500μg·日之间存在显着差异-1与治疗结束时的安慰剂组比较(p=0.04),但其他剂量间比较组则没有。同样,治疗后痰中嗜酸性粒细胞的唯一显著差异出现在100µg·d之间-1和500μg·日-1(p = 0.049)。使用两两比较没有发现其他显著差异。PD组无显著性差异15治疗之间的盐水。
讨论
在这项研究中,eNO测量为ICS的抗炎作用的剂量-反应关系提供了有用的信息。这不仅对监测个别患者的抗炎治疗有潜在的实际意义,而且对评估不同剂量吸入糖皮质激素的疗效也有潜在的实际意义。eNO的变化与ICS用量呈显著的线性关系(0-500µg·d范围内)-1BDP)被发现在中度支气管哮喘的患者中,其中被撤回并发生了对控制的丧失。这确保了呼吸道炎症足以进行测量的抗炎作用。在开始治疗后1周内,线性剂量 - 反应关系很大,并持续到8周,表明eno测量不仅迅速迅速响应于气道炎症的变化,而且还反映了IC的持续的抗炎作用随时间治疗。使用FEV也发现了类似的线性剂量 - 反应关系1在1-周和8周的治疗中。在最近报告的调查纯洁et al。25还在0-800μg·bdp·day的剂量范围内逐步降低eno-1在eNO水平升高的患者中。本研究的结果更进一步。eNO的变化与痰中嗜酸性粒细胞的变化高度相关,加之ICS剂量与治疗结束时痰中嗜酸性粒细胞变化之间的线性剂量-反应关系,证实了eNO中发生的剂量相关的下降与气道炎症的减少相对应,并为本研究的主要结果提供了验证。
先前已被证明在用吸入的预溶剂处理后,在eno中发生的变化与呼吸炎症后其他标记的变化见相关26和氟替卡松3..然而,目前的研究是迄今为止对这些抗炎作用的剂量依赖性进行调查的最大的研究。威尔逊和Lipworth27据报道,当剂量大于400时 每天微克布地奈德(布地奈德剂量范围研究的第一步),尽管FEV有进一步的剂量相关改善,但eNO没有进一步降低1和痰中嗜酸性阳离子蛋白。在一项较小的研究中,Jatakanonet al。28据报道,尽管痰液嗜酸性嗜酸性粒细胞的持续减少,但在1,600μg培养基·日-1,ENO的变化达到了400μg·日的高原-1. 相比之下,在本研究中,eNO和ICS之间的剂量-反应关系是线性的,没有证据表明在研究的剂量范围内(0-500)存在平台 微克·天-1)痰嗜酸性粒细胞和FEV的结果相似1.然而,目前的研究无法就>500µg·day剂量是否会出现剂量-反应关系的平台期提供评论-1.
这些结果与以前的研究结果之间的明显冲突可能是由于在调查时哮喘严重程度的差异。在目前的研究中,治疗被停止,直到发生失控,那些没有表现出失控的患者被排除在外。其他研究人员在评估ICS的剂量反应时也使用了类似的研究设计29那30.. 这种方法的基本原理是ICS的治疗率可能受到哮喘严重程度的影响:哮喘较轻的患者可能没有多少改善的余地。这可能影响了先前研究的结果27那28.这进一步得到了Silkoff的发现的支持et al。25世卫组织指出,基线eNO水平较高的患者在较高剂量范围(0-800)内表现出剂量反应降低 µg·BDP·天-1)基线(0-200μg·bdp·日期,eno水平较低的人-1).
对目前的研究有许多潜在的批评。首先,患者随机接受的BDP剂量范围不包括1000 微克·天-1. 这是因为早期的建议,即eNO测量不仅对ICS剂量的变化非常敏感,而且ICS的临床益处在较高剂量时受到限制31,甚至对患有严重哮喘的患者也是如此32.因此,目前的作者希望解决ICS在较低剂量范围内的抗炎作用存在一个阈值的可能性。第二,研究模型IE。在研究的随机阶段开始前退出ICS33,导致大量患者的哮喘在随机化后仍未得到控制。出于伦理原因,这些患者被重新分配到1000µg·day-1.分析是有意治疗的基础,因此包括改变为更高剂量的患者的统计调整。分析时后HOC作为单独的治疗组,患者每天接受1000µg-1确实提供了有用的信息:在这组患者中,第8周的eNO水平(平均eNO,17.3个十亿分之一(ppb)(95%可信区间,11.1-23.5))高于接受500%治疗的患者 微克·天-1(平均eNO为10.4 ppb(95%可信区间,4.4-16.4))。由于选择偏差,未对各组之间的差异进行正式分析。然而,这表明,尽管ICS的剂量较高,但在更严重哮喘患者中,eNO水平仍然升高34,反映该亚组正在进行的气道炎症,并证实需要更高剂量的ICS。最后,尽管发现eNO与ICS剂量之间存在线性关系,但在成对比较中进行评估时,eNO测量无法一致区分相邻ICS剂量,尽管eNO在这方面优于所有其他测量参数。这似乎是几乎所有ICS剂量反应研究的一个特点,无论使用的终点是什么,而且患者数量更多29那30.那35.
即使在没有持续症状和肺功能异常的情况下,非特异性气道反应似乎也反映了气道炎症7..因此,AHR的变化可能提供了可以评估IC的抗炎作用的有用措施。然而,在目前的研究中,AHR对高渗盐水没有显着变化。这可以反映所使用的低剂量的IC或相对较短的治疗持续时间。其他作者报告了使用替代方法的对比结果27那28那35-37.通常,AHR直接支气管扩roners甲素和组胺似乎比间接支气管棘轮在检测与皮质类固醇治疗发生的变化中的间接支气管棘轮敏感27那38.不幸的是,对许多研究的解释是困难的,因为它们包括患有轻度哮喘的患者并使用高剂量的IC4..
为患者确定适当剂量的ICS的最佳方法仍未确定。有两个相关的问题。首先,将ICS的剂量增加到一定阈值以上是否会产生更大的疗效?在大多数患者中,当ICS剂量进行性增加时,肺功能只有很小的增加29那30.那35. 这就对高剂量ICS的有效性提出了质疑,或者更可能的是,在这种情况下简单肺功能测量的有效性提出了质疑。其次,为了获得最佳控制,是否有必要完全抑制气道炎症?如何最好地评估这一点?最小化气道对单磷酸腺苷或乙酰甲胆碱(作为气道炎症的替代物)的反应性7.)似乎与剂量有关27那36那37. 当抗炎治疗能够降低AHR时,临床结果会得到改善39.遗憾的是,反复测量AHR的不合适用于常规临床实践,因此他们的广泛应用不太可能成为普遍存在。相反,eno测量是可重复且易于执行的。
目前的作者最近表明,呼出的一氧化氮测量可用于预测哮喘控制恶化,并且它们反映了潜水道炎症的变化17.这些发现,连同本研究的结果,提供了一种可能性,即重复测量呼出的一氧化氮可能有助于指导持续性哮喘患者吸入糖皮质激素的剂量调整。这需要进一步的前瞻性研究。
致谢
作者要感谢3M制药公司提供的研究药物。
- 已收到二○○一年十月九日。
- 公认2002年4月3日。
- ©ERS期刊有限公司