摘要
慢性阻塞性肺疾病(COPD)急性加重伴低氧血症可诱发净蛋白分解代谢,而低氧血症可能是全身分解代谢反应的重要触发因素。本研究的目的是检测重组人胰岛素样生长因子- I (IGF - I)在缺氧大鼠中的合成代谢作用。虽然急性缺氧通常伴随着饮食摄入量的减少,但在本研究中仍维持正常的氮摄入量。
通过连续输注总肠外营养6天,通过连续输注Sprague-Dawley大鼠。然后将动物随机分配给常氧(n)或缺氧(h)组。在实验的最后3天期间,N和H大鼠随机接收IGF-I或车辆。
暴露于缺氧导致体重增加减少,伴随负氮平衡,这主要是由于尿氮排泄增加。在暴露于缺氧环境中,尽管氮平衡恢复正常,但重组人IGF‐I处理对体重没有影响。
联合输注重组人胰岛素样生长因子- 1和全肠外营养具有显著的净合成代谢效应,在大鼠中观察到的氮潴留和尿蛋白排泄减少证明了这一点。胰岛素样生长因子- 1可能有助于改善缺氧条件下观察到的蛋白质分解代谢。
该研究得到了日本卫生,劳工和福利部的呼吸失败研究小组的支持。
大量中重度慢性阻塞性肺疾病(COPD)患者表现出静息代谢率升高1.这些患者的子集显示外周血中急性期蛋白和可溶性肿瘤坏死因子(TNF)受体水平升高2,TNF系统可能有可能是相关的3..这些患者的特征是无脂肪物质的消耗,与身体质量指数无关2.因此,COPD患者的组织耗竭可以部分地部分地与炎症引起的全身分解代谢反应相关,这不能单独通过营养载体完全逆转。细胞能量代谢在患者的肌肉活组织检查中改变临床稳定COPD在休息,与其肌肉质量无关。慢性或间歇性低血值可能是这些代谢改变的重要触发4.
体重减轻和无脂质消耗是COPD患者的一个严重问题,对他们的运动能力和生存率产生负面影响4,5.正如对骨骼肌氨基酸水平的调查结果所提示的那样,COPD患者的蛋白质代谢可能发生改变6.在体重稳定、自由脂肪量低于对照组的临床稳定的重度COPD患者中,观察到全身蛋白质周转增加,包括蛋白质合成和分解水平的提高7.然而,目前尚不清楚这些患者的净蛋白分解代谢是由COPD急性加重还是进行性体重减轻引起的,后者通常发生在COPD中,并伴有低氧血症。
全肠外营养(TPN)虽然不能完全防止机体蛋白质损失,但通常用于为分解代谢疾病提供营养支持8.因此,使用合成代谢剂,如生长激素(GH)的可能性9或胰岛素样生长因子I (IGF‐I)10.,在TPN期间正在调查中。重组人IGF-I(Rhigf-i)的合成效应已在动物中证明,其中糖尿病诱导分解代谢11.或营养不足12..然而,需要评估IGF‐I在TPN分解代谢状态(如低氧血症)期间的合成代谢效应。本研究的目的是检测缺氧条件下rhIGF‐I与TPN共注入大鼠的合成代谢作用。
方法
动物设施和议定书由千叶大学医学院动物护理和使用委员会批准。
动物和手术
雄性,特异性无病原体,Sprague-Dawley大鼠(200-220 g;日本横滨的查尔斯河)被安置在独立的不锈钢笼子里,在12小时的明暗循环下,并允许免费取水。实验前让动物适应动物设施7天。麻醉后(50 mg·kg−1氯胺酮和5毫克·公斤−1通过肌内注射施用的木嗪),导管在上腔静脉上置于上腔静脉中通过颈外静脉13..手术之后是3天的恢复期,动物可以吃标准的大鼠食物随意.在恢复期间,一次电解质溶液(60 mL·d)−1)是在鼠粮的基础上进行的。
实验设计
在恢复期后,使用22型旋转输注组件(BRC,Nagoya,Japan),6天,通过连续输注TPN溶液来完全通过连续输注TPN溶液来保持动物(n = 24)。在整个输液期间,允许动物自由地在笼内移动。
动物被随机分为常氧组(N =12)和低氧组(H =12)。在常氧状态下进行3天基线测量后,将H大鼠置于常压低氧环境舱内3天,其中部分吸入氧(O2)浓度保持在10%,湿度多和二氧化碳(CO2),用钠石灰和硅胶去除。腔体体积为0.3645 m3.(90×90×45厘米)。以6 L·min的低氧空气流量维持缺氧环境−1.这种缺氧空气是通过改造吸附型氧气浓缩器来生产的,以利用排气(Teijin,Toijin,Tokyo,Japan)。气体定期采样,o2和有限公司2在天然气分析仪(NEC-SAN-EI仪器,1H26,东京)分析。分数启发的合作社2在整个实验过程中,浓度均小于0.04%。室内温度随室温在20-25°C之间变化。N只大鼠与H只大鼠保持在同一房间的空气中,并暴露在相同的光/暗循环中。每天打开一次,持续时间小于30分钟,测量体重,收集尿液样本。
在最后3天,N和H大鼠随机连续服用4 mg·kg−1·天−1IGF‐I(n=6) (IGF‐I(+))或等渗生理盐水(n=6)(对照组(IGF‐I(−))。四个治疗组最初由6只动物组成,但在实验结束时,一只动物因为导管问题而失去了生命。最后的样本大小是如下:N地理IGF I(−)(N = 5), N地理IGF I (+) (N = 6), H IGF必经我(−)(N = 6), H IGF必经我(+)(N = 6)。
本研究结束时,大鼠股静脉插管采血,测定血清总蛋白和白蛋白,注射过量戊巴比妥钠处死。取出胃肠道,用冷盐水冲洗,去除肠道内容物。取肝、肾、脾、胸腺、肺、胃、小肠(幽门至盲肠)、盲肠、结肠(盲肠至直肠之间)、腓肠肌进行解剖称重。然后将尸体保存在−5℃,直到可以测量每个器官的蛋白质浓度。
全肠外营养的组成
采用12%氨基酸(proteamine -12;田边制药有限公司,东京,日本),葡萄糖,20%脂乳液(脂内,Ootsuka制药有限公司,东京,日本),维生素,微量元素和电解质13..给予60±2 mL TPN·d−1,提供400毫克氮·日−1和62千卡·天−1.
身体蛋白质浓度
冻干后的尸体均质,每三次测定干鼠匀浆中的氮浓度。用微量凯氏定氮法测定0.20 g干大鼠匀浆中肺、肝、肾、胃、肠、结肠和腓肠肌中氮的浓度,用胴体中氮的浓度乘以6.25计算蛋白质浓度14..
分析测量
每日记录体重,收集尿液,4°C保存于0.01%硼酸中,然后测定氮浓度。采用改良的微凯氏法测定尿样中的氮含量15..通过从总氮气摄入中减去总尿氮来确定氮气平衡,从给出的TPN溶液的体积计算。随着粪便损失在维持TPN的动物中最小,未确定粪便氮。
统计分析
数值用平均值±se表示。采用方差分析(ANOVA)进行统计分析,随后采用Scheffe检验进行多重比较。为了检验暴露于缺氧的影响,比较了N型IGF‐I(-)和H型IGF‐I(-)。为了检验IGF - I治疗的效果,比较了N组和H组内的IGF - I(−)和IGF - I(+)亚组。显著性为p<0.05。
结果
在IGF-I( - )动物中,血清总蛋白质和白蛋白在H大鼠中低于N大鼠。相比之下,两组之间的总胆固醇和甘油三酯的水平没有差异(表1⇓).
由于所有四组的基线体重相似(平均值209-222 g),因此比较了体重增加(图1)⇓).在IGF-I( - )大鼠缺氧后第1天在第1天减少体重。暴露于缺氧对体重有重大影响,即IGF-I( - )动物在N大鼠中体重高于在10天1-3的大鼠中较高(P <0.05)。与IGF-I( - )大鼠相比(P <0.05)相比,仅在N大鼠中的第3天观察到IGF-I(+)处理对体重增加的影响(P <0.05),而IGF-I(+)治疗对H大鼠体重没有影响。
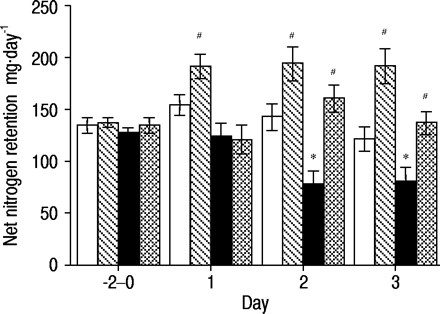
氮气排泄和保留数据总结在图2中⇓和3.⇓.各组预处理值取平均值,连续3天(−2-0天)。在IGF - I或对照剂处理前3天,各组氮的排泄和滞留无显著差异。因此,汇集的数据被呈现在预处理阶段。在TPN的整个6天内,各组的氮摄入量没有显著差异。
氮排泄在IGF-I( - )H大鼠中增加了〜20%,而IGF-I( - )N大鼠没有增加。IGF-I抑制了在第2天和第3天暴露于缺氧诱导的氮排泄的增加,从而氮排泄与在基线时观察到的氮排泄。类似地,IGF-1在N大鼠的治疗期(第1-3天)整个治疗期(第1-3天)减毒。
在IGF‐I(−)N大鼠中,氮平衡没有受到影响,因为氮的摄入是恒定的,而氮的排泄几乎保持不变。相比之下,IGF - I处理使N大鼠的氮平衡为正。IGF‐I(−)H大鼠显示负氮平衡,而IGF-I治疗阻止了它。只有在暴露于缺氧的第一天,水的正平衡度才会下降。在IGF‐I(−)和IGF‐I(+) H大鼠中,尿量增加导致水平衡下降(图4)⇓).
相对重量(g·kg体重)−1)列于表2⇓.观察缺氧对肺和胸腺的影响。与IGF‐I(−)N大鼠相比,IGF‐I(−)H大鼠的肺重量更高,胸腺重量更低。IGF‐I治疗对N和H大鼠肾脏、胃、肠和结肠重量的影响均被观察到。IGF - I处理的大鼠相对器官重量更高。N大鼠肠道蛋白质含量有升高趋势(p=0.07), H大鼠肠道蛋白质含量显著升高。除肠道外,在其他器官中未观察到IGF‐I的影响(表3)⇓).
讨论
的在活的有机体内rhIGF‐I的合成代谢效应已经在人和动物中进行了广泛的检测11.,12.,14.,16..然而,在缺氧期间IGF‐I与TPN共灌注的影响之前没有研究过14.,17..本研究的结果表明,给予TPN的N只大鼠IGF‐I可合成代谢,与给予TPN但未给予IGF‐I的N只大鼠相比,体重增加和氮潴留更大。此外,本研究结果证实了之前的研究结果,证明在缺氧条件下,与TPN共注入IGF‐I时,IGF‐I具有净合成代谢作用。本研究还表明,暴露于缺氧导致体重增加程度下降,并伴随负氮平衡,这主要是由于尿氮排泄增加。在暴露于缺氧的3天内,尽管氮平衡恢复正常,但未观察到IGF‐I治疗对体重的影响。
与缺氧有关的重量损失的原因仍然是未定义的。已知厌食患者几乎总是与缺氧相关,这归因于减肥的主要因素之一18.,19..而在本研究中,TPN持续维持总热量和总氮摄入量。因此,缺氧本身可能会对体重产生重大影响
在暴露于缺氧的最初24小时内,体重增加受损可能部分是由于相对负的水平衡18..在本研究的实验中,饮水量是恒定的,因此与缺氧相关的利尿作用可能影响了水分平衡。激素和细胞因子已知在急性应激下会发生变化20.因此,可能会受到缺氧的影响。例如,脂多糖诱导的TNF和白细胞介素(IL)‐β释放在暴露于缺氧后被证明是增强的21..在本研究中,任何与利尿剂相关的激素稳态变化都可能影响水平衡,尽管确切的机制尚未确定。
缺氧对蛋白质合成和分解之间的代谢平衡的直接影响可能影响了受损的体重增加。患有低氧血症的肺气肿患者由于蛋白质合成降低而出现肌肉萎缩,并伴有全身蛋白质周转的整体下降22..因此,缺氧可能导致蛋白质合成的减少而不是蛋白质水解的增加。此外,与常氧大鼠相比,空腹缺氧大鼠血浆氨基酸浓度较低,表明低氧血症期间蛋白质合成受到抑制23..
在禁食期间,循环IGF‐I可能在蛋白质代谢的控制中发挥整合作用17.它可以作为营养状况的指标24..蛋白质营养不良不仅降低IGF-I的生产,而且还提高了其血清间隙和降解24..因此,IGF‐I与营养密切相关。
IGF‐I对蛋白质代谢的影响可能在不同的营养条件和分解代谢状态下有所不同。IGF‐I在TPN期间的合成作用很可能是由蛋白质分解代谢和合成的变化介导的14.,17..在用IGF-I治疗期间的体内蛋白质分析在IGF-I次数仅在H大鼠的肠道上显着增加。虽然IGF-1对N大鼠的第3天没有观察到IGF-I对体重增加的影响,但在第1天已经观察到阳性氮气平衡。在H大鼠中,IGF-1对氮气平衡的影响出现在第2天,但它没有影响体重增加。本研究的结果表明IGF-I对氮气平衡的影响可以在常氧条件下的1天内识别,而在缺氧条件下需要2天。相反,在先前的人类研究中据报道,用IGF-1治疗1周后的正氮平衡25..
已显示IGF-I输注降低净蛋白分解代谢的速率,并在禁食和肠外喂养羊羔中增加心脏和膈肌蛋白的分数综合率。施用IGF-I对分解代谢动物的施用不仅降低了内源性蛋白质损失,而且在与营养载体一起施用时,增强基材的利用17..在本研究中,IGF‐I处理是否增加了蛋白质合成的速率尚不明确。然而,内源性蛋白的损失在给予IGF‐I期间减少,如尿氮排泄的减少所示。
IGF结合蛋白(IGFBP)循环水平的变化可能有助于IGF-I与TPN对氮气平衡的影响的影响,因为IGFBP在TPN期间影响IGF-1的间隙和/或组织分布26.,27..然而,这项研究没有对这些因素进行测量。其中,IGFBP‐3是血液中IGF‐I的主要载体。先前的研究16.,26.已经表明,在用TPN喂食过程中,IGFBP-3的水平增加,但通过IGF-I处理降低。虽然IGFBPS可以根据具体的实验条件抑制或增强IGF的生物学效应28.,需要进一步的研究来确定IGF‐I/ igfbp的变化如何影响TPN喂养过程中的合成代谢过程。
IGF-I治疗在胃肠道中影响器官重量,包括胃,肠和结肠,两种大鼠。在IGF-1(+)N大鼠中观察到的体重增加部分是由于胃肠道的增加。在若干实验条件下,IGF-I诱导脾脏和胸腺量的增加28.,29..然而,脾和胸腺重量的增加直到给予IGF - I 3天后才观察到,可能是因为治疗时间较短。相反,在缺氧条件下,胸腺的重量有下降的趋势,提示缺氧可能发挥免疫抑制作用。胸腺体重减轻可能与缺氧应激导致的皮质激素增加有关30..缺氧暴露也导致肺部重量增加。肺中的蛋白质含量在N和H大鼠中相似。肺部重量增加的原因尚不清楚,但缺氧肺水肿或血液再分配也许是一个解释。
有报道称GH可诱导盐和水潴留,从而导致体重和瘦体重的增加31..在本研究中,IGF‐I处理没有影响N或H大鼠的水平衡,而缺氧本身在早期暴露(24小时内)导致了负的水平衡,但它与氮平衡的变化无关。本研究的水平衡是通过TPN溶液体积减去尿量来计算的。它不包括呼吸水分损失和皮肤蒸发水分损失,因此这个平衡总是正的。急性缺氧导致尿量和钠排泄增加,部分原因是肾素-血管紧张素-醛固酮系统受到抑制,血浆醛固酮减少32..在暴露于缺氧时心房利钠肽的增加也可能与尿量的增加有关33..这可以部分解释H大鼠第一天的水分平衡下降和体重增加。
暴露于缺氧会导致通气增加,这可能伴随着呼吸失水的增加,但当大鼠暴露于缺氧3天时,通气增加约为10-15%34..由于漏气不含水,很难准确估算漏气含水量。据报道,水蒸气的数量取决于呼吸和环境因素,而不是温度35..如果一只重200克的大鼠换气约80毫升·分钟−1·100克−1在常氧条件下,排出的气体将完全饱和。如果这只老鼠的体温为38°C,而室内的温度为26°C,那么从室内排出的气体和从室内吸入的气体之间的水蒸气量的差值将达到约23 mg·L−1.在这种情况下,N和H大鼠之间的水损失差异为0.5-0.8g·日−1.因此,N大鼠和H大鼠的呼吸失水程度差异很小。
IGF‐I和GH联合给药比单独给药具有更强的合成代谢作用。先前的研究表明,虽然IGF‐I提供了一种更直接的方式来刺激蛋白质合成,因为生长激素的合成作用部分是由增加IGF‐I产生介导的,但联合治疗可以维持更正常的碳水化合物代谢和更正常的血清igfbp配置16..需要进一步的试验来确定这种联合疗法如何影响缺氧时的合成代谢过程。
热量限制和负能量平衡是急性呼吸衰竭分解代谢反应的重要组成部分。在由慢性阻塞性肺病引起的慢性呼吸衰竭的急性加重期间,通常不可能维持足够的口服热量摄入以防止加速蛋白质消耗,因此经常需要肠外营养。
综上所述,本研究结果表明,重组人胰岛素样生长因子‐1与全肠外营养共同输注具有显著的净合成代谢效应,这可以通过减少尿蛋白排泄、改善体重增加和氮潴留得到证明。与对照组全肠外营养大鼠相比。需要进一步的研究来确定类似的治疗干预在低氧慢性阻塞性肺疾病患者急性加重的情况下是否具有临床应用价值。
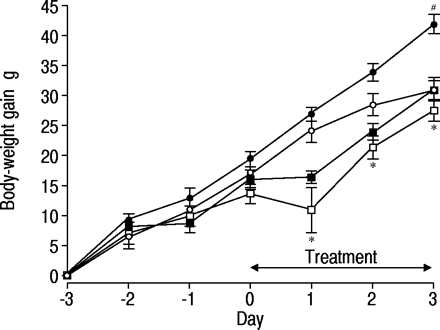
在常氧(N)或低氧(H)和胰岛素样生长因子- I处理(IGF - I(+))或未处理(IGF - I(-))大鼠中,持续输注全肠外营养液期间体重累积增加。〇N只大鼠IGF‐I(−);•:N只大鼠IGF‐I(+);□:H大鼠IGF‐I(−);▪:H大鼠IGF‐I(+)。*:与N大鼠IGF‐I相比,p<0.05(−);#:P <0.05与N大鼠IGF-I( - )相比。
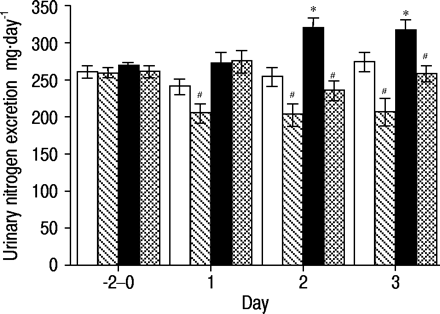
在常氧(N)或低氧(H)和胰岛素样生长因子- 1处理(IGF - I(+))或未处理(IGF - I(-))大鼠中,持续输注全肠外营养液时尿氮排泄。池中的数据显示为预处理周期(天−2-0)。□:N只大鼠IGF‐I(−);汉化:N只大鼠IGF‐I(+);▪:H大鼠IGF‐I(−); ;H鼠IGF我(+)。*:与N只大鼠相比,p<0.05(−);#:与IGF‐I(−)N或H相比,p<0.05。
;H鼠IGF我(+)。*:与N只大鼠相比,p<0.05(−);#:与IGF‐I(−)N或H相比,p<0.05。
在常氧(N)或低氧(H)和胰岛素样生长因子- 1处理(IGF - I(+))或未处理(IGF - I(-))大鼠中,持续输注全肠外营养液时尿氮潴留。Pooled的数据显示为预处理周期(天−2-0)。□:N只大鼠IGF‐I(−);汉化:N只大鼠IGF‐I(+);▪:H大鼠IGF‐I(−); ;H鼠IGF我(+)。*:与N只大鼠相比,p<0.05(−);#:与IGF‐I(−)N或H相比,p<0.05。
;H鼠IGF我(+)。*:与N只大鼠相比,p<0.05(−);#:与IGF‐I(−)N或H相比,p<0.05。
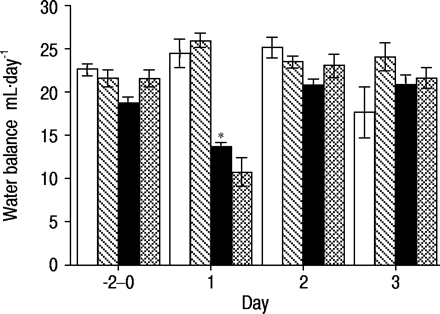
在常氧(n)或缺氧(h)和胰岛素样生长因子-1处理(IGF-I(+))或未治疗的(IGF-I( - ))大鼠中,在连续输注总肠外营养溶液期间的水平衡。池中的数据显示为预处理周期(天−2-0)。□:N只大鼠IGF‐I(−);汉化:N只大鼠IGF‐I(+);▪:H大鼠IGF‐I(−); ;H鼠IGF我(+)。*:p<0.05 compared with N rats IGF‐I(−).
;H鼠IGF我(+)。*:p<0.05 compared with N rats IGF‐I(−).
脚注
↵对于编辑评论,请参见第252页。
- 已收到2001年4月5日。
- 接受2002年1月12日。
- ©ers Journals Ltd