摘要
少数接受手术的慢性血栓栓塞性肺动脉高压(CTEPH)患者对肺内膜剥脱(PEA)难治,并经历持续的肺动脉高压(PH)。
我们回顾性评估了9例持续性PH患者(无效的PEA (inPEA)组)和8例PEA无法到达的远端CTEPH移植患者(非PEA组)的肺组织。显微镜下观察到的特征与最近在仔猪中开发的CTEPH模型的组织学进行了比较。收集并分析inPEA组和noPEA组患者介入前的临床/血流动力学数据和病史。
肺小动脉/小动脉、室间隔静脉和室间隔前小静脉明显重构,包括局灶性毛细血管瘤,以及支气管全身性血管明显肥大和增大,是两组的主要组织学形态。大多数发现在我们的猪CTEPH模型中得到了重现。墨水注射实验揭示了所谓的小血管或微血管疾病中大量的静脉受累,以及在人类和实验性CTEPH中毛细血管后支气管肺分流。
在人类和实验性CTEPH中,微血管疾病部分是由于毛细管重塑,似乎与支气管-肺静脉分流有关。需要进一步的临床研究来评估这一发现的功能重要性。
摘要
肺静脉和全身脉管系统参与CTEPH的微血管疾病http://ow.ly/yGK4U
简介
慢性血栓栓塞性肺动脉高压(CTEPH)是一种严重的疾病,如不治疗,可危及生命[1].CTEPH在最近的尼斯肺动脉高压分级(前达纳点分级)的第四组中有体现[2,3.].这种情况可能被低估了,因为临床症状可能有所不同,并不是CTEPH所特有的[4].据报道,1-3.8%的急性肺栓塞幸存者在第一次栓塞事件发生后2年内发展为CTEPH [5,6].
肺内膜切除术(PEA)已取代肺移植,是目前CTEPH患者的唯一治愈性治疗方法[7,8].然而,只有选定的患者符合PEA的条件,这取决于血栓栓塞残留物的手术可及性和潜在的合并症[9].众所周知,肺动脉阻塞和小的周围肺血管继发性重塑(称为小血管疾病)最有可能导致肺总阻力(TPR)升高[10,11].因此,影像学评估的血管阻塞与血流动力学严重程度之间的差异是可操作性的一个重要的附加标准:无法解释血管阻塞的TPR异常高的患者术后死亡率较高[11].据推测,PEA后的持续性肺动脉高压(PH)是术后死亡的主要原因,部分原因是手术切除无法到达的肺微血管重构[12].
我们的研究探讨了小血管疾病在CTEPH中的作用和重要性。为此,我们分析了无法手术的CTEPH患者在PEA或心肺移植后持续PH的组织学、临床、血流动力学和功能特征。在概念验证方法中,对人类CTEPH组织学的观察结果与我们机构最近建立的猪CTEPH模型的组织学进行了比较[13,14].
材料与方法
病人
我们回顾性回顾了1994年至2010年间接受移植的17例CTEPH患者的临床数据和组织学样本,这些患者要么是在PEA和持续PH后(无效的PEA (inPEA)组),要么是主要无法手术的CTEPH(非PEA组)。所有CTEPH病例术前都在肺科医生、胸外科医生和放射科医生的跨学科会议上进行了讨论,关于PEA可行性的最终决定已达成共识。所有inPEA组患者均有远端阻塞性疾病伴高水平肺阻力,但被认为是可手术的。然而,PEA导致持续PH伴右心衰。在紧急情况下,除1例患者外,其余患者均有心肺辅助作为心肺移植的桥梁。noPEA组患者最初被认为不能手术,最终被列入移植名单。临床资料见表1.
人体标本的组织学
所有患者的肺样本均采用常规光学显微镜进行回顾性分析。肺组织在肺移植后(n = 16)或尸检时(n = 1)系统采样,最终石蜡包埋。5 μm厚切片分别用苏木精-伊红染色或苏木精-伊红-藏红花染色,后者染色以橙色突出胶原/纤维区。所选样本进行弹性蛋白染色(兰奈龙四重染色:红色为细胞质/平滑肌,品红为纤维蛋白/红细胞,蓝色为胶原蛋白/纤维化,黑色为弹性纤维,棕色/黑色为细胞核)。分析与半定量评分评估相对应,使用前瞻性设计的带有几个组织学项目的评估表(表2而且3.).得出的每个项目的总分没有分类,而是显示为绝对值。由于支气管动脉肥厚的评估只能在少数中央肺样本上进行,因此这一项目没有得出结论,结果表示为流行的初级半定量评估(0-III分)。具体请参考在线补充资料。
一个人CTEPH病例和猪CTEPH模型的墨水注射程序
1例CTEPH病例,2只CTEPH动物和1只假动物的肺进行了肺移植体外墨水注射程序,以追踪重建微血管的起源,并揭示系统和肺血管之间可能的分流。简单地说,绿色墨水被注射到肺门水平的肺静脉,蓝色墨水被注射到支气管动脉,要么在肺门水平(人肺),要么在主动脉水平进入开口(猪模型)。具体请参考在线补充资料。
猪CTEPH模型
我们研究了10头21±3 kg的大白仔猪。该研究符合国家医学研究学会制定的实验动物护理原则,并得到了我们当地动物实验伦理委员会的批准。仔猪被随机分配到两组,每组5头。如前所述,实验CTEPH组在10周内诱导栓塞后PH [13,14].具体请参考在线补充资料。
猪样本的组织学/形态测量学
献祭后,收集所有动物的肺,进行大体解剖和组织学(苏木精-伊红-藏红花染色),最终用光学显微镜分析。左肺(结扎,完全闭塞),右下叶(部分,进展性闭塞)和右上叶(非闭塞区域)被定义和区分为感兴趣的组织学区域。结果与假手术对照组的左肺进行比较。对每只CTEPH动物的每个感兴趣区域进行一张载玻片的形态测量,并对所有假动物的左肺进行一张载玻片的形态测量。具体请参考在线补充资料。
统计分析
数据以均数±表示扫描电镜除非另有说明。根据变量类型,使用t检验或卡方检验比较组间的人口统计学和医学特征。采用单因素方差分析(ANOVA)和Tukey后验分析(post-test analysis)对仔猪组织学形态学数据进行比较。p值<0.05时,差异被认为是显著的。使用Graphpad Prism 6 (Graphpad Software, San Diego, CA, USA)进行统计分析。
结果
CTEPH的人口学特征和病史
患者的所有人口学特征显示在表1.除了术前纽约心脏协会(NYHA)分级和使用植入式心血管设备(ICD)病史外,两组患者特征相似。事实上,考虑到术前肺阻力水平和6分钟步行距离(6MWD)缩短,所有患者都是手术高危患者。值得注意的是,noPEA组包括更多的NYHA IV级患者,而inPEA组显示更多的患者具有无效手术(ICD使用)的风险因素。
人CTEPH的临床、血流动力学和肺功能特征
NYHA功能分级、6MWD、肺功能检查及血流动力学参数结果见表1.
人CTEPH的组织学特征
inPEA组和noPEA组肺样本基于评分的组织学评估总结在表2而且3..两组最显著的特征是大多数毛细血管前存在大量的动脉偏心性内膜纤维化。有组织的血栓性病变,或所谓的滤漏样病变,经常出现。常见的室间隔前小静脉和较大的室间隔静脉内膜纤维化,在inPEA组9例中有7例同时出现,而在noPEA组8例均同时出现。在所有9例pea病例中,有7例非pea病例中存在肺毛细血管瘤样灶的间质重塑。所有病例均表现为肺中心区全身支气管动脉和血管扩张的肌肉肥大。典型组织学表现见图1- - - - - -3..
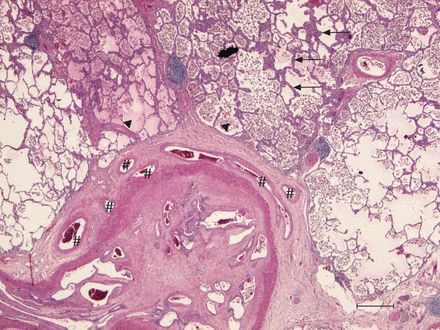
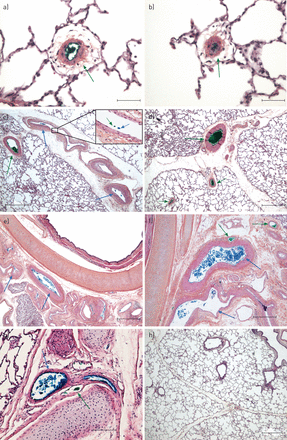
慢性血栓栓塞性肺动脉高压患者(无效肺内膜切除术组)的肺样本,苏木精-伊红染色。一个明显的,有组织的,部分再渗透的大肺动脉血栓栓塞病变。邻近的全身血管数量众多,并显示扩张和肥大(中心,#).同时,可见肺泡间隔增厚(右上,箭头),大量肺泡内巨噬细胞和局灶性水肿(左上,均为箭头所示)。比例尺= 500 μm。
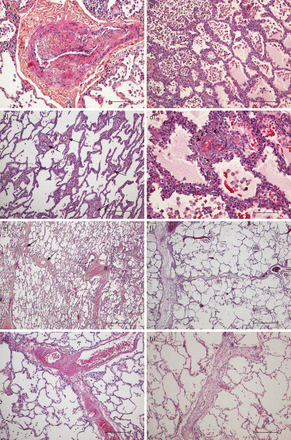
慢性血栓栓塞性肺动脉高压(CTEPH)患者的肺样本(无效肺内膜剥脱组),用苏木精-伊红和苏木精-伊红-藏红花染色。a)小肌性肺动脉,显示偏心性内膜纤维化,常见于CTEPH。b)肺泡间隔因毛细血管充血和增生而局灶性增厚,类似肺毛细血管血管瘤灶。左为肺泡内巨噬细胞/噬铁细胞,右为水肿。c)小血管疾病:可见大量毛细血管前或毛细血管后微血管,可见肌肉重塑(箭头)。d)微血管重塑(箭头)和肺泡间隔增厚。e)概述,包括肌肉性肺动脉和有组织的血栓性病变(右,#)及其毗邻的细支气管,重塑的静脉显示肌肉化和内膜纤维化(左,箭头)。f)小静脉流入室间隔静脉,均表现为准闭塞性疏松内膜纤维化。g)肌肉重塑和纤维化导致室间隔静脉部分闭塞。h)小静脉伴闭塞性内膜纤维化。比例尺:a-c, g, h) 250 μm;D) 100 μm;E和f) 500 μm。
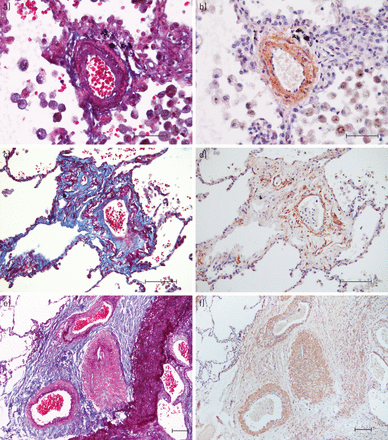
慢性血栓栓塞性肺动脉高压患者的肺样本(无效肺内膜剥脱组)。兰舌四重染色(细胞质/平滑肌:红色;纤维蛋白、红细胞:红色;胶原蛋白/纤维化:蓝色;弹力纤维:黑色;细胞核:棕色)和平滑肌细胞免疫染色。a和b)微血管,平滑肌细胞层分隔良好,内膜纤维化(超出内部弹性层)。c和d)间隔静脉附近的微血管(未显示),呈现少细胞、富含胶原蛋白的内膜纤维化(蓝色),部分堵塞管腔;注意肌化不发达(肌动蛋白染色)。e和f)大肺动脉的血管管,显示有组织的血栓物质阻塞; the systemic vessels show smooth muscle cell hypertrophy/hyperplasia (actin staining) and a more or less well defined internal elastic lamina, while the external elastic lamina is either ill-defined or missing. Scale bars: a and b) 50 μm; c–f) 100 μm.
inPEA组1例患者的墨水注射实验显示支气管周围系统血管和微血管充盈呈蓝色和绿色(图4),并强调小叶间隔内小支气管静脉与肺静脉的直接连接(图4 b).肌肉型肺外周动脉可见蓝绿混合墨水,显示偏心性内膜纤维化(图4摄氏度),以及较大的弹性型肺动脉有组织的栓子内的再通血管(图4 d).小叶间隔内重塑的肺静脉可见绿色墨迹(图4 e)和鼻中隔前小静脉(图4 f),以及经证实为毛细血管后小静脉的再造微血管(图4g和h).肺泡毛细血管与充满绿色墨水的微血管相邻,没有明显的墨水标记,排除了毛细血管前小动脉逆行填充的可能性。
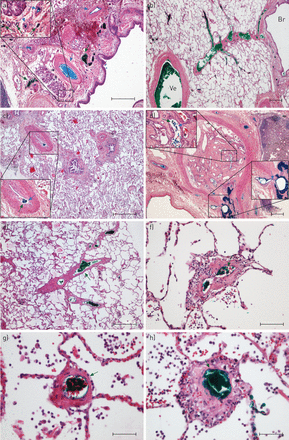
肺移植时注射蓝色(支气管动脉)和绿色墨水(肺静脉)的慢性血栓栓塞性肺动脉高压(CTEPH)患者(无效肺内膜剥脱组)的肺样本。a)支气管周围血管(箭头)填充蓝色(动脉样厚壁血管)或绿色墨水(静脉样薄壁血管);放大插图显示了同一支气管壁内微血管水平的相同模式。b)支气管壁内充满绿色墨水的血管(右;Br)流入更大的中隔静脉(中间),中隔静脉又连接到显示肌肉化的大(可能是节段性的)重塑静脉(左;Ve)。c)肌肉型肺动脉(<500 μm),偏心型内膜纤维化,狭窄的管腔内蓝绿相间(放大插图)。d)较大的弹性型肺动脉,被有组织的血栓栓塞物质阻塞,有许多再通血管;后者是用混合的蓝色和绿色墨水填充的(放大插图,左上角)。注意可见与动脉周围血管的连接,用蓝色墨水突出,提示系统性血管可能在解决肺栓塞中起作用(放大的插图,右下)。 e) Remodelled septal veins displaying intimal fibrosis and muscularisation are filled with green ink. f–h) Several examples of remodelled microvessels. f and h) Fibrotic thickening and some inflammatory infiltrate. g) Muscularisation. All microvessels are filled out with green ink, identifying them as pulmonary venules and strongly suggesting involvement of venules in CTEPH-associated small vessel disease. Scale bars: a–e) 500 μm; f) 100 μm; g and h) 50 μm.
实验猪CTEPH的血流动力学特性
与假手术动物相比,CTEPH动物的平均肺动脉压值更高(30.4±3.5)与14±1毫米汞柱;p = 0.001)和TPR(503±45与336±21达因·s·厘米−5;P = 0.01)。血流动力学结果总结于表4.
实验CTEPH的组织学特征
CTEPH组的5头仔猪组织学结果相似。与假手术组相比,除前面所述的阻塞性血管病变外,以及通畅区域的肌肉型肺动脉重构[13], CTEPH组的动物表现出严重的左肺间隔静脉重塑,在较低程度上,在右肺下叶(图5).静脉病变包括闭塞性内膜纤维化和动脉化。CTEPH左肺和右下叶微血管(直径<50 μm的小动脉或小静脉)肌肉重构比例呈下降趋势,而右上叶和假手术动物无肌肉重构(图5 b).在所有CTEPH动物的左肺和右下叶中,支气管动脉和血管血管的肌肉肥大和扩张令人印象深刻,并以相似的比例减少,而假动物的右上叶和肺没有表现出这种模式(图5度).
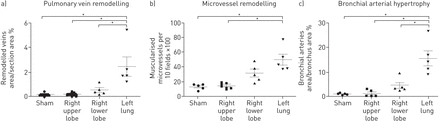
a)肺静脉,b)肺微血管(<50 μm)和c)假手术动物肺和慢性血栓栓塞性肺动脉高压动物右上叶(通畅区)、右下叶(反复栓塞区)和左肺(结扎,完全闭塞区)支气管动脉重构程度。请参考在线补充材料中的额外材料和方法部分。注意这三种组织学模式在所有四组的一致性,提示病理生理依赖。*: p < 0.05。
在两只CTEPH动物和一只假动物的肺门静脉注射绿色墨水,支气管动脉注射蓝色墨水后,我们发现重塑/肌肉化的微血管的很大一部分是静脉起源(小静脉)。此外,大的重塑/动脉化的间隔血管(解剖学上的静脉)被绿色或蓝色墨水填充。绿色肺静脉注射直接导致大量支气管静脉绿色充盈,肺泡毛细血管无明显充盈,提示全身血管与肺间隔静脉分流(图6).
仔猪慢性血栓栓塞性肺动脉高压模型。肺微血管、小叶间隔内血管和支气管血管的重塑。苏木精-伊红-藏红花染色用蓝色(支气管动脉)和绿色(肺静脉)墨水注射。a和b)强烈重塑的微血管显示肌肉化和外延增宽,部分显示为毛细血管后小静脉:管腔被绿色墨水(绿色箭头)填充,已逆行注入近端(肺门)肺静脉。c)小叶间隔内血管的强烈肌肉和纤维化重塑。中隔前静脉(强烈的肌肉增厚)显示绿色墨水充盈(绿色箭头),中隔内重塑血管显示蓝色和绿色墨水痕迹(蓝色和绿色箭头),放大插图显示蓝色和绿色墨水混合。d)重塑的间隔内静脉和间隔前静脉(绿色箭头)内填充绿色墨水。e)全身支气管动脉增生和肌肉肥大(蓝色墨水充盈,蓝色箭头)。f)支气管壁可见充满蓝色墨水的动脉(蓝色箭头)和充满绿色墨水的静脉(绿色箭头),可能是支气管静脉与注射的肺静脉相连。g)假动物:正常大小的小支气管动脉充满蓝色墨水(蓝色箭头),薄壁支气管静脉显示绿色墨水(绿色箭头),连接似乎是在生理条件下存在的。 h) Overview of a lung sample from a sham piglet. Note the slender lobular septa, lacking venous remodelling. Scale bars: a and b) 50 μm; c, d, f and h) 500 μm; e) 1000 μm; g) 100 μm.
讨论
患者的研究
肺栓塞和/或深静脉血栓形成(DVT)的发生是CTEPH诊断的公认标准,也是可手术性和近端疾病的预测因素。然而,大多数已发表的系列报道了CTEPH患者既往肺栓塞或深静脉血栓的发生率<50% [15- - - - - -17].如P所述epke -Z阿坝et al。[18],来自欧洲登记的最新报告显示,这些患者中肺栓塞和深静脉血栓病史的发生率高得惊人(分别为74.8%和56.1%),这可能是由于参与中心对血栓栓塞的认识提高了。我们的研究回顾了17例CTEPH患者的图表,他们经历了无效的PEA或因远端不能手术的疾病而接受了移植。由于所有病人都不适合做手术(如。PEA),我们可能选择了主要微血管疾病和近端梗阻性病变较少的患者。因此,低发生率的肺栓塞史符合我们本研究的选择标准(表1).
两组均为手术高危患者,肺阻力均为>900 dyn·s·cm−5, 6MWD <350 m, NYHA III或IV,既往无血栓栓塞性疾病史和/或使用ICDs。两组的手术风险都很高,但考虑到NYHA的地位,非pea组的手术风险更高。
人类组织学的发现
我们报告在CTEPH患者的肺样本中累及远端肌肉型肺动脉和微血管,明显的静脉重塑和血管瘤样灶。我们的研究结果表明,外周毛细血管前系统和更令人惊讶的毛细血管后系统的致病贡献。我们将我们的发现与最近建立的CTEPH猪模型进行了比较,并报告了所谓的CTEPH小血管疾病中显著的静脉受累,与增加的支气管肺分流有关。
肺动脉
经典的弹性型大动脉血栓栓塞重塑已被报道与远端、手术无法接近的小肺血管的继发性血管病变有关[12].这种所谓的小血管疾病具有慢性(如果不是进行性的话)特征,这可能解释了在没有任何可检测到的继发性栓塞事件的CTEPH患者中观察到的PH值升高的原因[12,19,20.].此外,手术无法到达的小外周血管重构可能是PEA后持续PH的主要因素[7].事实上,我们发现所有被分析的CTEPH患者的肺都表现出外周动脉重塑。内膜偏心性纤维增厚是最常观察到的组织学项目,在所有外周区域的玻片上均有出现(表2而且3.).在他们对31例CTEPH患者的描述性分析中,M奥泽和Bloor[10]同样报道了外周肌肉动脉中最突出的组织学特征是偏心型内膜增厚,其次是同心型内膜增厚。与M奥泽和Bloor[10],在我们的研究中没有发现丛状病变的显著证据。在过去,丛状病变并不总是被认为是CTEPH的一个特征[21].然而,其他研究小组报道了CTEPH以及几种形式的肺动脉高压(PAH)中存在此类病变,对此的讨论仍有争议[10,22,23].
肺静脉和毛细血管
组织学结果提示累及毛细血管后肺血管。在大多数玻片上观察到纤维性病变,但强度中等,未达到肺静脉闭塞性疾病(PVOD)中静脉重塑的重要性/优势。最重要的是,墨水注射实验用绿色突出了许多典型重构的小微血管,揭示了它们是小静脉,并提示cteph相关小血管疾病涉及肺小静脉(图4).我们的弹性蛋白染色和突出微血管平滑肌细胞的免疫组化实验证实了这一推断(图3).应该概述的是,与血液相比,温和的墨水注射和较高的染料粘度的组合防止了毛细血管床以逆行方式填充。因此可以排除通过毛细管床的绿色墨水显著回填小动脉的情况。所述的处理方法和染料特性也可能是分流前血管中墨水浓度显著,而分流点后墨水浓度非常小的原因,如绿色墨水在肺动脉中,蓝色墨水在肺静脉/动脉中。毛细血管瘤样区域存在,但不像PVOD那样经常遇到。值得注意的是,这些病灶的分布与PVOD不同:我们观察到与节段或亚节段肺动脉密切相关的地形,显示有组织的动脉血栓栓塞性梗阻。相比之下,PVOD的特征是血管瘤样病灶在实质内呈斑块状分布,与大动脉无关[24].据我们所知,这种静脉和毛细血管模式在人类CTEPH中首次被描述。
肺内系统血管
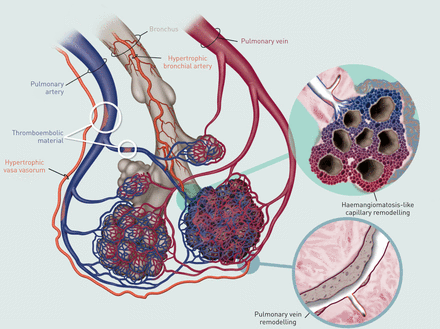
inPEA组和非pea组的所有肺均有明显的支气管血管和血管血管肥大。支气管周围动脉肌肉增厚,全身动脉和静脉均肿大。在我们的墨水注射病例中,我们发现支气管系统血管以蓝色或绿色突出显示。我们的实验证实了已知的事实:支气管血管直接连接到毛细血管后肺血管[25].然而,我们的墨水实验表明,大(绿色)支气管/肺静脉位于支气管外膜内,与(蓝色)支气管动脉直接相邻。我们没有观察到发育良好的“支气管毛细血管床”,这可能表明连接或多或少类似于支气管小动脉和肺静脉之间的直接连接/吻合,仅在必要时显著增加并具有高功能。如。支气管动脉肥大。有组织肺动脉栓塞内的再通血管,以及外周肺动脉表现为偏心性内膜纤维化,可见绿色和蓝色墨水的混合,这不仅表明系统动脉和肺动脉之间存在直接连接,而且后者与肺静脉之间也存在直接连接,即肺动静脉分流。虽然我们不会广泛讨论这一点,因为这些发现在我们的分析中是稀疏的,但在运动条件下,人类和动物都显示出了这种现象[26- - - - - -28].全身支气管动脉肥大和扩张的模式在CTEPH中是众所周知的[25,29].据推测,阻塞性后肺动脉压力的降低和支气管动脉与肺动脉之间压力梯度的最终增加可能导致预先存在的支气管肺动脉吻合口的打开[30.,31].有趣的是,我ohnsonet al。[32]报告了持续空气栓塞肺动脉主动脉后,绵羊的肌化静脉数量显著增加,肺静脉壁厚度也显著增加。作者还发现,在连续空气栓塞的第12天,与对照组相比,小支气管血管的体积密度增加[32].由于支气管动脉分支与毛细管前肺小动脉之间以及支气管动脉与肺静脉之间的吻合在过去已被描述,因此对毛细管后血管和毛细血管网络本身的直接全身性影响似乎是可能的[25,33,34].在这方面,系统回路中升高的压力与肺静脉低压系统之间前所未有的定量显著联系,可以解释静脉壁腔室的广泛反应,包括介质的肌肉化和内膜的纤维化增厚,以及毛细血管网络上连续的充血反应,最终导致毛细血管增生。此外,毛细血管床内的重塑和毛细血管前小动脉的肌肉增厚可能部分是由于先前描述的支气管肺动脉吻合口的打开。这种机制的局灶性分布是由动脉栓塞闭塞引起的,因此发生在闭塞的肺动脉附近,这可以解释病理性血管壁反应对局灶性的、不相称的强压力刺激的反应。本文概述了所提出的机制图7.
一种提议的支气管肺静脉(和动脉)分流机制,在人类和实验性慢性血栓栓塞性肺动脉高压中得到证实。注意全身动脉(以支气管动脉和血管血管表示)与肺动脉和毛细血管后肺静脉/小静脉的毛细血管前连接示意图。放大插图(上)显示肺小动脉反应性增厚,支气管肺动脉分流口外可见一血管瘤样灶,可见肺泡毛细血管增殖。另一张放大的插图(下)显示肺静脉壁在支气管肺静脉连接处的反应性纤维化重塑,将全身压力与肺部低压静脉系统联系起来。
猪组织学的发现
在左肺和右下叶内,所有CTEPH动物(n = 5)均表现出重要的肌肉肥大、支气管动脉和血管血管数量的增大和增加。微血管的肌肉化是持续存在的,而在右上叶和假对照组中仅零星存在。假手术动物肺、CTEPH动物右上叶(无闭塞)、右下叶(部分和进步性闭塞)和左肺(结扎,从第1天开始完全闭塞)的组间比较显示,肺静脉重塑程度、支气管动脉肥大和微血管肌肉化程度存在显著差异,表明这三种血管变化的功能一致。这三个形态学参数的变化峰值出现在结扎导致的全肺动脉闭塞区,而重复栓塞导致的部分和进展性闭塞区也产生了同样的变化,但程度较小。至少在支气管动脉重建方面,这一观察结果与Shimizuet al。[29],其对59例CTEPH患者的计算机断层血管造影的回顾性分析显示,与节段水平上的梗阻相比,支气管动脉的横截面积与血栓栓塞物质的中心范围正相关。他们还将CTEPH组与16名PAH患者(尼斯分类第1组)进行了比较,发现与PAH相比,CTEPH患者的支气管动脉总面积显著增加。但远端(节段)型CTEPH与多环芳烃的支气管动脉总面积无明显差异。有趣的是,24例CTEPH组患者接受了PEA, 21例患者最终接受了PEA后的计算机断层血管摄影,结果显示支气管动脉总面积明显减少。这些结果反映了我们的实验发现,血栓栓塞性梗阻的中心范围与支气管动脉肥大之间的正相关。此外,它们还说明了CTEPH支气管动脉肥大的可逆性。
此外,实验表明,新生羔羊左肺动脉结扎1-3年后,会导致全身性支气管血管沿支气管分支肥大,形成密集的血管丛,最终充满肺毛细血管[35].解剖分析通过宏观观察支气管动脉树模型。我们对年幼仔猪的观察证实了这些关于支气管血管肥大的结果,甚至早在左肺动脉结扎后10周。重要的是,我们的肺静脉逆行注射绿色墨水没有通过肺泡毛细血管网络,而是直接进入支气管静脉,这表明支气管血液流动和肺静脉的连接是未经过滤的。这一观察结果得到了最近一项对麻醉绵羊使用明胶微气球进行回声对比的超声研究的支持[36].根据他们的观察,P纵火et al。[36]推断在肺泡毛细血管之外还有连接支气管循环和肺静脉循环的支气管肺吻合口。这些观察是值得注意的,因为C哈兰et al。[37他们的实验表明,到目前为止,支气管动脉血液的大部分流入肺循环,只有大约13%的血液全身回流到右心。因此,由于全身-肺毛细血管后吻合对肺静脉的血流有显著影响是可以想象的。事实上,这一机制可以解释我们猪模型中所有三个形态参数的密切相关性:由于支气管动脉流量/肥厚增加,静脉和微血管重塑的增加。
此外,在我们的猪模型中,我们发现支气管动脉特异性的蓝色墨水填充在小叶间隔内的大肌肉化血管中,直接靠近充满绿色墨水的肺间隔静脉,以及在肺胸膜下。后者的观察结果与C哈兰和Carvalho[35]在羔羊中:在左肺动脉结扎模型中,他们描述了供应肺胸膜的血管扩大,这些血管部分直接连接到供应终端气道的支气管血管。这一发现是特别有趣的,因为在正常的人类肺部,支气管动脉不知道在小叶间隔内运行;后者包括肺静脉和淋巴管[34,38].因此,在这种情况下,可以假设肺或支气管的间隔静脉动脉化。尽管在猪肺的一些区域存在充血和肺泡间隔轻度增厚的迹象,但在我们的CTEPH模型中,我们没有发现完全生长的毛细血管瘤样区域。与人类CTEPH差异的原因可能在于我们的模型缺乏真正的慢性,因为所有仔猪都是在10周后牺牲的。
结论
我们对人类CTEPH的研究,包括与最近开发的猪模型的组织学比较,证实了不能手术患者或PEA后PH持续的肺小血管或微血管疾病的重要性。我们新发现了CTEPH相关小血管疾病中毛细血管后肺静脉腔室的显著累及,并能够在实验猪CTEPH中重现这些修饰。事后剖析在一个人类CTEPH病例和我们的模型中,墨水注射手术使我们能够将毛细血管后静脉重塑与肥大的全身性支气管血管连接起来。我们的结论是,支气管肺静脉分流是存在的,可能是重要的病理生理在人类CTEPH。为了进一步证实这一怀疑,并最终开发出可以量化微血管疾病的成像工具,需要前瞻性研究在活的有机体内.
脚注
有关编辑评论,请参阅1121页.
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2013年9月27日。
- 接受2014年6月13日。
- ©2014人队