摘要
背景
新出现的传染病没有已知的治疗方法。评估潜在药物的安全性和有效性使临床医生能够做出基于证据的治疗决定,并有助于全面控制疫情。但是,在不可预测的疫情环境下很难开展临床试验。我们对2009年流感大流行进行了文献计量学系统综述,以确定治疗证据生成的速度和质量。这为这次和未来大流行的高质量证据生成方法提供了信息。
方法
我们在PubMed搜索了所有描述甲型H1N1流感患者pdm09治疗的临床数据(包括临床试验、观察性和病例系列),并在ClinicalTrials.gov上搜索了旨在招募该疾病患者的研究。
结果
160份出版物详细介绍了甲型H1N1 pdm09住院患者的33869个疗程。大多数是回顾性观察性研究或病例系列。592名患者作为注册的介入临床试验的参与者接受了治疗(或安慰剂),其结果可以公开。在大流行期间,没有一项已登记的试验结果可用,发表的中位日期是国际关注的突发公共卫生事件结束后的213天。
结论
患者经常使用未针对这一适应症注册的药物治疗大流行性流感,但很少在高质量数据采集的情况下进行治疗。结果是依赖于在同情的情况下使用,导致抗病毒治疗的潜在收益和危害持续不确定。在大流行期间,快速扩大临床试验规模对于建立高质量的证据基础至关重要。
背景
病毒性大流行对全球卫生安全构成重大威胁。未来的流感大流行被认为是可能的。在过去20年里,我们还看到出现了具有大流行潜力的人畜共患人类呼吸道冠状病毒。这些都是严重急性呼吸道病毒(SARS;由SARS-CoV-1引起的)、中东呼吸综合征(MERS)以及目前由SARS-CoV-2引起的2019冠状病毒病(COVID-19) [1].对2009年甲型H1N1流感毒株(A(H1N1)pdm09)大流行(近年来最大的呼吸道病毒疫情)的研究可以为大流行期间的研究过程提供见解,目的是改进包括COVID-19在内的其他疫情的研究过程。
减少大流行的一个重要内容是预防和治疗病人。对于新出现的病毒感染,抗病毒治疗是一种关键的医疗对策,因为疫苗生产需要几个月或几年的时间,而有效的抗病毒药物可能已经存在。对于COVID-19,几种现有药物(包括瑞德西韦、洛匹那韦/利托那韦、羟氯喹和托珠单抗)的潜力令人感兴趣。在甲型(H1N1)pdm09流感大流行期间,人们对神经氨酸酶抑制剂(NAIs)作为抗流感药物产生了兴趣,尽管缺乏支持其使用的足够的安全性和有效性数据。这一证据现已大大加强了[2];然而,这其中大部分是在大流行之后产生的。尚未对大流行期间产生的关于治疗的信息的数量和质量进行定量评估。这些数据很重要,因为它代表了临床医生在重大不确定性条件下为患者做出治疗决定时可以获得的数据[3.],在患者人数激增期间[4].
本系统综述的目的是调查甲型H1N1 pdm09药物治疗数据在大流行期间是如何积累的(详细目标列于表中)1).本综述不仅限于已完成的临床试验,还包括未完成的注册试验,以及正式试验环境之外的治疗报告(案例研究或系列研究和观察性研究)。其中包括这些证据,因为它们既可能代表当时可用的最高质量证据,也可能代表失去收集高质量证据的机会。
方法
我们进行了系统搜索,以确定在大流行期间接受a (H1N1)pdm09治疗的患者。我们搜索了两种类型的证据:同行评审的出版物和临床试验注册记录。一位有经验的图书管理员就搜索策略提出建议。我们前瞻性地注册了该综述(PROSPERO数据库记录CRD42016039549)。有关遵守MOOSE和PRISMA指南的详细信息请参见附加文件1:附录1。
已发表文献检索
我们根据附加文件中的搜索策略搜索PubMed数据库1:附录2。为了获取有多少患者在试验之外接受治疗的信息,除了介入研究外,我们还包括案例研究、病例系列和观察性研究。唯一的例外是将奥司他韦的使用描述限制在有10个或更多患者的出版物上,因为病例报告非常丰富。我们纳入了描述住院患者和报告急性临床结局的研究(定义为住院时间、重症监护住院时间或住院时间、医疗并发症、机械通气需求或死亡率)。我们纳入了仅经实验室确诊疾病的患者。虽然A(H1N1)pdm09是疫情爆发期间的主要毒株,但论文之间在定义可能病例方面的不一致意味着不可能采用一致的纳入方法。我们只纳入了在2009年4月1日(病毒株首次被发现时)和世界卫生组织(WHO)在2010年8月10日(国际关注的突发公共卫生事件结束时)之前开放报名的论文。当A(H1N1)pdm09成为季节性毒株后,为了将专门针对大流行的研究与常规季节性流感报告进行区分,这一限制是必要的。这些标准不适用于临床试验(不可能与季节性报告混淆)。
我们排除了对治疗的描述不能量化或治疗名称缺失(包括使用通用术语“抗病毒治疗”)的论文。我们将治疗定义为病原体定向治疗(例如抗病毒药物)或有特定适应症的a (H1N1)pdm09的宿主定向治疗。因此,我们排除了标准重症监护干预措施的描述,包括皮质类固醇和体外膜氧合。当一个患者队列(相同的样本量、入组期、作者和研究地点)出现在一篇以上的论文中时,重复项被排除。我们排除了英语以外的语言。
临床试验注册中心检索
我们进行了两次临床试验登记检索。第一个调查的目的是审查为应对这一流行病而计划进行的研究。使用条件“H1N1”搜索ClinicalTrials.gov,日期限制为大流行开始后的注册日期。进行了第二次搜索,以确定能够纳入A(H1N1)pdm09感染患者的已有流感研究。ClinicalTrials.gov搜索条件为“influenza”。两种搜索的详细纳入和排除标准以及子组分析计划包含在附加文件中1:附录3。
数据提取
一位审稿人(AR)根据预先指定的纳入和排除标准进行数据提取。使用电子系统检讨软件(Rayyan [5]),供资深作者(PWH)使用。我们没有要求作者提供缺失的数据,因为这对本综述的目标没有帮助。数据提取的详细信息在附加文件中1:附录3。
统计分析
描述性统计表示为类别变量的频率和连续变量的四分位范围的中位数。来自已发表文献和试验登记的研究结果分别报告。文献分析按研究类型分层。中药作为一个单一的类别,因为单个成分无法区分。由于文献中不同的报告实践,不可能对联合治疗进行评估。采用Stata MP/15.0和Microsoft Excel for Mac/15.21.1进行统计分析和图形描述。
资金来源的作用
研究的资助者在研究设计、数据收集、数据分析、数据解释或报告的撰写中没有任何作用。
结果
来自已发表文献的发现
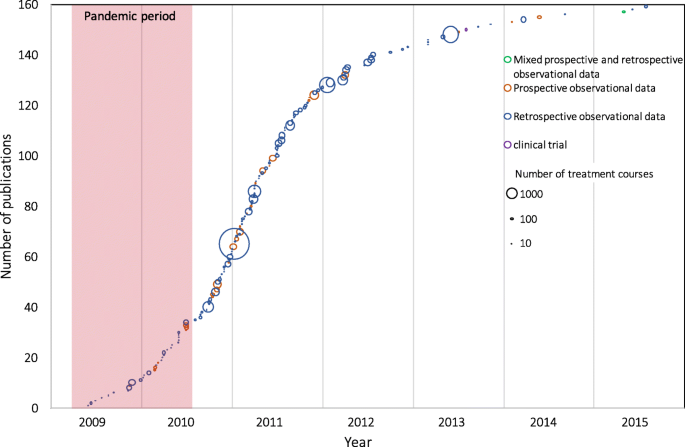
这篇综述包括160篇论文(摘要见图。1,详情见附加文件1:附录4),描述了39,577名A(H1N1)pdm09住院患者和33,869个疗程(表2).使用了12种不同的治疗方法,奥司他韦是最常见的(表2)2).每篇稿件描述的处理数量中位数为63(四分位范围,IQR 22-193)。在收录的160篇论文中,有两篇是介入性试验(n= 73例,占报告患者总数的0.2%),[6,728项为前瞻性观察性研究(n= 6102例,占总患者的15.4%),129例为回顾性观察性研究或病例报告(n= 33,342,占总患者的84.2%)和一名前瞻性和回顾性纳入的患者(n= 98,0.2%的患者)。
尽早开展前瞻性研究可最大限度地提高在疫情减弱之前达到样本量目标的概率。自确定大流行病毒毒株(2009年4月1日)以来,首次纳入前瞻性观察研究患者的中位延迟为102天(IQR 61-172天)。这两项临床试验在延迟244天和275天后开始登记。
对于前瞻性观察性研究,在病毒鉴定后,入组停止的中位数为274天(IQR 195-313)。这是国际关注的突发公共卫生事件结束前223天(2010年8月10日),但当时病例数正在下降。两项临床试验分别在病毒鉴定后699天和944天(2011年3月和11月)关闭登记。
所有文章随时间的发表日期如图所示。2.没有(0/2)项介入性试验在国际关注的突发公共卫生事件结束前发表。25%(7/28)的前瞻性观察性研究和22%(28/130)的回顾性或混合入组研究在国际关注的公共卫生事件结束前发表。所有论文的中位发表日期为2011年3月18日(IQR 2010年9月28日至2011年10月24日);这是国际关注的突发公共卫生事件结束后的213天。总体而言,最终患者登记(或纳入)与发表日期之间的中位延迟为444天(IQR 281-684)。患者最终登记和提交之间的中位数日期为302天(IQR 142-534),提交和接受之间的中位数日期为93天(IQR 63-144),接受到发表的中位数日期为56天(IQR 24-94)。
39个国家报告了治疗数据。论文数量最多的是美国(n= 25个,报告2559个疗程),其次是中国(n= 16,报告14,680个疗程)和西班牙(n= 16,报告4103疗程)。国家一级的数据描述了所描述的出版物和治疗课程的数量以及前瞻性研究中患者登记的第一次日期(如相关)显示在附加文件中1:附录5)。
88%(140/160)的文章描述了患者的妊娠状况。文章描述了88%(140/160)的文章纳入老年患者,93%(149/160)的文章纳入儿童。
23%(36/160)的论文描述了治疗的不良反应。42%的病例出现了不良反应或严重不良事件。13%(21/159)的文章测试了耐药性并描述了一些耐药样本,4%(6/159)的文章测试了耐药性但没有发现突变,3%(5/159)的文章报告了抗病毒耐药性的临床怀疑,而在剩余的81%(129/159)的论文中没有关于抗病毒耐药性的声明;一篇论文没有描述抗病毒药物的使用,因此被排除在外。
H1N1试验注册的结果
15项H1N1研究注册记录被纳入综述(附加文件1附录6)包括在大流行期间计划的10项介入试验和5项观察性研究(2项为治疗疗效结果,3项为一般急性临床结果)。总共研究了8种不同的治疗方法:奥司他韦、扎那米韦、恢复期血浆、静脉注射免疫球蛋白、瑞舒伐他汀、西罗莫司、中草药和维生素补充剂(维生素A、C和E)。
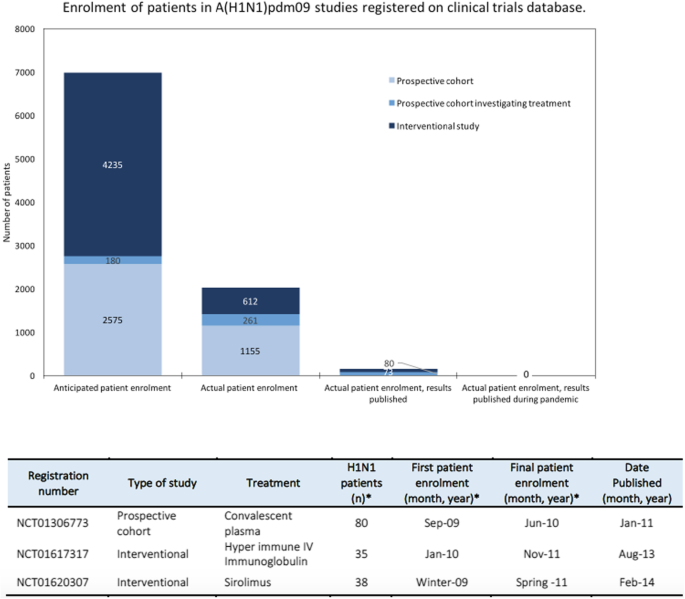
在这15项研究中,据报告有9项已完成,4项因H1N1大流行结束或病例数下降而终止,2项研究的状态没有记录。所有研究中患者的预期和实际入组情况如图所示。3..一些研究方案排除了年轻(25%)和怀孕(50%)的患者。在已完成的研究中,有3项的结果可在文献中查阅(图2)。3.),代表153名患者,并可用于另外两项终止研究的临床试验注册。附加文件中提供了只包括住院或严重病例的临床试验的亚组分析1:附录7。
流感试验注册的结果
审查了18个流感登记记录(附加文件1在A(H1N1)pdm09大流行期间,有16项介入试验和2项观察性研究纳入患者。正在调查的治疗方法是奥司他韦,sambucol补充剂,zanamivir, peramivir,金刚烷胺,石榴补充剂,nitazoxanide和favipiravir。
11项研究已完成,4项提前终止,2项研究的状态未知,1项研究正在进行登记。11项已完成的研究中有9项结果可用3.),代表439名A(H1N1)pdm09患者。
讨论
一直有人批评说,对疾病暴发的研究反应是断裂的和滞后的[13,14,15].然而,很少有人对这些假定的不足进行定量研究。这篇论文证明,尽管在大流行期间为住院的A(H1N1)pdm09流感患者描述了超过33000个治疗疗程,但在一项已注册的介入临床试验中,只有不到600人接受了治疗(或安慰剂),其结果可在同行评审的文献中获得。在大流行期间,这些已登记的试验结果均不可用,因为观察性研究的结果也很少。这是收集高质量数据的重大失败。
我们的研究结果表明,我们必须做出改进,以便在大流行期间,包括COVID-19大流行期间,为患者及其治疗临床医生提供循证护理。正在研究几种药物作为COVID-19的潜在治疗方法,但我们注意到一些早期发表的研究控制得很差[16,17].我们必须从甲型H1N1 pdm09大流行中吸取教训,并确保在能够收集高质量、可解释的数据的条件下进行治疗试验,为未来的临床护理提供信息。
我们发现大多数治疗过程的描述都是回顾性观察性研究或病例系列,很少开展前瞻性研究。然而,在将A(H1N1)pdm09患者纳入正在进行的或季节性流感研究方面取得了相对的成功——在一项试验中纳入的582名患者中,有439人是以这种方式纳入的。实际上,有人提议在流行间期对类似疾病(如季节性流感)进行治疗试验,作为改进疫情研究反应的解决办法[18].这不仅通过允许在疾病爆发时迅速招募人员(如本文所述),而且通过测试试验设计和建立研究能力来实现。还应采用新的试验设计,如适应性平台试验,作为加快暴发研究的一种方式[18].使用这种方法,可以在一个总体方案和监管框架下评估多种治疗方法(甚至多种呼吸道病毒),从而提高效率[19].本文提出的2009年的研究结果支持对包括COVID-19在内的呼吸道病毒大流行采取这种方法的必要性。事实上,两项针对COVID-19治疗的大型平台试验正在进行(RECOVERY [ISRCTN50189673]和Solidarity [ISRCTN83971151]),并已经产生了高质量的证据[20.].睡眠者协议的研究可能会提供进一步的解决方案。这些预先准备和预先批准的方案可以处于休眠状态,等待大流行性呼吸道病毒病例,并允许事先对方案的后勤和可行性进行评估。严重急性呼吸道感染有一个此类方案的例子(NCT02498587),并已用于快速纳入COVID-19患者。
在西非埃博拉病毒病(EVD)流行后提出的建议表明,临床研究应在疫情达到高峰时启动、实施和完成[21].我们发现,从首次检测到甲型H1N1流感pdm09起,在前瞻性数据收集开始前超过3个月,在首次介入试验开始招募前8个月。虽然这些延迟与最近对其他流行病观察研究延迟的评估相比很好[22]或临床试验[23),它仍然太慢。
此外,在我们的综述中纳入的小样本量的文献表明了断裂的研究反应。据估计,需要800名患者的样本量,才能在住院患者中进行NAI的随机对照试验[24].这里确定的前瞻性研究没有那么大的规模。除了增加登记人数和外部有效性的好处之外,多中心研究在流行病方面有特殊的优势。它可以弥补区域一级流行病学的意外变化(例如利比里亚埃博拉病毒病爆发的突然结束导致临床治疗试验过早停止)[25]或因医院传播而暂时关闭卫生保健设施(如2003年SARS爆发期间发生的情况)[26].
为确保研究结果的普遍性,对疫情的研究应对也应具有地理多样性和全球流行病学的代表性。在本文报告的结果中,中国有大量代表性,并报告了所描述的大多数治疗疗程(14,680;占总数的43.3%)。患者特征(包括年龄、性别和其他风险因素)和卫生保健系统因国家/地区而有很大差异,这可能会影响在这些不同环境下干预措施的适用性和相对有效性。来自一个区域的及时研究反应不一定有利于全球大多数高危人群,特别是如果低收入和中等收入国家在流行病证据库中的代表性不高。事实上,在埃博拉病毒病流行之后,强调了加强中低收入国家的研究能力和基础设施以有效应对疫情的重要性[21,27].
纳入高危人群(如老年人、孕妇和儿童)对确保疫情研究的普遍性也很重要。在甲型H1N1流感pdm09大流行期间,老年人和儿科个体分别被纳入88%和93%的出版物,再次注意到这些研究中的绝大多数仅为观察性研究。然而,在大流行开始时,批准的神经氨酸酶抑制剂的试验仅在健康成人中进行,用于轻度季节性流感[28),而没有包括风险最高的人群。在新药物的初步前瞻性试验中未能纳入高危人群,可能会进一步推迟在疫情情况下使用药物时对这些人群的证据基础。
我们报告了临床数据获取和同行评审文献发表之间的长时间延迟。这与对其他疾病暴发的分析一致,包括对SARS的流行病学报告(其中只有7%的文章是在流行期间发表的)[29]和大流行性H1N1疫苗的随机对照试验(在大流行结束近一年后,只有29%的临床试验结果发表)[30.].目前世卫组织介入临床试验的标准是,主要研究结果应在研究完成后12个月内提交发表[31尽管对于观察性临床数据没有这样的指导方针,但在及时报告方面有类似的科学和伦理要求。
虽然延迟报告的后果在其他领域有所描述[32],在流行病期间,有特别的必要进行快速数据报告。例如,为了设计介入试验,必须累积观察数据(如接近结果的类型和率)。新出现的证据还可以优先考虑试验,以便在疫情后期病例数量下降时,最有希望的继续招募[18].
减少出版延迟的措施包括对可能改变临床实践的手稿进行快速审查[33];这种方法在COVID-19大流行期间被期刊广泛采用。试验方案的预批准(在进行研究之前进行一些同行评审)或无结果评审(评审不包括结果和一些讨论)是可选的同行评审模式,旨在提高对研究质量的关注,减少对仅发表积极发现的偏见[34].通过允许同行评议与数据收集同时开始,这些方法还可能有助于在疫情环境下加速传播高质量临床研究;事实是否如此还有待检验。还支持初步研究结果的出版前在线发布。事实上,发布前服务器(如medRxiv)使用率的增加已经反映在COVID-19的爆发中。通过发表前(同行评议之前)传播研究成果减少了延迟,但也带来了方法验证、数据准确性和研究结果解释的风险。提交到预出版服务器的COVID-19文章数量惊人[35]导致开发了几个快速、开放的COVID-19预印本同行评审平台[36,37].这些措施旨在改善预印本传播和正式同行评审/出版过程之间的质量控制;这种“叠加”审查模式是新的,它们将如何影响数据生成和传播的质量尚不清楚。
这种系统的综述有几个局限性。由于讨论A(H1N1)pdm09的大量临床文献,我们的综述范围被缩小。特别是,我们只关注使用大多数抗病毒药物的住院患者[38].在需要住院治疗的疾病严重程度方面可能存在相当大的地理差异,这可能限制了来自护理模式不同的国家(包括中低收入国家)的研究。此外,只纳入英语手稿,这可能导致纳入研究地理的类似偏见。我们纳入了几种类型的出版物,包括病例系列或观察性研究,以提供可能有资格纳入临床试验的患者的估计(注意,这一估计不代表接受治疗的住院患者的真实数量)。由于排除了治疗方法没有明确定义和流感大流行毒株未经实验室证实的论文,任何估计的准确性都会受到影响。我们对参加临床试验的患者人数的估计几乎肯定是低估的——强制注册临床试验的势头很大程度上是这样的[39]发生在大流行之后,而且试验可能已在其他地方注册,因此很可能在公众不知情的情况下计划、启动甚至完成了其他试验。我们将观测数据收集限制在国际关注的突发公共卫生事件结束之前,虽然我们认识到在第二波和第三波流行期间继续进行研究,但很难将这项工作与常规季节性流感研究区分开来。最后,出于实用主义的考虑,只有一位审稿人。
结论
在这里,我们展示了在甲型H1N1流感pdm09大流行期间,在富有同情心的护理环境下对治疗的容忍与获取治疗使用高质量数据的承诺是如何不相匹配的,因此未能达到现代循证医学所期望的标准。此外,我们发现在患者身上收集的数据在长时间延迟后被不完整地报告和发表。我们建议尽早启动多中心合作试验和预先批准的或卧铺方案,作为在大流行期间改善治疗数据积累的潜在解决方案。
数据和材料的可用性
本系统综述中包含的所有研究的细节可在附加文件中获得1:附录4。在合理的要求下,提取的数据可从主要作者处获得。
缩写
- COVID-19:
-
2019冠状病毒病
- EVD:
-
埃博拉病毒病
- 差:
-
四分位范围
- 中低收入国家的要求:
-
低收入和中等收入国家
- 即:
-
中东呼吸综合征
- 奈:
-
神经氨酸酶抑制剂
- 国际关注的突发公共卫生事件:
-
国际关注的突发公共卫生事件
- “非典”:
-
严重急性呼吸道病毒
- 人:
-
世界卫生组织
参考文献
- 1.
朱楠,张东,王伟,李霞,杨波,宋杰,等。2019年中国肺炎患者的新型冠状病毒。中华实用医学杂志,2015;29(4):344 - 344。
- 2.
杜布森,王志强,王志强,王志强。奥司他韦治疗成人流感:随机对照试验的荟萃分析柳叶刀》。2015;385(9979):1729 - 37。
- 3.
Lipsitch M, Riley S, Cauchemez S, Ghani AC, Ferguson NM。管理和减少新出现的流感大流行的不确定性。中华实用医学杂志,2009;29(2):344 - 344。
- 4.
王晓玲,王敏敏,陈克勤,陈桂平,曹福平,Peiris JM,等。2009年香港甲型H1N1流感大流行病例的住院风险。BMC感染疾病2014;14:32。
- 5.
Ouzzani M, Hammady H, Fedorowicz Z, Elmagarmid A. rayyan -一个用于系统评论的网络和移动应用程序。系统版本2016;5(1):210。
- 6.
洪耀文,杜家强,李志强,李建林,闫文伟,陈凯,等。高免疫IV免疫球蛋白治疗:2009年甲型H1N1流感严重感染患者的多中心双盲随机对照试验胸部。2013;144(2):464 - 73。
- 7.
王超,钟富峰,林淑敏,黄淑云,周春林,李建基,等。哺乳动物雷帕霉素抑制剂、西罗莫司和类固醇的辅助治疗改善了严重H1N1肺炎和急性呼吸衰竭患者的预后。重症监护医学。2014;42(2):313-21。
- 8.
东南亚传染病临床研究。双剂量奥司他韦对因严重流感住院的儿童和成人临床和病毒学结果的影响:双盲随机对照试验BMJ。2013; 346: f3039。
- 9.
金伯林DW,阿科斯塔EP,普里查德MN,桑切斯PJ, Ampofo K,朗D,等。奥司他韦在2岁以下流感儿童中的药代动力学、剂量和耐药性中华流行病学杂志,2013;37(5):339 - 339。
- 10.
李志强,李志强,李志强,等。住院患者静脉注射帕拉米韦治疗流感的疗效观察。中国航空学报。2014;19(4):349-61。
- 11.
Marty FM, Man CY, van der Horst C, Francois B, Garot D, Manez R,等。静脉注射扎那米韦治疗住院成人流感的安全性和药代动力学:一项开放标签、多中心、单臂、II期研究中华传染病杂志,2014;39(4):542-50。
- 12.
李宁,许世升,左忠,倪建林,吕国昌,吴SK,等。高剂量奥司他韦治疗甲型和乙型流感住院成人的前瞻性干预研究中华流行病学杂志,2013;29(4):344 - 344。
- 13.
罗杰克AM,霍比PW。使流行病科学现代化:在流行病期间开展以病人为中心的研究。BMC医学2016;14(1):212。
- 14.
Tran TH, Ruiz-Palacios GM, Hayden FG, Farrar J.以患者为导向的大流行性流感研究。柳叶刀》。2009;373(9681):2085 - 6。
- 15.
海登FG,法勒J,佩里斯JS。提高中东呼吸综合征冠状病毒感染的临床管理水平。《柳叶刀》感染杂志2014;14(7):544 - 46。
- 16.
郭志刚,张志刚,张志刚,张志刚,等。同情地使用瑞德西韦治疗重症Covid-19患者。新英格兰J医学2020;[Epub提前付印]。
- 17.
李志强,李志强,李志强,等。羟氯喹和阿奇霉素治疗COVID-19:一项开放标签非随机临床试验结果Int J Antimicrob Agents. 2020;105949 [Epub在印刷前]。
- 18.
罗杰克AM,霍比PW。为患者提供更多:西非埃博拉疫情如何影响新兴和流行感染治疗研究的创新。中国生物医学工程学报(自然科学版),2017;
- 19.
伍德考克J,拉瓦吉LM。掌握研究多种疗法、多种疾病或两者兼而有之的方案。中华实用医学杂志,2017;29(1):344 - 344。
- 20.
组RC, Horby P, Lim WS, Emberson JR, Mafham M, Bell JL,等。地塞米松在Covid-19住院患者中的应用-初步报告。英国医学,2020年。
- 21.
国家科学院出版社。将临床研究纳入流行病应对:埃博拉经验。华盛顿特区:美国国家科学院、工程院、医学院;2017.
- 22.
李志强,李志强,李志强,等。启动暴发和大流行观察研究所需的时间。重症监护杂志。2017;40:7-10。
- 23.
Rojek AM, Dunning J, Leliogdowicz A, Castle L, Van Lieshout M, Carson G,等。在埃博拉病毒疾病流行期间进行临床治疗试验的监管和操作复杂性。中国临床感染杂志,2018;26(9):1454-7。
- 24.
威康基金会和医学科学院神经氨酸酶抑制剂在2015年流感中的使用。可以从:https://acmedsci.ac.uk/file-download/38069-561595082cd83.pdf.2020年4月29日访问。
- 25.
邓宁J,肯尼迪SB,安蒂伦斯A,怀特海德J, Ciglenecki I,卡森G,等。brincidofovir治疗埃博拉病毒病的实验研究。PLoS One. 2016;11(9):e0162199。
- 26.
郑维文,陈俊峰,杜家强,袁俊凯。SARS的临床管理和感染控制:经验教训。中国生物医学工程学报,2013;30(2):344 - 344。
- 27.
陈志强,李志强,李志强,等。针对低收入和中等收入国家的疫情期间临床研究(CREDO)培训。新兴感染杂志2019;25(11):2084-7。
- 28.
Gubareva LV, Kaiser L, Hayden FG。流感病毒神经氨酸酶抑制剂。柳叶刀》。2000;355(9206):827 - 35。
- 29.
邢伟,Hejblum G,梁GM, Valleron AJ。2003年SARS在香港和多伦多爆发的流行病学文献解剖:时间分层回顾。公共科学图书馆。2010;7(5):e1000272。
- 30.
Ioannidis JP, Manzoli L, De Vito C, D'Addario M, Villari P. 2009年甲型H1N1流感疫苗随机试验的发表延迟。公共科学学报,2011;6(12):e28346。
- 31.
世界卫生组织。世卫组织关于公开披露2015年临床试验结果的声明[可从:https://www.who.int/ictrp/results/WHO_Statement_results_reporting_clinical_trials.pdf?ua=1.2020年4月29日访问。
- 32.
Moorthy VS, Karam G, Vannice KS, Kieny MP。世卫组织呼吁迅速报告和公开公开介入临床试验结果的新立场的理由。公共科学图书馆。2015;12(4):e1001819。
- 33.
《柳叶刀》编辑团队。10+ 10:随机对照试验的快速决策和快速发表。柳叶刀》。2015;385(9968):578。
- 34.
Button KS, Bal L, Clark A, Shipley T.防止目的证明手段:隐瞒结果以解决同行评审中的发表偏见。BMC精神病学。2016;4(1):59。
- 35.
Kupferschmidt K.预印本带来疫情数据的“消防水管”。科学。2020;367(6481):963 - 4。
- 36.
Johansson MA, Saderi D.为COVID-19预印本开放同行评审平台。自然。2020;579(7797):29。
- 37.
麻省理工学院出版社和加州大学伯克利分校启动快速审查:COVID-19 2020[2020年6月29日更新]。可以从:https://rapidreviewscovid19.mitpress.mit.edu/pub/press-release.
- 38.
严重流感治疗的进展:2009年大流行的教训和治疗的新前景。中华流行病学杂志,2014;27(6):560-5。
- 39.
DeAngelis CD, Drazen JM, Frizelle FA, Haug C, Hoey J, Horton R,等。临床试验注册:来自国际医学期刊编辑委员会的声明。《美国医学协会杂志》上。2004年,292(11):1363 - 4。
致谢
不适用。
资金
这项工作得到了威康基金会的支持[授予编号107834/Z/15/Z和106491/Z/14/Z]。AR由开放慈善基金会支持。
作者信息
从属关系
贡献
AR和PH构思和设计了这项研究,并可以完全访问研究中的所有数据。AR和GM在ph的输入下起草稿件。AR进行统计分析,对数据的完整性和数据分析的准确性负责,并作为保证人。所有作者均已阅读并批准最终稿。
相应的作者
道德声明
伦理批准并同意参与
这项工作不需要伦理批准。
发表同意书
不适用。
相互竞争的利益
我们宣布有一个相互竞争的利益。我们在这份手稿中提出了大规模协调大流行试验的理由,高级作者(Peter Horby)正在领导COVID-19治疗随机评估(RECOVERY)试验,这是目前在英国登记的最大的COVID-19治疗临床试验。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1:附录1。
核对表总结符合MOOSE和PRISMA指南。附录2。搜索策略的细节。附录3。临床注册表检索策略和数据提取的细节。附录4。纳入系统综述的研究。附录5。说明文献中描述的治疗课程数量的国家一级数据,以及首次参加前瞻性研究的日期(如相关)。附录6。用于描述A(H1N1)pdm09患者临床试验注册记录筛选、资格和纳入的棱镜流程图。附录7。纳入A(H1N1)pdm09患者的研究纳入指标,当分析仅限于“严重”和住院患者时。附件8。描述在大流行期间开放的旨在招募流感患者的研究的临床试验注册记录的筛查、资格和纳入的棱镜流程图。
权利和权限
188滚球软件本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
Rojek, a.m., Martin, G.E.和Horby, P.W.大流行期间同情性药物(错误)使用:2009年COVID-19的教训。BMC医学18日,265(2020)。https://doi.org/10.1186/s12916-020-01732-5
收到了:
接受:
发表:
关键字
- 流感大流行
- 临床试验
- 流感
- 甲型H1N1流感
- 系统综述