摘要
背景
慢性阻塞性肺病(COPD)中的一个典型特征是氧化剂/抗氧化剂平衡的干扰。谷氨酸(GRX)是硫醇二硫化物氧化还原酶,其具有与谷胱甘肽密切相关的抗氧化能力和催化功能,人肺的主要小分子量抗氧化剂。然而,GRX在吸烟相关疾病中的作用尚不清楚。
方法
用肺试样(n = 45和n = 32)进行免疫组织化学和Western印迹分析,并诱导痰(n = 50)的健康非吸烟者和吸烟者,而没有COPD的不同阶段。
结果
GRX1主要以肺泡巨噬细胞表达。Glx1阳性巨噬细胞的百分比在黄金阶段IV COPD中显着低于健康吸烟者(P = 0.021),并且在I-II期(P = 0.045)和阶段IV COPD中,总肺匀浆的GRX1水平降低(P = 0.045)(P= 0.022)。GRX1阳性巨噬细胞的百分比与肺功能参数相关(FEV1,R = 0.45,P = 0.008; FEV1%,r = 0.46,P = 0.007,FEV / FVC%,R = 0.55,P = 0.001)。还可以在痰上清液中检测到GRX1,与非吸烟者(P = 0.013)和吸烟者(P = 0.051),对COPD的急性加剧的上清液中的水平增加。
结论
本横断面研究显示,Grx1主要表达于肺泡巨噬细胞,COPD患者Grx1表达水平下降。此外,研究结果还表明,Grx1存在于包括痰上清在内的细胞外液中。综上所述,本研究提示Grx1是一种潜在的氧化还原调节蛋白,调节人肺中谷胱甘肽化蛋白和谷胱甘肽的细胞内外稳态。
背景
慢性阻塞性肺疾病(COPD)的发病机制可能与活性氧代谢物密切相关。香烟烟雾不仅含有高水平的氧化剂,而且还会导致中性粒细胞和巨噬细胞在肺部积聚并激活它们[1- - - - - -3.].许多研究在卷烟烟雾暴露细胞和慢性卷烟吸烟者中调查了抗氧化防御机制。这些研究发现,谷胱甘肽(GSH),含有高浓度的上皮衬里液(ELF)中存在的三肽在保护人类气道免受外源性和内源性氧化剂和香烟烟雾中起重要作用[1,4,5].然而,在人肺中,只有部分酶系统参与GSH的调控,从而可能也参与了COPD的发病机制。
谷胱甘肽在慢性吸烟者的ELF中浓度增加[6]急性和慢性暴露于卷烟烟雾的实验动物导致细胞内GSH浓度的枯竭[7].GSH通过多种机制从细胞输送,而血浆膜不可渗透到GSH,以防止其运输回电池。细胞内GSH的补充是通过减少氧化谷胱甘肽,即谷胱甘肽(GSSG),从蛋白质和De Novo GSH合成中释放GSH [8].已知调节GSH代谢的酶机制包括GSH合成中的速率限制酶,谷氨酸半胱氨酸连接酶(GCl,也称为γ-谷氨酸琥珀酸盐合成酶,γ-GCS),谷胱甘肽过氧化物酶(GPX),谷胱甘肽还原酶(GR),γ-戊二酰转肽酶(γ-GT)和谷胱甘肽-S-转移酶(GST)。在慢性吸烟者的支气管上皮中GCL,GPX和一些GST的MRNA表达似乎增加,但在香烟吸烟者或COPD进展期间降低了这些酶中的几种免疫反应或活动的免疫反应或活性[9].戊二酮(GRX)代表氧化还原调制蛋白家族,对GSH调节和稳态潜在影响,但直到现在他们尚未在吸烟相关的肺病中进行评估。
经典的glutaredoxin是小型硫醇二硫氧化还原酶,具有保守的活性位点序列CXXC-和谷胱甘肽结合位点。它们属于硫氧还蛋白褶皱超家族[10,11],硫昔林是人肺中已知的氧化还原调节酶[12,13].人类有两个Grxs,细胞质Grx1和线粒体Grx2 [14,15].它们通过利用NADPH和谷胱甘肽还原酶存在下的GSH的还原功率,催化二硫化物减少,优选GSH-混合二硫化物作为基质的底物[16].Grxs可以被假设参与在吸烟者和COPD中氧化应激期间和之后,将含硫醇蛋白的gsh混合二硫化物还原到其活性形式。
在本研究中,我们研究了Grxs在非吸烟者和吸烟者肺标本中以及不同阶段的表达[17研究主要集中在巨噬细胞上,因为Grx1主要在这些细胞中表达[18由于慢性阻塞性肺病的一个典型特征是肺内巨噬细胞的聚集。考虑到Grx1可能也存在于细胞外空间[19,20.],也检测了诱导痰标本、非吸烟者、吸烟者和慢性阻塞性肺病患者的细胞和上清中Grx1的水平。
材料和方法
组织
组织材料包括来自肺手术的未受累的周围肺组织(错瘤、类癌肿瘤、肺癌),代表来自非吸烟者、非COPD吸烟者和I-II期COPD的健康肺(Oulu大学医院病学系)。来自非常严重的COPD或肺气肿患者的α-1抗胰蛋白酶缺乏症(IV期)的标本从肺移植中提取(赫尔辛基大学医院病学系)。根据Dail和Hammar的描述,免疫组化组织材料被保存[21].更详细的描述可从随附的数据补充中找到[见附加文件1].用于Western分析的组织材料立即在液氮中冷冻并保存在-80°C中。免疫组化(n = 44)和免疫印迹(n = 32)中包含单独受试者的标本的患者特征见表1和表2,分别。
痰的诱导及处理
根据欧洲呼吸学会工作小组的指导方针,采用4.5%高渗盐水进行痰诱导的标准程序,每隔5分钟给予最多20分钟[188bet官网地址22].详情见资料补充[见附加文件1].痰标本立即离心、冷冻保存于-80℃。入选诱导痰标本研究的患者(n = 50)的特征见表3..受试者包括非吸烟者,健康吸烟者和轻度稳定的COPD(第0阶段),并且为了比较,由于COPD加剧(COPD EXA)导致更严重的疾病和住院病例。患者没有患有其他疾病或肺炎。COPD Exacterbation患者的所有样品在入院48小时内收集。用圣乔治呼吸问卷评估症状。
Grx1在肺中的免疫组化和评估
多克隆山羊抗人Grx1抗体石蜡切片的制备和染色方案[19]已被较早地描述[18,23].更详细的描述在数据补充中提供[见附加文件1].两名研究人员通过将染色强度从阴性(0)分级到强(3),对10个显微镜场的免疫组化染色强度进行半定量评估。此外,通过Zeiss AxioHOME Morphometry程序(Zeiss, Jena, Germany)计算Grx1阳性和阴性巨噬细胞的绝对数量,对至少10个显微镜场进行评估。
免疫印迹分析
冷冻组织样品在冰冷的磷酸盐缓冲盐水中快速均化。从组织匀浆和痰样品中进行蛋白质印迹分析如前所述进行[18,23]与针对Grx1的抗体[19]及Grx2 [15].可以在数据补充中找到对方法的更详细描述[参见附加文件1].β-肌动蛋白没有被用作组织匀浆的负荷控制,因为它显示了较高的个体可变性,如前所述[24,25].相反,通过染色刺激膜(Sigma Aldrich,St.Louis,Mo,Mo,Mo,Mo,Mo)通过染色纸质膜来仔细地测量蛋白质浓度。
道德考虑因素
奥卢大学医院和赫尔辛基大学医院的伦理委员会接受了研究议定书,它符合1975年赫尔辛基宣言的伦理标准。这项研究是由赫尔辛基大学医院注册的。26].
统计数据
使用社会研究统计软件包(SPSS) 11.5版(芝加哥,IL,美国)进行统计分析。对照和选定疾病之间的差异采用方差分析进行比较,事后比较采用双尾分析t测试。使用Fisher的确切测试进行比较分类数据。P-值小于0.05被认为有统计学意义。肺功能相关性采用Spearman秩相关检验。使用Cohen's kappa统计数据比较两种免疫组化样本的独立评估[27].
结果
组织标本中肺泡巨噬细胞的数量
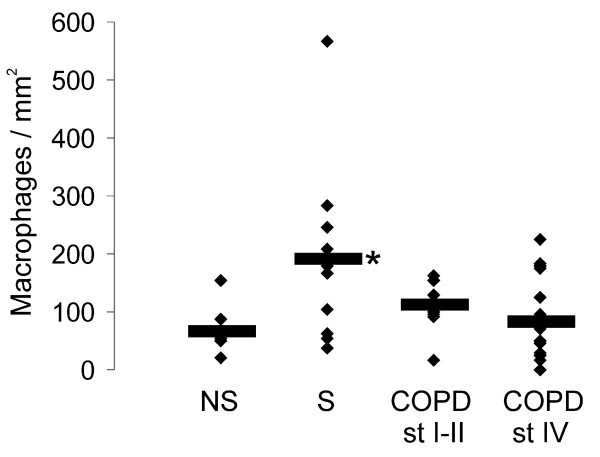
由于Grx1已知在肺泡巨噬细胞中高表达[18],进行了详细的分析,分析了所有受试者(即非吸烟者、吸烟者、I-II期COPD和IV期COPD)每平方毫米组织标本的肺泡巨噬细胞数量。这些分析显示,与非吸烟者相比,吸烟者的肺组织中巨噬细胞的数量尤其增加(p = 0.020)1).
在健康人肺和慢性阻塞性肺病不同阶段的Grx1
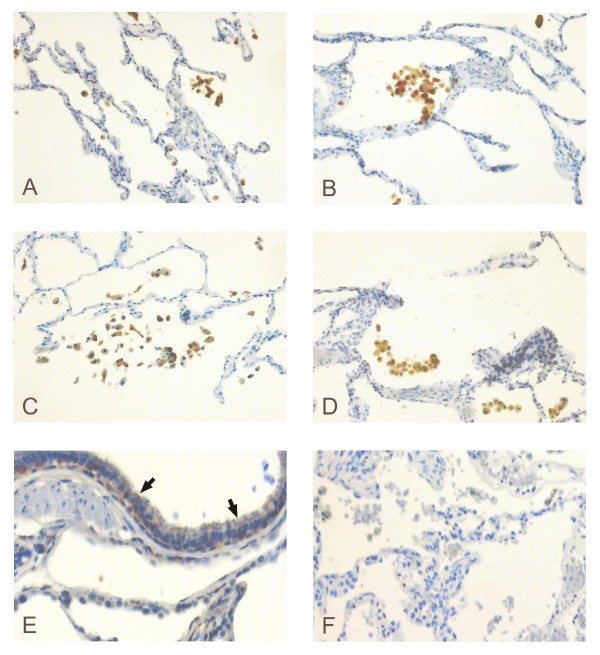
健康肺和COPD免疫组化研究显示,Grx1主要表达于肺泡巨噬细胞(图2模拟).在某些病例中,偶尔也可在支气管上皮中检测到微弱阳性(图)2 e).阴性同型对照未见免疫反应(图2 f).两组患者免疫组化染色强度的半定量分析无统计学差异(p = 0.097)。根据Cohen’s kappa统计(κ = 0.552),两名独立研究者的评估结果显示,双方的一致性适中。
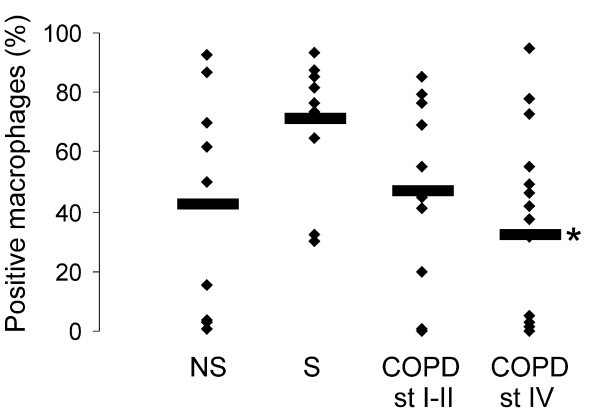
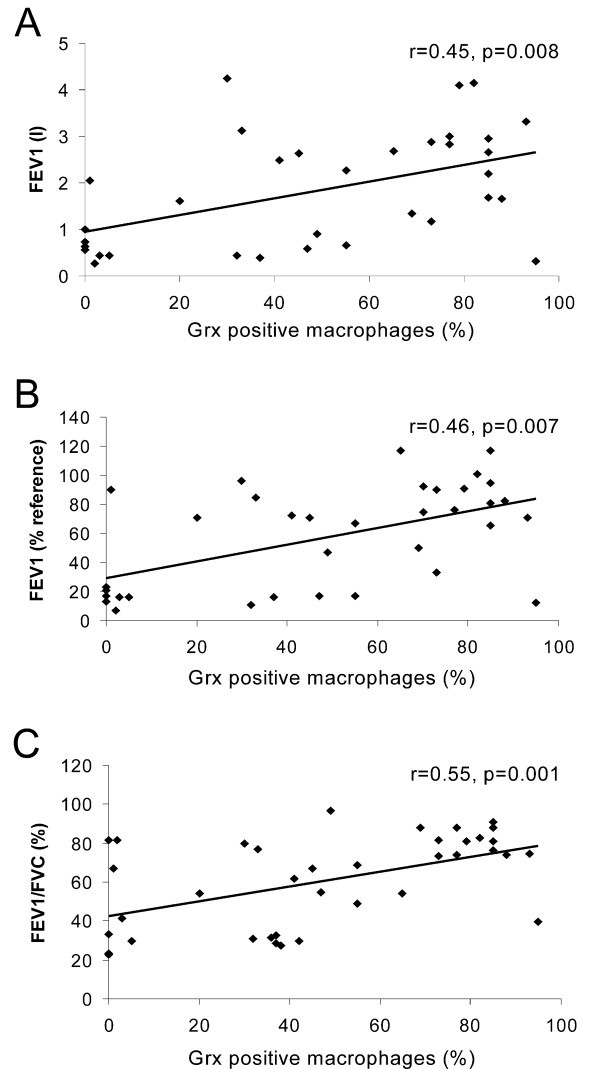
当将细胞分为Grx1阳性和阴性两组时,Grx1阳性巨噬细胞占总巨噬细胞的百分比在疾病进展过程中呈下降趋势,在COPD期最低。与吸烟者相比,这种降低具有统计学意义(p = 0.021)(图3.).pack年份与阳性巨噬细胞百分率无相关性。有趣的是,肺组织标本(包括所有吸烟者和COPD不同阶段的肺标本)中Grx1阳性巨噬细胞与肺功能参数之间存在显著相关性(FEV1, r = 0.45, p = 0.008;FEV1%, r = 0.46, p = 0.007, FEV/FVC%, r = 0.55, p = 0.001)如图所示4(面板A-C)。
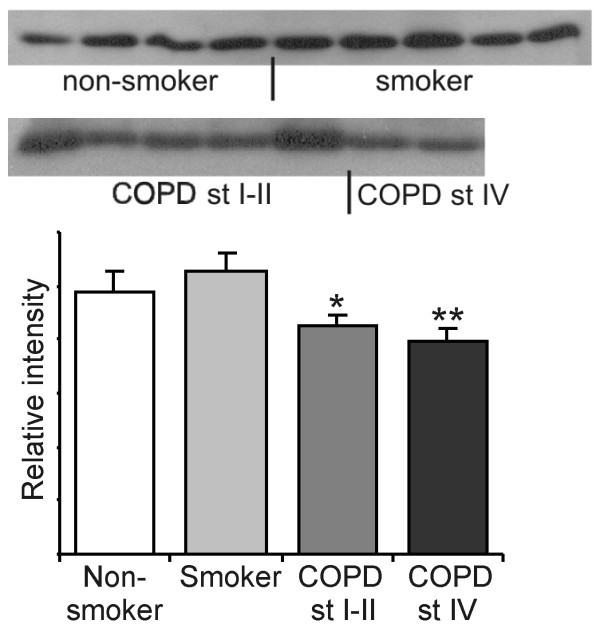
与此结果一致的是,肺匀浆的Western blot分析(n = 32)显示,与健康吸烟者相比,COPD患者中Grx1水平降低(I-II期p = 0.045, IV期p = 0.022)5).在这些受试者中,吸烟者和COPD之间的包装年没有统计学意义(p = 0.818)。
与细胞质Grx1不同,线粒体Grx2无法通过免疫组化检测到。在Western blot分析中,Grx2几乎检测不到,仅在吸烟者中发现(数据未显示)。
诱导痰上清中含有Grx1
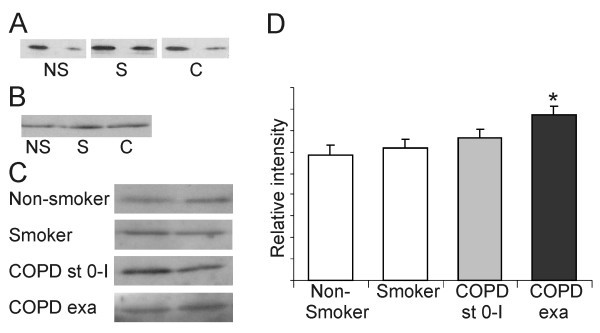
在非吸烟者、吸烟者和慢性阻塞性肺病患者的血浆样本中,可以通过Western blot分析检测到Grx1,但个体差异较大(见图)6A)证实了此前在血浆中发现的Grx1 [19,20.].由于Grx1在液泡中的细胞内定位[18,28]提示Grx1可能从细胞外输出,进一步研究使用非吸烟者(n = 15)、吸烟者(n = 11)和COPD患者(n = 24)的诱导痰标本。正如预期的那样,通过免疫细胞化学和Western blot分析,在诱导的痰液中发现了显著的Grx1免疫反应性(图6B.).但是,还可以从诱导的健康对照,吸烟者,稳定COPD和COPD诱导痰上清液中检测到GRX1(图6C).与非吸烟者(P = 0.013)相比,从急性加剧患者获得的上清液中的GRX1蛋白水平增加(P = 0.013),并且在某种程度上与吸烟者相比(p = 0.051)(图6D.).细胞外Grx1的一种解释可能是质膜的破坏,因此对标本进行了β-肌动蛋白和锰超氧化物歧化酶(一种抗氧化酶,以前发现在人肺泡巨噬细胞中表达)的分析[29];两种抗原的免疫反应均为阴性。
讨论
本研究表明GRX1是一种潜在的氧化还原调制蛋白,其不仅在健康的肺部,而且在香烟吸烟者和COPD患者中调节谷胱甘肽化蛋白和GSH的稳态。此外,细胞外空间中GRX1的存在可能在呼吸道中补充谷胱甘肽的补充,特别是在氧化胁迫增加的急性加重期间。
最近的一项微阵列研究发现,与不吸烟者相比,健康吸烟者的支气管上皮中Grx1 mRNA水平没有变化[30.].在另一项培养的支气管上皮细胞的研究中,发现GRX在暴露于香烟烟雾的前10小时内升高10倍[31].然而,迄今为止,还没有关于吸烟者或慢性阻塞性肺疾病患者Grxs蛋白水平或调节的人类研究。众所周知,吸烟可增加上皮内壁液中谷胱甘肽的水平,导致细胞内游离谷胱甘肽的耗竭[6,7].似乎在初始谷胱甘肽消耗后,细胞内谷胱甘肽水平升高的原因尚不清楚,其中一种机制是谷胱甘肽合成增加[4,7,9].氧化应激还会引起蛋白-谷胱甘肽混合二硫化物的积累[32].由于蛋白质中的半胱氨酸残基的细胞内浓度高于自由GSH的浓度,因此蛋白质-GSH混合二硫化物的形成具有潜力作为GSH在活细胞中的显着存放物。此外,已经表明,在氧化环境中,GSH的主要部分实际上存在于与蛋白质的混合二硫化[33].通过保护酶免受可能导致酶失活的不可逆氧化来形成调节和抗氧化函数的这些混合二硫化物。一旦氧化应激被缓解,通过甘露甘露肠道,蛋白-GSH混合二硫化物被有效地减少了自由谷胱甘肽。
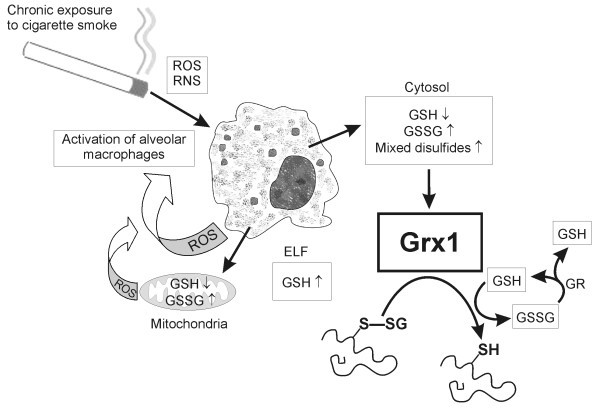
本研究表明,GRX1可能参与谷胱甘肽化蛋白水平和GSH稳态在人肺中的调节(图7).免疫组化研究显示,Grx1主要表达于非吸烟者和吸烟者以及COPD不同阶段的肺泡巨噬细胞中,Grx1水平随病情严重程度而降低。这些结论得到了Western blot分析的支持。并不是所有切片中的巨噬细胞都Grx1阳性,可能是由于各种巨噬细胞群体的存在和这些细胞的年龄。总的来说,这些变化明显与肺中巨噬细胞的数量以及Grx在巨噬细胞中表达水平的差异有关。
目前的研究证实,如前所述,Grx1可以从血浆中检测到[19,20.,更重要的是证明了Grx1也可以从痰液中检测到,无论是从细胞还是上清中。后者提示Grx1可能从肺泡巨噬细胞出口到细胞外间隙(即痰液)。COPD急性加重组的痰上清中Grx1水平明显高于对照组。这表明,在COPD氧化应激过程中,细胞外Grx1试图减少gsh混合二硫化物,以恢复活性蛋白并增加游离谷胱甘肽的浓度。
从肺或痰标本中评估功能性Grx活性是困难的,因为现有的分析方法可能对Grx单独不具有特异性。在我们最近的论文中[34我们描述了一种测量脱氮硫化活性的新方法在体外但该方法也不适用于测定组织或细胞匀浆中glutaredoxin的活性。在这项特别的研究中,其他硫氧还蛋白家族成员也显示出脱谷胱甘肽化活性,进一步表明目前的方法对Grx活性的评估不是特异性的体内.支持本研究的发现,我们最近的观察表明大肠杆菌与人GRX1类似的GRX1在模仿氧化应激的条件下显着降低[35].
无法使用此处使用的方法可靠地检测GRX2表达。然而,这并不排除GRX2在肺的抗氧化防御中的重要性。GRX2是线粒体蛋白[14,15],因此可能在调控线粒体氧化还原状态和凋亡事件中发挥作用。Grx2显然需要进一步研究,以便更好地了解巯基氧化还原酶在人肺和COPD进展中的抗氧化防御机制中的作用。
GRX1的调节理解得很差,但我们实验室和其他结果的最近结果表明氧化剂的轻微或非显着的GLX1诱导[35,36]以及通过转化生长因子-β (TGF-β)显著下调Grx1 [18].然而,Grx1只是调节人肺中谷胱甘肽稳态的一种酶。谷胱甘肽合成中的限速酶是GCL这种酶已经被证明是由氧化应激,香烟烟雾和慢性阻塞性肺病短暂诱导的[1,8,30.,37],但TGF-β降低在体外[38以及COPD进展期间体内[9,39].这里发现的严重COPD /肺气肿的GRX1的降低与COPD中其他GSH相关酶的同时下调相关联,从而进一步增加了肺中的氧化剂负荷。这些调节途径清楚地需要更详细地研究。
结论
综上所述,Grx1是与谷胱甘肽和谷胱甘肽混合二硫化物还原密切相关的蛋白。Grx1主要定位于肺泡巨噬细胞,随着COPD的严重程度而降低。Grx1也可从痰上清中检测到,COPD急性加重组中Grx1水平高于健康对照组。Grx1水平的增加可能是试图恢复谷胱甘肽化蛋白的功能活性,并增加细胞外游离谷胱甘肽的水平。总的来说,这些发现表明Grx1参与了细胞内和细胞外谷胱甘肽稳态的调节,并与严重COPD中谷胱甘肽依赖性抗氧化防御的降低有关。
参考文献
- 1.
Rahman I, MacNee W:肺谷胱甘肽和氧化应激:对吸烟引起的气道疾病的影响。是杂志1999年,277:L1067-88。
- 2.
Rahman I, MacNee W:肺炎中谷胱甘肽的氧化应激和调节。欧元和J2000年,16:534 - 554。
- 3.
巴恩斯PJ:肺泡巨噬细胞作为COPD的协调者。慢性阻塞性肺疾病杂志2004年,1:59 - 70。
- 4.
Langen Rc,Korn Sh,Wouters EF:ROS在COPD局部和全身性发病机制中的作用。自由基生物医学2003年,35:226-235。
- 5.
Contin Am,North Sl,Hubbard Rc,Crystal RG:正常肺泡上皮内壁液中谷胱甘肽含量高。J Appl Physiol.1987年,63:152 - 157。
- 6。
Morrison D,Rahman I,Lannan S,Macnee W:吸烟者空气空间中的上皮渗透性,炎症和氧化胁迫。呼吸危重症护理医学杂志1999年,159:473 - 479。
- 7。
Rahman I, Li XY, Donaldson K, Harrison DJ, MacNee W:氧化应激下肺泡上皮细胞和肺内谷胱甘肽稳态的研究。是杂志1995年,269:l285 - 92。
- 8。
迪金森,福尔曼细胞谷胱甘肽和硫醇代谢。生物化学杂志2002年,64:1019 - 1026。
- 9。
Kinnula六世:专注于抗氧化酶及吸烟型呼吸道疾病的抗氧化策略。胸部2005年,60:693 - 700。
- 10。
Holmgren答:硫氧还蛋白和谷氧还蛋白系统的抗氧化功能。Antioxid氧化还原信号2000年,2(4):811-820。
- 11.
马丁·杰:Thioredoxin - 折叠出所有原因。结构1995年,3:245 - 250。
- 12.
Kahlos K, Soini Y, Säily M, Koistinen P, Kakko S, Pääkkö P, Holmgren A, Kinnula VL:人体恶性胸腔间皮瘤中硫昔宁和硫氧化昔林还原酶的上调。Int J癌症2001年,95:198 - 204。
- 13.
Tiitto L, Kaarteenaho-Wiik R, Sormunen R, Holmgren A, Pääkkö P, Soini Y, Kinnula VL:硫氧还蛋白系统在间质性肺病中的表达。J Pathol.2003年,201:363 - 370。
- 14.
Gladyshev VN, Liu A, Novoselov SV, Krysan K, Sun QA, Kryukov VM, Kryukov GV, Lou MF:新哺乳动物谷氨酸(硫醇转移酶),GRX2的鉴定与表征。J临床生物化学2001年,276:30374 - 30380。
- 15.
Lundberg M,Johansson C,Chandra J,Enoksson M,Jacobsson G,Ljung J,Johansson M,Holmgren A:一种新的人戊二氧还蛋白(Grx2)的克隆和表达。J临床生物化学2001年,276:26269 - 26275。
- 16。
Holmgren答:依赖谷胱甘肽的脱氧核糖核酸合成。大肠杆菌glutaredoxin酶促机制的表征。J临床生物化学1979年,254:3672 - 3678。
- 17。
Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS:诊断、管理和预防慢性阻塞性肺病的全球战略。NHLBI/世卫组织全球慢性阻塞性肺病倡议讲习班摘要。呼吸危重症护理医学杂志2001年,163:1256-1276。
- 18。
Peltoniemi M,Kaarteenho-Wiik R,SäilyM,Sormunen R,Pääkköp,霍尔格伦A,Soini Y,Kinnula VL:戊二胺毒素的表达是人肺的高度细胞,通过体外转化生长因子-β并在体内间质肺病中降低。哼哼2004年,35:1000 - 1007。
- 19。
Nakamura H,Vaage J,Valen G,Padilla Ca,Bjornstedt M,Holmgren A:健康志愿者和心内直视手术期间血浆glutaredoxin和thioredoxin的测量自由基生物医学1998年,24:1176 - 1186。
- 20。
Lundberg M, Fernandes AP, Kumar S, Holmgren A:通过敏感的ELISA系统检测的人类戊二糖蛋白1和2的细胞和血浆水平。生物化学与生物物理2004年,319:801 - 809。
- 21。
dardh, Hammar SP:肺病理学.斯普林格出版社,纽约;1994:1-17。
- 22。
Djukanovic R, Sterk PJ, Fahy JV, Hargreave FE:痰液诱导和加工的标准化方法。EUR RESPIR J SCHIC2002年,37:1s-2s。
- 23。
Kinnula VL,Lehtonen S,Kaarteenho-Wiik R,Lakari E,Pääkköp,康SW,Rhee SG,Soini Y:细胞特异性毒素在人肺和肺结结中的表达。胸部2002年,57:157-164。
- 24.
耀眼EM, Divjak M, Bailey MJ, Walters EH:β-肌动蛋白和GAPDH家务在哮喘气通中的总基因表达是可变的,不适合归一化mRNA水平。胸部2002年,57:765 - 770。
- 25.
Ishii T, Wallace AM, Zhang X, Gosselink J, Abboud RT, English JC, Paré PD, Sandford AJ:COPD患者肺泡巨噬细胞家务基因的稳定性。欧元和J2006年,27日:300-306。
- 26.
临床试验,赫尔辛基和Uusimaa医院区[http://www.hus.fi/clinicaltrials]
- 27.
Stenkvist B,Bengtsson E,Eriksson O,Jarkrans T,Nordin B,Westman-Naeser S:乳腺癌分类组织病理学系统:再现性和临床意义。中国中草药1983年,36:392-398。
- 28。
Ivarsson R, Quintens R, Dejonghe S, Tsukamoto K, In't Veld P, Renström E, Schuit FC:外毒性症的氧化还原控制:NADPH,Thioredoxin和戊糖胺毒素的调节作用。糖尿病2005年,54:2132 - 2142。
- 29。
Lakari E, Pääkkö P, Kinnula VL:锰超氧化物歧化酶在肺结节病肉芽肿和外源性变异性肺泡炎中高表达,而CuZn超氧化物歧化酶不表达。呼吸危重症护理医学杂志1998年,158:589 - 596。
- 30.
哈克特NR, Heguy A, Harvey BG, O'Connor TP, Luettich K, Flieder DB, Kaplan R, Crystal RG:吸烟者气道上皮抗氧化相关基因表达的变异性。Am J Respir Cell Mol Biol2003年,29:331-343。
- 31。
Yoneda K, Chang MM, Chmiel K, Chen Y, Wu R:高密度DNA芯片在研究烟雾和过氧化氢诱导的人支气管上皮细胞损伤和修复中的应用。J Am Soc Nephrol2003年,14:s284页- 89。
- 32。
Cotgreave IA, Gerdes RG:最近谷胱甘肽生物化学趋势 - 谷胱甘肽 - 蛋白质相互作用:氧化应激与细胞增殖之间的分子链接?生物化学与生物物理1998年,242:1 - 9。
- 33。
Bass R,Ruddock LW,Klappa P,Freedman RB:成分的内质网的谷胱甘肽的主要部分作为与蛋白质的混合二硫化物存在。J临床生物化学2004年,279:5257-5262。
- 34。
Peltoniemi M, Karala A, Jurvansuu J, Kinnula VL, Ruddock LW:对脱谷胱甘肽化反应的认识:在谷胱甘肽和蛋白二硫化物异构酶催化的反应中,不同的中间产物是由谷胱甘肽中的γ -连接定义的。J临床生物化学在出版社。2006年9月5日
- 35。
Okuda M, Inoue N, Azumi H, Seno T, Sumi Y, Hirata K, Kawashima S, Hayashi Y, Itoh H, Yodoi J,横山M:glutaredoxin在人冠状动脉中的表达:它在抗氧化保护抗动脉粥样硬化中的潜在作用。动脉硬化血栓血管生物学2001年,21:1483 - 1487。
- 36.
Prieto-Alamo MJ,朱拉多J,Gallardo-Maduenoo R,Monje Casas F,Holmgren A,Pueyo C:glutaredoxin和thioredoxin途径及其相关酶在氧化应激反应中的转录调控。J临床生物化学2000年,275:13398 - 13405。
- 37.
Rahman I,Van Schadewijk AA,Hiemstra PS,Stolk J,Van Krieken JH,Macnee W,De Boer Wi:-谷氨酰基半胱氨酸合成酶信使RNA在吸烟者和慢性阻塞性肺疾病患者肺中的表达定位自由基生物医学2000年,28:920 - 925。
- 38.
Arsalane K, Dubois CM, Muanza T, Begin R, Boudreau F, Asselin C, Cantin AM:转化生长因子-β1是肺上皮细胞系A549中的谷胱甘肽合成的有效抑制剂:对GSH速率限制酶γ-谷氨酸氨基 - 谷氨酸合成酶的转录作用。Am J Respir Cell Mol Biol1997年,17:599 - 607。
- 39.
Behr J, Degenkolb B, Krombach F, Vogelmeier C纤维肺炎细胞内谷胱甘肽和支气管肺泡细胞:N-乙酰半胱氨酸的作用。欧元和J2002年,19:906-911。
确认
作者希望感谢Arne Holmgren (Karolinska institutet, Stockholm, Sweden)为Grx1和Grx2提供了抗体。作者感谢Tiina Marjomaa、Raija Sirviö和Manu Tuovinen的出色技术援助。这项工作得到了芬兰科学院、芬兰抗结核病协会基金会、Magnus Ehrnrooth基金会、芬兰文化基金会、Ahokas基金会和Sigrid Juselius基金会的资助。
作者信息
隶属关系
通讯作者
额外的信息
相互竞争的利益
两位作者宣称他们没有相互竞争的利益。这项研究没有得到烟草业的支持。
作者的贡献
MJP进行了西方印迹研究,参与分析免疫组化数据,表现了部分统计分析并起草了手稿。PHR参与患者材料的选择和收集,分析免疫组织化学结果并进行了部分统计分析。THH参与了研究和选择患者材料的设计,并进行了部分统计分析。YMS和KMS参与了患者材料的选择并分析免疫组织化学结果。LWR参加了研究协调并帮助起草了稿件。VLK构思了这项研究,并参与了其设计和协调,并帮助起草了稿件。所有作者都已经阅读并赞成最终的手稿。
电子补充材料
12931_2006_524_moesm1_esm.doc.
附加文件1:材料和方法。附加文档包括研究中使用的方法的更详细描述。(Doc 32 KB)
权利和权限
188滚球软件本文在“生物资源”中央有限公司的许可下公布了这是一个开放式访问条款,分配根据创意公约归因许可证的条款(188滚球软件https://creativecommons.org/licenses/by/2.0)提供任何介质中的不受限制使用,分发和再现,所以提供了正确的工作。
关于这篇文章
引用这篇文章
Peltoniemi,M.J.,Rytilä,P.H.,Harju,T.H.等等。戊二醛还蛋白在吸烟者和慢性阻塞性肺疾病肺、痰中的调节作用。respir res.7,133(2006)。https://doi.org/10.1186/1465-9921-7-133
已收到:
接受:
发表:
关键词
- 慢性阻塞性肺疾病
- 慢性阻塞性肺病患者
- 肺泡巨噬细胞
- 严重慢性阻塞性肺疾病
- 慢性阻塞性肺病加剧