摘要
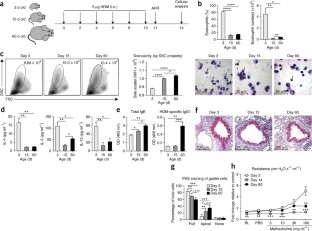
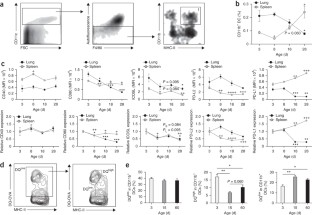
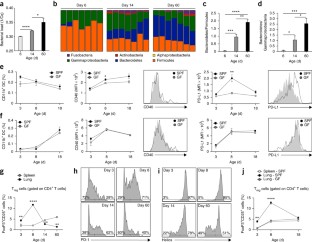
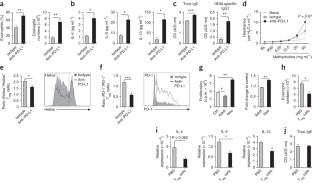
流行病学数据表明,在生命早期的一个关键时期,环境因素可以使一个人走上呼吸系统健康或疾病的轨道1那2那3.那4.那5.那6.那7.那8..新生儿的免疫系统在这一时期成熟9.,尽管人们对导致其成熟的信号知之甚少。在这里,我们报道了肺微生物群的形成是这一过程中的一个关键参数。出生后不久,新生小鼠容易出现气道嗜酸性粒细胞增多,释放2型辅助性T细胞因子,暴露于尘螨过敏原后表现出气道高反应性,尽管它们的肺部含有大量的天然CD4+Foxp3+CD25+赫利俄斯+调节性T (Treg)细胞。在出生后的前2周,肺部的细菌载荷增加,并且细菌植物的代表从丙曲曲线菌的主要偏移和对抗杆菌的常规。微生物群的变化与气孔良好响应性和Helios的出现有关。−T.reg需要与程序性死亡配体1 (PD-L1)相互作用才能发育的细胞子集。没有微生物定植10或者在产后的前2周阻断PD-L1,一直持续到成年对过敏原的过度反应。Treg暴露于空气变应原前的成年小鼠至新生儿的细胞可改善疾病因此,气道微生物群的形成在生命早期就诱导了调节细胞,当调节失调时,可导致成年后对过敏性气道炎症的持续易感性。
访问选项
订阅杂志
获得完整的日志访问1年
59.00美元
每个问题只需4.92美元
所有价格均为净价。
VAT将在结账后稍后添加。
税收计算将在结账时完成。
租赁或购买物品
在ReadCube上获取时间限制或全文访问。
从8.99美元
所有价格均为净价。
参考文献
- 1
在农场生活:对哮喘诱导和临床过程的影响。Immunol。过敏中国。北。28, 631-647, ix-x(2008)。
- 2
Von Mutius,E.&Vercelli,D.农场生活:对儿童哮喘和过敏的影响。启Immunol Nat。10,861-868(2010年)。
- 3.
Burke, H.等。产前和被动烟雾暴露与哮喘和哮鸣的发生率:系统回顾和荟萃分析儿科129,735-744(2012)。
- 4.
李,S.L.等等。胎儿被动吸烟的胎儿接触与儿童哮喘,过敏性鼻炎和湿疹有关。ScientificWorldJournal2012年542983(2012)。
- 5.
Stensballe,L.G.,Simonsen,J.,Jensen,S.M.,Bonnelykke,K。和Bisgaard,H.在妊娠期间使用抗生素会增加童年早期哮喘的风险。J. Pediastr。162, 832 - 838。e3(2013)。
- 6.
Gern,J.E.,Rosenthal,L.A.,Sorkness,R.L.&Lemanske,R.F.JR.病毒呼吸道感染对肺发育和儿童哮喘的影响。j .过敏中国。Immunol。115, 668-674,测验675(2005)。
- 7.
杰克逊,D.J.鼻病毒感染在早期儿童哮喘发展中的作用。咕咕叫。当今。过敏中国。Immunol。10, 133 - 138(2010)。
- 8.
呼吸道合胞病毒感染与哮喘之间的因果关系。专家Rev.反感染。它。9., 731 - 745(2011)。
- 9.
HOLT,P.G.&jones,c.a.怀孕和早年期间免疫系统的发展。过敏55, 688 - 697(2000)。
- 10
Herbst,T.等。在没有微生物定植的情况下,过敏气道炎症的失调。点。j .和。暴击。保健医疗。184,198-205(2011)。
- 11
微生物群和免疫系统之间的相互作用。科学336, 1268 - 1273(2012)。
- 12
肠道共生细菌与免疫系统的相互作用。启Immunol Nat。4., 478 - 485(2004)。
- 13
Hilty,M.等。在哮喘呼吸道中的微生物群落无序。《公共科学图书馆•综合》5.,e8578(2010)。
- 14
黄玉杰等。非最佳控制哮喘患者的气道微生物群和支气管高反应性。J.过敏临床免疫杂志。127,372-381.e1-E3(2011)。
- 15
Pragman,A.A.,Kim,H.B.,Reilly,C.S.,Wendt,C.&Isaacson,R.E.中度和严重慢性阻塞性肺病的肺部微生物组。《公共科学图书馆•综合》7.e47305(2012)。
- 16
Erb-Downward,J.R.等。“健康”吸烟者和COPD中的肺部微生物分析。《公共科学图书馆•综合》6.,E16384(2011)。
- 17
呼吸道微生物群与疾病。胸部144, 632 - 637(2013)。
- 18
Twigg,H.L.III等。使用支气管肺泡灌洗评估呼吸微生物组:噪声中的信号。和出版的《柳叶刀》杂志上。Med。1, 354 - 356(2013)。
- 19
Trompette, A.等。膳食纤维的肠道微生物代谢影响变应性气道疾病和造血。NAT。Med。20., 159 - 166(2014)。
- 20.
弗朗西斯科,L.M.等。PD-L1调控诱导调节性T细胞的发育、维持和功能。J. Exp。Med。206,3015-3029(2009)。
- 21
王磊等。程序性死亡1配体信号调节适应性Foxp3的生成+CD4+调节性T细胞。Proc。国家的。学会科学。美国105,9331-9336(2008)。
- 22
Geuking, M.B.等。肠道细菌定植诱导互惠调节性T细胞反应。免疫34,794-806(2011)。
- 23
圆形,J.L.&Mazmanian,S.K.诱导狐p3.+调节t细胞的发展由肠道微生物群的共生细菌。Proc。国家的。学会科学。美国107, 12204 - 12209(2010)。
- 24
Curotto de Lafaille, M.A.等。自适应Foxp3+调节性T细胞依赖性和非依赖性对过敏性炎症的控制。免疫29, 114 - 126(2008)。
- 25
Curotto de Lafaille, M.A. & Lafaille, J.J. Natural and adaptive foxp3+调节性T细胞:更多的相同还是分工?免疫30., 626 - 635(2009)。
- 26
Rangel-Moreno, J.等。诱导性支气管相关淋巴组织的发展依赖于IL-17。Immunol Nat。12,639-646(2011)。
- 27
T. Olszak等。生命早期接触微生物对自然杀伤T细胞功能有持久的影响。科学336, 489 - 493(2012)。
- 28
早期生命定植过程中的肠道微生物多样性决定了长期IgE水平。细胞宿主微生物14,559-570(2013)。
- 29
Nembrini等。通过多组分免疫调节机制,细菌诱导的对过敏性炎症的保护。胸部66,755-763(2011)。
- 30.
Hagner, S.等。Farm-derived革兰氏阳性细菌葡萄球菌Sciuri.W620可防止HDM和ova暴露小鼠的哮喘表型。过敏68,322-329(2013)。
- 31
基于实时荧光定量PCR技术的细菌分类门和类特异性引物的改进。j . Microbiol。方法86, 351 - 356(2011)。
确认
这项工作得到了洛桑Leenaards基金会和瑞士国家科学基金310030_146983的资助,授予B.J.M. B.J.M.是Cloetta医学研究员,通过持有这个头衔,获得了财政支持。B.J.M.和C.M.L.是欧洲科学技术合作行动BM1201的一部分,慢性肺病的发展起源。S.S.和C.M.L.由惠康信托基金087618/Z/08/Z和083586/Z/07/Z资助。C.M.L.是Wellcome基础生物医学高级研究员,并获得财政支持。我们感谢D. Pinschewer和S. Kallert的宝贵讨论和批评性反馈。
作者信息
隶属关系
贡献
B.J.M.构思了这项研究。B.J.M.和E.S.G.设计了这项研究。E.S.G, A.T.和K.Y.做了实验。S.S.和R.S.进行新生儿肺功能实验。kdm提供无菌小鼠。E.S.G, a.t., K.Y, s.s., c.m.l., L.P.N.和B.J.M.提供了批判性的分析和讨论。esg和B.J.M.写了论文。
通讯作者
道德声明
竞争利益
作者声明没有竞争的财务利益。
补充信息
补充文本及数字
补充图1-7 (pdf652kb)
权利和权限
关于这篇文章
引用这篇文章
Gollwitzer, E, Saglani, S, Trompette, A。等等。肺微生物群通过PD-L1促进新生儿对过敏原的耐受。Nat Med.20,642 - 647(2014)。https://doi.org/10.1038/nm.3568
收到:
接受:
发表:
发行日期:
进一步阅读
全肺组织是基于扩增子的小鼠肺微生物群特征的首选取样方法
微生物组(2021)
γδ T细胞、Tregs和上皮细胞与IL-33相互作用
细胞与分子免疫学(2021)
γδ T细胞在组织生理学和监测中的作用
自然评论免疫学(2021)
胚胎巨噬细胞在生命早期的功能是确定屏障表面不变的自然杀伤T细胞水平
自然免疫学(2021)
益生菌通过调节微生物-肺泡-巨噬细胞轴保护呼吸道合胞病毒感染
Acta Pharmacologica Sinica.(2021)
