早期使用抗生素对流感样疾病患儿风险(奇):双盲随机安慰剂对照试验
- 凯王1⇑,
- 马尔科姆·g·出身低微的2,3,
- 迈克尔·摩尔4,
- 阿拉斯泰尔·d·干草5,
- 沙龙吨1,
- 阿诗玛河加拉是离小岛很近1,
- 詹娜Grabey1,
- 特里西娅·卡弗1,
- 拉斐尔·佩雷拉1,
- Ly-Mee余1,
- 吉尔Mollison1,
- 保罗小3,
- 安德鲁的农民1,
- 克里斯托弗·c·巴特勒1和
- 安东尼Harnden1
- 1纳菲尔德初级保健健康科学部门,牛津大学拉德克里夫初级保健,英国牛津大学
- 2NIHR健康保护研究单位在新兴和人畜共患传染病,感染,学院兽医和生态科学、英国利物浦,利物浦大学
- 3呼吸医学部门,桤木嘿,儿童医院,英国利物浦
- 4学术单位、初级保健和人口科学,南安普顿大学就开始健康中心,英国南安普顿
- 5学术中心的初级保健、人口健康科学、布里斯托尔医学院,英国布里斯托尔
- 通讯作者:凯王(kay.wang在{}phc.ox.ac.uk)
文摘
介绍英国政府储备co-amoxiclav治疗流感大流行期间细菌并发症。这种务实试验检查是否早期co-amoxiclav使用减少reconsultation由于临床恶化“风险”孩子出现流感样疾病(伊犁)在初级或门诊。
方法“风险”从6个月到12岁儿童呈现伊犁发病后5天内被随机分配到口腔co-amoxiclav 400/57或安慰剂连续5天每天两次(根据年龄±体重剂量)。“风险”组织包括儿童呼吸系统、心脏和神经系统的条件。随机分层区域和非确定性最小化算法用于平衡年龄和当前的季节性流感疫苗接种的地位。我们的目标样本大小是650名儿童将会允许我们检测减少儿童的比例reconsulting由于临床恶化从40%提高到26%,与90%的力量和5%的双尾α错误(包括追踪损失备抵25%和1.041的通货膨胀因素)。参与者,护理人员和调查人员对治疗分配也不清楚。意向处理分析与主要结果数据包括所有随机参与者reconsultation由于在28天内临床恶化。安全分析包括所有随机参与者。试验注册:ISRCTN 70714783。EudraCT 2013-002822-21。
结果我们招募了271名孩子在2月11日,2015年和2018年4月20日。主要结果数据可供265名儿童。只有61的265名儿童(23.0%)reconsulted由于临床恶化。没有证据表明reconsultation由于观察治疗效果的临床恶化(33 133 co-amoxiclav 28(24.8%)和132例(21.2%),安慰剂;调整风险比率(RR) 1.16, 95%可信区间(CI) 0.75 - -1.80)。也没有证据表明有区别的群体比例的儿童来说,一个或多个不良事件(AEs)报告(32 co-amoxiclav 136(23.5%),安慰剂22 135 (16.3%);调整相对危险度1.45,95%可信区间0.90 - -2.34)。总共报告了66 AEs (co-amoxiclav n = 37;安慰剂,n = 29)。九个严重AEs每组报道,虽然被认为是与研究药物有关。
结论我们的试验没有发现证据表明,治疗co-amoxiclav降低风险reconsultation由于临床恶化“风险”儿童早期流感季节期间与伊犁。因此我们的研究结果不支持儿童早期co-amoxiclav使用季节性伊犁。
文摘
这个试验没有发现证据表明早期co-amoxiclav使用减少reconsultation由于临床恶化“风险”的孩子现在在流感季节流感样疾病https://bit.ly/3stZwnn
介绍
流感主要是一个温和,自限性疾病。然而,儿童呼吸系统、心脏、肝脏和神经系统的条件,以及糖尿病和免疫抑制1),和过早出生的孩子2),被认为是肺炎等并发症的风险。增长近6倍住院是在从5岁儿童14年临床风险组(3]。
英国政府储备co-amoxiclav治疗细菌性流感大流行期间的并发症。已经证明了一贯高易感性co-amoxiclav下呼吸道细菌分离与流感相关的(4]。临床实践指南建议立即抗生素治疗应考虑患者急性呼吸道感染(rti)被认为是风险较高的并发症(5]。然而,初级保健医生报告开出抗生素处方的不确定性对儿童有轻度或中度风险因素(6]。定期收集惯例数据显示,抗生素处方并发症患者的28%与18%的健康人流感样疾病(伊犁)[7]。
虽然不推荐常规使用抗生素对病毒rti [5),初步数据表明,早期的抗生素治疗可能减少流感患者临床恶化或伊犁。一随机安慰剂对照试验发现,sultamicillin治疗儿童肺炎的发病率显著降低与伊犁8]。成人的开放性试验证实流感发现使用奥司他韦进行治疗和阿奇霉素与更频繁的改善喉咙痛2天比奥司他韦(9]。此外,观测数据从实验室确诊流感患儿证明,到第七天,发烧已经定居在所有儿童早期与抗生素治疗但持续超过7天在那些没有接受抗生素的五分之一(10]。
因为点保健测试流感不是目前在大多数小学和门诊设置,我们进行了一个务实的试验来确定早期co-amoxiclav使用降低风险reconsultation由于临床恶化伊犁的孩子“风险”。
方法
研究设计和参与者
在这个双盲,随机,安慰剂对照IV期临床试验中,参与者被招募从通用实践和其他门诊设置在英格兰和威尔士。招聘开始于2015年2月11日。后续招聘季节10月份开始,一直持续到次年3月底,或者以后如果皇家全科医师学院的数据研究和监测中心表示,每周伊犁全科医生(GP)协商利率仍高于基线季节性阈值计算每个季节使用移动流行法[11]。总的来说,我们开设了151通用实践,42医院和两间中心招聘。
我们招募了“风险”的孩子知道相关并发症的风险因素从6个月到12岁和谁提出了在伊犁的前5天(12]。附录1列出了我们完整的合格标准。附录2总结我们的“风险”组。伊犁被定义为咳嗽和发烧的存在;发烧可能child-reported,父/据《卫报》报道,腋窝或鼓膜的温度> 37.8°C。我们排除了fda co-amoxiclav知道儿童和儿童需要立即抗生素或住院基于临床医生的判断。我们也排除已知的囊性纤维化,因为直接的抗生素治疗儿童急性rti建议在这些孩子13]。
增加我们的潜在的新成员,我们做了小修改合格标准2017/2018前招聘季节。首先,我们包括孩子永久注册在英国的任何地方,在通用实践不仅仅是英格兰。其次,我们只有排除孩子给予抗生素在过去72 h急性感染,而不是长期的预防措施。第三,我们澄清,要求立即住院的孩子只会被排除在外如果这是治疗相关并发症或观察期持久> 24小时。试验得到国家研究伦理学的伦理批准服务委员会(北部西海岸——利物浦东部)。额外收到批准的卫生研究权威,医药和保健产品管理机构,在适用情况下,地方治理机构。书面知情同意了所有参与者的家长或监护人。
试验是在ISRCTN注册(标识符ISRCTN707147832013-002822-21))和EudraCT数据库(标识符。
随机和盲
资格和基线评估描述后,参与者被随机分配(1:1)接收co-amoxiclav 400/57(阿莫西林(400毫克)三水合/克拉维酸钾(57毫克);5毫升时重组与水)或安慰剂。任务是执行使用抽签,开发一个基于网络的随机系统,充分验证了初级护理临床试验单位牛津大学。
随机分层的地区(五个地区)和最小化,使用非确定性算法,对年龄(6-23月或12年)和当前的季节性流感疫苗接种状态(是的或其他)。分配给的机会最小化组设置为80%。每个站点被研究药物在八块。分配是电脑使用块随机生成(2和4块大小)的试验统计学家(占据13.1版本,占据Corp .)、大学城,TX,美国)。这确保了每个站点维护平等co-amoxiclav供应和安慰剂。
医疗保健专业人士研究药物。医疗专家,研究团队,参与者和父母/监护人对治疗分配也不清楚。Co-amoxiclav和安慰剂有相同的包装和外观当重组但并不匹配。致盲因此由只允许每个孩子招募了一次。
程序
我们的协议12)描述了我们的研究过程。总之,我们收集基线数据的年龄,性别,并存病,家庭吸烟情况,接种流感疫苗状态,药物在当前疾病发作,持续发烧、症状持续时间、心率(HR)和呼吸速率。鼻拭子获得并放置在病毒传输介质。咽喉拭子也获得尽可能和放置在一个细菌的传输媒介。附录3拭子样本的实验室分析细节。
参与者被要求服用研究药物口服连续5天每天两次。附录4总结我们的给药方案,这是基于英国国家规定指导处方co-amoxiclav 400/57。
父母/监护人有四个1周日记记录研究药物的剂量(星期1日记),腋窝温度(每天睡前或之前给予退烧药,哪个更早发生),症状和不良事件(AEs)。症状数据收集每天直到他恢复(如果症状复发收集数据恢复)。父母/监护人被要求每天记录温度为28天或之前< 37.5°C连续两天。医疗保健专业人员通过电话联系父母/监护人1周和2周后随机收集数据AEs,发热持续时间和研究药物剂量的日记数据没有提供。
医疗条件的数据,常规药物、疫苗接种、急性磋商随机前12个月期间,抗生素处方前三个月期间随机和reconsultations从参与者的医疗记录。reconsultations、药物处方,数据调查,住院和死亡的28天内随机提取。
结果
我们的主要结果是reconsultation由于随机的临床恶化在28天。我们定义临床恶化的症状恶化,开发新的症状或并发症需要药物治疗或住院治疗的发展。这个定义被成功地用于一个大型试验涉及成人RTI较低(14)和一个队列研究涉及儿童急性咳嗽(15]。“恶化的症状”是通过记录的证据确定恶化症状指数咨询报告。从务实的角度看我们的审判,我们不需要医护人员使用验证量表得分症状严重程度指数咨询或在reconsultation集。“新症状”包括任何症状不报道指数咨询。住院治疗上包括住院后初级保健推荐和直接招生从医院门诊设置。确保临床结果数据的准确记录,临床医生独立于研究小组回顾医疗记录的随机选择。
次要结果药物处方和/或进一步调查,AEs,住院或死亡(所有随机后28天内),发热持续时间和持续时间的症状。我们的协议不需要招聘网站报道口腔黏膜与皮肤的念珠菌病(鹅口疮)、腹泻、恶心、呕吐或皮疹AEs如果他们评估为轻度或中度的临床严重程度并没有导致一个严重的AE,因为这些co-amoxiclav已知常见的副作用。
其他数据结果与健康相关的生活质量的措施,医疗资源利用率,细菌马车和抗生素耐药性也收集,但将在单独的论文报告。
统计分析
初级保健数据报告的并发症发生在17.6%的儿童患有慢性基础疾病与伊犁(现在16),由于并发症,占44%的计划外reconsultations新的症状或推迟决议呈现在初级保健儿童急性rti(61 138儿童)17]。因此,我们估计,40%的参与者在安慰剂组reconsult由于临床恶化。
我们的目标样本大小是650参与者,包括追踪损失备抵25%和1.041允许潜在的通货膨胀因素聚类在招聘网站(由于医生治疗和处方率差异)(12]。我们的估算是基于一个保守的星团内相关性的估计0.03 [18],变异系数值0.6 [19)和平均集群大小两个参与者(20.]。这将允许检测减少参与者reconsulting由于临床恶化的比例从40%到26%(相对风险降低35%)与90%的力量和5%的双尾α错误。
由于缓慢招聘临时讨论与我们的资助者,讨论后同意支持的延续试验策略提高招聘(12),认识到一个有效的266个参与者的样本容量仍将允许减少检测在临床恶化从40%到23%(相对风险降低42.5%)与80%的力量和5%的双尾α错误。这效果仍然被认为是保守的,因为之前的试验(8]报道相对风险降低85%的儿童肺炎的发生率与伊犁治疗sultamicillin(42岁的儿童)与安慰剂(七43岁的孩子)。虽然这个试验是相对较小的,没有收集结果数据reconsultations由于临床恶化,目前审判有相似之处,它还与伊犁招募儿童(而不是实验室确诊流感)和相关药物,像co-amoxiclav,含有青霉素抗生素(氨苄青霉素)和β-lactamase抑制剂(sulbactam)。
在开源软件数据double-entered和验证(OpenClinica 3.13版本,OpenClinica沃尔瑟姆,妈,美国)。统计分析使用占据15.1版(占据corp .)。我们进行了意向性治疗分析和参与者团体,他们分配进行分析。儿童的比例reconsulting由于临床恶化两组比较采用卡方检验和log-binomial回归模型与调整地区,年龄和当前的季节性流感疫苗接种的地位。治疗效果是报道的相对风险95%可信区间(CI)和假定值。未经调整的风险差异也出现95%可信区间。
发烧和症状持续时间组间比较使用Wilcoxon rank-sum测试和分位数回归。使用分位数回归分析进行调整的区域,年龄和当前的季节性流感疫苗接种的地位。二进制结果(规定比例的儿童药物和/或需要进一步调查,孩子谁报告AEs和儿童住院或死亡的28天内随机)比较使用卡方测试(或确切概率法的小数字)未经调整的分析和log-binomial回归,调整地区、年龄和当前的季节性流感疫苗接种的地位。
探索性的子群分析主要结果统计分析计划中预先确定探索实验室确诊流感是否和抗病毒药物治疗指数伊犁集慢化治疗的效果。log-binomial回归模型拟合的结果reconsultation由于临床恶化和调整的区域,年龄和季节性流感接种现状(额外的子群的主要影响变量和随机变量组和子群的交互项)。
结果
招聘
2015年2月11日至4月20日,2018年,我们筛选756名儿童。然而,370年不符合合格标准研究,另有115名儿童被合格的家长/监护人却不同意参与研究。我们决定在2017/2018赛季只有排除孩子给予抗生素在过去72 h如果这些是急性感染没有增加儿童的比例筛选要排除这个原因(2015/2016:9 197 (4.6%);2016/2017:23 229 (10.0%);2017/2018:25 330 (7.6%))。预防性抗生素处方只是记录在五个参与者(阿奇霉素,n = 2;阿莫西林,n = 1;复方磺胺甲恶唑,n = 1;和甲氧苄氨嘧啶,n = 1)。
我们随机选取了271名参与者接受co-amoxiclav (n = 136)或安慰剂(n = 135)。父母/监护人报告说,所有研究药物剂量是由81年的95名参与者co-amoxiclav组(85%)和74年的89名参与者(83%),安慰剂组的依从性数据(即。数据是否所有10个剂量的研究药物了)。附录5总结数据的研究药物剂量由参与者父母/监护人报告说,他们用了不到10剂量。附录5还包括参与者的父母/监护人数据报道,不到10剂量了但无法指定剂量的确切数字。
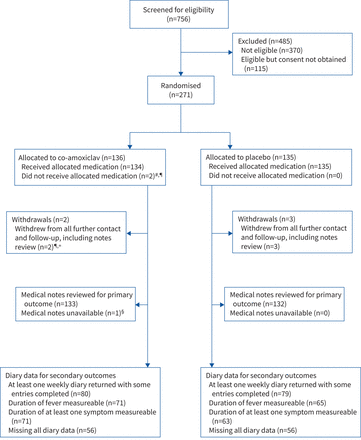
图1总结招聘和后续的参与者。数据reconsultations由于临床恶化可供265名参与者(co-amoxiclav n = 133;安慰剂,n = 132)。五个参与者的父母/监护人撤回同意从医学笔记数据提取(co-amoxiclav, n = 2;安慰剂,n = 3)。惯例的一个孩子(co-amoxiclav)拒绝研究小组访问医疗记录的内部原因。
参与招聘和随访。#:协议偏差(治疗临床医生撤回了研究药物;医疗记录供审核);¶:父母没有研究药物(撤回同意与孩子的父亲讨论后);+:儿童接受研究药物(父随后撤销了同意进一步联系和票据审核);§:医学笔记主要结果扣留医生手术内部原因(参与者不撤回;日记数据用于次要结果)。
参与者的特征
表1总结了参与者的基线特征。近四分之三的风险因素在呼吸道类别(198个席位中赢得了271个参与者(73.1%),最常见的哮喘(n = 99)和复发性病毒喘息(n = 70)。大约三分之一的参与者收到接种流感疫苗有关季节期间,他们招募了。实验室确诊流感中检测出37岁的271名儿童(13.7%);然而,犀牛/肠道病毒更常见的隔离(119,271名儿童(43.9%))。咽喉拭子从225名参与者(co-amoxiclav n = 114;安慰剂,n = 111)。最常见的细菌隔离流感嗜血杆菌发现在52 225咽喉拭子(23.1%)和13的37个参与者与实验室确诊流感(35.1%)。
结果
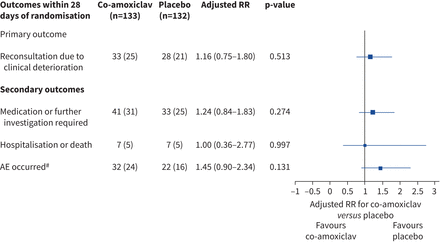
图2总结reconsultations由于随机的临床恶化在28天。至少一个reconsultation被记录在33 133名儿童(24.8%)随机co-amoxiclav和28 132名儿童(21.2%)随机安慰剂。没有证据表明组织之间的差异在临床恶化后分层和最小化因素调整(调整风险比率(RR) 1.16, 95%可信区间0.75 - -1.80;未经调整的相对危险度1.17,95%可信区间0.75 - -1.82;未经调整的风险差异3.6%,95% CI 6.5−13.7%)。没有集群进行调整,因为集群大小平均只有1.4(从195个站点271个参与者)(21]。没有统计上显著的差异观察儿童的比例需要药物治疗或进一步的调查,或需要住院治疗(图2)。没有死亡的记录。
调整风险比率(RRs)和95%置信区间(CIs)主要和二进制次要结果。数据提出了n(%)或调整RR (95% CI)。百分数是基于参与者的数量至少有一个结果事件报道的是谁(相对于参与者的数量分析的结果与reconsultation由于临床恶化,药物或需要进一步的调查,以及住院治疗或死亡)。所有模型都是调整的区域,年龄和当前的季节性流感疫苗接种状况,除了住院或死亡的模型只是调整年龄和季节性疫苗接种现状(如没有住院或死亡的报道在一些地区)。护士:数量的参与者来说,医学综述了笔记。AE:不良事件。#所有随机参与者:数据分析(co-amoxiclav n = 136;安慰剂,n = 135)。
图3总结日记数据时间发烧等症状。干扰睡眠时间明显短中值的孩子收到co-amoxiclav与安慰剂(中位数(co-amoxiclav) 4天,四分位范围(差)2 - 6天与中位数(安慰剂)7天,IQR 3-11天;p = 0.021)。组织被发现没有证据表明区别其他症状或发烧。
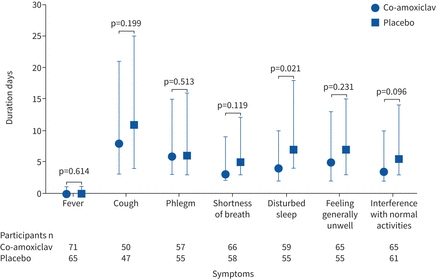
发烧和症状的持续时间。持续时间数据中位数(四分位范围)。假定值计算使用Wilcoxon rank-sum测试。
表2总结调整值的差异之间的发热和其它症状持续时间co-amoxiclav和安慰剂组。调整后,统计上的显著差异在时间打扰睡眠不再是观察co-amoxiclav和安慰剂组之间。然而,气短时间被发现显著短co-amoxiclav组(调整值差异−2.00天,95% CI 3.89−−0.11;p = 0.038)。
不良事件
表3总结了AEs发生后28天内随机。至少一个AE被报道在32 co-amoxiclav组的136名儿童(24%)和22的135名儿童(16%),安慰剂组。37 AEs报道co-amoxiclav组和安慰剂组29。一个不良事件报告在44名儿童(co-amoxiclav, n = 27个;安慰剂,n = 17)和两个不良事件报告了22个孩子(co-amoxiclav, n = 5;安慰剂,n = 6)。只有12个被报告为不良事件可能与研究药物(co-amoxiclav, n = 5;安慰剂,n = 7),只有三个是可能与研究药物(co-amoxiclav, n = 2;安慰剂,n = 1)。最常报道的AEs是皮肤的投诉和rti。 These RTIs were considered as separate from the index ILI episode for which the participant was entered into the trial. Nine serious adverse events (SAEs) were reported per group. All reported SAEs required participants to be hospitalised; however, none were considered related to study medication.附录6总结这些节约的更多细节。
子群和探索性分析
表4呈现我们的预先确定的亚组分析儿童与实验室确诊流感。儿童临床恶化的比例较低co-amoxiclav组21例(23.8%)(五)比安慰剂组(六16 (37.5%));然而,没有统计上的显著差异。此外,没有证据表明治疗手臂和实验室确诊流感之间的交互的状态(p = 0.241)。我们没有执行我们的计划亚组分析在儿童抗病毒药物或基线访问之前,参与者获得抗病毒药物。
我们做两个事后探索性分析。首先,我们持续时间之间的热组相比,在电话跟进,收集的数据被认为是与日记数据(数据来自两个来源是可行的,最长持续时间进行了分析)。这种方法允许分析99名儿童在92年co-amoxiclav组和安慰剂组。发热持续时间中值为1天(差0 - 3天)两组。其次,我们总结的数据比例需要药物或进一步调查的参与者中那些reconsulted由于临床恶化。这些类似的co-amoxiclav组33例(70%)(23)和安慰剂组28例(75%)(21)。
讨论
我们没有发现证据表明早期co-amoxiclav治疗可以减少临床恶化“风险”的孩子商量伊犁在初级或门诊。这一发现是高度generalisable社区医疗保健设置non-pandemic时期由于我们广泛的地理范围,招聘主要和其他门诊设置,务实伊犁病例定义为我们的主要结果和高保留率。
“风险”儿童的百分比reconsulted由于临床恶化在我们的样例(61年的265名参与者(23%)低于预期,但仍近6高于4%在初级护理的儿童急性RTI那些没有已知的流感并发症的危险因素或伊犁(22]。四分之三的“风险”患儿临床恶化我们的安慰剂组需要药物或进一步的调查(21的28个孩子)。然而,样本容量的估计认为并发症只有发生在44%的临床恶化事件(17]。这些数据是基于一般儿科人口初级保健,没有等价的数据在“风险”孩子们可以告知我们的估计。
我们试验的统计力量有限的结果只能招募了271名参与者与我们最初的目标650个参与者的样本大小。然而,我们最初的样本量估算允许25%的损失为主要结果随访率,这是远高于追踪损失2%(271名儿童)的观察。此外,样本仍足以检测从21%减少主要结果(比例在安慰剂组)到6.5%(绝对风险降低14.5%)与90%的力量或从21%到8%(绝对风险降低13%)与80%的力量和5%的双尾α错误。这些绝对风险降低治疗效果类似我们考虑目标样本大小(绝对风险降低40%至26%,14%),但从一个较低的基线。更大的样本将会允许我们估计结果更精确和检测更为保守的治疗效果。然而,我们需要考虑影响较小的临床重要性大小的数字需要治疗的好处与伤害。
相对较少的参与者与实验室确诊流感在我们的样例意味着我们没有足够的统计能力确定早期co-amoxiclav治疗降低风险的临床恶化这群。我们探索亚组分析发现,较低比例的儿童co-amoxiclav集团reconsulted由于临床恶化相比安慰剂组。然而,群体之间的差异没有统计学意义。然而,这一发现是两个试验的结果一致,证明临床受益于抗生素在流感积极参与者9)或面对伊犁流感流行期间(8]。
低比例的流感病例样本最有可能造成适度的季节性流感活动(23- - - - - -26)和季节性流感疫苗接种计划2013年开始对所有儿童在2岁(在连续几年推出包括学校疫苗接种计划和增加的意识“风险”儿童预防接种的资格27])。我们没有收集数据是否孩子们收到了减毒活疫苗和灭活流感疫苗;然而,很可能参与者收到了每种类型的疫苗的比例应该是平衡co-amoxiclav和安慰剂组之间年龄因为随机最小化(6-23月与12年)。没有禁忌症的情况下,孩子2岁,是减毒活疫苗疫苗和“风险”岁儿童6-23月包容了灭活疫苗,减毒活疫苗疫苗不许可使用在这个年龄段1]。
我们承认,伊犁病例定义是广泛的和非特异性;然而,包括额外的症状可能不增加我们的流感积极性率(28),使用快速检测generalisable会使我们的研究少。此外,初级保健医生认为一个孩子是否有流感与另一种病毒以外的重要流行设置(6]。越高数量的孩子在我们的审判人口其他呼吸道病毒被发现,尤其是鼻病毒和呼吸道合胞病毒,符合当前没有相关国家儿童疫苗接种规划这些感染和国家实验室数据表明更高的检测率这些感染在每个招聘季节的早期(29日]。
相对较低的细菌马车速度我们在试验中观察到的可能限制我们的能力来评估的有效性co-amoxiclav在我们的目标人群。中一个或多个细菌隔离只有大约四分之一的参与者。此外,近三分之一的儿童在安慰剂组被发现有一个或多个细菌分离株相比,只有大约五分之一的孩子co-amoxiclav组。这些百分比高于那些执行的一项研究报告的实时PCR分析儿童鼻咽拭子的发烧或伊犁,发现细菌感染的证据在5日至18日期间召开岁16.7%的儿童和6.5%的五岁以下儿童不知道流感或ILI-related并发症的危险因素(30.]。然而,安慰剂对照试验,招募了成人感冒相关报道,co-amoxiclav治疗只有提高临床治愈率群人从鼻咽分泌物细菌培养31日]。
我们没有足够的资源或基础设施来说明获得咽喉拭子细菌培养的孩子当他们reconsulted。然而,纵向研究的结果嵌套在审判将报告数据长期细菌co-amoxiclav马车与安慰剂的手臂在一个单独的纸上。我们也无法持续获得明确诊断儿童reconsulted由于临床恶化,立即或现场获得进一步的调查(如血液测试和胸部x线摄影)还没有在所有医疗保健设置,尤其是在通用做法。
我们的发现在发烧和其他症状持续时间进行解释时应特别谨慎。我们观察到的显著减少睡眠时间(未调整的分析)和呼吸短促(调整分析)可能是机会的发现反映了来自7个相互关联的多个观测父/卫报报道的结果。我们只能分析日志数据发烧或其他症状的持续时间大约一半的孩子。然而,这些后续利率接近一个diary-based队列研究的儿童急性rti [32]。
虽然我们co-amoxiclav和安慰剂准备匹配了外观,味道是不可能与他们尽管广泛努力这样做。因此,孩子和他们的照顾者的机会降到最低检测不同,我们只允许每个孩子被招募到试验一次。此外,使用完全验证了基于网络的随机系统意味着医疗专业人士的研究药物分配不能受到任何意识的差别。我们组间相似的药物治疗依从性和追踪损失利率表明这些措施是否足够。
我们只能够获得药物治疗依从性的数据从184年的271名参与者(68%)尽管我们使用两种不同的方法来收集这些数据(研究日记和电话跟进)。我们试验的实际性质意味着我们没有做出进一步努力跟踪家庭没有回应这两种方法,我们使用更多的资源密集型等措施也没有收集和重研究药物瓶。尽管如此,我们不认为这种过度影响我们的发现自从我们获得药物治疗依从性的数据相似的比例两组的参与者(co-amoxiclav: 95 136 (70%)与安慰剂:89 135 (66%))。
总之,我们的研究结果不支持直接抗生素处方与伊犁“风险”的孩子现在在初级或门诊外面流感大流行时期。然而,医疗专业人员可能希望考虑非预先存在的条件因素的风险评估,包括临床症状和体征33),和潜在的疾病控制34]。我们不能排除这种可能性,co-amoxiclav可能有效地减少临床恶化“风险”实验室确诊流感或儿童目前伊犁在流感流行或大流行。抗生素使用库存仍应保持在这样的时期,当流感感染的发生率和细菌并发症可能会高35]。未来的试验应该确定早期的抗生素治疗是有益的“风险”的孩子确诊流感感染时期通过招募高为流感流感活动或使用即时测试[36]。
结论
我们的研究结果并不支持“风险”的早期抗生素治疗儿童在小学或门诊呈现季节性伊犁。未来的研究应该确定抗生素减少临床恶化患者确诊流感或流感大流行期间伊犁。
补充材料
可共享的PDF
确认
该研究小组承认的支持国家卫生研究所(NIHR)临床研究网络(CRN)。我们感谢曼迪Wan(儿科研究药剂师,NIHR CRN儿童专业)对于试验药物对她的支持和指导,从采购处理。员工在牛津大学的初级护理临床试验单位负责随机软件设计(David法官),数据库开发(赛迪Kelly),试验协调(桑娅Beecher)和病人招聘(Heather鲁特,Karen Madronal艾琳诺埃尔,路易莎Saldana奥尔特加,皮帕布莱德,伯纳黛特芒迪的观点,贝琳达前去和萨曼莎塔尖)。我们感谢我们的项目指导委员会(威利汉密尔顿,朱迪·布鲁尔,莫林·贝克和罗伯特·纽比),我们的数据和安全监测委员会(Lorcan McGarvey, Mike Bradburn萨伦德出生和尼克·弗朗西斯)和我们的区域试验协调员(Lyn Liddiard, Tammy托马斯和克莱尔麦金太尔)为他们的有价值的建议和支持交付审判。我们感谢米尔德里德福斯特(牛津大学)和丹Richards-Doran(牛津大学)来开发我们的研究网站和其他进一步的宣传材料。我们还要感谢奥利弗van Hecke(牛津大学)帮助他与监测数据reconsultation从医疗记录中提取数据。最后,但并非最不重要的,我们要感谢所有的医疗专业人士,惯例和医院的工作人员、儿童和父母/监护人参加我们的研究。
脚注
可以从本文的补充材料www.qdcxjkg.com
这项研究被注册为ISRCTN 70714783/ EudraCT 2013-002822-21。试用协议,统计分析计划并去除了识别信息的参与者水平数据收集试验可用的请求。研究数据请求应提交相应的作者考虑的研究团队。
作者贡献:k, t·卡佛,s .吨M.G.出身低微的,公元干草,m·摩尔,p,林祖嘉巴特勒,a .农民,r·佩雷拉,l m。Yu和a . Harnden导致了研究协议。k .小王是首席调查员试验直到2018年9月产假,之后Harnden成为首席调查员。k, t·卡佛和s .吨导致了审判的日常管理和数据收集。j . Grabey负责数据管理。l m。Yu和j·Mollison监督统计分析计划的发展。美国又进行了统计分析。r·佩雷拉提供总体统计监督。公元M.G.出身低微的k . Wang,干草,m·摩尔j . Mollison p,林祖嘉巴特勒,a .农民和a . Harnden导致数据解释。 K. Wang wrote the first draft of the manuscript. All authors contributed comments and edits to the manuscript.
利益冲突:k .王举行了国家卫生研究所(NIHR)学术临床讲师职务期间进行的研究,目前持有NIHR博士后奖学金。
利益冲突:M.G.出身低微的报告赠款从英国NIHR健康保护研究单位在新兴和利物浦大学的人畜共患传染病疫情和威康信托基金会加强研究活动期间(时代)项目研究的开展,和威康信托基金会的资助和比尔和梅林达•盖茨基金会,以及资助来自英国NIHR评价疗效和机制,在提交工作;少数Integrum科学LLC的所有者,格林斯博罗,数控,美国以外的提交工作。
利益冲突:m·摩尔没有披露。
利益冲突:公元干草没有披露。
利益冲突:美国吨没有披露。
利益冲突:美国加拉没有披露。
利益冲突:j . Grabey没有披露。
利益冲突:t·卡佛没有披露。
利益冲突:r·佩雷拉收到资金从NIHR牛津生物医学研究中心(BRC),牛津医学技术和体外诊断NIHR合作(MIC), NIHR应用研究协作(电弧)牛津和泰晤士河谷和牛津马丁学校。
利益冲突:l m。于没有披露。
利益冲突:j . Mollison没有披露。
利益冲突:p没有披露。
利益冲突:a .农民收到资金从牛津BRC NIHR和NIHR的高级研究员。
利益冲突:林祖嘉巴特勒报告赠款NIHR作为NIHR高级调查员和NIHR卫生技术评估项目支持这项研究,以及资助NIHR健康保护研究单位的卫生保健相关感染和抗菌素耐药性的麦克风和赠款从NIHR健康创新诊断和监测技术,以提高社区医疗,在进行研究;个人费用咨询委员会工作从罗氏分子系统和辉瑞、罗氏分子诊断和赠款,在提交工作。Afinion CRP设备和相关的培训参与一般实践提供免费为阿勒尔和公司的研究是财团的公共资金资助的研究的一部分,包括工业合作伙伴。
利益冲突:a . Harnden没有披露。
支持声明:这个项目是由国家卫生研究所(NIHR)应用研究计划项目资助(项目参考rp - pg - 1210 - 12012)。作者的观点是,不一定的NIHR或卫生部和社会关怀。这项研究的资助者没有参与这项研究的设计和实施;的收集、管理、分析和解释数据;手稿的准备,审查和批准;或决定提交出版的手稿。k . Wang和美国加拉有完全访问所有的数据研究,负责数据的完整性和数据分析的准确性。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2020年7月17日。
- 接受2021年2月18日。
- 版权©2021年作者。生殖权利和权限接触权限在}{ersnet.org